МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРИКАЗ
от 21 октября 1997 г. N 308
ОБ УТВЕРЖДЕНИИ ИНСТРУКЦИИ
ПО ИЗГОТОВЛЕНИЮ В АПТЕКАХ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ
В целях повышения качества лекарственных средств, изготовляемых в аптеках, приказываю:
1. Ввести в действие с 1 января 1998 года Инструкцию по изготовлению в аптеках жидких лекарственных форм (Приложение).
2. Считать недействующим на территории Российской Федерации Приказ Министерства здравоохранения СССР от 11.11.90 N 435 «Об утверждении Инструкции по изготовлению в аптеках жидких лекарственных форм».
3. Контроль за выполнением настоящего Приказа возложить на заместителя министра Вилькена А.Е.
Министр
Т.Б.ДМИТРИЕВА
1. ОБЩИЕ ПОЛОЖЕНИЯ
1.1. Настоящая Инструкция содержит основные методы и правила изготовления в аптеках жидких лекарственных форм для внутреннего и наружного применения, качество которых должно соответствовать требованиям, регламентированным действующей Государственной фармакопеей (ГФ), нормативными документами, приказами и инструкциями Министерства здравоохранения Российской Федерации.
1.2. Действие Инструкции распространяется на все аптеки, находящиеся на территории России, независимо от форм собственности и ведомственной принадлежности.
1.3. При изготовлении жидких лекарственных форм, а также при получении, хранении и подаче на рабочее место воды очищенной и для инъекций в аптеках должны соблюдаться требования действующей Инструкции по санитарному режиму аптек.
В асептических условиях изготавливают: растворы для инъекций и инфузий; ирригационные растворы, вводимые в полости, не содержащие микроорганизмов; жидкие лекарственные формы для новорожденных и детей до 1 года; препараты в жидкой лекарственной форме, содержащие антибиотики и другие антимикробные вещества, а также предназначенные для нанесения на раны и ожоговые поверхности; капли глазные, офтальмологические растворы для орошений и примочки; концентрированные растворы (в том числе гомеопатические разведения); жидкие лекарственные средства в виде внутриаптечной заготовки.
1.4. Внутриаптечный контроль жидких лекарственных форм на стадиях изготовления, после изготовления и при отпуске из аптеки осуществляется в соответствии с требованиями действующих нормативных документов, приказов и инструкций.
1.5. Растворы и другие жидкие лекарственные формы изготавливают методами: массо-объемным, по массе, по объему. Действующей Государственной фармакопеей принят, как основной, массо-объемный метод изготовления жидких лекарственных форм.
1.6. В зависимости от метода изготовления содержание лекарственных веществ в жидких лекарственных формах выражается в концентрациях: массо-объемной, по массе, по объему.
Массо-объемная концентрация — количество лекарственного средства или индивидуального вещества (в граммах) в общем объеме жидкой лекарственной формы (в миллилитрах); концентрация по массе — количество лекарственного средства или индивидуального вещества (в граммах) в общей массе жидкой лекарственной формы (в граммах); объемная концентрация — количество жидкого лекарственного средства или индивидуального вещества (в миллилитрах) в общем объеме жидкой лекарственной формы (в миллилитрах).
1.7. В прописях рецептов концентрации: массо-объемная (а), по массе (б) и объемная концентрация (в) могут быть обозначены:
- В процентах (%)
Rp.: Solutionis Natrii bromidi 2% - 200 ml (а)
#
Rp.: Solutionis Camphorae oleosae 2% - 50,0 (б)
#
Rp.: Solutionis Acidi hydrochlorici 2% - 200 ml (в)
- Раздельным перечислением лекарственного средства (вещества)
и дисперсионной среды (растворителя)
Rp.: Natrii bromidi 4,0
Aquae purificatae 200 ml (а)
#
Rp.: Camphorae 1,0
Olei Helianthi 49,0 (б)
#
Rp.: Acidi hydrochlorici 4 ml
Aquae purificatae 196 ml (в)
- С указанием растворителя до заданного объема или массы
Rp.: Natrii bromidi 4,0
Aquae purificatae ad 200 ml (а)
#
Rp.: Camphorae 1,0
Olei Helianthi ad 50,0 (б)
#
Rp.: Acidi hydrochlorici 4 ml
Aquae purificatae ad 200 ml (в)
- С указанием соотношения массы или объема растворяемого
лекарственного средства (вещества) и объема или массы раствора
Rp.: Solutionis Natrii bromidi ex 4,0 - 200 ml
(seu 1:50 - 200 ml) (а)
#
Rp.: Solutionis Camphorae oleosae ex 1,0 - 50,0 (б)
#
Rp.: Solutionis Acidi hydrochlorici ex 4 ml - 200 ml
(seu 1:50 - 200 ml) (в)
При массо-объемном методе изготовления обозначение концентрации, например, 1:10 или 1:20 означает содержание вещества или лекарственного средства по массе (г) в указанном объеме изготавливаемой жидкой лекарственной формы (мл), т.е. следует взять 1 г вещества или лекарственного средства и растворителя до получения 10 мл или 20 мл жидкой лекарственной формы.
При изготовлении лекарственных форм методом по массе обозначение концентрации 1:10 или 1:20 означает содержание вещества или лекарственного средства по массе (г) в указанной массе жидкой лекарственной формы (г), т.е. следует взять 1 г вещества или лекарственного средства и 9 г или 19 г растворителя.
При изготовлении методом по объему обозначение концентрации 1:10 или 1:20 означает содержание вещества или лекарственного средства по объему (мл) в указанном объеме лекарственной формы (мл), т.е. следует взять 1 мл жидкого лекарственного вещества или средства и растворителя до получения 10 мл или 20 мл раствора.
1.8. В массо-объемной концентрации изготавливают водные и водно-спиртовые растворы твердых лекарственных веществ; водные и водно-спиртовые суспензии с содержанием твердых веществ менее 3%; разведения стандартных растворов, выписанных в рецепте под химическим названием, с указанием концентрации лекарственного вещества в растворе (раздел 2, пп. 2.5.2, 2.5.3).
В концентрации по массе изготавливают растворы твердых и жидких лекарственных веществ в вязких и летучих растворителях, дозируемых по массе, а также суспензии и эмульсии.
По массе дозируют: жирные и минеральные масла, глицерин, димексид, полиэтиленгликоли (полиэтиленоксиды), силиконовые жидкости, эфир, хлороформ, а также: бензилбензоат, валидол, винилин (бальзам Шостаковского), деготь березовый, ихтиол, кислоту молочную, масла эфирные, скипидар, метилсалицилат, нитроглицерин, пергидроль.
В концентрации по массе изготавливают гомеопатические жидкие лекарственные средства.
В объемной концентрации изготавливают растворы спирта различной концентрации, кислоты хлористоводородной и стандартные растворы, выписанные в рецепте под условным названием (раздел 2, пп. 2.5.1, 2.5.3), по объему дозируют: воду очищенную и для инъекций, водные растворы лекарственных веществ, (в том числе сироп сахарный), галеновые и новогаленовые лекарственные средства (настойки, жидкие экстракты, адонизид и др.).
Если требуется установить объем жидкости, выписываемой в прописи рецепта и дозируемой по массе, или, наоборот, массу жидкости, выписываемой в прописи рецепта и дозируемой по объему, используют значение их плотности (Приложения 1, 2).
1.9. Если в прописи не указан растворитель, изготавливают водный раствор.
Под названием «вода» при отсутствии особых указаний понимают воду очищенную.
Под названием «спирт» понимают спирт этиловый. При отсутствии указаний о концентрации спирта (в рецепте или соответствующей нормативной документации) следует использовать 90% спирт.
Под названием «эфир» понимают эфир медицинский.
Под названием «глицерин» понимают глицерин, содержащий 10 — 16% воды, с плотностью 1,223 — 1,233 г/см куб.
1.10. При изготовлении водных растворов веществ, содержащих в составе молекулы кристаллизационную воду, пересчет количества лекарственного вещества с учетом содержания кристаллизационной воды осуществляют в соответствии с действующей ГФ или иной нормативной документацией в тех случаях, когда это регламентируется составом прописи и методом количественного определения.
Сильно гигроскопичные вещества используют для изготовления жидких лекарственных форм в виде концентрированных растворов (например, кальция хлорид, калия ацетат).
1.11. Изготовление жидких лекарственных форм основано на применении: бюреточных установок и мерной посуды, откалиброванных в соответствии с ГОСТом, заранее изготовленных концентрированных растворов лекарственных веществ (концентратов), а также на соблюдении определенных правил изготовления.
1.12. Жидкости, выпускаемые фармацевтическими производствами и предприятиями (меновазин, раствор йода спиртовой и др.), на состав и технологию которых имеется нормативная документация, могут изготавливаться в соответствии с этой документацией и указаниями настоящей Инструкции (разд. 2, п. 2.7, Приложение 3).
1.13. После изготовления жидкой лекарственной формы отклонение общего объема или массы от указанных в прописи рецепта не должно превышать норму допустимого отклонения, установленную действующей нормативной документацией.
2. ОСНОВНЫЕ ПРАВИЛА ИЗГОТОВЛЕНИЯ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ
2.1. Общие правила изготовления, последовательность
растворения и смешивания лекарственных средств
При изготовлении жидких лекарственных форм с водной дисперсионной средой в первую очередь отмеривают рассчитанный объем воды (очищенной, для инъекций или ароматной), в котором последовательно растворяют твердые лекарственные и вспомогательные вещества с учетом растворимости и возможного их взаимодействия.
Первыми в отмеренном объеме воды растворяют ядовитые и наркотические вещества (список А), затем наркотические и сильнодействующие (список Б), а далее несильно действующие с учетом их растворимости.
Для повышения растворимости веществ умеренно, мало или медленно растворимых их предварительно измельчают, а в процессе изготовления их растворы нагревают с учетом физико-химических свойств и перемешивают.
При изготовлении растворов очень мало растворимых или практически нерастворимых веществ, кроме вышеперечисленных операций используют получение растворимых производных (комплексообразование, образование растворимых солей) и солюбилизацию в соответствии с нормативной документацией.
Изготовленный раствор фильтруют через фильтр, материал которого подбирают с учетом физико-химических свойств веществ и назначения раствора.
Твердые лекарственные вещества в состав лекарственной формы могут быть введены в виде заранее изготовленных концентрированных растворов, которые добавляются после растворения твердых веществ и фильтрования раствора (Приложения 4 — 7).
Если в состав лекарственной формы входят другие жидкие лекарственные средства, их добавляют к водному раствору в следующей последовательности:
— водные нелетучие и непахучие жидкости,
— иные нелетучие жидкости, смешивающиеся с водой,
— водные летучие жидкости,
— жидкости, содержащие спирт, в порядке возрастания его концентрации (Приложение 8),
— летучие и пахучие жидкости.
При добавлении всех жидкостей также следует учитывать их принадлежность к определенному списку, растворимость и способность смешиваться с водой.
При изготовлении растворов в вязких и летучих растворителях непосредственно в сухой флакон для отпуска дозируют лекарственное средство или вещество, вспомогательные вещества, затем взвешивают растворитель (спирт отмеривают).
При использовании вязких растворителей (глицерин, масла) применяют нагревание с учетом физико-химических свойств лекарственных веществ.
При растворении в спирте или хлороформе — нагревают только в случае необходимости и с соблюдением мер предосторожности.
Растворы, содержащие летучие вещества, нагревают при температуре не более 40 — 45° C.
Не нагревают жидкости, содержащие эфир и его смеси со спиртом.
Растворы фильтруют через сухой фильтрующий материал, который подбирают с учетом вязкости и летучести растворителя, соблюдая меры предосторожности для снижения потерь, связанных с испарением.
2.2. Общий объем жидкой лекарственной формы
при изготовлении в массо-объемной или объемной концентрации
2.2.1. При раздельном выписывании компонентов общий объем лекарственной формы определяют суммированием объемов всех жидкостей, перечисленных в прописи рецепта.
Пример 1. Rp.: Solutionis Glucosi 10% - 200 ml
Solutionis Citrali spirituosae 1% - 2 ml
Magnesii sulfatis 4,0
Natrii bromidi 2,0
Sirupi simplicis
Tincturae Valerianae ana 10 ml
Общий объем микстуры равен 222 мл (200 + 2 + 10 + 10).
Если в состав лекарственной формы входит жидкость, выписанная по массе (М), ее объем (V) определяют с учетом плотности (p).
M
V = ---
p
(Приложения 1, 2)
Пример 2. Rp.: Solutionis Kalii acetatis 10% - 100 ml
Adonisidi 5 ml
Glycerini 10,0
В прописи присутствует жидкость, выписанная по массе, — глицерин. Для определения объема глицерина используют среднее значение его плотности. Объем 10 г глицерина равен 8 мл.
Общий объем лекарственной формы — 113 мл (100 + 5 + 8).
2.2.2. Общий объем микстуры указан в прописи рецепта.
Пример 3. Rp.: Codeini phosphatis 0,12
Natrii bromidi 4,0
Tincturae Belladonnae 5 ml
Tincturae Valerianae 20 ml
Aquae purificatae ad 200 ml
Общий объем микстуры указан в прописи рецепта и равен 200 мл.
Пример 4. Rp.: Adonisidi 5 ml
Solutionis Natrii bromidi 3% ad 100 ml
Общий объем микстуры указан в прописи рецепта и равен 100 мл.
2.3. Общая масса жидкой лекарственной формы
при изготовлении в концентрации по массе
При раздельном выписывании в прописи рецепта общую массу определяют суммированием масс всех компонентов, входящих в пропись.
Общая масса может быть указана в прописи (например, «ad 200,0»; «5% — 200,0», «1:20 — 200,0»).
Если в прописи присутствует жидкость, выписанная по объему, ее массу определяют с учетом плотности (p)
(M = V x p).
2.4. Изменение общего объема жидких лекарственных форм
при массо-объемном изготовлении из твердых растворимых
веществ и концентрированных растворов
Изменение общего объема при растворении твердого вещества можно не учитывать, если оно укладывается в норму допустимого отклонения.
Для каждого лекарственного вещества максимальная концентрация в процентах (C max), при которой изменение общего объема укладывается в норму допустимого отклонения, вычисляют по формуле:
N
C max(%) = ---,
КУО
где: N — норма допустимого отклонения для данного общего объема препарата, %,
КУО — коэффициент увеличения объема при растворении 1 г вещества при 20° C, мл/г (Приложение 9).
Пример 5. Rp: Analgini 3,0
Natrii bromidi 4,0
Aquae purificatae 200 ml
Микстуру изготавливают, используя концентрированный 20% раствор натрия бромида.
Максимальную концентрацию (C max, %) анальгина, при которой наблюдается изменение объема выше нормы допустимого отклонения, вычисляют по указанной выше формуле
2
C max = ------ = 2,94%,
0,68
В прописи анальгин выписан в концентрации 1,5%, поэтому изменение объема при растворении 3 г анальгина можно не учитывать.
В 180 мл воды очищенной растворяют 3 г анальгина, фильтруют во флакон для отпуска и добавляют 20 мл 20% раствора натрия бромида.
Пример 6. Rp.: Solutionis Calcii chloridi 5% - 200 ml
Glucosi 60,0
Natrii bromidi 3,0
Микстуру изготавливают с использованием концентрированных растворов кальция хлорида 50% и натрия бромида 20%. Концентрированный раствор глюкозы в аптеке в данный момент отсутствует.
Максимальная концентрация глюкозы безводной, при которой наблюдается изменение объема выше нормы допустимого отклонения, — 3,1%.
2
C max = ---- = 3,1%
0,64
В данной прописи глюкоза выписана в 30% концентрации, т.е. необходимо учитывать изменение объема при ее растворении.
Вместо 60 г глюкозы безводной, указанной в прописи рецепта, требуется взять 66,6 г глюкозы с содержанием влаги 10%. Изменение объема при растворении водной глюкозы составит 46 мл (66,6 x x 0,69). В 119 мл горячей воды очищенной растворяют 66,6 г глюкозы, фильтруют во флакон для отпуска, отмеривают 20 мл раствора кальция хлорида 50% и 15 мл раствора натрия бромида 20%.
При изготовлении жидкой лекарственной формы путем растворения нескольких твердых веществ, изменение общего объема учитывают, если их суммарное содержание составляет 3% и более.
2.5. Разведение стандартных фармакопейных растворов
Таблица 1
Стандартные растворы
┌────────────────────────┬────────────────┬──────────────────────┐ │ Химическое название │Концентрация, % │ Условное название │ ├────────────────────────┼────────────────┼──────────────────────┤ │Кислота хлористоводо- │ │ │ │родная │ 24,8 - 25,2 │ - │ ├────────────────────────┼────────────────┼──────────────────────┤ │Кислота хлористоводо- │ │ │ │родная разведенная │ 8,2 - 8,4 │ - │ ├────────────────────────┼────────────────┼──────────────────────┤ │Раствор аммиака │ 9,5 - 10,5 │ - │ ├────────────────────────┼────────────────┼──────────────────────┤ │Кислота уксусная │ не менее 98,0 │ - │ ├────────────────────────┼────────────────┼──────────────────────┤ │Кислота уксусная │ │ │ │разведенная │ 29,5 - 30,5 │ - │ ├────────────────────────┼────────────────┼──────────────────────┤ │Раствор алюминия │ │ │ │ацетата основного │ 7,6 - 9,2 │ Жидкость Бурова │ ├────────────────────────┼────────────────┼──────────────────────┤ │Раствор калия ацетата │ │ Жидкость калия │ │ │ 33,0 - 35,0 │ ацетата или │ │ │ │ раствор жидкости │ │ │ │ калия ацетата │ ├────────────────────────┼────────────────┼──────────────────────┤ │Раствор водорода пере- │ │ │ │киси концентрированный │ 27,5 - 30,1 │ Пергидроль │ ├────────────────────────┼────────────────┼──────────────────────┤ │Раствор водорода пере- │ │ │ │киси разведенный │ 2,7 - 3,3 │ - │ ├────────────────────────┼────────────────┼──────────────────────┤ │Раствор формальдегида │ 36,5 - 37,5 │ Формалин │ └────────────────────────┴────────────────┴──────────────────────┘
2.5.1. Растворы кислоты хлористоводородной
Растворы кислоты хлористоводородной любой концентрации изготавливают из кислоты хлористоводородной разведенной (8,2 — 8,4%), принимая ее за единицу (100%).
Кислота хлористоводородная разведенная используется также для получения 10% (1:10) раствора в качестве внутриаптечной заготовки (концентрация кислоты при этом будет 0,82 — 0,84%).
Пример 7. Rp.: Acidi hydrochlorici diluti 4 ml
Pepsini 4,0
Aquae purificatae 150 ml
Общий объем микстуры 154 мл. Во флакон для отпуска отмеривают 114 мл воды очищенной и 40 мл раствора кислоты хлористоводородной разведенной 1:10 (или 150 мл воды очищенной и 4 мл кислоты хлористоводородной разведенной 8,3%). В подкисленной воде растворяют 4 г пепсина.
Кислота хлористоводородная с концентрацией 24,8 — 25,2% отпускается только в тех случаях, когда в прописи рецепта имеется соответствующее указание.
Без дополнительного указания кислота хлористоводородная с концентрацией 24,8 — 25,2% используется при изготовлении раствора 2 по прописи Демьяновича.
Пример 8. Rp.: Solutionis Acidi hydrochlorici 6% - 100 ml
(Раствор N 2 по Демьяновичу)
Объем раствора — 100 мл.
Во флакон для отпуска отмеривают 94 мл воды очищенной и 6 мл кислоты хлористоводородной 24,8 — 25,2%.
При отсутствии кислоты хлористоводородной с концентрацией 24,8 — 25,2% можно использовать кислоту хлористоводородную разведенную с концентрацией 8,2 — 8,4%, которой следует взять в 3 раза больше.
Во флакон для отпуска отмеривают 82 мл воды очищенной и 18 мл кислоты хлористоводородной разведенной.
2.5.2. Растворы аммиака и кислоты уксусной
Растворы аммиака и кислоты уксусной изготавливают, исходя из фактического содержания лекарственного вещества в стандартном растворе. При расчетах используют формулу разведения:
V1 x C1
V = ---------,
C
где: V - объем стандартного раствора, мл;
V1 - требуемый объем изготавливаемого раствора, мл;
C1 - требуемая концентрация раствора, %;
C - концентрация стандартного раствора, %.
2.5.3. Растворы алюминия ацетата основного, калия ацетата,
водорода перекиси, формальдегида
При выполнении расчетов для разведения этих стандартных растворов до требуемой концентрации учитывается, под каким (химическим или условным) названием выписан раствор в прописи рецепта.
Если растворы этих веществ выписаны под химическим названием (табл. 1), расчет проводят с учетом их фактического содержания в стандартном растворе, а если под условным названием, то при изготовлении стандартный раствор принимают за единицу (100%).
Для изготовления разведенных растворов формальдегида и водорода перекиси разрешается использовать формалин с содержанием формальдегида менее 36,5% и раствор пергидроля с содержанием водорода перекиси более 30%.
При расчетах разницу концентраций учитывают с помощью коэффициента пересчета (КП).
В аптеку поступил раствор с концентрацией формальдегида 34%.
Пример 9. Rp.: Solutionis Formaldehydi 5% — 200 ml
Раствор выписан под химическим названием.
Количество миллилитров стандартного раствора формальдегида (X), требуемое для разведения, рассчитывают по формуле с учетом его фактического (34%) содержания в растворе:
200 x 5
X = ------- = 29,4 мл
34
Воды очищенной — 170,6 мл (200 — 29,4) мл
Пример 10. Rp.: Solutionis Formalini 5% — 200 ml
Раствор выписан под условным названием. При расчетах стандартный раствор принимают за единицу (100%).
Стандартного раствора формальдегида (36,5 — 37,5%) следует взять 10 мл и 190 мл воды очищенной.
В случае использования раствора формальдегида 34% величина КП равна 1,08 (37:34). Рассчитанное количество стандартного 34% раствора формальдегида умножают на 1,08 (10 x 1,08), т.е. следует взять 11 мл этого раствора и 189 мл воды очищенной.
В аптеку поступил пергидроль с концентрацией водорода перекиси 40%.
Пример 11. Rp.: Solutionis Hydrogenii peroxydi 20% — 100 ml
Раствор выписан под химическим названием. Количество граммов пергидроля 40% (X), требуемое для разведения, вычисляют по формуле:
20 x 100
X = -------- = 50 г
40
Отвешивают 50 г пергидроля 40% и добавляют воду очищенную до получения 100 мл раствора.
Пример 12. Rp.: Solutionis Perhydroli ex 20,0 — 100 ml
Раствор выписан под условным названием. Для изготовления выписанного раствора следует взять 20 г стандартного раствора пергидроля и воды очищенной до 100 мл. При изготовлении из пергидроля 40% концентрации последнего следует взять меньше. Величина КП равна 0,75 (30:40), т.е. 15 г (20 x 0,75).
Отвешивают 15 г пергидроля 40% концентрации и добавляют воду очищенную до 100 мл.
При дозировании пергидроля по объему необходимо сделать расчеты с учетом его плотности (Приложение 2).
При изготовлении внутриаптечной заготовки раствора водорода перекиси 3% следует добавлять стабилизатор натрия бензоат в количестве 0,05%.
Если в прописи рецепта концентрация раствора не указана, то отпускают растворы:
- кислоты хлористоводородной разведенной 8,3%
- водорода перекиси 3%
- кислоты уксусной 30%
- аммиака 10%
- формальдегида 37%
2.6. Изготовление жидких лекарственных форм, содержащих
ароматные воды
Ароматные воды изготавливают и хранят в соответствии с требованиями действующей нормативной документации (Приложение 10).
Ароматные воды дозируют по объему. При растворении твердых лекарственных веществ объем воды ароматной, выписанный в рецепте, не уменьшают на величину изменения объема.
В случае точного указания объема воды ароматной в прописи рецепта, изменение объема при растворении твердых лекарственных веществ учитывают при контроле качества изготовленной лекарственной формы. При расчете общего объема используют значения КУО лекарственных веществ (Приложение 9).
При изготовлении микстур, в которых основной дисперсионной средой является вода ароматная, концентрированные растворы лекарственных веществ не используют.
Пример 13. Rp.: Glucosi 10,0
Kalii iodidi 4,0
Adonisidi
Tincturae Menthae ana 5 ml
Sirupi simplicis
Tincturae Valerianae ana 10 ml
Aquae Menthae 200 ml
В прописи рецепта указан точный объем воды мятной и не указан общий объем микстуры, который учитывают при контроле. В этом случае общий объем (238,6 мл) определяют суммированием объемов всех жидких компонентов, выписанных в прописи (230 мл), и прироста объема (8,6 мл) при растворении 11,11 г глюкозы с учетом содержания кристаллизационной воды (11,11 x 0,69) и 4 г калия иодида (4 x 0,23).
В подставку отмеривают 200 мл воды мятной, растворяют при перемешивании 11,11 г глюкозы и 4 г калия иодида.
Раствор фильтруют во флакон для отпуска. Добавляют при перемешивании 10 мл сиропа сахарного, 5 мл адонизида (сильнодействующее средство, содержание спирта 18 — 20%), 10 мл настойки валерианы (концентрация спирта 70%), 5 мл настойки мяты (концентрация спирта 90%).
Пример 14. Rp.: Glucosi 10,0
Kalii iodidi 4,0
Adonisidi
Tincturae Menthae ana 5 ml
Sirupi simplicis
Tincturae Valerianae ana 10 ml
Aquae Menthae ad 200 ml
Точный объем воды мятной в прописи рецепта не указан, а общий объем микстуры указан. В этом случае объем воды ароматной определяют, вычитая из общего объема (200 мл) объемы всех жидких компонентов (30 мл) и прирост объема при растворении глюкозы и калия иодида.
Объем воды мятной для изготовления микстуры составит 161,4 мл (200-5-5-10-10-8,6).
Особенности изготовления некоторых растворов представлены в Приложении 14.
2.7. Расчеты и правила дозирования спирта различной
концентрации при изготовлении лекарственных форм
для внутреннего и наружного применения
Выписанное в рецепте количество спирта соответствует объемным единицам измерения.
При разведении спирта используют таблицы, приведенные в действующей ГФ и в настоящей Инструкции (Приложения 10, 11).
Норма отпуска спирта учетной концентрации в пересчете на массу составляет 50 г. В случае указания в рецепте «По специальному назначению» — не более 100 г. Для учета спирта по массе используют таблицы (Приложение 12, таблицы 1 — 11).
При изготовлении лекарственных форм спирт дозируют по объему, не уменьшая объем, указанный в рецепте, на величину его прироста при растворении лекарственных веществ.
Общий объем учитывают при контроле качества лекарственной формы.
Изменение объема при растворении лекарственных веществ, учитываемое при контроле, рассчитывают, используя значения КУО лекарственных веществ (Приложение 9).
При изготовлении стандартных спиртовых растворов используют спирт в концентрации, указанной в нормативной документации (Приложение 3).
Если в прописи рецепта без указания концентрации выписан раствор, представленный в нормативной документации несколькими концентрациями лекарственного вещества, отпускают раствор с меньшей концентрацией, т.е. растворы:
- бриллиантового зеленого 1%,
- йода 1%,
- кислоты борной 1%,
- кислоты салициловой 1%,
- левомицетина 0,25%,
- ментола 1%,
- резорцина 1%,
- камфоры 2%.
Пример 15. Rp.: Mentholi 1,0
Novocaini 3,0
Anaesthaesini 2,5
Spiritus aethylici 50 ml
Во флакон для отпуска отвешивают 3 г новокаина, 2,5 г анестезина и 1 г ментола, отмеривают 50 мл спирта 90%.
Общий объем раствора с учетом прироста объема при растворении лекарственных веществ равен 55,6 мл. Отклонение в объеме превышает норму допустимого отклонения (+/- 4%), что учитывают при контроле раствора.
Пример 16. Rp.: Solutionis Novocaini
spirituosae 6% - 50 ml
Mentholi 1,0
Anaesthaesini 2,5
В прописи не указан объем спирта, указан объем спиртового раствора новокаина.
Максимальная концентрация новокаина, при которой изменение объема укладывается в норму допустимого отклонения (+/- 4%), составляет 4,97% (4:0,81).
В прописи рецепта выписан 6% раствор новокаина (3 г вещества в 50 мл раствора).
Следовательно, чтобы получить указанный в прописи рецепта объем раствора новокаина (КУО 0,81 мл/г), следует взять 47,6 мл 90% спирта (50 — 3 x 0,81).
После растворения ментола и анестезина в 47,6 мл 90% спирта общий объем раствора будет равен 53,2 мл, (50 мл раствора новокаина и прирост объема 3,2 мл при растворении ментола (1 x x 1,1) и анестезина (2,5 x 0,85).
Отклонение общего объема также не укладывается в норму допустимого отклонения (+/- 4%), что необходимо учитывать при контроле.
Пример 17. Rp.: Mentholi 1,5
Novocaini
Anaesthaesini ana 2,0
Spiritus aethylici 70% - 70 ml
В 70 мл 70% спирта содержится 51,04 мл 96% спирта, что по массе составляет 41,23 (Приложения 11, 12, табл. 2), поэтому лекарственная форма подлежит изготовлению (норма отпуска 50 г спирта учетной концентрации не превышена).
Общий объем препарата после растворения лекарственных веществ — 74,97 мл, что превышает норму допустимого отклонения (+/- 3%), поэтому изменение объема учитывают при анализе.
Пример 18. Rp.: Anaesthaesini 2,0
Acidi borici 1,5
Picis liquidae 5,0
Olei Ricini 2,5
Spiritus aethylici 96% ad 50 ml
В рецепте не указан объем спирта. Указан общий объем лекарственной формы. Объем 96% спирта определяют, вычитая из общего объема лекарственной формы объемы, занимаемые дегтем и маслом касторовым (Приложение 1), а также изменение объема, возникающее при растворении анестезина и кислоты борной (Приложение 9), т.к. оно не укладывается в норму допустимого отклонения.
2,5 г масла касторового занимают объем 2,6 мл (2,5:0,958); 5 г дегтя — 5,3 мл (5:0,938); изменение объема при растворении анестезина — 1,7 мл (2 x 0,85), кислоты борной — 0,97 мл (1,5 x x 0,65). Всего — 10,6 мл.
Объем 96% спирта составляет 39,4 мл.
В предварительно взвешенный флакон для отпуска отвешивают касторовое масло и деготь, добавляют заранее изготовленный спиртовой раствор анестезина и борной кислоты в 39,4 мл 96% спирта.
2.8. Изготовление лекарственных форм, содержащих
водные извлечения
Водные извлечения (настои и отвары) изготавливают в соответствии с требованиями действующей ГФ экстракцией лекарственного растительного сырья водой очищенной, а также растворением сухих или жидких экстрактов (концентратов) в рассчитанном объеме воды очищенной.
Запрещается изготовление в аптеках и использование водных извлечений заведомо более высокой концентрации с целью последующего разбавления, так как при изготовлении концентрированных извлечений из сырья не достигается полнота экстракции биологически активных веществ.
При изготовлении настоев и отваров запрещается заменять лекарственное растительное сырье настойками, эфирными маслами и экстрактами, не предназначенными для изготовления водных извлечений.
При расчете требуемого для экстракции объема воды очищенной и количества сырья используют значения коэффициентов водопоглощения или расходных коэффициентов (Приложение 13).
При изготовлении водных извлечений обеспечивают оптимальные условиях экстракции, учитывая стандартность лекарственного растительного сырья; его измельченность и гистологическую структуру; соотношение массы сырья и объема экстрагента; физико-химические свойства действующих и сопутствующих веществ; материал аппаратуры и другие факторы, влияющие на качество водного извлечения.
Изготовленные водные извлечения после отжатия сырья и фильтрования доводят водой очищенной до объема, указанного в прописи рецепта.
Галеновые и новогаленовые лекарственные средства следует добавлять к изготовленному водному извлечению в последовательности, изложенной в пункте 2.1.
2.8.1. Многокомпонентные водные извлечения
из лекарственного растительного сырья, требующего
одинаковых условий экстракции
Водные извлечения из лекарственного растительного сырья, требующего одинакового режима экстракции, обусловленного физико — химическими свойствами действующих и сопутствующих веществ, изготавливают в одном инфундирном стакане без учета гистологической структуры сырья.
Пример 19. Rp.: Infusi rhizomatis cum radicibus
Valerianae ex 10,0 - 200 ml
Infusi foliorum Menthae
piperitae ex - 4,0
Измельченное растительное сырье (10 г корневищ с корнями валерианы и 4 г листьев мяты) помещают в перфорированный цилиндр инфундирного стакана, заливают 238 мл воды очищенной. Объем воды для экстракции рассчитывают по формуле:
V = V1 + (Кв1 x М1 + Кв2 x М2),
где: V — объем воды очищенной, взятой для экстракции, мл;
V1 — объем водного извлечения, указанный в прописи рецепта, мл;
М1 — масса корневищ с корнями валерианы, взятая для экстракции, г;
М2 — масса листьев мяты, взятая для экстракции, г;
Кв1 — коэффициент водопоглощения корневищ с корнями валерианы, 2,9 мл/г;
Кв2 — коэффициент водопоглощения листьев мяты, 2,4 мл/г.
Инфундирный стакан плотно закрывают крышкой, помещают в инфундирный аппарат и настаивают на кипящей водяной бане 15 мин., не открывая крышку инфундирного стакана. Охлаждают при комнатной температуре не менее 45 мин. Фильтруют, отжимают сырье, измеряют объем изготовленного настоя и, при необходимости, доводят водой объем до 200 мл.
2.8.2. Многокомпонентные водные извлечения
из лекарственного растительного сырья, требующего различных
условий экстракции
Изготавливают раздельно, используя для экстракции максимально возможный объем воды очищенной, но не менее, чем 10-кратный по отношению к массе сырья.
Пример 20. Rp.: Radicum Althaeae 10,0
Rhizomatis cum radicibus
Valerianae 8,0
Herbae Leonuri
Foliorum Farfarae ana 20,0
Corticis Viburni 25,0
Aquae purificatae ad 1000 ml
В состав прописи входят виды сырья, требующие различных режимов экстракции:
— корни алтея — настаивания при комнатной температуре;
— корневища с корнями валерианы, трава пустырника и листья мать-и-мачехи — настаивания по общим правилам, регламентированным действующей ГФ;
— кора калины — изготовления отвара по общим правилам ГФ.
Для максимального извлечения полисахаридов слизистой природы из 10 г корней алтея изготавливают 200 мл водного извлечения 5% концентрации.
Массу сырья и объем воды очищенной рассчитывают с учетом расходного коэффициента (К расх). Значения К расх для различных концентраций настоя корней алтея представлены в Приложении 14.
Для 5% настоя корня алтея К расх = 1,3; масса сырья — 13 г (10 г x 1,3); объем воды очищенной — 260 мл (200 x 1,3).
Отвар коры калины изготавливают в соотношении 1 : 10, т.е. из 25 г коры — 250 мл отвара. Объем воды для экстракции коры калины с учетом коэффициента водопоглощения (2 мл/г) — 300 мл (250 + 25 x x 2). Настои корневищ с корнями валерианы, травы пустырника и листьев мать-и-мачехи изготавливают в объеме 550 мл (1000 — 200 — — 250). Объем воды очищенной для экстракции составляет 673 мл (550 + 8 x 2,9 + 20 x 2 + 20 x 3).
Все три извлечения изготавливают отдельно, доводят водой очищенной до требуемого объема: 200 мл, 250 мл и 550 мл соответственно и затем объединяют.
2.8.3. Лекарственные формы, содержащие водные
извлечения из сырья и твердые вещества, растворимые
в водных извлечениях
При изготовлении водных извлечений из сырья использование концентрированных растворов лекарственных веществ не допускается. Твердые лекарственные вещества растворяют в готовом водном извлечении при перемешивании и фильтруют во флакон для отпуска через тот же фильтр, который использовался для фильтрования водного извлечения. При необходимости объем лекарственной формы доводят водой очищенной до указанного в прописи.
Пример 21. Rp.: Infusi rhizomatis cum radicibus
Valerianae ex 10,0 - 200 ml
Infusi foliorum Menthae piperitae ex 4,0
Coffeini Natrii benzoatis 0,4
Natrii bromidi 3,0
Magnesii sulfatis 0,8
Изготовленный настой фильтруют в подставку (изготовление настоя см. пример 19), растворяют 0,4 г кофеина-натрия бензоата, 3 г натрия бромида, 0,8 г магния сульфата при перемешивании и фильтруют во флакон для отпуска, как было указано выше.
Объем микстуры после растворения лекарственных веществ увеличился на 1,44 мл (Приложение 9), что укладывается в норму допустимого отклонения (+/- 2%) и при ее контроле не учитывается.
Пример 22. Rp.: Infusi herbae Leonuri 200 ml
Analgini 5,0
Kalii bromidi
Natrii bromidi ana 4,0
Tincturae Valerianae 6 ml
Изменение объема при растворении анальгина, калия бромида и натрия бромида составляет 5,5 мл (5 x 0,68 + 4 x 0,27 + 4 x 0,26), не укладывается в норму допустимого отклонения. Суммарная концентрация растворенных веществ более 3%. Поэтому объем воды, который необходимо взять для изготовления настоя, рассчитывают с учетом коэффициента водопоглощения травы пустырника и изменения объема микстуры при растворении твердых веществ.
Для изготовления настоя 20 г измельченной травы пустырника заливают 234,5 мл воды очищенной (200 + 20 x 2 — 5,5), настаивают по общим правилам технологии и фильтруют. В полученном водном извлечении растворяют лекарственные вещества и вновь фильтруют.
Измеряют объем фильтрата, при необходимости доводят его водой очищенной до 200 мл и добавляют 6 мл настойки валерианы.
Общий объем изготовленной микстуры равен 206 мл.
2.8.4. Изготовление водных извлечений
из экстрактов (концентратов)
Экстракты (концентраты) — стандартизованные сухие (1:1) и жидкие (1:2) вводят в состав жидких лекарственных форм по правилам растворения твердых лекарственных средств (пункт 2.8.3) и введения галеновых и новогаленовых лекарственных средств (пункт 2.1).
2.8.5. Изготовление водных извлечений при совместном
использовании лекарственного растительного сырья
и экстрактов (концентратов)
см. Пример 20.
Микстуру изготавливают, используя экстракт алтея сухой (1:1), экстракты (концентраты) валерианы и пустырника жидкие (1:2) и лекарственное растительное сырье (листья мать-и-мачехи и кору калины).
Учитывая, что жидкого экстракта валерианы следует взять 16 мл, а жидкого экстракта пустырника — 40 мл, водное извлечение из сырья должно быть изготовлено в объеме 944 мл.
Для обеспечения раздельной экстракции объемы извлечений устанавливают пропорционально выписанной массе сырья: из 25 г коры калины изготавливают 524 мл отвара; из 20 г листьев мать-и-мачехи — 420 мл настоя.
Объем воды очищенной для изготовления отвара коры калины составит 574 мл (524 + 25 x 2); для изготовления настоя листьев мать-и-мачехи — 480 мл (420 + 20 x 3).
Режимы экстракции регламентируются действующей ГФ.
После объединения изготовленных водных извлечений в них растворяют 10 г экстракта алтея сухого (изменение объема укладывается в норму допустимого отклонения), фильтруют во флакон для отпуска, добавляют 16 мл экстракта валерианы и 40 мл экстракта пустырника.
Общий объем микстуры составляет 1000 мл (524 + 420 + 16 + 40).
2.8.6. Лекарственные формы, содержащие водные
извлечения из лекарственного растительного сырья,
экстрактов (концентратов) и твердые растворимые
лекарственные вещества
см. Пример 21.
Учитывая то, что при изготовлении лекарственной формы может быть использован жидкий экстракт (концентрат) валерианы (1:2) — 20 мл, из 4 г листьев мяты изготавливают 180 мл настоя по общим правилам ГФ.
Объем воды очищенной для изготовления водного извлечения из листьев мяты составит 189,6 мл (180 + 4 x 2,4).
В изготовленном настое растворяют твердые лекарственные вещества и после фильтрования непосредственно во флакон для отпуска отмеривают 20 мл жидкого экстракта валерианы.
При изготовлении водных извлечений из экстрактов (концентратов) могут быть использованы концентрированные растворы лекарственных веществ.
см. Пример 22.
При изготовлении лекарственной формы с использованием концентрированных растворов следует учесть изменение объема при растворении анальгина, концентрированный раствор которого отсутствует.
Максимальная концентрация анальгина, при которой изменение объема укладывается в норму допустимого отклонения, составляет 1,47%, а концентрация анальгина в прописи — 2,43%.
В подставку отмеривают 116,6 мл воды очищенной (120 — 5 x x 0,68) и растворяют 5 г анальгина. Раствор фильтруют во флакон для отпуска и добавляют 20 мл 20% раствора калия бромида, 20 мл 20% раствора натрия бромида, 40 мл экстракта (концентрата) пустырника жидкого (1:2) и 6 мл настойки валерианы.
Общий объем микстуры — 206 мл.
2.9. Некоторые особенности изготовления суспензий
и эмульсий
Суспензии и эмульсии для внутреннего, наружного и парентерального применения изготавливают в соответствии с требованиями действующей ГФ.
Суспензии с содержанием нерастворимых твердых лекарственных веществ 3% и более, а также эмульсии независимо от концентрации веществ изготавливают по массе, концентрированные растворы водорастворимых лекарственных веществ при изготовлении суспензий не используют.
Пример 23. Rp.: Zinci oxydi
Talci ana 20,0
Glycerini 30,0
Aquae purificatae 100 ml
Во флакон для отпуска известной массы предварительно отвешивают 30 г глицерина. В ступке измельчают цинка окись, добавляют тальк и около 20 г глицерина из флакона для отпуска. Смесь тщательно перемешивают и постепенно, небольшими порциями, добавляют воду очищенную, смывая суспензию во флакон для отпуска.
Масса суспензии — 170 г.
Пример 24. Rp.: Sulfuris praecipitati 7,0
Acidi salicylici 2,0
Glycerini 5,0
Streptocidi albi 3,0
Camphorae 3,5
Spiritus aethylici 50 ml
Solutionis Acidi borici 3% - 50 ml
В ступке измельчают 3 г стрептоцида, 7 г серы с 5 г глицерина, добавляют 12,5 мл воды очищенной и смесь перемешивают. К смеси частями добавляют 37,5 мл 4% раствора кислоты борной (1,5 г), смывая содержимое ступки во флакон для отпуска известной массы. В последнюю очередь добавляют предварительно изготовленный раствор кислоты салициловой и камфоры в 50 мл 90% спирта, содержимое флакона перемешивают и тщательно укупоривают.
Масса суспензии составляет 112,41 г, т.к. масса 50 мл 90% спирта — 41,46 г (плотность — 0,829 г/мл); масса 37,5 мл 4% раствора кислоты борной — 37,95 г (плотность — 1,010 г/мл).
Состав и изготовление эмульсии бензилбензоата см. Приложение 15.
3. КОНЦЕНТРИРОВАННЫЕ РАСТВОРЫ
3.1. Общие положения
Концентрированные растворы (концентраты) — заранее изготовленные растворы лекарственных веществ более высокой концентрации, чем концентрация, в которой эти вещества выписываются в рецептах.
К концентратам относят также концентрированные экстракты из некоторых лекарственных растений, изготовленные на фармацевтических производственных предприятиях: экстракты (концентраты) валерианы, горицвета, пустырника и др.
Концентраты предназначены для быстрого и качественного изготовления жидких лекарственных форм.
Рекомендуется изготавливать концентраты из веществ гигроскопичных, выветривающихся, содержащих значительное количество кристаллизационной воды.
Номенклатура концентрированных растворов определяется спецификой рецептуры и объемом работы аптеки и утверждается в соответствии с требованиями действующей Инструкции.
Концентраты изготавливают по мере необходимости, с учетом срока их годности.
Перечень концентрированных растворов и ряда жидких лекарственных средств, рекомендованных для использования при изготовлении в аптеках жидких лекарственных форм (в том числе применяемых в глазной практике), условия их хранения и сроки годности приведены в Приложениях 4 — 6.
Концентрированные растворы изготавливают массо-объемным методом в мерной посуде в асептических условиях в соответствии с требованиями действующей Инструкции, используя свежеполученную воду очищенную.
В случае отсутствия мерной посуды объем воды очищенной рассчитывают, используя значение плотности концентрата или коэффициент, соответствующий увеличению его объема при растворении 1 г лекарственного вещества (Приложения 7, 9).
Изготовленные растворы фильтруют, подвергают полному химическому контролю и проверяют на отсутствие механических включений.
При изготовлении концентрированных растворов следует избегать концентраций, близких к насыщенным, т.к. при понижении температуры возможна кристаллизация растворенного вещества.
Отклонение в концентрации растворов допускается в пределах:
— до 20% концентрации раствора (включительно) — не более +-2%;
— более 20% концентрации раствора — не более +-1%.
Например, для 10% от 9,8% до 10,2%,
20% от 19,6% до 20,4%,
50% от 49,5% до 50,5%.
В случае превышения нормы допустимого отклонения производят исправление концентрации раствора (см. п. 3.3).
Емкости с концентрированными растворами оформляют этикетками с указанием наименования и концентрации раствора, номера серии и анализа, даты изготовления, срока годности.
Концентрированные растворы хранят в соответствии с физико — химическими свойствами лекарственных веществ, входящих в их состав, в простерилизованных, плотно укупоренных емкостях (баллонах, штангласах), в защищенном от света месте, при температуре 3 — 5° C или не выше 25° C (Приложения 4 — 6).
Изменение цвета, помутнение, появление хлопьев, налетов ранее установленного срока годности являются признаками непригодности растворов.
3.2. Расчеты при изготовлении концентрированных растворов
3.2.1. Расчет массы лекарственного вещества
Требуется изготовить 1 л 50% раствора глюкозы.
Для изготовления 1 л 50% раствора необходимо взять 500 г глюкозы. Однако глюкозу следует брать в большем количестве, с учетом содержания в ней 10% влаги.
Расчет производят по формуле:
а x 100
X = ---------,
100 - б
где: X - масса глюкозы, необходимая для изготовления
раствора, г;
а - масса безводной глюкозы, требуемая для изготовления
раствора, г;
б - содержание влаги в глюкозе, %.
500 x 100
X = --------- = 555,55 г
100 - 10
555,55 г глюкозы с влажностью 10% помещают в мерную емкость и растворяют в части горячей воды при перемешивании. После охлаждения объем раствора доводят водой очищенной до 1 л и фильтруют.
3.2.2. Расчет объема воды с использованием значения
плотности раствора или КУО
Требуется изготовить 1 л 50% раствора кальция хлорида.
Плотность 50% раствора кальция хлорида 1,207 г/мл, и 1 л этого раствора имеет массу 1207 г (1000 x 1,207).
Масса кальция хлорида для изготовления 1 л раствора — 500 г, следовательно, масса воды составит 707 г (1207 — 500) или 707 мл при плотности воды очищенной 1 г/мл.
КУО для кальция хлорида — 0,58 мл/г. При растворении 500 г этого вещества объем раствора увеличивается на 290 мл (500 x x 0,58). Поэтому для изготовления 1 л 50% раствора кальция хлорида следует взять 710 мл воды очищенной (1000 — 290).
3.3. Исправление концентрации растворов
3.3.1. Концентрация раствора оказалась выше требуемой.
Объем воды, необходимый для разбавления полученного раствора, вычисляют по формуле:
A x (C - B)
X = -------------,
B
где X — объем воды, необходимый для разбавления полученного раствора, мл;
A — объем изготовленного раствора, мл;
C — фактическая концентрация раствора, % ;
B — требуемая концентрация раствора, %.
Например, при анализе установлено, что концентрация раствора калия бромида 23% вместо 20%.
1000 x (23 - 20)
Отсюда: X = ---------------- = 150 мл,
20
т.е. к 1 л 23% раствора калия бромида следует добавить 150 мл воды очищенной для получения 20% раствора.
После исправления концентрации общий объем раствора будет равен 1150 мл.
3.3.2. Концентрация раствора оказалась ниже требуемой
Массу лекарственного вещества для укрепления полученного раствора вычисляют по формуле:
A x (B - C)
X = -------------,
100 x p - B
где: X — масса вещества, которую следует добавить к раствору, г;
A — объем изготовленного раствора, мл;
B — требуемая концентрация раствора, %;
C — фактическая концентрация раствора, %;
p — плотность раствора при 20° C, г/мл.
Например, при анализе установлено, что концентрация раствора калия бромида составляет 18% вместо 20%.
1000 x (20 - 18)
Отсюда: X = ---------------- = 21,19 г
100 x 1,144 - 20
После растворения 21,19 г калия бромида объем раствора увеличился на 5,7 мл (КУО — 0,27 мл/г) и стал равен 1005,7 мл.
В случае укрепления растворов глюкозы расчеты проводят с учетом % влажности.
Концентрированные растворы после их разбавления или укрепления следует проанализировать повторно.
4. АПТЕЧНЫЕ БЮРЕТОЧНЫЕ УСТАНОВКИ И МЕРНАЯ ПОСУДА
При изготовлении жидких лекарственных форм массо-объемным методом используют мерную посуду, градуированную на «налив» (мерные колбы, цилиндры, мензурки, градуированные пробирки) и на «вылив» (аптечные бюретки, каплемеры и пипетки) и откалиброванную в соответствии с ГОСТом.
4.1. Общие правила работы с аптечными бюретками и пипетками
В аптеках выделяют фармацевта, контролирующего состояние и правильную эксплуатацию аптечных бюреток, пипеток и каплемеров в соответствии с Положением о ведомственном надзоре за измерительными приборами в системе МЗ РФ, положениями настоящей Инструкции и Инструкции по санитарному режиму аптек.
Перед сборкой все резиновые и стеклянные детали бюреток, пипеток и каплемеров тщательно моют и дезинфицируют в соответствии с требованиями действующей Инструкции.
Аптечные бюретки, пипетки и каплемеры моют по мере надобности, но не реже 1 раза в 10 дней. Для этого их освобождают от жидкостей, моют горячей водой (50 — 60° C), взвесью горчичного порошка или 3% раствором водорода перекиси с добавлением 0,5% моющих, дезинфицирующих и моюще-дезинфицирующих средств, разрешенных для применения в аптечной практике; промывают водой водопроводной и очищенной, с обязательным контролем на полноту смывания моющих средств (в соответствии с нормативной документацией).
Перед началом работы сливные краны, концы бюреток и пипеток очищают от налета солей, настоек, экстрактов и протирают спирто-эфирной смесью (1:1).
Заполняют питающие сосуды в бюреточной установке концентрированными растворами, настойками, экстрактами (концентратами), предназначенными для изготовления водных извлечений. Проверяют правильность их заполнения путем качественного химического анализа в соответствии с требованиями действующей Инструкции.
Малые объемы жидкостей отмеривают бюретками и пипетками с малым диаметром.
Уровень бесцветных жидкостей в бюретках и пипетках устанавливают по нижнему мениску, окрашенных — по верхнему.
Слив жидкостей из пипеток и бюреток производят полностью, после полного стекания жидкости выжидают еще 2 — 3 секунды.
Отмеривание жидкости по разности делений не допускается. Вязкие и летучие жидкости не отмеривают по объему во избежание большой ошибки дозирования.
Не разрешается использовать бюретки, пипетки и каплемеры с отломанными концами, а также с плохо смачивающейся внутренней поверхностью стенок.
Малые количества жидких лекарственных средств (менее 1 мл или 1 г) дозируют каплями. При отсутствии стандартного каплемера (ГФ) последний может быть заменен эмпирическим каплемером — пипеткой, откалиброванной путем пятикратного взвешивания 20 капель соответствующего жидкого лекарственного средства.
На этикетке штангласа (флакона) с прикрепленным каплемером следует указать наименование лекарственного средства, число капель в 1 мл или 1 г и соответствие 1 капли стандартного каплемера числу капель нестандартного.
4.2. Аптечные пипетки
Аптечные пипетки предназначены для отмеривания небольших объемов жидкости — от 1 до 15 мл.
Выпускаются вместимостью 3, 6, 10 и 15 мл.
Штангласы к ним — 100 и 250 мл и резиновые баллончики — 7,5; 15 и 30 мл.
Таблица 2
┌────────────────────────────────────────────────────────────────┐ │ Соотношения вместимости (мл) пипетки, емкости баллончика │ │ и штангласа │ ├──────────────────────────┬───────┬────────┬───────┬────────────┤ │Аптечная пипетка │ 15 │ 10 │ 6 │ 3 │ ├──────────────────────────┼───────┼────────┼───────┼────────────┤ │Баллончик │ 30 │ 30 │ 15 │ 7,5 │ ├──────────────────────────┼───────┼────────┼───────┼────────────┤ │Штанглас │ 250 │ 250 │ 100 │ 100 │ └──────────────────────────┴───────┴────────┴───────┴────────────┘
Устройство аптечной пипетки
Пипетка состоит из:
— стеклянной градуированной трубки, суженной книзу;
— стеклянного шара с двумя тубусами (верхним и боковым);
— резинового баллончика, надетого на верхний тубус стеклянного шара;
— резиновой трубки с бусинкой или пробкой, надетой на боковой тубус.
Пипетка крепится в горловине штангласа с помощью прокладки (резинового кольца) и не должна доходить до дна штангласа на 3 — 5 мм.
Для наполнения пипетку слегка приподнимают над штангласом и сжимают резиновый баллончик.
Не допускается попадание жидкости в баллончик во избежание загрязнения.
Для установления мениска на необходимом уровне пользуются боковым тубусом, нажимая резиновую трубку у бусинки.
Жидкость из пипетки выливают сплошной струей, сжимая резиновый баллончик, опустив кончик пипетки в горлышко флакона для отпуска.
4.3. Аптечные бюретки с 2-ходовым краном и бюреточные
установки с механическим приводом
Аптечные бюретки выпускаются вместимостью 10, 25, 60, 100, 200 мл.
Бюретки монтируются на специальных установках — вертушках (на 20, 16 и 8 бюреток) или на специальных штативах.
При сборке и эксплуатации бюреточных установок следует руководствоваться инструкцией, прилагаемой к ним.
Высота всех бюреток независимо от вместимости — 450 мм при соответственно различном диаметре (12 — 32 мм), в этом случае середина шкалы бюреток, смонтированных на вертушке, находится на уровне глаз фармацевта, работающего сидя, что позволяет уменьшить ошибку при дозировании.
Жидкие лекарственные средства отмеривают, контролируя требуемый объем визуально по шкале бюретки.
4.3.1. Бюретки с 2-ходовым краном выпускаются в 4 наборах. Комплекты N 1 — 3 могут быть использованы для фасовки жидкостей. Набор N 4 используется для дозирования воды.
Бюретки с 2-ходовым краном монтируются на специальном штативе и через питающую трубку соединяются с питающим сосудом. Нулевая отметка бюретки находится на уровне крана. Проходные отверстия в штоке крана расположены под углом 90° C.
Открытую верхнюю часть бюретки закрывают стеклянным колпачком, а баллон с водой — стеклянной пробкой.
Для наполнения бюретки 2-ходовой кран ставят в положение наполнения бюретки (окрашенным концом ручки крана вверх). Для слива отмеренного объема жидкости кран переводят в положение слива из бюретки (окрашенным концом ручки крана вниз).
Если жидкость подтекает через закрытый кран бюретки, следует произвести его шлифовку.
Материалом для шлифовки служат: очень тонкий наждак (грубый наждак может дать царапины), цинка оксид, тонко размолотый алюминия оксид.
Перед шлифовкой пробку крана и муфту очищают, смачивая водой или 10% раствором камфоры в скипидаре и покрывают одним из указанных порошков для шлифовки. Пробку крана вставляют в муфту и быстро вращают то в одну, то в другую сторону, вынимая и снова вставляя. При остановке вращения пробку из муфты обязательно вынимают.
Хорошо притертый шлиф не мутный, а почти прозрачный.
Для кранов используют летнюю и зимнюю смазки следующего состава (в частях):
┌─────┬─────────────────────┬────────────────────────────────────┐ │ N │ Компоненты │ Соотношения компонентов для смазки │ │ п/п │ смазки ├─────────────────┬──────────────────┤ │ │ │ летней │ зимней │ ├─────┼─────────────────────┼─────────────────┼──────────────────┤ │ 1. │ Парафин (церезин) │ 1 │ 1 │ │ │ Вазелин │ 1 │ 2 │ ├─────┼─────────────────────┼─────────────────┼──────────────────┤ │ 2. │ Ланолин безводный │ 3 │ 5 │ │ │ Вазелин │ 1 │ 3 │ └─────┴─────────────────────┴─────────────────┴──────────────────┘
Смазку изготавливают, сплавляя составные части в выпарительной чашке на водяной бане, процеживают через двойной слой марли в банку с плотно навинчивающейся крышкой.
4.3.2. Бюреточная установка с механическим приводом
Установка состоит из металлической вертушки на опорной стойке в виде треноги. По окружности вертушки размещено 16 полиэтиленовых питающих сосудов вместимостью 1 л, стеклянных соединительных трубок и градуированных бюреток.
Каждая бюретка и питающая трубка крепятся в гнездах соответствующего крана с помощью резиновых уплотнительных колечек (втулок) и резьбовых колпачков (штуцеров). Каждый кран имеет два диафрагменных клапана — заполняющий и сливной.
Клапанами управляют с помощью двух механических тросиковых приводов с пружинными захватами, нажимая на клавиши «наполнение» или «слив», смонтированные на основании треноги вертушки.
Бюреточную установку на рабочем месте располагают таким образом, чтобы клавиши управления располагались справа.
При работе вертушку поворачивают и фиксируют с помощью специального фиксатора так, чтобы штоки клапанов диафрагменного крана соответствующей бюретки расположились напротив пружинных захватов рычажно-тросиковых приводов.
При нажатии на клавишу «наполнение» один из пружинных захватов оттягивает шток клапана наполнения. Шток оттягивает диафрагму, открывая сообщение между бюреткой и питающей трубкой. Бюретка заполняется жидкостью до необходимого объема.
При нажатии на клавишу «слив» другой пружинный захват тросикового привода оттягивает шток диафрагмы сливного клапана. Диафрагма оттягивается. Жидкость сливается во флакон.
Диафрагма клапана наполнения в это время плотно закрывает сообщение бюретки с питающей трубкой.
Перед эксплуатацией бюреточную установку вытирают от пыли и антикоррозийного покрытия, проверяют работу фиксатора. Вертушка должна двигаться плавно и хорошо фиксироваться при попадании шарика в отверстие. При необходимости регулирования используют гайку фиксатора.
Проверяют работу системы управления кранами. Винты на кранах при вращении вертушки должны свободно проходить через скобы пружинных захватов системы управления. В фиксированном положении между винтами и скобами должен быть просвет 1 — 3 мм.
В зафиксированном положении винты кранов должны останавливаться строго против соответствующих скоб пружинного захвата системы управления. Нарушение совпадения оси винта крана с осью скобы захвата регулируют с помощью болта закрепления кронштейна.
Открытие кранов производится при помощи тросиков, натяжением ручек управления. В рабочем режиме тросик должен находиться в натянутом положении и плавно двигаться в блоках при нажатии ручки управления. Необходимая степень натяжения тросика регулируется с помощью специального винта и гайки.
Если перемещение ручки системы управления до конца не обеспечивает полного открытия крана, о чем свидетельствует медленное наполнение бюретки и выливание жидкости из крана, необходимо завинтить опорную планку или дополнительно натянуть тросик.
Для надежной работы бюреточной установки и ее длительной эксплуатации необходимо периодически при сборке бюреточной установки после мойки закапывать вазелиновое масло на концы штоков клапанов кранов, куда ввернуты винты с полиэтиленовыми головками. При выполнении этой операции следует нажимать на клавиши механического привода для того, чтобы концы штоков вышли из отверстий корпуса крана. Смазка предохраняет штоки от коррозии и кристаллизации остатков лекарственных средств на концах штоков.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌─────────────────────────────────┬──────────────────────────────┐ │ Наименование │ Плотность г/куб. см (г/мл) │ ├─────────────────────────────────┼──────────────────────────────┤ │Бензилбензоат │ 1,048 │ │Валидол │ 0,894 - 0,907 │ │Винилин (Бальзам Шостаковского) │ 0,903 - 0,921 │ │Глицерин │ 1,223 - 1,233 │ │Деготь березовый │ 0,925 - 0,950 │ │Димексид │ 1,101 │ │Жидкость Бурова │ 1,036 - 1,040 │ │Кислота хлористоводородная │ 1,038 - 1,039 │ │разведенная (8,2% - 8,4%) │ │ │Кислота хлористоводородная │ 1,122 - 1,124 │ │(24,8 - 25,2%) │ │ │Кислота уксусная разведенная │ 1,038 - 1,039 │ │(29,5 - 30,5%) │ │ │Кислота уксусная (98%) │ 1,055 │ │Масло вазелиновое │ 0,875 - 0,890 │ │Масло касторовое │ 0,948 - 0,968 │ │Масло миндальное │ 0,913 - 0,918 │ │Масло мяты перечной │ 0,900 - 0,910 │ │Масло персиковое │ 0,914 - 0,920 │ │Масло подсолнечное │ 0,920 - 0,930 │ │Масло терпентинное очищенное │ │ │(скипидар) │ 0,855 - 0,863 │ │Масло эвкалиптовое │ 0,910 - 0,930 │ │Метилсалицилат │ 1,178 - 1,185 │ │Настойка валерианы │ 0,920 │ │Настойка зверобоя │ 0,970 │ │Настойка ландыша │ 0,910 │ │Настойка мяты перечной │ 0,858 │ │Настойка полыни │ 0,910 │ │Настойка пустырника │ 0,910 │ │Настойка эвкалипта │ 0,910 │ │Нашатырно-анисовые капли │ 0,875 │ │Пергидроль (27,5 - 30,0%) │ 1,096 - 1,105 │ │Полиэтиленгликоль - 400 │ │ │(полиэтиленоксид - 400) │ 1,125 │ │Раствор аммиака (9,5 - 10,5%) │ 0,956 - 0,959 │ │Раствор ацетата свинца основного │ 1,223 - 1,228 │ │Рыбий жир тресковый │ 0,917 - 0,927 │ │Сироп сахарный │ 1,301 - 1,313 │ │Сироп алтейный │ 1,322 - 1,327 │ │Спирт камфорный 10% │ 0,884 - 0,888 │ │Спирт этиловый 40% │ 0,949 - 0,951 │ │Спирт этиловый 70% │ 0,885 - 0,887 │ │Спирт этиловый 90% │ 0,827 - 0,831 │ │Спирт этиловый 95% │ 0,809 - 0,813 │ │Формалин (36,5 - 37,5%) │ 1,078 - 1,093 │ │Хлороформ │ 1,474 - 1,483 │ │Эфир медицинский │ 0,714 - 0,717 │ └─────────────────────────────────┴──────────────────────────────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───────────────────┬────────────────────────────────────────────┐ │ Плотность │ Концентрация, % │ │ г/куб. см ├─────────────────────┬──────────────────────┤ │ │ по массе │ массо-объемная │ ├───────────────────┼─────────────────────┼──────────────────────┤ │ 1,096 │ 27,5 │ 29,18 │ │ 1,098 │ 28 │ 30,72 │ │ 1,101 │ 29 │ 31,94 │ │ 1,105 │ 30 │ 33,15 │ │ 1,109 │ 31 │ 34,36 │ │ 1,112 │ 32 │ 35,59 │ │ 1,116 │ 33 │ 36,82 │ │ 1,119 │ 34 │ 38,05 │ │ 1,123 │ 35 │ 39,29 │ │ 1,126 │ 36 │ 40,55 │ │ 1,130 │ 37 │ 41,81 │ │ 1,134 │ 38 │ 43,07 │ │ 1,137 │ 39 │ 44,34 │ │ 1,141 │ 40 │ 45,62 │ └───────────────────┴─────────────────────┴──────────────────────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌────────────────────┬──────────────────────────┬────────────────┐ │ Спиртовые │ Состав │ Нормативная │ │ растворы │ │ документация │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Бриллиантового │ Бриллиантового зеленого │ФС 42-1459-89 │ │ зеленого 1% и 2% │ (ГФ Х, ст. 733 или │ │ │ │ ТУ 6-09-4278-76) │ │ │ │ 1 г или 2 г │ │ │ │ Спирта этилового 60% │ │ │ │ (ГОСТ 5962-67) до 100 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Йода 1% и 2% │ Йода (ГФ Х, ст. 354) │ФС 42-2295-92 │ │ │ 10 г или 20 г │ │ │ │ Спирта этилового 96% │ │ │ │ (ГОСТ 5962-67, ГФ Х, │ │ │ │ ст. 631) │ │ │ │ до 1000 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Йода 5% │ Йода 50 г │ГФ Х, ст. 355 │ │ │ Калия иодида 20 г │ │ │ │ Воды очищенной │ │ │ │ (ФС 42-2689-97) <*> │ │ │ │ Спирта этилового 95% │ │ │ │ (ФС 42-3071-94) │ │ │ │ поровну до 1000 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Кислоты борной │ Кислоты борной (ГФ Х, │ФС 42-1512-92 │ │ 0,5%, 1%, 2%, 3% │ ст. 10; ГОСТ 18704-78, │ │ │ │ марка Б) 5 г, 10 г, │ │ │ │ 20 г или 30 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 1000 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Кислоты салициловой│ Кислоты салициловой │ФС 42-2215-84 │ │ 1% и 2% │ (ГФ Х, ст. 21) 10 г или │ │ │ │ 20 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 1000 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Кислоты салициловой│ Кислоты салициловой │ВФС 42-917-79 │ │ Левомицетина │ (ГФ Х, ст. 21) 2 г │ │ │ поровну по 2% │ Левомицетина │ │ │ │ (ГФ Х, ст. 371) 2 г │ │ │ │ Спирта этилового 95% │ │ │ │ (ФС 42-3072-94) │ │ │ │ до 100 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Левомицетина │ Левомицетина (ГФ Х, │ФС 42-2366-85 │ │ 0,25%, 1%, 3%, │ ст. 371) │ │ │ 5% │ 0,25; 1 г; 3 г или 5 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 100 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Левомицетина 2% │ Левомицетина │ВФС 42-920-79 │ │ Новокаина 1% │ (ГФ Х, ст. 371) 2 г │ │ │ │ Новокаина │ │ │ │ (ФС 42-2709-90) │ │ │ │ (ГФ Х, ст. 467) 1 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 100 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Меновазин │ Ментола рацемического │ФС 42-1738-93 │ │ │ (ФС 42-1866-90) 2,5 г │ │ │ │ Новокаина │ │ │ │ (ФС 42-2709-90) 1 г │ │ │ │ Анестезина │ │ │ │ (ГФ Х, ст. 55) 1 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 100 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Ментола 1% и 2% │ Ментола (ГФ Х, ст. 387) │ФС 42-2294-85 │ │ │ или │ │ │ │ Ментола рацемического │ │ │ │ (ФС 42-1866-90) │ │ │ │ 10 или 20 г │ │ │ │ Спирта этилового 90% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 1000 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Метиленового │ Метиленового синего │ФС 42-1525-80 │ │ синего 1% │ (ГФ Х, ст. 407) 10 г │ │ │ │ Спирта этилового 95% │ │ │ │ (ФС 42-3072-94) 600 мл │ │ │ │ Воды очищенной │ │ │ │ (ФС 42-2619-97) 400 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Новокаина 2% │ Новокаина │ВФС 42-884-79 │ │ Кислоты борной 3% │ (ФС 42-2709-90) 2 г │ │ │ │ Кислоты борной │ │ │ │ (ГФ Х, ст. 10) 3 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 100 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Водорода перекиси │ Раствора водорода пере- │ФС 42-278-72 │ │ 1,5% │ киси (ГФ 1Х, ст. 621) │ │ │ │ 50 мл │ │ │ │ Спирта этилового 95% │ │ │ │ (ФС 42-3072-94) 50 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Резорцина 1% и 2% │ Резорцина (ГФ Х, ст. │ФС 42-2048-93 │ │ │ 577) 10 г или 20 г │ │ │ │ Натрия пиросернистокис- │ │ │ │ лого (метабисульфита │ │ │ │ натрия) (ГОСТ 10575-76 │ │ │ │ или ГОСТ 11683-76, │ │ │ │ сорт 1) 1 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 1000 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Танина 4% │ Танина (ГФ Х, ст. 658) │ФС 42-1965-83 │ │ │ 40 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 1000 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Фурацилина 1:1500 │ Фурацилина (ГФ Х, │ФС 42-2087-83 │ │ │ ст. 295) 1 г │ │ │ │ Спирта этилового 70% │ │ │ │ (ФС 42-3071-94) │ │ │ │ до 1500 мл │ │ ├────────────────────┼──────────────────────────┼────────────────┤ │ Цитраля 1% │ Цитраля (ТУ 18-16-6-81) │ФС 42-2005-83 │ │ │ 1 г │ │ │ │ Спирта этилового 96% │ │ │ │ (ГФ Х, ст. 631; │ │ │ │ ГОСТ 5962-67) │ │ │ │ до 100 мл │ │ └────────────────────┴──────────────────────────┴────────────────┘
———————————
<*> Здесь и далее указана новая нормативная документация.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───────────────────────────┬──────────────────┬─────────────────┐ │ Наименование │ Концентрация, │ Срок годности │ │ │ % │ (сутки) при t° │ │ │ │ хранения │ │ │ ├──────────┬──────┤ │ │ │ не выше │3 - 5°│ │ │ │ 25° C │ C │ ├───────────────────────────┼──────────────────┼──────────┼──────┤ │ Адонизид <*> │ - │ - │ - │ │ Аммония хлорид │ 20 │ 15 │ │ │ Барбитал-натрия │ 10 │ 10 │ │ │ Гексаметилентетрамин <*> │ 10, 20, 40 │ 20 │ │ │ Глюкоза безводная │ 5 │ 2 │ │ │ -"- │ 10, 20, 40, 50 │ 4 │ 10 │ │ Калия бромид <*> │ 20 │ 20 │ │ │ Калия иодид <*> │ 20 │ 15 │ │ │ Кальция хлорид │ 5, 10, 20 │ 10 │ │ │ -"- │ 50 │ 30 │ │ │ Кислота аскорбиновая <*> │ 5 │ 5 │ │ │ Кислота хлористоводород- │ │ │ │ │ ная │ 10 (1:10) │ 30 │ │ │ Кофеина-натрия бензоат │ 5 │ 7 │ 15 │ │ -"- │ 20 │ 20 │ │ │ Магния сульфат │ 10, 25, 50 │ 15 │ │ │ Натрия бензоат │ 10 │ 20 │ │ │ Натрия бромид <*> │ 20 │ 20 │ │ │ Натрия гидрокарбонат │ 5 │ 4 │ 10 │ │ Натрия салицилат <*> │ 40 │ 20 │ │ │ Настойка валерианы <*> │ - │ │ │ │ Настойка красавки <*> │ - │ │ │ │ Настойка ландыша <*> │ - │ │ │ │ Настойка ландыша и │ │ │ │ │ валерианы поровну <*> │ - │ │ │ │ Хлоралгидрат <*> │ 10 │ 5 │ │ │ -"- <*> │ 20 │ 15 │ │ │ Экстракт (концентрат) │ │ │ │ │ валерианы <*> │ 1:2 │ │ │ │ Экстракт (концентрат) │ │ │ │ │ горицвета <*> │ 1:2 │ │ │ │ Экстракт (концентрат) │ │ │ │ │ пустырника <*> │ 1:2 │ │ │ │ Вода очищенная │ │ 3 │ │ │ Вода мятная │ │ 15, 30 │ │ │ │ │(см. При- │ │ │ │ │ ложе- │ │ │ │ │ ние 10) │ │ │ Вода укропная │ │ 30 │ │ └───────────────────────────┴──────────────────┴──────────┴──────┘
———————————
<*> Хранить в защищенном от света месте.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───────────────────────────────────┬────────────────────────────┐ │ Наименование │ Концентрация │ ├───────────────────────────────────┼────────────────────────────┤ │Кордиамин │ │ │Раствор адреналина гидрохлорида │ 1:1000 │ │Раствор фурацилина │ 1:5000 │ │Раствор этакридина лактата │ 1:500, 1:1000 │ │Раствор цитраля спиртовой │ 1:100 │ │Настойка мяты перечной │ │ │Настойка полыни │ │ │Настойка пустырника │ │ │Нашатырно-анисовые капли │ │ │Экстракт боярышника жидкий │ │ └───────────────────────────────────┴────────────────────────────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───┬────────────────┬──────────────┬───────────────┬───────────────────┐ │ N │ Наименование, │Сроки годности│ Режим │ Условия │ │п/п│ состав │ в сутках при │ стерилизации │ изготовления, │ │ │ │ температуре │ (объемы │ хранения и │ │ │ │ не менее │ до 100 мл) │ применения │ │ │ ├─────┬────────┤ │ │ │ │ │25° C│3 - 5° C│ │ │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │1. │Раствор калия │ 30 │ │120° C - 8 мин.│Хранят в защищен-│ │ │иодида 20% │ │ │ │ном от света месте │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │2. │Растворы кислоты│ 5 │ 30 │ 100° C - │Раствор изготавли-│ │ │аскорбиновой 2, │ │ │ 30 мин. │вают на воде очи-│ │ │5, 10% │ │ │ │щенной свежепроки-│ │ │ │ │ │ │пяченой. При фа- │ │ │ │ │ │ │совке раствора фла-│ │ │ │ │ │ │коны заполняют │ │ │ │ │ │ │доверху. │ │ │ │ │ │ │Хранят в защищен- │ │ │ │ │ │ │ном от света месте │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │3. │Раствор кислоты │ 30 │ │120° C - 8 мин.│ │ │ │борной 4% │ │ │ │ │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │4. │Раствор натрия │ 30 │ │ 100° C - │ │ │ │тиосульфата 1% │ │ │ 30 мин. │ │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │5. │Раствор рибофла-│ 90 │ 30 │120° C - 8 мин.│Хранят в защищен- │ │ │вина 0,02% │ │ │ │ном от света месте │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │6. │Рибофлавина │ 5 │ 30 │ 100° C - │При фасовке раст- │ │ │0,02 г │ │ │ 30 мин. │вора флакон запол- │ │ │Кислоты аскорби-│ │ │ │няют доверху. │ │ │новой 2 г или │ │ │ │Хранят в защищен- │ │ │10 г │ │ │ │ном от света месте │ │ │Воды очищенной │ │ │ │ │ │ │свежепрокипяче- │ │ │ │ │ │ │ной до 100 мл │ │ │ │ │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │7. │Рибофлавина │ 30 │ │ 100° C - │Хранят в защищен- │ │ │0,02 г │ │ │ 30 мин. │ном от света месте │ │ │Кислоты борной │ │ │ │ │ │ │4 г │ │ │ │ │ │ │Воды очищенной │ │ │ │ │ │ │до 100 мл │ │ │ │ │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │8. │Рибофлавина │ 30 │ │ 100° C - │Хранят в защищен- │ │ │0,02 г │ │ │ 30 мин. │ном от света месте │ │ │Кислоты никоти- │ │ │ │ │ │ │новой 0,1 г │ │ │ │ │ │ │Воды очищенной │ │ │ │ │ │ │до 100 мл │ │ │ │ │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │9. │Растворы цинка │ 30 │ │120° C - 8 мин.│Хранят в защищен- │ │ │сульфата 1 или │ │ │ │ном от света месте │ │ │2% │ │ │ │ │ ├───┼────────────────┼─────┼────────┼───────────────┼───────────────────┤ │10.│Раствор цитраля │ 2 │ │ │Изготавливают в │ │ │0,02% │ │ │ │асептических усло- │ │ │ │ │ │ │виях на стерильной │ │ │ │ │ │ │очищенной воде. │ │ │ │ │ │ │Хранят в защищенном│ │ │ │ │ │ │от света месте │ └───┴────────────────┴─────┴────────┴───────────────┴───────────────────┘
Примечание. Вскрытые флаконы с концентратами для глазных капель должны быть использованы в течение суток.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌──────────────────────┬───────────┬──────────────┬────────────────┐ │ Наименование │Концен- │ Плотность, │ Количества │ │ │трация, % │ г/мл или ├────────┬───────┤ │ │ │ г/куб. см │лекарст-│воды │ │ │ │ │венного │очищен-│ │ │ │ │вещества│ной │ │ │ │ │(г) │(мл) │ ├──────────────────────┼───────────┼──────────────┼────────┼───────┤ │Аммония хлорид │ 20 │ 1,055 │ 200,0 │ 855 │ │Барбитал натрия │ 10 │ 1,035 │ 100,0 │ 935 │ │Гексаметилентетрамин │ 10 │ 1,021 │ 100,0 │ 921 │ │Гексаметилентетрамин │ 20 │ 1,042 │ 200,0 │ 842 │ │Гексаметилентетрамин │ 40 │ 1,088 │ 400,0 │ 688 │ │Глюкоза (безводная) │ 5 │ 1,018 │ 50,0 │ 968 │ │Глюкоза (безводная) │ 10 │ 1,034 │ 100,0 │ 934 │ │Глюкоза (безводная) │ 20 │ 1,068 │ 200,0 │ 868 │ │Глюкоза (безводная) │ 40 │ 1,150 │ 400,0 │ 749 │ │Глюкоза (безводная) │ 50 │ 1,186 │ 500,0 │ 685 │ │Калия бромид │ 20 │ 1,144 │ 200,0 │ 944 │ │Калия иодид │ 20 │ 1,148 │ 200,0 │ 848 │ │Кальция глюконат │ 10 │ 1,044 │ 100,0 │ 944 │ │Кальция хлорид │ 5 │ 1,020 │ 50,0 │ 970 │ │Кальция хлорид │ 10 │ 1,041 │ 100,0 │ 941 │ │Кальция хлорид │ 20 │ 1,078 │ 200,0 │ 878 │ │Кальция хлорид │ 50 │ 1,207 │ 500,0 │ 707 │ │Кислота аскорбиновая │ 5 │ 1,018 │ 50,0 │ 968 │ │Кислота борная │ 3 │ 1,008 │ 30,0 │ 978 │ │Кислота борная │ 4 │ 1,010 │ 40,0 │ 970 │ │Кофеин-натрия бензоат │ 10 │ 1,034 │ 100,0 │ 934 │ │Кофеин-натрия бензоат │ 20 │ 1,073 │ 200,0 │ 873 │ │Магния сульфат │ 10 │ 1,048 │ 100,0 │ 948 │ │Магния сульфат │ 20 │ 1,093 │ 200,0 │ 893 │ │Магния сульфат │ 25 │ 1,116 │ 250,0 │ 866 │ │Магния сульфат │ 50 │ 1,221 │ 500,0 │ 721 │ │Натрия бензоат │ 10 │ 1,038 │ 100,0 │ 938 │ │Натрия бромид │ 20 │ 1,149 │ 200,0 │ 949 │ │Натрия гидрокарбонат │ 5 │ 1,033 │ 50,0 │ 988 │ │Натрия салицилат │ 10 │ 1,030 │ 100,0 │ 940 │ │Натрия салицилат │ 20 │ 1,083 │ 200,0 │ 883 │ │Натрия салицилат │ 40 │ 1,160 │ 400,0 │ 760 │ │Сульфацил-натрия │ 20 │ 1,072 │ 200,0 │ 872 │ │Сульфацил-натрия │ 30 │ 1,108 │ 300,0 │ 808 │ │Хлоралгидрат │ 20 │ 1,086 │ 200,0 │ 886 │ └──────────────────────┴───────────┴──────────────┴────────┴───────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌──────────────────────────────────┬─────────────────────────────┐ │ Наименование │ Содержание спирта, % │ ├──────────────────────────────────┼─────────────────────────────┤ │ Адонизид │ 20 │ │ Грудной эликсир │ не менее 14 │ │ Настойка аралии │ 70 │ │ -"- боярышника │ 70 │ │ -"- валерианы │ 70 │ │ -"- жень-шеня │ 70 │ │ -"- заманихи │ 70 │ │ -"- зверобоя │ 40 │ │ -"- календулы │ 70 │ │ -"- красавки │ 40 │ │ -"- ландыша │ 70 │ │ -"- лимонника │ 95 │ │ -"- мяты │ 90 │ │ -"- полыни │ 70 │ │ -"- пустырника │ 70 │ │ -"- стручкового перца │ 90 │ │ -"- эвкалипта │ 70 │ │ -"- эвкомии │ 30 │ │ Нашатырно-анисовые капли │ 75 - 80 │ │ Раствор йода 5% │ не менее 46 │ │ -"- цитраля 1% │ 96 │ │ Экстракт жидкий боярышника │ 70 │ │ -"- водяного перца │ 70 │ │ -"- калины │ 50 │ │ -"- крапивы │ 50 │ │ -"- тимиана │ 20 │ │ -"- тысячелистника │ 40 │ │ -"- элеутерококка │ 40 │ │ Экстракты жидкие стандартизован- │ │ │ ные (концентраты) │ 20 - 30 │ └──────────────────────────────────┴─────────────────────────────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───────────────────┬────────┬──────────────────────┬────────────┐ │ Наименование │ Водные │ Спиртовые растворы │ Водные │ │ │растворы├───────┬──────────────┤ суспензии │ │ │ КУО, │ КУО, │ концентрация │ КУО, │ │ │ мл/г │ мл/г │ спирта (%) │ мл/г │ ├───────────────────┼────────┼───────┼──────────────┼────────────┤ │Амизил │ 0,80 │ 0,89 │ 70 │ │ │Аммония хлорид │ 0,72 │ │ │ │ │Анальгин │ 0,68 │ 0,67 │ 30 │ │ │Анестезин │ │ 0,85 │ 70, 90, 96 │ │ │Антипирин │ 0,85 │ 0,88 │ 70 │ │ │Барбамил │ 0,76 │ │ │ │ │Барбитал │ │ 0,77 │ 70 │ │ │Барбитал-натрий │ 0,64 │ │ │ │ │Бензилпенициллина │ │ │ │ │ │натриевая соль │ 0,68 │ │ │ │ │Бромкамфора │ │ 0,80 │ 70 │ │ │Висмута нитрат │ │ │ │ │ │основной │ │ │ │ 0,19 │ │Гексаметилентетра- │ │ │ │ │ │мин │ 0,78 │ 0,79 │ 70, 90 │ │ │Глюкоза (безводная)│ 0,64 │ │ │ │ │-"- (влажность 10%)│ 0,69 │ │ │ │ │Глина белая │ │ │ │ 0,39 │ │Дибазол │ 0,82 │ 0,86 │ 30 │ │ │Дикаин │ 0,86 │ │ │ │ │Димедрол │ 0,86 │ 0,87 │ 70, 90, 96 │ │ │Желатин │ 0,75 │ │ │ │ │Желатоза │ 0,73 │ │ │ │ │Изониазид │ 0,72 │ │ │ │ │Йод │ │ 0,22 │ 70, 90, 96 │ │ │Йод (в растворе │ │ │ │ │ │калия иодида) │ 0,23 │ │ │ │ │Калия бромид │ 0,27 │ 0,36 │ 70 │ │ │-"- йодид │ 0,25 │ │ │ │ │-"- перманганат │ 0,36 │ │ │ │ │-"- хлорид │ 0,37 │ │ │ │ │Кальция глицерофос-│ │ │ │ │ │фат │ │ │ │ 0,46 │ │-"- глюконат │ 0,50 │ │ │ │ │-"- карбонат │ │ │ │ 0,38 │ │-"- лактат │ 0,67 │ │ │ │ │-"- хлорид │ 0,58 │ │ │ │ │Камфора │ │ 1,03 │ 70, 90, 96 │ │ │Карбамид │ 0,73 │ │ │ │ │Кислота аминокапро-│ │ │ │ │ │новая │ 0,79 │ │ │ │ │Кислота аскорбино- │ │ │ │ │ │вая │ 0,61 │ │ │ │ │-"- ацетилсалицило-│ │ │ │ │ │вая │ │ 0,72 │ 90 │ │ │-"- бензойная │ │ 0,87 │ 70, 90, 96 │ │ │-"- борная │ 0,68 │ 0,65 │ 70, 90, 96 │ │ │-"- глютаминовая │ 0,62 │ │ │ │ │-"- лимонная │ 0,62 │ │ │ │ │-"- салициловая │ │ 0,77 │ 70, 90, 96 │ │ │Колларгол │ 0,61 │ │ │ │ │Крахмал │ 0,68 │ │ │ 0,67 │ │Кофеин-бензоат │ │ │ │ │ │натрия │ 0,65 │ │ │ │ │Левомицетин │ │ 0,66 │ 70, 90, 96 │ │ │Магния окись │ │ │ │ 0,34 │ │Магния сульфат │ 0,50 │ │ │ │ │Мезатон │ 0,77 │ │ │ │ │Ментол │ │ 1,10 │ 70, 90, 96 │ │ │Метилурацил │ │ │ │ 0,69 <*> │ │Метилцеллюлоза │ 0,61 │ │ │ │ │Натрия ацетат │ 0,71 │ │ │ │ │ -"- (безводный) │ 0,52 │ │ │ │ │Натрия бензоат │ 0,60 │ │ │ │ │ -"- бромид │ 0,26 │ 0,30 │ 70 │ │ │ -"- гидрокарбонат │ 0,30 │ │ │ │ │ -"- гидроцитрат │ 0,46 │ │ │ │ │ -"- йодид │ 0,38 │ │ │ │ │ -"- нитрат │ 0,38 │ │ │ │ │ -"- нитрит │ 0,37 │ │ │ │ │ -"- нуклеинат │ 0,55 │ │ │ │ │ -"- пара-амино- │ │ │ │ │ │ салицилат │ 0,64 │ │ │ │ │ -"- салицилат │ 0,59 │ │ │ │ │ -"- сульфат │ │ │ │ │ │ (кристалло- │ │ │ │ │ │ гидрат) │ 0,53 │ │ │ │ │ -"- тетраборат │ 0,47 │ │ │ │ │ -"- тиосульфат │ 0,51 │ │ │ │ │ -"- хлорид │ 0,33 │ │ │ │ │ -"- цитрат │ 0,48 │ │ │ │ │Новокаин │ 0,81 │ 0,81 │ 70, 90 │ │ │Новокаинамид │ 0,83 │ │ │ │ │Норсульфазол │ │ │ │ 0,65 │ │Норсульфазол-натрий│ 0,71 │ │ │ │ │Осарсол │ │ │ │ 0,59 │ │Осарсол (в раство- │ │ │ │ │ │ре натрия гидрокар-│ │ │ │ │ │боната) │ 0,67 │ │ │ │ │Папаверина гидро- │ │ │ │ │ │хлорид │ 0,77 │ 0,81 │ 30 │ │ │Пахикарпина гидро- │ │ │ │ │ │йодид │ 0,70 │ │ │ │ │Пепсин │ 0,61 │ │ │ │ │Пилокарпина гидро- │ │ │ │ │ │хлорид │ 0,77 │ │ │ │ │Пиридоксина гидро- │ │ │ │ │ │хлорид │ 0,71 │ │ │ │ │Поливинилпирроли- │ │ │ │ │ │дон │ 0,81 │ │ │ │ │Протаргол │ 0,64 │ │ │ │ │Резорцин │ 0,79 │ 0,77 │ 70, 90, 96 │ │ │Сахароза │ 0,63 │ │ │ │ │Свинца ацетат │ 0,30 │ │ │ │ │Сера │ │ │ │ 0,48 <**>│ │Серебра нитрат │ 0,18 │ │ │ │ │Спазмолитин │ 0,86 │ │ │ │ │Спирт поливиниловый│ 0,77 │ │ │ │ │Стрептомицина суль-│ │ │ │ │ │фат │ 0,58 │ │ │ │ │Стрептоцид │ │ │ │ 0,69 │ │Стрептоцид раство- │ │ │ │ │ │римый │ 0,54 │ │ │ │ │Сульгин │ │ │ │ 0,65 │ │Сульфадимезин │ │ │ │ 0,68 │ │Сульфацил-натрий │ 0,62 │ 0,65 │ 70 │ │ │Тальк │ │ │ │ 0,34 │ │Танин │ 0,65 │ 0,60 │ 70, 90, 96 │ │ │Терпингидрат │ │ 0,77 │ 96 │ │ │Тиамина бромид │ 0,61 │ │ │ │ │Тримекаин │ 0,89 │ │ │ │ │Тимол │ │ 1,01 │ 70, 90, 96 │ │ │Уросульфан │ │ │ │ 0,66 │ │Фенол кристалличес-│ │ │ │ │ │кий │ 0,90 │ │ │ │ │Фетанол │ 0,79 │ │ │ │ │Фталазол │ │ │ │ 0,65 │ │Хинина гидрохлорид │ 0,81 │ │ │ │ │Хлорамин Б │ 0,61 │ │ │ │ │Хлоралгидрат │ 0,76 │ 0,59 │ 70, 90, 96 │ │ │Холина хлорид │ 0,89 │ │ │ │ │Цинка окись │ │ │ │ 0,21 │ │Цинка сульфат │ │ │ │ │ │(кристаллогидрат) │ 0,41 │ │ │ │ │Экстракт (концент- │ │ │ │ │ │рат) горицвета │ │ │ │ │ │сухой стандартизо- │ │ │ │ │ │ванный 1:1 │ 0,60 │ │ │ │ │Экстракт (концент- │ │ │ │ │ │рат) алтея сухой │ │ │ │ │ │стандартизованный │ │ │ │ │ │1:1 │ 0,61 │ 0,61 │ 12 │ │ │Эритромицин │ │ 0,84 │ 70 │ │ │Этазол │ │ │ │ 0,65 │ │Этазол-натрий │ 0,66 │ │ │ │ │Этилморфина гидро- │ │ │ │ │ │хлорид │ 0,76 │ │ │ │ │Эуфиллин │ 0,70 │ 0,71 │ 12 │ │ │Эфедрина гидрохло- │ │ │ │ │ │рид │ 0,84 │ │ │ │ └───────────────────┴────────┴───────┴──────────────┴────────────┘
———————————
<*> Суспензия в 30% спирте.
<**> Суспензия в 70, 90, 96% спирте.
Примечание. КУО — коэффициент увеличения объема (КУО) показывает увеличение объема раствора в мл при растворении 1 г лекарственного или вспомогательного вещества при 20° C (мл/г).
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌─────────┬──────────┬──────────┬──────────┬──────────┬──────────┬──────────┬──────────┬──────────┬──────────┐ │ Концент-│ │ │ │ │ │ │ │ │ │ │ рация │ 30% │ 40% │ 50% │ 60% │ 70% │ 80% │ 90% │ 95% │ 96% │ │ взятого ├────┬─────┼────┬─────┼────┬─────┼────┬─────┼────┬─────┼────┬─────┼────┬─────┼────┬─────┼────┬─────┤ │спирта, %│вода│спирт│вода│спирт│вода│спирт│вода│спирт│вода│спирт│вода│спирт│вода│спирт│вода│спирт│вода│спирт│ ├─────────┼────┼─────┼────┼─────┼────┼─────┼────┼─────┼────┼─────┼────┼─────┼────┼─────┼────┼─────┼────┼─────┤ │ 96,1 │738 │ 262 │646 │ 354 │548 │ 452 │446 │ 554 │336 │ 664 │218 │ 782 │ 88 │ 912 │ 17 │ 983 │ 2 │ 998 │ │ 96,2 │739 │ 261 │646 │ 354 │549 │ 451 │447 │ 553 │337 │ 663 │219 │ 781 │ 90 │ 910 │ 18 │ 982 │ 3 │ 997 │ │ 96,3 │739 │ 261 │647 │ 353 │550 │ 450 │447 │ 553 │338 │ 662 │221 │ 779 │ 91 │ 909 │ 20 │ 980 │ 5 │ 995 │ │ 96,4 │739 │ 261 │647 │ 353 │551 │ 449 │448 │ 552 │339 │ 661 │222 │ 778 │ 93 │ 907 │ 21 │ 979 │ 7 │ 994 │ │ 96,5 │740 │ 260 │648 │ 352 │551 │ 449 │449 │ 551 │340 │ 660 │222 │ 777 │ 94 │ 906 │ 23 │ 977 │ 8 │ 992 │ │ 96,6 │740 │ 260 │648 │ 352 │552 │ 448 │450 │ 550 │341 │ 659 │224 │ 776 │ 96 │ 904 │ 24 │ 976 │ 9 │ 991 │ │ 96,7 │741 │ 259 │649 │ 351 │553 │ 447 │451 │ 549 │342 │ 658 │225 │ 775 │ 97 │ 903 │ 26 │ 974 │ 11 │ 989 │ │ 96,8 │741 │ 259 │650 │ 350 │553 │ 447 │452 │ 548 │343 │ 657 │226 │ 773 │ 98 │ 902 │ 27 │ 973 │ 12 │ 988 │ │ 96,9 │741 │ 259 │650 │ 350 │554 │ 446 │453 │ 547 │344 │ 656 │228 │ 772 │100 │ 900 │ 29 │ 971 │ 14 │ 986 │ └─────────┴────┴─────┴────┴─────┴────┴─────┴────┴─────┴────┴─────┴────┴─────┴────┴─────┴────┴─────┴────┴─────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌─────────┬───────────┬───────────┬───────────┬───────────┬───────────┬───────────┬──────────┬──────────┐ │ Концент-│ │ │ │ │ │ │ │ │ │ рация │ 30% │ 40% │ 50% │ 60% │ 70% │ 80% │ 90% │ 95% │ │ взятого ├─────┬─────┼─────┬─────┼─────┬─────┼─────┬─────┼─────┬─────┼─────┬─────┼────┬─────┼────┬─────┤ │спирта, %│вода │спирт│вода │спирт│вода │спирт│вода │спирт│вода │спирт│вода │спирт│вода│спирт│вода│спирт│ ├─────────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼────┼─────┼────┼─────┤ │ 96,5 │713,1│310,9│615,3│414,5│513,8│518,1│409,1│621,8│301,8│725,4│192,0│829,0│78,2│932,6│18,6│984,5│ │ 96,4 │712,7│311,2│614,8│419,9│513,1│518,7│408,3│622,4│300,9│726,1│190,9│829,9│77,1│933,6│17,3│985,5│ │ 96,3 │712,3│311,5│614,3│415,4│512,5│519,2│407,6│623,1│300,0│726,9│189,9│830,7│75,9│934,6│16,1│986,5│ │ 96,2 │712,0│311,9│613,7│415,8│511,8│519,8│406,8│623,7│299,1│727,7│188,8│831,6│74,7│935,6│14,9│987,5│ │ 96,1 │711,6│312,2│613,2│416,2│511,2│520,3│406,0│624,3│298,2│728,4│187,8│832,5│73,6│936,5│13,6│988,6│ │ 96,0 │711,2│312,5│612,7│416,7│510,5│520,8│405,2│625,0│297,2│729,2│186,8│833,3│72,4│937,5│12,4│989,6│ │ 95,9 │710,8│312,8│612,2│417,1│509,9│521,4│404,4│625,7│296,3│729,9│185,7│834,2│71,2│938,5│11,2│990,6│ │ 95,8 │710,4│313,2│611,7│417,5│509,2│521,9│403,7│626,3│295,4│730,7│184,7│835,1│70,0│939,5│ 9,9│991,6│ │ 95,7 │710,0│313,5│611,1│418,0│508,6│522,5│402,9│627,0│294,5│731,5│183,6│835,9│68,9│940,4│ 8,7│992,7│ │ 95,6 │709,6│313,8│610,6│418,4│507,9│523,0│402,1│627,6│293,6│732,2│182,6│836,8│67,7│941,4│ 7,5│993,7│ │ 95,5 │709,2│314,1│610,1│418,8│507,3│523,6│401,3│628,3│292,7│733,0│181,6│837,7│66,5│942,4│ 6,2│994,8│ │ 95,4 │708,8│314,5│609,6│419,3│506,6│524,1│400,5│628,9│291,8│733,7│180,5│838,6│65,4│943,4│ 5,0│995,8│ │ 95,3 │708,4│314,8│609,1│419,7│506,0│524,7│399,7│629,6│290,9│734,5│179,5│839,5│64,2│944,4│ 3,7│996,8│ │ 95,2 │708,0│315,1│608,5│420,2│505,3│525,2│399,0│630,3│290,0│735,3│178,4│840,3│63,0│945,4│ 2,5│997,9│ │ 95,1 │707,6│315,5│608,0│420,6│504,7│528,8│398,2│630,9│289,0│736,1│177,4│841,2│61,8│946,4│ 1,3│998,9│ └─────────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴────┴─────┴────┴─────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───────────┬────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬──────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼──────┤ │ 95 │4,06│8,11│12,17│16,23│20,29│24,34│32,46│40,57│81,14 │ │ 90 │3,84│7,69│11,53│15,37│19,22│23,06│30,75│38,44│76,87 │ │ 80 │3,42│6,83│10,25│13,66│17,08│20,50│27,33│34,16│68,32 │ │ 70 │2,99│5,98│ 8,97│11,95│14,94│17,93│23,91│29,89│59,77 │ │ 60 │2,56│5,13│ 7,69│10,26│12,82│15,38│20,51│25,64│51,28 │ │ 50 │2,14│4,27│ 6,41│ 8,54│10,68│12,81│17,08│21,35│42,70 │ │ 40 │1,71│3,41│ 5,12│ 6,83│ 8,53│10,24│13,65│17,07│34,13 │ │ 30 │1,28│2,56│ 3,84│ 5,12│ 6,40│ 7,68│10,24│12,30│25,60 │ │ 20 │0,85│1,70│ 2,56│ 3,41│ 4,26│ 5,11│ 6,82│ 8,52│17,04 │ └───────────┴────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴──────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Таблица 2
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96% СПИРТА 20° C
┌───────────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┤ │ 96 │4,04│ 8,08│12,11│16,15│20,19│24,23│32,30│40,38│80,75│ │ 90 │3,79│ 7,57│11,36│15,14│18,93│22,71│30,28│37,86│75,71│ │ 80 │3,37│ 6,73│10,09│13,46│16,82│20,19│26,92│33,65│67,29│ │ 70 │2,95│ 5,89│ 8,83│11,78│14,72│17,67│23,56│29,45│58,89│ │ 60 │2,52│ 5,05│ 7,57│10,09│12,62│15,14│20,18│25,23│50,46│ │ 50 │2,10│ 4,20│ 6,31│ 8,41│10,51│12,61│16,82│21,02│42,04│ │ 40 │1,68│ 3,37│ 5,05│ 6,73│ 8,42│10,10│13,46│16,83│33,66│ │ 30 │1,26│ 2,52│ 3,78│ 5,04│ 6,30│ 7,56│10,08│12,61│25,21│ │ 20 │0,84│ 1,68│ 2,53│ 3,37│ 4,21│ 5,03│ 6,74│ 8,42│16,84│ └───────────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┘
Таблица 3
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,1% СПИРТА 20° C
┌───────────┬────┬────┬─────┬─────┬──────┬─────┬─────┬─────┬─────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼────┼─────┼─────┼──────┼─────┼─────┼─────┼─────┤ │ 96,1 │4,04│8,07│12,11│16,14│ 20,18│24,12│32,28│40,35│80,71│ │ 96 │4,03│8,06│12,09│16,12│ 20,16│24,19│32,25│40,31│80,62│ │ 95 │3,99│7,98│11,97│15,96│ 19,95│23,94│31,92│39,99│79,79│ │ 90 │3,78│7,56│11,34│15,12│ 18,90│22,68│30,24│37,80│75,59│ │ 80 │3,36│6,72│10,08│13,44│ 16,80│20,16│26,88│33,60│67,19│ │ 70 │2,94│5,88│ 8,82│11,76│ 14,70│17,64│23,52│29,40│58,80│ │ 60 │2,52│5,04│ 7,56│10,08│ 12,60│15,12│20,16│25,20│50,40│ │ 50 │2,10│4,20│ 6,30│ 8,40│ 10,50│12,60│16,80│21,00│42,00│ │ 40 │1,68│3,36│ 5,04│ 6,72│ 8,40│10,08│13,44│16,80│33,59│ │ 30 │1,26│2,52│ 3,78│ 5,04│ 6,30│ 7,56│10,08│12,60│25,20│ │ 20 │0,84│1,68│ 2,52│ 3,36│ 4,20│ 5,04│ 6,72│ 8,40│16,79│ └───────────┴────┴────┴─────┴─────┴──────┴─────┴─────┴─────┴─────┘
Таблица 4
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,2% СПИРТА 20° C
┌───────────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┤ │ 96,2 │4,03│ 8,07│12,10│16,13│20,17│24,20│32,27│40,33│80,67│ │ 96 │4,02│ 8,05│12,07│16,10│20,12│24,14│32,19│40,24│80,48│ │ 95 │3,98│ 7,97│11,95│15,93│19,92│23,90│31,86│39,83│79,65│ │ 90 │3,77│ 7,55│11,32│15,09│18,87│22,64│30,18│37,73│75,45│ │ 80 │3,35│ 6,71│10,06│13,41│16,77│20,12│26,83│33,54│67,07│ │ 70 │2,94│ 5,87│ 8,81│11,74│14,68│17,61│23,48│29,35│58,69│ │ 60 │2,52│ 5,03│ 7,55│10,06│12,58│15,09│20,12│25,15│50,30│ │ 50 │2,10│ 4,19│ 6,29│ 8,38│10,48│12,58│16,77│20,96│41,92│ │ 40 │1,68│ 3,35│ 5,03│ 6,71│ 8,39│10,06│13,41│16,77│33,53│ │ 30 │1,26│ 2,52│ 3,77│ 5,03│ 6,29│ 7,55│10,06│12,58│25,15│ │ 20 │0,84│ 1,68│ 2,52│ 3,35│ 4,20│ 5,03│ 6,71│ 8,39│16,77│ └───────────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┘
Таблица 5
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,3% СПИРТА 20° C
┌───────────┬────┬────┬──────┬─────┬─────┬─────┬─────┬─────┬─────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼────┼──────┼─────┼─────┼─────┼─────┼─────┼─────┤ │ 96,3 │4,03│8,06│12,09 │15,12│20,16│24,19│32,25│40,31│80,62│ │ 96 │4,02│8,04│12,05 │16,07│20,09│24,11│32,14│40,18│80,36│ │ 95 │3,98│7,95│11,93 │15,91│19,89│23,86│31,82│39,77│79,54│ │ 90 │3,77│7,54│11,30 │15,07│18,84│22,61│30,14│37,68│75,35│ │ 80 │3,35│6,70│10,05 │13,40│16,75│20,09│26,79│33,49│66,98│ │ 70 │2,93│5,86│ 8,79 │11,72│11,65│17,58│23,44│29,31│58,61│ │ 60 │2,51│5,02│ 7,54 │10,05│12,56│15,07│20,09│25,12│50,23│ │ 50 │2,09│4,19│ 6,28 │ 8,37│10,47│12,56│16,74│20,93│41,86│ │ 40 │1,68│3,35│ 5,03 │ 6,70│ 8,37│10,05│13,40│16,75│33,49│ │ 30 │1,26│2,51│ 3,77 │ 5,02│ 6,28│ 7,54│10,05│12,56│25,12│ │ 20 │0,84│1,67│ 2,51 │ 3,35│ 4,19│ 5,02│ 6,70│ 8,37│16,74│ └───────────┴────┴────┴──────┴─────┴─────┴─────┴─────┴─────┴─────┘
Таблица 6
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,4% СПИРТА 20° C
┌───────────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┤ │ 96,4 │4,03│ 8,06│12,09│16,12│20,15│24,17│32,23│40,29│80,58│ │ 96 │4,01│ 8,03│12,04│16,05│20,06│24,08│32,10│40,13│80,25│ │ 95 │3,97│ 7,94│11,91│15,88│19,85│23,82│31,76│39,71│79,41│ │ 90 │3,76│ 7,53│11,29│15,05│18,81│22,58│30,10│37,63│75,25│ │ 80 │3,34│ 6,69│10,03│13,47│16,72│20,06│26,75│33,44│66,87│ │ 70 │2,93│ 5,85│ 8,78│11,70│14,63│17,56│23,30│29,26│58,52│ │ 60 │2,51│ 5,02│ 7,52│10,03│12,54│15,05│20,06│25,08│50,16│ │ 50 │2,09│ 4,18│ 6,27│ 8,36│10,45│12,54│16,72│20,90│41,80│ │ 40 │1,67│ 3,34│ 5,02│ 6,69│ 8,36│10,03│13,38│16,72│33,44│ │ 30 │1,25│ 2,51│ 3,76│ 5,02│ 6,27│ 7,52│10,03│12,54│25,08│ │ 20 │0,84│ 1,67│ 2,51│ 3,34│ 4,18│ 5,02│ 6,69│ 8,36│16,72│ └───────────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┘
Таблица 7
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,5% СПИРТА 20° C
┌───────────┬─────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼─────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┤ │ 96,5 │4,03 │8,05│12,08│16,11│20,14│24,16│32,22│40,27│80,54│ │ 96 │4,01 │8,01│12,02│16,02│20,03│24,04│32,05│40,06│80,12│ │ 95 │3,57 │7,93│11,90│15,86│19,82│23,76│31,72│39,65│79,29│ │ 90 │3,76 │6,68│11,27│15,02│18,78│22,53│30,04│37,56│75,11│ │ 80 │3,34 │6,68│10,02│13,35│16,69│20,03│25,71│33,39│66,77│ │ 70 │2,92 │5,34│ 8,77│11,69│14,61│17,53│23,37│29,22│58,43│ │ 60 │2,50 │5,01│ 7,51│10,02│12,52│15,02│20,03│25,04│50,18│ │ 50 │2,09 │4,17│ 6,26│ 8,35│10,44│12,52│16,70│20,87│41,74│ │ 40 │1,67 │3,34│ 5,01│ 6,86│ 8,35│10,01│13,35│16,69│33,38│ │ 30 │1,25 │2,50│ 3,76│ 5,01│ 6,26│ 7,51│10,02│12,52│25,04│ │ 20 │0,84 │1,67│ 2,51│ 3,34│ 4,17│ 5,01│ 6,68│ 8,35│16,69│ └───────────┴─────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┘
Таблица 8
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,6% СПИРТА 20° C
┌───────────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┬─────┐ │ │ │ │ │ │ │ │ │ │ │ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┼─────┤ │ 96,6 │4,03│ 8,05│12,07│16,10│20,12│24,15│32,20│40,25│80,50│ │ 96 │4,00│ 8,00│12,00│16,00│20,00│24,00│32,00│40,00│79,99│ │ 95 │3,96│ 7,92│11,87│15,83│19,79│23,75│31,66│39,58│79,16│ │ 90 │3,75│ 7,50│11,25│15,00│18,75│22,50│30,00│37,50│75,00│ │ 80 │3,33│ 6,67│10,00│13,33│16,67│20,00│25,67│33,34│66,67│ │ 70 │2,92│ 5,83│ 8,75│11,67│14,59│17,50│23,34│29,17│58,34│ │ 60 │2,50│ 5,00│ 7,50│10,00│12,50│15,00│20,00│25,00│50,00│ │ 50 │2,08│ 4,17│ 6,25│ 8,33│10,42│12,50│16,67│20,84│41,67│ │ 40 │1,67│ 3,33│ 5,00│ 6,67│ 8,33│10,00│13,33│16,67│33,33│ │ 30 │1,25│ 2,50│ 3,75│ 5,00│ 6,25│ 7,50│10,00│12,50│25,00│ │ 20 │0,83│ 1,67│ 2,50│ 3,33│ 4,17│ 5,00│ 6,66│ 8,33│16,66│ └───────────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┴─────┘
Таблица 9
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,7% СПИРТА 20° C
┌───────────┬────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬──────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼──────┤ │ 96,7 │4,02│8,05│12,07│16,09│20,11│24,14│32,18│40,23│ 80,46│ │ 96 │3,99│7,99│12,11│15,97│19,97│23,96│31,95│39,94│ 79,87│ │ 95 │3,95│7,91│11,86│15,81│19,76│23,72│31,62│39,53│ 79,05│ │ 90 │3,74│7,49│11,23│14,98│18,72│22,46│29,95│37,44│ 74,88│ │ 80 │3,33│6,66│ 9,98│13,31│16,64│19,97│26,62│33,28│ 66,56│ │ 70 │2,91│5,83│ 8,74│11,65│14,56│17,48│23,30│29,13│ 58,25│ │ 60 │2,50│4,99│ 7,46│ 9,98│12,48│14,96│19,97│24,96│ 49,92│ │ 50 │2,08│4,16│ 6,24│ 8,32│10,40│12,48│16,64│20,81│ 41,61│ │ 40 │1,66│3,33│ 4,99│ 6,66│ 8,32│ 9,98│13,31│16,64│ 33,28│ │ 30 │1,25│2,50│ 3,74│ 4,99│ 6,24│ 7,49│ 9,98│12,48│ 24,96│ │ 20 │0,83│1,66│ 2,50│ 3,33│ 4,16│ 4,99│ 6,66│ 8,32│ 16,64│ └───────────┴────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴──────┘
Таблица 10
СООТНОШЕНИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,8% СПИРТА 20° C
┌───────────┬────┬────┬─────┬─────┬─────┬─────┬─────┬─────┬──────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼────┼─────┼─────┼─────┼─────┼─────┼─────┼──────┤ │ 96,8 │4,02│8,04│12,06│16,08│20,11│24,13│32,17│40,21│ 80,42│ │ 96 │3,99│7,98│11,96│15,95│19,94│23,93│31,90│39,88│ 79,75│ │ 95 │3,95│7,89│11,84│15,78│19,73│23,68│31,57│39,46│ 78,92│ │ 90 │3,74│7,48│11,22│14,95│18,69│22,43│29,91│37,39│ 74,77│ │ 80 │3,32│6,65│ 9,97│13,29│16,62│19,94│26,58│33,23│ 66,46│ │ 70 │2,91│5,82│ 8,72│11,63│14,54│17,45│23,26│29,08│ 58,16│ │ 60 │2,49│4,99│ 7,48│ 9,97│12,46│14,96│19,94│24,93│ 49,85│ │ 50 │2,08│4,15│ 6,23│ 8,31│10,39│12,46│16,62│20,77│ 41,54│ │ 40 │1,66│3,32│ 4,99│ 6,65│ 8,31│ 9,97│13,29│16,62│ 33,23│ │ 30 │1,25│2,49│ 3,74│ 4,98│ 6,23│ 7,48│ 9,97│12,46│ 24,92│ │ 20 │0,83│1,66│ 2,49│ 3,32│ 4,15│ 4,98│ 6,64│ 8,31│ 16,61│ └───────────┴────┴────┴─────┴─────┴─────┴─────┴─────┴─────┴──────┘
Таблица 11
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,9% СПИРТА 20° C
┌───────────┬────┬────┬─────┬──────┬─────┬─────┬─────┬─────┬─────┐ │Объем, мл \│ 5 │ 10 │ 15 │ 20 │ 25 │ 30 │ 40 │ 50 │ 100 │ │Концентра- │ │ │ │ │ │ │ │ │ │ │ция (об. %)│ │ │ │ │ │ │ │ │ │ ├───────────┼────┼────┼─────┼──────┼─────┼─────┼─────┼─────┼─────┤ │ 96,9 │4,02│8,04│12,06│16,08 │20,10│24,11│32,15│40,19│80,38│ │ 96 │3,98│7,96│11,95│15,93 │19,91│23,89│31,85│39,82│79,63│ │ 95 │3,94│7,88│11,82│15,76 │19,70│23,64│31,52│39,41│78,81│ │ 90 │3,73│7,47│11,20│14,93 │18,67│22,40│29,86│37,33│74,66│ │ 80 │3,32│6,64│ 9,94│13,27 │16,59│19,91│26,55│33,19│66,37│ │ 70 │2,90│5,81│ 8,71│11,61 │14,52│17,42│23,22│29,04│58,07│ │ 60 │2,49│4,98│ 7,48│ 9,96 │12,45│14,93│19,91│24,94│49,78│ │ 50 │2,07│4,15│ 6,22│ 8,30 │10,37│12,44│16,59│20,74│41,48│ │ 40 │1,66│3,32│ 4,98│ 6,64 │ 8,30│ 9,95│13,27│16,59│33,18│ │ 30 │1,24│2,49│ 3,73│ 4,98 │ 6,22│ 7,46│ 9,95│12,44│24,88│ │ 20 │0,83│1,66│ 2,49│ 3,32 │ 4,15│ 4,98│ 6,64│ 8,30│16,59│ └───────────┴────┴────┴─────┴──────┴─────┴─────┴─────┴─────┴─────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌────────────────────────────────────┬──────────────────────────┐ │ Наименование сырья │ Коэффициент │ ├────────────────────────────────────┼──────────────────────────┤ │ Кора дуба │ 2,0 │ │ -"- калины │ 2,0 │ │ -"- крушины │ 1,6 │ │ Корни аира │ 2,4 │ │ -"- истода │ 2,2 │ │ -"- солодки │ 1,7 │ │ Корневища змеевика │ 2,0 │ │ Корневища с корнями валерианы │ 2,9 │ │ Корневища с корнями кровохлебки │ 1,7 │ │ Корневища лапчатки │ 1,4 │ │ Листья брусники │ 1,5 │ │ -"- крапивы │ 1,8 │ │ -"- мать-и-мачехи │ 3,0 │ │ -"- мяты │ 2,4 │ │ -"- подорожника │ 2,8 │ │ -"- сенны │ 1,8 │ │ -"- толокнянки │ 1,4 │ │ -"- шалфея │ 3,3 │ │ Плоды рябины │ 1,5 │ │ -"- шиповника │ 1,1 │ │ Трава горицвета │ 2,8 │ │ -"- зверобоя │ 1,6 │ │ -"- ландыша │ 2,5 │ │ -"- полыни │ 2,1 │ │ -"- пустырника │ 2,0 │ │ -"- сушеницы │ 2,2 │ │ -"- хвоща полевого │ 3,0 │ │ -"- череды │ 2,0 │ │ Цветки липы │ 3,4 │ │ -"- ромашки │ 3,4 │ │ Шишки хмеля │ 3,2 │ └────────────────────────────────────┴──────────────────────────┘
Примечания. 1. Коэффициент водопоглощения соответствует количеству жидкости (мл), удерживаемому 1,0 г лекарственного растительного сырья после его отжатия в перфорированном стакане инфундирки.
2. Если коэффициент водопоглощения для сырья отсутствует, рекомендуется использовать следующие значения:
- для корней и корневищ - 1,5 мл/г;
- для коры, травы и цветков - 2,0 мл/г;
- семян - 3,0 мл/г;
- для брикетов - 2,3 мл/г.
3. Расходный коэффициент, используемый при изготовлении настоя корней алтея, показывает, во сколько раз следует увеличить массу сырья и объем экстрагента, чтобы получить заданный объем извлечения необходимой концентрации.
4. Расходные коэффициенты для изготовления настоя корней алтея различной концентрации:
1% — 1,05
2% — 1,10
3% — 1,15
4% — 1,20
5% — 1,30
5. Для настоя корней алтея концентраций более 5% расходный коэффициент рассчитывают по формуле:
100
Кр = -------------,
100 - (C x V)
где Кр - расходный коэффициент
C - выписанная в рецепте концентрация настоя (%)
V - объем настоя, удерживаемый 1 г сырья (4,6 мл).
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───────────────────────┬─────────────────────┬───────────────────┐ │ Состав │ Особенности │ Примечание │ │ │ изготовления │ │ ├───────────────────────┼─────────────────────┼───────────────────┤ │ 1 │ 2 │ 3 │ ├───────────────────────┼─────────────────────┼───────────────────┤ │Раствор натрия │Для изготовления 100 │Запрещается изго- │ │тиосульфата 60%- │мл 60% раствора в │товление раствора │ │100 мл │массо-объемной кон- │в массо-объемной │ │Раствор по Демья- │центрации следует │концентрации путем │ │новичу N 1 │взять 85 г натрия │растворения 60 г │ │ │тиосульфата │натрия тиосульфата │ │ │70,6 - 60 г │и доведения объема │ │Натрия тиосульфата 60 г│100 - x │до 100 мл, т.к. в │ │Воды очищенной 40 г │x = 85 г │этом случае масса │ │-----------------------│ │раствора увеличится│ │Масса раствора - 100 г │В мерной посуде в │на 29,4 │ │Объем раствора - │части прокипяченной │(100 - 70,6) = │ │70,6 мл │и охлажденной воды │= 29,4 мл и концен-│ │70,6 = 40 мл + │очищенной растворяют │трация по массе │ │+ (60 x 0,51), │85 г натрия тиосуль- │становится 46,37% │ │где 0,51 мл/г - КУО │фата и объем раство- │129,4 - 60,0 │ │(Приложение 6) │ра доводят до 100 мл.│100,0 - x │ │ │При отсутствии мер- │x = 46,37% │ │ │ной посуды объем │ │ │ │воды рассчитывают с │ │ │ │использованием КУО │ │ │ │100 - (85 x 0,51) = │ │ │ │= 57 мл │ │ │ │После растворения │ │ │ │натрия тиосульфата │ │ │ │раствор фильтруют │ │ │ │во флакон для от- │ │ │ │пуска. │ │ ├───────────────────────┼─────────────────────┼───────────────────┤ │Водные и водно-глице- │В мерной посуде ра- │Водные растворы │ │риновые растворы йода │створяют калия иодид │Люголя изготавли- │ ├──────────┬─┬──┬──┬────┤в приблизительно рав-│вают в массо-объ- │ │Состав (г)│1│2 │3 │4 │ном объеме воды. В │емной концентрации,│ ├──────────┼─┼──┼──┼────┤насыщенном растворе │глицериновые в кон-│ │Йод │1│5 │1 │0,25│калия иодида раство- │центрации по массе.│ │Калий │ │ │ │ │ряют йод. Объем рас- │Препараты, изготов-│ │иодид │2│10│2 │0,5 │твора доводят до │ленные по прописям │ ├──────────┴─┴──┼──┼────┤требуемого. В случае │1, 3, 4 применяют │ │Вода │ │ │отсутствия мерной │наружно; по пропи- │ │очищен- │ │ │посуды объем воды │сям 1, 2 - внутрь в│ │ная до 100 мл│3 │0,75│рассчитывают с ис- │виде капель │ │ │ │ │пользованием КУО │ │ ├──────────┬─┬──┼──┼────┼─────────────────────┼───────────────────┤ │ │ │ │ │ │При изготовлении │ │ │Глице- │ │ │ │ │глицериновых раство- │ │ │рин (г) │-│- │94│98,5│ров в предварительно │ │ │----------│-│--│--│----│старированном флаконе│ │ │Кон- │ │ │ │ │известной массы раст-│ │ │цент- │ │ │ │ │воряют калий иодид в │ │ │рация │ │ │ │ │указанном в прописи │ │ │(%) │1│5 │ 1│0,25│количестве воды. В │ │ ├──────────┴─┴──┴──┴────┤насыщенном растворе │ │ │ │калия иодида раство- │ │ │ │ряют йод, отвешивают │ │ │ │глицерин. Все смеши- │ │ │ │вают │ │ ├───────────────────────┼─────────────────────┼───────────────────┤ │ Ароматные воды │В асептических усло- │ВО Союзфармация │ │ (мятная и укропная) │виях указанное коли- │"Методические ука- │ │ │чество соответствую- │зания по приготов- │ │ Вода укропная 0,005 % │щего эфирного масла │лению и контролю │ │ │в течение 1 минуты │качества воды мяты │ │ Масла фенхелевого │энергично смешивают │перечной и укроп- │ │ 0,05 г │с водой до растворе- │ной" от 10.07.89 │ │ Воды очищенной до 1 л │ния │ │ │ │ │ │ │ Вода мятная 0,044% │Хранение: │ │ │ │вода укропная - 30 │ │ │ Масло мяты перечной │суток; │ │ │ 0,44 г │вода мятная - в виде │ │ │ Воды очищенной до 1 л │фасовки (200 мл) - │ │ │ │30 суток; в виде │ │ │ │полуфабриката по 500 │ │ │ │и 1000 мл - 15 суток │ │ └───────────────────────┴─────────────────────┴───────────────────┘
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
┌───────┬────────┬───────────────────────┬────────────┬──────────┐ │N про- │Концент-│ Эмульгаторы, г │Воды очищен-│Масса бен-│ │писи │рация, %├──────┬─────────┬──────┤ной, мл │зилбензоа-│ │ │ │мыло │мыло хо- │эмуль-├───────┬────┤та, г │ │ │ │калий-│зяйствен-│гатор │ I │ II │ │ │ │ │ное │ное │Т-2 │ │ │ │ ├───────┼────────┼──────┼─────────┼──────┼───────┼────┼──────────┤ │ 1 │ 10 │ 5 │ - │ - │ 7,5 │77,5│ 10 │ │ 2 │ 20 │ 5 │ - │ - │ 12,5 │62,5│ 20 │ │ 3 │ 20 │ 10 │ - │ - │ 15 │55 │ 20 │ │ 4 │ 10 │ 1 │ - │ 1 │ 5,5 и│72,5│ 10 │ │ │ │ │ │ │ 10 │ │ │ │ 5 │ 20 │ 1 │ - │ 1 │ 10,5 и│72,5│ 20 │ │ │ │ │ │ │ 10 │ │ │ │ 6 │ 10 │ - │ 2 │ - │ 18 │70 │ 10 │ │ 7 │ 20 │ - │ 2 │ - │ 18 │60 │ 20 │ └───────┴────────┴──────┴─────────┴──────┴───────┴────┴──────────┘
Изготовление эмульсии
Прописи 1, 2, 3. В ступке смешивают мыло калийное с соответствующим количеством горячей воды очищенной (I). Постепенно добавляют бензилбензоат, тщательно эмульгируя. Первичную эмульсию разбавляют остальным количеством горячей воды (II). Готовую эмульсию фильтруют через двойной слой марли и после охлаждения массу эмульсии доводят водой до 100,0 г.
Прописи 4, 5. Отдельно в ступке изготавливают раствор мыла калийного с 5,5 мл (10% эмульсия) или 10,5 мл (20% эмульсия) горячей воды очищенной. В фарфоровой чашке расплавляют 1,0 эмульгатора Т-2 и смешивают с 10 мл горячей воды. Оба эмульгатора смешивают в ступке и эмульгируют соответствующее количество бензилбензоата, добавляют оставшееся количество горячей воды очищенной (II) и далее поступают как описано выше (Прописи 1, 2, 3).
Прописи 6,7. Стружку 2 г мыла хозяйственного заливают 18 мл горячей воды (I). Полученным 10% раствором мыла эмульгируют соответствующее количество бензилбензоата и далее поступают, как описано выше (Прописи 1, 2, 3).
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Общие правила и технологии изготовления жидких лекарственных форм в аптеке
Нормы, допустимые отклонения и основные способы приготовления стерильных и нестерильных ЖЛФ описаны в Приказе Министерства здравоохранения РФ от 22 мая 2023 г. № 249н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность». Стандарты действуют для всех аптек: и государственных, и частных.
К жидким лекарственным формам, которые можно приготовить в производственной аптеке для медицинского и личного пользования, относятся:
- растворы;
- водные извлечения — настои и отвары;
- капли;
- суспензии;
- эмульсии.
Подробно про виды ЖЛФ можно прочитать в статье «Жидкие лекарственные формы». Здесь же кратко рассмотрим особенности их приготовления.
Особенности изготовления растворов
Раствор — это лекарственная форма, которая получается при полном растворении одного или нескольких активных веществ в растворителе. Также возможно разбавление концентратов или стандартных фармакопейных растворов.
Показатели растворимости ингредиентов, то есть их способность растворяться в разных растворителях, приведены в Государственной фармакопеи (далее — ГФ). Важно, чтобы растворители не вступали с веществами в химико-физическую реакцию, а также не изменяли их фармакологических свойств. Компонент считают растворившемся, если при наблюдении в проходящем свете не видно твердых частиц.
Для получения водных растворов используют очищенную воду. Неводных — этиловый спирт или жирные масла различного происхождения, например, природные или глицерин. В качестве вспомогательных компонентов применяют антимикробные консерванты, антиоксиданты, стабилизаторы, сорастворители и другие средства, разрешенные к использованию в фармакологии.
Чтобы приготовить раствор, провизор выполняет следующие этапы:
- Рассчитывает и проверяет дозировку всех компонентов, нужных для ЖЛФ.
- Организует рабочее место, готовит приборы, в том числе создает специальные условия для нагревания или охлаждения, чтобы лекарства быстро и полностью растворились.
- Растворяет компоненты.
- Очищает и фильтрует раствор.
- Упаковывает и закупоривает его.
- Оформляет упаковку.
- Проходит проверку качества.
Наглядно и более подробно этот процесс представлен на рисунке.
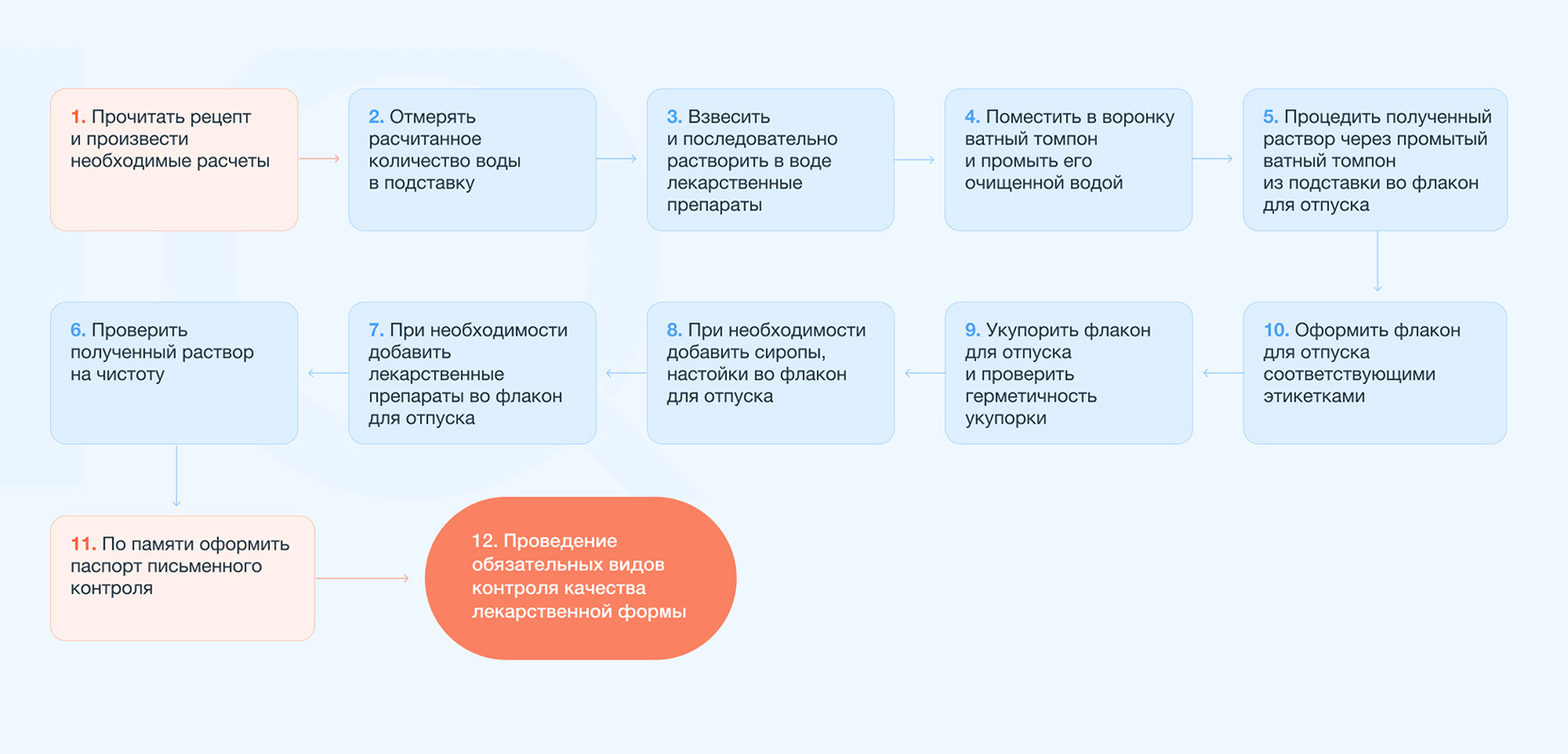
В условиях аптеки растворы дозируют по массе, объему или массообъемным способом. В последнем случае растворяемое вещество берут по массе, а растворитель добавляют до получения требуемого объема раствора.

Особенности технологии изготовления водных извлечений
К водным извлечениям относятся отвары и настои. Их готовят из цельного, измельченного или порошкообразного растительного сырья, обладающего лечебными свойствами. Допустимые нормы его измельчения и показатели, сколько в нем должно содержаться активных веществ, установлены фармакопеей.
Настои и отвары готовят массообъемным способом. Обычно в рецепте врач пишет, сколько нужно растительного сырья. Если таких пояснений нет, провизор руководствуется соотношением 1:10 — из 10 массовых частей сырья получают 100 объемных частей водного извлечения. Для ядовитого сырья нормы составляют 1:400.
Этапы технологии изготовления настоев и отваров:
1. Предварительные работы: подготовка оборудования и измельчение сырья.
2. Непосредственно изготовление:
- настаивание на водяной бане;
- охлаждение при комнатной температуре;
- фильтрование через промытый ватный тампон и двойной слой марли.
3. Контроль качества приготовления ЖЛФ.
4. Оформление лекарственной формы.
Если компонентов несколько и нужны разные режимы настаивания, извлечения готовят раздельно. Максимальное количество воды должно быть не менее 10-кратного количества по отношению к сырью.
Технология приготовления суспензии
Суспензия — ЖЛФ, которая содержит одно или несколько твердых лекарственных веществ.
Она получается, если:
- вещества не растворяются в растворителе;
- превышен предел растворимости компонента;
- растворитель изменен;
- в результате химического взаимодействия между компонентами образовалось новое вещество.
В условиях аптеки суспензии могут быть изготовлены одним из двух методов: диспергирование или конденсация. Диспергирование заключается в том, что в ступке сначала измельчают твердое вещество, а потом к нему добавляют растворитель и доводят консистенцию до тончайшей кашицы.
Конденсация может проходить двумя способами. В первом соединяют ингредиенты, которые порознь растворимые, но реагируют при сливании растворов с образованием взвеси. Во втором разводят водой или водными растворами солей жидких экстрактов или настоек.
Частицы в суспензиях обычно равномерно распределяются в растворе. Если осадок прилипает к стенкам флакона для отпуска, используют стабилизатор.
Инструкция по изготовлению эмульсии в условиях аптеки
Эмульсия — жидкая лекарственная форма, в которой используют две несмешиваемые друг с другом жидкости. Обычно это масло в воде или наоборот.
Для приготовления масляных эмульсий рекомендуют применять различные растительные масла, например, персиковое, миндальное, подсолнечное, также разрешены к использованию рыбий жир и бальзамы. Если в рецепте врача нет указаний, сколько нужно масла, исходят из пропорции 10 г масла для 100 г эмульсии.
Технология изготовления включает следующие этапы:
- Нагрев масла до температуры 40-50 ℃, чтобы снизить его вязкость.
- Приготовление первичной эмульсии. Для этого провизор пестиком растирает в ступке масло с эмульгатором — вспомогательным веществом, которое обеспечивает связь несмешивающихся жидкостей.
- Добавление в первичную эмульсию очищенную воду.
Если в рецепте эмульгатор не написан, провизор сам определяет, какое вещество лучше всего выступит в этой роли. Готовую эмульсию процеживают через два слоя марли.

Внутриаптечный контроль изготовления жидких лекарственных форм
Контрольные мероприятия проводит провизор-аналитик. Он проверяет все лекарственные формы, которые изготавливают в аптеке. Ранее его действия регламентировались инструкцией, утвержденной Приказом М3 РФ № 214 от 1997 г. Сейчас документ не действует, и перечень контрольных и проверочных мероприятий можно посмотреть в уже упомянутом Приказе № 249н.
Виды внутриаптечного контроля представлены в таблице.

В ходе письменного контроля провизор вносит всю информацию о рецепте и технологии изготовления лекарственной формы в паспорт. Он указывает в нем дату и номер рецепта, латинские названия средства, количество, дозирование, все дополнительные вещества и коэффициенты, формулы и расчеты. Последние записываются на оборотной стороне паспорта. Документ подписывает провизор-технолог, специалист, который занимался фасовкой, и контролер. Сразу после изготовления жидких лекарственных форм в паспорт записывают использованные вещества и их количество.
Органолептический контроль подразумевает оценку внешнего вида лекарства, его запаха, цвета и однородности.
Во время контроля при отпуске провизор проверяет, правильно ли оформлена этикетка, соответствует ли состав рецепту, назначенная дозировка — возрасту больного и прочие формальные требования, которые перечислены в нормативных актах.
Выборочно провизор-аналитик может провести опросный контроль. Он называет фармацевту первое вещество из прописи, а тот перечисляет использованные лекарственные средства и их количество.
При физическом контроле провизор проверяет качество упаковки, объем и массу ЖЛС и его доз. В ходе химического контроля аналитик оценивает чистоту воды, качество лекарств, расфасованных непосредственно в аптеке, используемые концентраты и полуфабрикаты.
Результаты контрольных проверок записывают в специальные журналы. Всю проверочную информацию провизор должен завизировать подписью.
Источники
- Зюбр Т.П. и др. «Жидкие лекарственные формы. Раздел 2. Суспензии и эмульсии» // Учебное пособие;
- Гроссман В. А. «Технология изготовления лекарственных форм» // Учебник;
- Илларионова Е.А., Сыроватский И.П. «Внутриаптечный контроль лекарственных средств» // Учебно-методическое пособие.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРИКАЗ
от 21 октября 1997 г. N 308
ОБ УТВЕРЖДЕНИИ ИНСТРУКЦИИ
ПО ИЗГОТОВЛЕНИЮ В АПТЕКАХ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ
В целях повышения качества лекарственных средств, изготовляемых в аптеках, приказываю:
1. Ввести в действие с 1 января 1998 года Инструкцию по изготовлению в аптеках жидких лекарственных форм (Приложение).
2. Считать недействующим на территории Российской Федерации Приказ Министерства здравоохранения СССР от 11.11.90 N 435 «Об утверждении Инструкции по изготовлению в аптеках жидких лекарственных форм».
3. Контроль за выполнением настоящего Приказа возложить на заместителя министра Вилькена А.Е.
Министр
Т.Б.ДМИТРИЕВА
Приложение
Утверждена
Приказом Министерства здравоохранения
Российской Федерации
от 21 октября 1997 г. N 308
ИНСТРУКЦИЯ
ПО ИЗГОТОВЛЕНИЮ В АПТЕКАХ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ
1. ОБЩИЕ ПОЛОЖЕНИЯ
1.1. Настоящая Инструкция содержит основные методы и правила изготовления в аптеках жидких лекарственных форм для внутреннего и наружного применения, качество которых должно соответствовать требованиям, регламентированным действующей Государственной фармакопеей (ГФ), нормативными документами, приказами и инструкциями Министерства здравоохранения Российской Федерации.
1.2. Действие Инструкции распространяется на все аптеки, находящиеся на территории России, независимо от форм собственности и ведомственной принадлежности.
1.3. При изготовлении жидких лекарственных форм, а также при получении, хранении и подаче на рабочее место воды очищенной и для инъекций в аптеках должны соблюдаться требования действующей Инструкции по санитарному режиму аптек.
В асептических условиях изготавливают: растворы для инъекций и инфузий; ирригационные растворы, вводимые в полости, не содержащие микроорганизмов; жидкие лекарственные формы для новорожденных и детей до 1 года; препараты в жидкой лекарственной форме, содержащие антибиотики и другие антимикробные вещества, а также предназначенные для нанесения на раны и ожоговые поверхности; капли глазные, офтальмологические растворы для орошений и примочки; концентрированные растворы (в том числе гомеопатические разведения); жидкие лекарственные средства в виде внутриаптечной заготовки.
1.4. Внутриаптечный контроль жидких лекарственных форм на стадиях изготовления, после изготовления и при отпуске из аптеки осуществляется в соответствии с требованиями действующих нормативных документов, приказов и инструкций.
1.5. Растворы и другие жидкие лекарственные формы изготавливают методами: массо-объемным, по массе, по объему. Действующей Государственной фармакопеей принят, как основной, массо-объемный метод изготовления жидких лекарственных форм.
1.6. В зависимости от метода изготовления содержание лекарственных веществ в жидких лекарственных формах выражается в концентрациях: массо-объемной, по массе, по объему.
Массо-объемная концентрация — количество лекарственного средства или индивидуального вещества (в граммах) в общем объеме жидкой лекарственной формы (в миллилитрах); концентрация по массе — количество лекарственного средства или индивидуального вещества (в граммах) в общей массе жидкой лекарственной формы (в граммах); объемная концентрация — количество жидкого лекарственного средства или индивидуального вещества (в миллилитрах) в общем объеме жидкой лекарственной формы (в миллилитрах).
1.7. В прописях рецептов концентрации: массо-объемная (а), по массе (б) и объемная концентрация (в) могут быть обозначены:
При массо-объемном методе изготовления обозначение концентрации, например, 1:10 или 1:20 означает содержание вещества или лекарственного средства по массе (г) в указанном объеме изготавливаемой жидкой лекарственной формы (мл), т.е. следует взять 1 г вещества или лекарственного средства и растворителя до получения 10 мл или 20 мл жидкой лекарственной формы.
При изготовлении лекарственных форм методом по массе обозначение концентрации 1:10 или 1:20 означает содержание вещества или лекарственного средства по массе (г) в указанной массе жидкой лекарственной формы (г), т.е. следует взять 1 г вещества или лекарственного средства и 9 г или 19 г растворителя.
При изготовлении методом по объему обозначение концентрации 1:10 или 1:20 означает содержание вещества или лекарственного средства по объему (мл) в указанном объеме лекарственной формы (мл), т.е. следует взять 1 мл жидкого лекарственного вещества или средства и растворителя до получения 10 мл или 20 мл раствора.
1.8. В массо-объемной концентрации изготавливают водные и водно-спиртовые растворы твердых лекарственных веществ; водные и водно-спиртовые суспензии с содержанием твердых веществ менее 3%; разведения стандартных растворов, выписанных в рецепте под химическим названием, с указанием концентрации лекарственного вещества в растворе (раздел 2, пп. 2.5.2, 2.5.3).
В концентрации по массе изготавливают растворы твердых и жидких лекарственных веществ в вязких и летучих растворителях, дозируемых по массе, а также суспензии и эмульсии.
По массе дозируют: жирные и минеральные масла, глицерин, димексид, полиэтиленгликоли (полиэтиленоксиды), силиконовые жидкости, эфир, хлороформ, а также: бензилбензоат, валидол, винилин (бальзам Шостаковского), деготь березовый, ихтиол, кислоту молочную, масла эфирные, скипидар, метилсалицилат, нитроглицерин, пергидроль.
В концентрации по массе изготавливают гомеопатические жидкие лекарственные средства.
В объемной концентрации изготавливают растворы спирта различной концентрации, кислоты хлористоводородной и стандартные растворы, выписанные в рецепте под условным названием (раздел 2, пп. 2.5.1, 2.5.3), по объему дозируют: воду очищенную и для инъекций, водные растворы лекарственных веществ, (в том числе сироп сахарный), галеновые и новогаленовые лекарственные средства (настойки, жидкие экстракты, адонизид и др.).
Если требуется установить объем жидкости, выписываемой в прописи рецепта и дозируемой по массе, или, наоборот, массу жидкости, выписываемой в прописи рецепта и дозируемой по объему, используют значение их плотности (Приложения 1, 2).
1.9. Если в прописи не указан растворитель, изготавливают водный раствор.
Под названием «вода» при отсутствии особых указаний понимают воду очищенную.
Под названием «спирт» понимают спирт этиловый. При отсутствии указаний о концентрации спирта (в рецепте или соответствующей нормативной документации) следует использовать 90% спирт.
Под названием «эфир» понимают эфир медицинский.
Под названием «глицерин» понимают глицерин, содержащий 10 — 16% воды, с плотностью 1,223 — 1,233 г/см куб.
1.10. При изготовлении водных растворов веществ, содержащих в составе молекулы кристаллизационную воду, пересчет количества лекарственного вещества с учетом содержания кристаллизационной воды осуществляют в соответствии с действующей ГФ или иной нормативной документацией в тех случаях, когда это регламентируется составом прописи и методом количественного определения.
Сильно гигроскопичные вещества используют для изготовления жидких лекарственных форм в виде концентрированных растворов (например, кальция хлорид, калия ацетат).
1.11. Изготовление жидких лекарственных форм основано на применении: бюреточных установок и мерной посуды, откалиброванных в соответствии с ГОСТом, заранее изготовленных концентрированных растворов лекарственных веществ (концентратов), а также на соблюдении определенных правил изготовления.
1.12. Жидкости, выпускаемые фармацевтическими производствами и предприятиями (меновазин, раствор йода спиртовой и др.), на состав и технологию которых имеется нормативная документация, могут изготавливаться в соответствии с этой документацией и указаниями настоящей Инструкции (разд. 2, п. 2.7, Приложение 3).
1.13. После изготовления жидкой лекарственной формы отклонение общего объема или массы от указанных в прописи рецепта не должно превышать норму допустимого отклонения, установленную действующей нормативной документацией.
2. ОСНОВНЫЕ ПРАВИЛА ИЗГОТОВЛЕНИЯ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ
2.1. Общие правила изготовления, последовательность
растворения и смешивания лекарственных средств
При изготовлении жидких лекарственных форм с водной дисперсионной средой в первую очередь отмеривают рассчитанный объем воды (очищенной, для инъекций или ароматной), в котором последовательно растворяют твердые лекарственные и вспомогательные вещества с учетом растворимости и возможного их взаимодействия.
Первыми в отмеренном объеме воды растворяют ядовитые и наркотические вещества (список А), затем наркотические и сильнодействующие (список Б), а далее несильно действующие с учетом их растворимости.
Для повышения растворимости веществ умеренно, мало или медленно растворимых их предварительно измельчают, а в процессе изготовления их растворы нагревают с учетом физико-химических свойств и перемешивают.
При изготовлении растворов очень мало растворимых или практически нерастворимых веществ, кроме вышеперечисленных операций используют получение растворимых производных (комплексообразование, образование растворимых солей) и солюбилизацию в соответствии с нормативной документацией.
Изготовленный раствор фильтруют через фильтр, материал которого подбирают с учетом физико-химических свойств веществ и назначения раствора.
Твердые лекарственные вещества в состав лекарственной формы могут быть введены в виде заранее изготовленных концентрированных растворов, которые добавляются после растворения твердых веществ и фильтрования раствора (Приложения 4 — 7).
Если в состав лекарственной формы входят другие жидкие лекарственные средства, их добавляют к водному раствору в следующей последовательности:
— водные нелетучие и непахучие жидкости,
— иные нелетучие жидкости, смешивающиеся с водой,
— водные летучие жидкости,
— жидкости, содержащие спирт, в порядке возрастания его концентрации (Приложение 8),
— летучие и пахучие жидкости.
При добавлении всех жидкостей также следует учитывать их принадлежность к определенному списку, растворимость и способность смешиваться с водой.
При изготовлении растворов в вязких и летучих растворителях непосредственно в сухой флакон для отпуска дозируют лекарственное средство или вещество, вспомогательные вещества, затем взвешивают растворитель (спирт отмеривают).
При использовании вязких растворителей (глицерин, масла) применяют нагревание с учетом физико-химических свойств лекарственных веществ.
При растворении в спирте или хлороформе — нагревают только в случае необходимости и с соблюдением мер предосторожности.
Растворы, содержащие летучие вещества, нагревают при температуре не более 40 — 45° C.
Не нагревают жидкости, содержащие эфир и его смеси со спиртом.
Растворы фильтруют через сухой фильтрующий материал, который подбирают с учетом вязкости и летучести растворителя, соблюдая меры предосторожности для снижения потерь, связанных с испарением.
2.2. Общий объем жидкой лекарственной формы
при изготовлении в массо-объемной или объемной концентрации
2.2.1. При раздельном выписывании компонентов общий объем лекарственной формы определяют суммированием объемов всех жидкостей, перечисленных в прописи рецепта.
Если в состав лекарственной формы входит жидкость, выписанная по массе (М), ее объем (V) определяют с учетом плотности (p).
В прописи присутствует жидкость, выписанная по массе, — глицерин. Для определения объема глицерина используют среднее значение его плотности. Объем 10 г глицерина равен 8 мл.
Общий объем лекарственной формы — 113 мл (100 + 5 + 8).
2.2.2. Общий объем микстуры указан в прописи рецепта.
Общий объем микстуры указан в прописи рецепта и равен 100 мл.
2.3. Общая масса жидкой лекарственной формы
при изготовлении в концентрации по массе
При раздельном выписывании в прописи рецепта общую массу определяют суммированием масс всех компонентов, входящих в пропись.
Общая масса может быть указана в прописи (например, «ad 200,0»; «5% — 200,0», «1:20 — 200,0»).
Если в прописи присутствует жидкость, выписанная по объему, ее массу определяют с учетом плотности (p)
2.4. Изменение общего объема жидких лекарственных форм
при массо-объемном изготовлении из твердых растворимых
веществ и концентрированных растворов
Изменение общего объема при растворении твердого вещества можно не учитывать, если оно укладывается в норму допустимого отклонения.
Для каждого лекарственного вещества максимальная концентрация в процентах (C max), при которой изменение общего объема укладывается в норму допустимого отклонения, вычисляют по формуле:
где: N — норма допустимого отклонения для данного общего объема препарата, %,
КУО — коэффициент увеличения объема при растворении 1 г вещества при 20° C, мл/г (Приложение 9).
Микстуру изготавливают, используя концентрированный 20% раствор натрия бромида.
Максимальную концентрацию (C max, %) анальгина, при которой наблюдается изменение объема выше нормы допустимого отклонения, вычисляют по указанной выше формуле
В прописи анальгин выписан в концентрации 1,5%, поэтому изменение объема при растворении 3 г анальгина можно не учитывать.
В 180 мл воды очищенной растворяют 3 г анальгина, фильтруют во флакон для отпуска и добавляют 20 мл 20% раствора натрия бромида.
Микстуру изготавливают с использованием концентрированных растворов кальция хлорида 50% и натрия бромида 20%. Концентрированный раствор глюкозы в аптеке в данный момент отсутствует.
Максимальная концентрация глюкозы безводной, при которой наблюдается изменение объема выше нормы допустимого отклонения, — 3,1%.
В данной прописи глюкоза выписана в 30% концентрации, т.е. необходимо учитывать изменение объема при ее растворении.
Вместо 60 г глюкозы безводной, указанной в прописи рецепта, требуется взять 66,6 г глюкозы с содержанием влаги 10%. Изменение объема при растворении водной глюкозы составит 46 мл (66,6 x x 0,69). В 119 мл горячей воды очищенной растворяют 66,6 г глюкозы, фильтруют во флакон для отпуска, отмеривают 20 мл раствора кальция хлорида 50% и 15 мл раствора натрия бромида 20%.
При изготовлении жидкой лекарственной формы путем растворения нескольких твердых веществ, изменение общего объема учитывают, если их суммарное содержание составляет 3% и более.
2.5. Разведение стандартных фармакопейных растворов
Таблица 1
Стандартные растворы
2.5.1. Растворы кислоты хлористоводородной
Растворы кислоты хлористоводородной любой концентрации изготавливают из кислоты хлористоводородной разведенной (8,2 — 8,4%), принимая ее за единицу (100%).
Кислота хлористоводородная разведенная используется также для получения 10% (1:10) раствора в качестве внутриаптечной заготовки (концентрация кислоты при этом будет 0,82 — 0,84%).
Общий объем микстуры 154 мл. Во флакон для отпуска отмеривают 114 мл воды очищенной и 40 мл раствора кислоты хлористоводородной разведенной 1:10 (или 150 мл воды очищенной и 4 мл кислоты хлористоводородной разведенной 8,3%). В подкисленной воде растворяют 4 г пепсина.
Кислота хлористоводородная с концентрацией 24,8 — 25,2% отпускается только в тех случаях, когда в прописи рецепта имеется соответствующее указание.
Без дополнительного указания кислота хлористоводородная с концентрацией 24,8 — 25,2% используется при изготовлении раствора 2 по прописи Демьяновича.
Объем раствора — 100 мл.
Во флакон для отпуска отмеривают 94 мл воды очищенной и 6 мл кислоты хлористоводородной 24,8 — 25,2%.
При отсутствии кислоты хлористоводородной с концентрацией 24,8 — 25,2% можно использовать кислоту хлористоводородную разведенную с концентрацией 8,2 — 8,4%, которой следует взять в 3 раза больше.
Во флакон для отпуска отмеривают 82 мл воды очищенной и 18 мл кислоты хлористоводородной разведенной.
2.5.2. Растворы аммиака и кислоты уксусной
Растворы аммиака и кислоты уксусной изготавливают, исходя из фактического содержания лекарственного вещества в стандартном растворе. При расчетах используют формулу разведения:
2.5.3. Растворы алюминия ацетата основного, калия ацетата,
водорода перекиси, формальдегида
При выполнении расчетов для разведения этих стандартных растворов до требуемой концентрации учитывается, под каким (химическим или условным) названием выписан раствор в прописи рецепта.
Если растворы этих веществ выписаны под химическим названием (табл. 1), расчет проводят с учетом их фактического содержания в стандартном растворе, а если под условным названием, то при изготовлении стандартный раствор принимают за единицу (100%).
Для изготовления разведенных растворов формальдегида и водорода перекиси разрешается использовать формалин с содержанием формальдегида менее 36,5% и раствор пергидроля с содержанием водорода перекиси более 30%.
При расчетах разницу концентраций учитывают с помощью коэффициента пересчета (КП).
В аптеку поступил раствор с концентрацией формальдегида 34%.
Пример 9. Rp.: Solutionis Formaldehydi 5% — 200 ml
Раствор выписан под химическим названием.
Количество миллилитров стандартного раствора формальдегида (X), требуемое для разведения, рассчитывают по формуле с учетом его фактического (34%) содержания в растворе:
Воды очищенной — 170,6 мл (200 — 29,4) мл
Пример 10. Rp.: Solutionis Formalini 5% — 200 ml
Раствор выписан под условным названием. При расчетах стандартный раствор принимают за единицу (100%).
Стандартного раствора формальдегида (36,5 — 37,5%) следует взять 10 мл и 190 мл воды очищенной.
В случае использования раствора формальдегида 34% величина КП равна 1,08 (37:34). Рассчитанное количество стандартного 34% раствора формальдегида умножают на 1,08 (10 x 1,08), т.е. следует взять 11 мл этого раствора и 189 мл воды очищенной.
В аптеку поступил пергидроль с концентрацией водорода перекиси 40%.
Пример 11. Rp.: Solutionis Hydrogenii peroxydi 20% — 100 ml
Раствор выписан под химическим названием. Количество граммов пергидроля 40% (X), требуемое для разведения, вычисляют по формуле:
Отвешивают 50 г пергидроля 40% и добавляют воду очищенную до получения 100 мл раствора.
Пример 12. Rp.: Solutionis Perhydroli ex 20,0 — 100 ml
Раствор выписан под условным названием. Для изготовления выписанного раствора следует взять 20 г стандартного раствора пергидроля и воды очищенной до 100 мл. При изготовлении из пергидроля 40% концентрации последнего следует взять меньше. Величина КП равна 0,75 (30:40), т.е. 15 г (20 x 0,75).
Отвешивают 15 г пергидроля 40% концентрации и добавляют воду очищенную до 100 мл.
При дозировании пергидроля по объему необходимо сделать расчеты с учетом его плотности (Приложение 2).
При изготовлении внутриаптечной заготовки раствора водорода перекиси 3% следует добавлять стабилизатор натрия бензоат в количестве 0,05%.
Если в прописи рецепта концентрация раствора не указана, то отпускают растворы:
2.6. Изготовление жидких лекарственных форм, содержащих
ароматные воды
Ароматные воды изготавливают и хранят в соответствии с требованиями действующей нормативной документации (Приложение 10).
Ароматные воды дозируют по объему. При растворении твердых лекарственных веществ объем воды ароматной, выписанный в рецепте, не уменьшают на величину изменения объема.
В случае точного указания объема воды ароматной в прописи рецепта, изменение объема при растворении твердых лекарственных веществ учитывают при контроле качества изготовленной лекарственной формы. При расчете общего объема используют значения КУО лекарственных веществ (Приложение 9).
При изготовлении микстур, в которых основной дисперсионной средой является вода ароматная, концентрированные растворы лекарственных веществ не используют.
В прописи рецепта указан точный объем воды мятной и не указан общий объем микстуры, который учитывают при контроле. В этом случае общий объем (238,6 мл) определяют суммированием объемов всех жидких компонентов, выписанных в прописи (230 мл), и прироста объема (8,6 мл) при растворении 11,11 г глюкозы с учетом содержания кристаллизационной воды (11,11 x 0,69) и 4 г калия иодида (4 x 0,23).
В подставку отмеривают 200 мл воды мятной, растворяют при перемешивании 11,11 г глюкозы и 4 г калия иодида.
Раствор фильтруют во флакон для отпуска. Добавляют при перемешивании 10 мл сиропа сахарного, 5 мл адонизида (сильнодействующее средство, содержание спирта 18 — 20%), 10 мл настойки валерианы (концентрация спирта 70%), 5 мл настойки мяты (концентрация спирта 90%).
Точный объем воды мятной в прописи рецепта не указан, а общий объем микстуры указан. В этом случае объем воды ароматной определяют, вычитая из общего объема (200 мл) объемы всех жидких компонентов (30 мл) и прирост объема при растворении глюкозы и калия иодида.
Объем воды мятной для изготовления микстуры составит 161,4 мл (200-5-5-10-10-8,6).
Особенности изготовления некоторых растворов представлены в Приложении 14.
2.7. Расчеты и правила дозирования спирта различной
концентрации при изготовлении лекарственных форм
для внутреннего и наружного применения
Выписанное в рецепте количество спирта соответствует объемным единицам измерения.
При разведении спирта используют таблицы, приведенные в действующей ГФ и в настоящей Инструкции (Приложения 10, 11).
Норма отпуска спирта учетной концентрации в пересчете на массу составляет 50 г. В случае указания в рецепте «По специальному назначению» — не более 100 г. Для учета спирта по массе используют таблицы (Приложение 12, таблицы 1 — 11).
При изготовлении лекарственных форм спирт дозируют по объему, не уменьшая объем, указанный в рецепте, на величину его прироста при растворении лекарственных веществ.
Общий объем учитывают при контроле качества лекарственной формы.
Изменение объема при растворении лекарственных веществ, учитываемое при контроле, рассчитывают, используя значения КУО лекарственных веществ (Приложение 9).
При изготовлении стандартных спиртовых растворов используют спирт в концентрации, указанной в нормативной документации (Приложение 3).
Если в прописи рецепта без указания концентрации выписан раствор, представленный в нормативной документации несколькими концентрациями лекарственного вещества, отпускают раствор с меньшей концентрацией, т.е. растворы:
Во флакон для отпуска отвешивают 3 г новокаина, 2,5 г анестезина и 1 г ментола, отмеривают 50 мл спирта 90%.
Общий объем раствора с учетом прироста объема при растворении лекарственных веществ равен 55,6 мл. Отклонение в объеме превышает норму допустимого отклонения (+/- 4%), что учитывают при контроле раствора.
В прописи не указан объем спирта, указан объем спиртового раствора новокаина.
Максимальная концентрация новокаина, при которой изменение объема укладывается в норму допустимого отклонения (+/- 4%), составляет 4,97% (4:0,81).
В прописи рецепта выписан 6% раствор новокаина (3 г вещества в 50 мл раствора).
Следовательно, чтобы получить указанный в прописи рецепта объем раствора новокаина (КУО 0,81 мл/г), следует взять 47,6 мл 90% спирта (50 — 3 x 0,81).
После растворения ментола и анестезина в 47,6 мл 90% спирта общий объем раствора будет равен 53,2 мл, (50 мл раствора новокаина и прирост объема 3,2 мл при растворении ментола (1 x x 1,1) и анестезина (2,5 x 0,85).
Отклонение общего объема также не укладывается в норму допустимого отклонения (+/- 4%), что необходимо учитывать при контроле.
В 70 мл 70% спирта содержится 51,04 мл 96% спирта, что по массе составляет 41,23 (Приложения 11, 12, табл. 2), поэтому лекарственная форма подлежит изготовлению (норма отпуска 50 г спирта учетной концентрации не превышена).
Общий объем препарата после растворения лекарственных веществ — 74,97 мл, что превышает норму допустимого отклонения (+/- 3%), поэтому изменение объема учитывают при анализе.
В рецепте не указан объем спирта. Указан общий объем лекарственной формы. Объем 96% спирта определяют, вычитая из общего объема лекарственной формы объемы, занимаемые дегтем и маслом касторовым (Приложение 1), а также изменение объема, возникающее при растворении анестезина и кислоты борной (Приложение 9), т.к. оно не укладывается в норму допустимого отклонения.
2,5 г масла касторового занимают объем 2,6 мл (2,5:0,958); 5 г дегтя — 5,3 мл (5:0,938); изменение объема при растворении анестезина — 1,7 мл (2 x 0,85), кислоты борной — 0,97 мл (1,5 x x 0,65). Всего — 10,6 мл.
Объем 96% спирта составляет 39,4 мл.
В предварительно взвешенный флакон для отпуска отвешивают касторовое масло и деготь, добавляют заранее изготовленный спиртовой раствор анестезина и борной кислоты в 39,4 мл 96% спирта.
2.8. Изготовление лекарственных форм, содержащих
водные извлечения
Водные извлечения (настои и отвары) изготавливают в соответствии с требованиями действующей ГФ экстракцией лекарственного растительного сырья водой очищенной, а также растворением сухих или жидких экстрактов (концентратов) в рассчитанном объеме воды очищенной.
Запрещается изготовление в аптеках и использование водных извлечений заведомо более высокой концентрации с целью последующего разбавления, так как при изготовлении концентрированных извлечений из сырья не достигается полнота экстракции биологически активных веществ.
При изготовлении настоев и отваров запрещается заменять лекарственное растительное сырье настойками, эфирными маслами и экстрактами, не предназначенными для изготовления водных извлечений.
При расчете требуемого для экстракции объема воды очищенной и количества сырья используют значения коэффициентов водопоглощения или расходных коэффициентов (Приложение 13).
При изготовлении водных извлечений обеспечивают оптимальные условиях экстракции, учитывая стандартность лекарственного растительного сырья; его измельченность и гистологическую структуру; соотношение массы сырья и объема экстрагента; физико-химические свойства действующих и сопутствующих веществ; материал аппаратуры и другие факторы, влияющие на качество водного извлечения.
Изготовленные водные извлечения после отжатия сырья и фильтрования доводят водой очищенной до объема, указанного в прописи рецепта.
Галеновые и новогаленовые лекарственные средства следует добавлять к изготовленному водному извлечению в последовательности, изложенной в пункте 2.1.
2.8.1. Многокомпонентные водные извлечения
из лекарственного растительного сырья, требующего
одинаковых условий экстракции
Водные извлечения из лекарственного растительного сырья, требующего одинакового режима экстракции, обусловленного физико — химическими свойствами действующих и сопутствующих веществ, изготавливают в одном инфундирном стакане без учета гистологической структуры сырья.
Измельченное растительное сырье (10 г корневищ с корнями валерианы и 4 г листьев мяты) помещают в перфорированный цилиндр инфундирного стакана, заливают 238 мл воды очищенной. Объем воды для экстракции рассчитывают по формуле:
где: V — объем воды очищенной, взятой для экстракции, мл;
V1 — объем водного извлечения, указанный в прописи рецепта, мл;
М1 — масса корневищ с корнями валерианы, взятая для экстракции, г;
М2 — масса листьев мяты, взятая для экстракции, г;
Кв1 — коэффициент водопоглощения корневищ с корнями валерианы, 2,9 мл/г;
Кв2 — коэффициент водопоглощения листьев мяты, 2,4 мл/г.
Инфундирный стакан плотно закрывают крышкой, помещают в инфундирный аппарат и настаивают на кипящей водяной бане 15 мин., не открывая крышку инфундирного стакана. Охлаждают при комнатной температуре не менее 45 мин. Фильтруют, отжимают сырье, измеряют объем изготовленного настоя и, при необходимости, доводят водой объем до 200 мл.
2.8.2. Многокомпонентные водные извлечения
из лекарственного растительного сырья, требующего различных
условий экстракции
Изготавливают раздельно, используя для экстракции максимально возможный объем воды очищенной, но не менее, чем 10-кратный по отношению к массе сырья.
В состав прописи входят виды сырья, требующие различных режимов экстракции:
— корни алтея — настаивания при комнатной температуре;
— корневища с корнями валерианы, трава пустырника и листья мать-и-мачехи — настаивания по общим правилам, регламентированным действующей ГФ;
— кора калины — изготовления отвара по общим правилам ГФ.
Для максимального извлечения полисахаридов слизистой природы из 10 г корней алтея изготавливают 200 мл водного извлечения 5% концентрации.
Массу сырья и объем воды очищенной рассчитывают с учетом расходного коэффициента (К расх). Значения К расх для различных концентраций настоя корней алтея представлены в Приложении 14.
Для 5% настоя корня алтея К расх = 1,3; масса сырья — 13 г (10 г x 1,3); объем воды очищенной — 260 мл (200 x 1,3).
Отвар коры калины изготавливают в соотношении 1 : 10, т.е. из 25 г коры — 250 мл отвара. Объем воды для экстракции коры калины с учетом коэффициента водопоглощения (2 мл/г) — 300 мл (250 + 25 x x 2). Настои корневищ с корнями валерианы, травы пустырника и листьев мать-и-мачехи изготавливают в объеме 550 мл (1000 — 200 — — 250). Объем воды очищенной для экстракции составляет 673 мл (550 + 8 x 2,9 + 20 x 2 + 20 x 3).
Все три извлечения изготавливают отдельно, доводят водой очищенной до требуемого объема: 200 мл, 250 мл и 550 мл соответственно и затем объединяют.
2.8.3. Лекарственные формы, содержащие водные
извлечения из сырья и твердые вещества, растворимые
в водных извлечениях
При изготовлении водных извлечений из сырья использование концентрированных растворов лекарственных веществ не допускается. Твердые лекарственные вещества растворяют в готовом водном извлечении при перемешивании и фильтруют во флакон для отпуска через тот же фильтр, который использовался для фильтрования водного извлечения. При необходимости объем лекарственной формы доводят водой очищенной до указанного в прописи.
Изготовленный настой фильтруют в подставку (изготовление настоя см. пример 19), растворяют 0,4 г кофеина-натрия бензоата, 3 г натрия бромида, 0,8 г магния сульфата при перемешивании и фильтруют во флакон для отпуска, как было указано выше.
Объем микстуры после растворения лекарственных веществ увеличился на 1,44 мл (Приложение 9), что укладывается в норму допустимого отклонения (+/- 2%) и при ее контроле не учитывается.
Изменение объема при растворении анальгина, калия бромида и натрия бромида составляет 5,5 мл (5 x 0,68 + 4 x 0,27 + 4 x 0,26), не укладывается в норму допустимого отклонения. Суммарная концентрация растворенных веществ более 3%. Поэтому объем воды, который необходимо взять для изготовления настоя, рассчитывают с учетом коэффициента водопоглощения травы пустырника и изменения объема микстуры при растворении твердых веществ.
Для изготовления настоя 20 г измельченной травы пустырника заливают 234,5 мл воды очищенной (200 + 20 x 2 — 5,5), настаивают по общим правилам технологии и фильтруют. В полученном водном извлечении растворяют лекарственные вещества и вновь фильтруют.
Измеряют объем фильтрата, при необходимости доводят его водой очищенной до 200 мл и добавляют 6 мл настойки валерианы.
Общий объем изготовленной микстуры равен 206 мл.
2.8.4. Изготовление водных извлечений
из экстрактов (концентратов)
Экстракты (концентраты) — стандартизованные сухие (1:1) и жидкие (1:2) вводят в состав жидких лекарственных форм по правилам растворения твердых лекарственных средств (пункт 2.8.3) и введения галеновых и новогаленовых лекарственных средств (пункт 2.1).
2.8.5. Изготовление водных извлечений при совместном
использовании лекарственного растительного сырья
и экстрактов (концентратов)
см. Пример 20.
Микстуру изготавливают, используя экстракт алтея сухой (1:1), экстракты (концентраты) валерианы и пустырника жидкие (1:2) и лекарственное растительное сырье (листья мать-и-мачехи и кору калины).
Учитывая, что жидкого экстракта валерианы следует взять 16 мл, а жидкого экстракта пустырника — 40 мл, водное извлечение из сырья должно быть изготовлено в объеме 944 мл.
Для обеспечения раздельной экстракции объемы извлечений устанавливают пропорционально выписанной массе сырья: из 25 г коры калины изготавливают 524 мл отвара; из 20 г листьев мать-и-мачехи — 420 мл настоя.
Объем воды очищенной для изготовления отвара коры калины составит 574 мл (524 + 25 x 2); для изготовления настоя листьев мать-и-мачехи — 480 мл (420 + 20 x 3).
Режимы экстракции регламентируются действующей ГФ.
После объединения изготовленных водных извлечений в них растворяют 10 г экстракта алтея сухого (изменение объема укладывается в норму допустимого отклонения), фильтруют во флакон для отпуска, добавляют 16 мл экстракта валерианы и 40 мл экстракта пустырника.
Общий объем микстуры составляет 1000 мл (524 + 420 + 16 + 40).
2.8.6. Лекарственные формы, содержащие водные
извлечения из лекарственного растительного сырья,
экстрактов (концентратов) и твердые растворимые
лекарственные вещества
см. Пример 21.
Учитывая то, что при изготовлении лекарственной формы может быть использован жидкий экстракт (концентрат) валерианы (1:2) — 20 мл, из 4 г листьев мяты изготавливают 180 мл настоя по общим правилам ГФ.
Объем воды очищенной для изготовления водного извлечения из листьев мяты составит 189,6 мл (180 + 4 x 2,4).
В изготовленном настое растворяют твердые лекарственные вещества и после фильтрования непосредственно во флакон для отпуска отмеривают 20 мл жидкого экстракта валерианы.
При изготовлении водных извлечений из экстрактов (концентратов) могут быть использованы концентрированные растворы лекарственных веществ.
см. Пример 22.
При изготовлении лекарственной формы с использованием концентрированных растворов следует учесть изменение объема при растворении анальгина, концентрированный раствор которого отсутствует.
Максимальная концентрация анальгина, при которой изменение объема укладывается в норму допустимого отклонения, составляет 1,47%, а концентрация анальгина в прописи — 2,43%.
В подставку отмеривают 116,6 мл воды очищенной (120 — 5 x x 0,68) и растворяют 5 г анальгина. Раствор фильтруют во флакон для отпуска и добавляют 20 мл 20% раствора калия бромида, 20 мл 20% раствора натрия бромида, 40 мл экстракта (концентрата) пустырника жидкого (1:2) и 6 мл настойки валерианы.
Общий объем микстуры — 206 мл.
2.9. Некоторые особенности изготовления суспензий
и эмульсий
Суспензии и эмульсии для внутреннего, наружного и парентерального применения изготавливают в соответствии с требованиями действующей ГФ.
Суспензии с содержанием нерастворимых твердых лекарственных веществ 3% и более, а также эмульсии независимо от концентрации веществ изготавливают по массе, концентрированные растворы водорастворимых лекарственных веществ при изготовлении суспензий не используют.
Во флакон для отпуска известной массы предварительно отвешивают 30 г глицерина. В ступке измельчают цинка окись, добавляют тальк и около 20 г глицерина из флакона для отпуска. Смесь тщательно перемешивают и постепенно, небольшими порциями, добавляют воду очищенную, смывая суспензию во флакон для отпуска.
Масса суспензии — 170 г.
В ступке измельчают 3 г стрептоцида, 7 г серы с 5 г глицерина, добавляют 12,5 мл воды очищенной и смесь перемешивают. К смеси частями добавляют 37,5 мл 4% раствора кислоты борной (1,5 г), смывая содержимое ступки во флакон для отпуска известной массы. В последнюю очередь добавляют предварительно изготовленный раствор кислоты салициловой и камфоры в 50 мл 90% спирта, содержимое флакона перемешивают и тщательно укупоривают.
Масса суспензии составляет 112,41 г, т.к. масса 50 мл 90% спирта — 41,46 г (плотность — 0,829 г/мл); масса 37,5 мл 4% раствора кислоты борной — 37,95 г (плотность — 1,010 г/мл).
Состав и изготовление эмульсии бензилбензоата см. Приложение 15.
3. КОНЦЕНТРИРОВАННЫЕ РАСТВОРЫ
3.1. Общие положения
Концентрированные растворы (концентраты) — заранее изготовленные растворы лекарственных веществ более высокой концентрации, чем концентрация, в которой эти вещества выписываются в рецептах.
К концентратам относят также концентрированные экстракты из некоторых лекарственных растений, изготовленные на фармацевтических производственных предприятиях: экстракты (концентраты) валерианы, горицвета, пустырника и др.
Концентраты предназначены для быстрого и качественного изготовления жидких лекарственных форм.
Рекомендуется изготавливать концентраты из веществ гигроскопичных, выветривающихся, содержащих значительное количество кристаллизационной воды.
Номенклатура концентрированных растворов определяется спецификой рецептуры и объемом работы аптеки и утверждается в соответствии с требованиями действующей Инструкции.
Концентраты изготавливают по мере необходимости, с учетом срока их годности.
Перечень концентрированных растворов и ряда жидких лекарственных средств, рекомендованных для использования при изготовлении в аптеках жидких лекарственных форм (в том числе применяемых в глазной практике), условия их хранения и сроки годности приведены в Приложениях 4 — 6.
Концентрированные растворы изготавливают массо-объемным методом в мерной посуде в асептических условиях в соответствии с требованиями действующей Инструкции, используя свежеполученную воду очищенную.
В случае отсутствия мерной посуды объем воды очищенной рассчитывают, используя значение плотности концентрата или коэффициент, соответствующий увеличению его объема при растворении 1 г лекарственного вещества (Приложения 7, 9).
Изготовленные растворы фильтруют, подвергают полному химическому контролю и проверяют на отсутствие механических включений.
При изготовлении концентрированных растворов следует избегать концентраций, близких к насыщенным, т.к. при понижении температуры возможна кристаллизация растворенного вещества.
Отклонение в концентрации растворов допускается в пределах:
— до 20% концентрации раствора (включительно) — не более +-2%;
— более 20% концентрации раствора — не более +-1%.
В случае превышения нормы допустимого отклонения производят исправление концентрации раствора (см. п. 3.3).
Емкости с концентрированными растворами оформляют этикетками с указанием наименования и концентрации раствора, номера серии и анализа, даты изготовления, срока годности.
Концентрированные растворы хранят в соответствии с физико — химическими свойствами лекарственных веществ, входящих в их состав, в простерилизованных, плотно укупоренных емкостях (баллонах, штангласах), в защищенном от света месте, при температуре 3 — 5° C или не выше 25° C (Приложения 4 — 6).
Изменение цвета, помутнение, появление хлопьев, налетов ранее установленного срока годности являются признаками непригодности растворов.
3.2. Расчеты при изготовлении концентрированных растворов
3.2.1. Расчет массы лекарственного вещества
Требуется изготовить 1 л 50% раствора глюкозы.
Для изготовления 1 л 50% раствора необходимо взять 500 г глюкозы. Однако глюкозу следует брать в большем количестве, с учетом содержания в ней 10% влаги.
Расчет производят по формуле:
555,55 г глюкозы с влажностью 10% помещают в мерную емкость и растворяют в части горячей воды при перемешивании. После охлаждения объем раствора доводят водой очищенной до 1 л и фильтруют.
3.2.2. Расчет объема воды с использованием значения
плотности раствора или КУО
Требуется изготовить 1 л 50% раствора кальция хлорида.
Плотность 50% раствора кальция хлорида 1,207 г/мл, и 1 л этого раствора имеет массу 1207 г (1000 x 1,207).
Масса кальция хлорида для изготовления 1 л раствора — 500 г, следовательно, масса воды составит 707 г (1207 — 500) или 707 мл при плотности воды очищенной 1 г/мл.
КУО для кальция хлорида — 0,58 мл/г. При растворении 500 г этого вещества объем раствора увеличивается на 290 мл (500 x x 0,58). Поэтому для изготовления 1 л 50% раствора кальция хлорида следует взять 710 мл воды очищенной (1000 — 290).
3.3. Исправление концентрации растворов
3.3.1. Концентрация раствора оказалась выше требуемой.
Объем воды, необходимый для разбавления полученного раствора, вычисляют по формуле:
где X — объем воды, необходимый для разбавления полученного раствора, мл;
A — объем изготовленного раствора, мл;
C — фактическая концентрация раствора, % ;
B — требуемая концентрация раствора, %.
Например, при анализе установлено, что концентрация раствора калия бромида 23% вместо 20%.
т.е. к 1 л 23% раствора калия бромида следует добавить 150 мл воды очищенной для получения 20% раствора.
После исправления концентрации общий объем раствора будет равен 1150 мл.
3.3.2. Концентрация раствора оказалась ниже требуемой
Массу лекарственного вещества для укрепления полученного раствора вычисляют по формуле:
где: X — масса вещества, которую следует добавить к раствору, г;
A — объем изготовленного раствора, мл;
B — требуемая концентрация раствора, %;
C — фактическая концентрация раствора, %;
p — плотность раствора при 20° C, г/мл.
Например, при анализе установлено, что концентрация раствора калия бромида составляет 18% вместо 20%.
После растворения 21,19 г калия бромида объем раствора увеличился на 5,7 мл (КУО — 0,27 мл/г) и стал равен 1005,7 мл.
В случае укрепления растворов глюкозы расчеты проводят с учетом % влажности.
Концентрированные растворы после их разбавления или укрепления следует проанализировать повторно.
4. АПТЕЧНЫЕ БЮРЕТОЧНЫЕ УСТАНОВКИ И МЕРНАЯ ПОСУДА
При изготовлении жидких лекарственных форм массо-объемным методом используют мерную посуду, градуированную на «налив» (мерные колбы, цилиндры, мензурки, градуированные пробирки) и на «вылив» (аптечные бюретки, каплемеры и пипетки) и откалиброванную в соответствии с ГОСТом.
4.1. Общие правила работы с аптечными бюретками и пипетками
В аптеках выделяют фармацевта, контролирующего состояние и правильную эксплуатацию аптечных бюреток, пипеток и каплемеров в соответствии с Положением о ведомственном надзоре за измерительными приборами в системе МЗ РФ, положениями настоящей Инструкции и Инструкции по санитарному режиму аптек.
Перед сборкой все резиновые и стеклянные детали бюреток, пипеток и каплемеров тщательно моют и дезинфицируют в соответствии с требованиями действующей Инструкции.
Аптечные бюретки, пипетки и каплемеры моют по мере надобности, но не реже 1 раза в 10 дней. Для этого их освобождают от жидкостей, моют горячей водой (50 — 60° C), взвесью горчичного порошка или 3% раствором водорода перекиси с добавлением 0,5% моющих, дезинфицирующих и моюще-дезинфицирующих средств, разрешенных для применения в аптечной практике; промывают водой водопроводной и очищенной, с обязательным контролем на полноту смывания моющих средств (в соответствии с нормативной документацией).
Перед началом работы сливные краны, концы бюреток и пипеток очищают от налета солей, настоек, экстрактов и протирают спирто-эфирной смесью (1:1).
Заполняют питающие сосуды в бюреточной установке концентрированными растворами, настойками, экстрактами (концентратами), предназначенными для изготовления водных извлечений. Проверяют правильность их заполнения путем качественного химического анализа в соответствии с требованиями действующей Инструкции.
Малые объемы жидкостей отмеривают бюретками и пипетками с малым диаметром.
Уровень бесцветных жидкостей в бюретках и пипетках устанавливают по нижнему мениску, окрашенных — по верхнему.
Слив жидкостей из пипеток и бюреток производят полностью, после полного стекания жидкости выжидают еще 2 — 3 секунды.
Отмеривание жидкости по разности делений не допускается. Вязкие и летучие жидкости не отмеривают по объему во избежание большой ошибки дозирования.
Не разрешается использовать бюретки, пипетки и каплемеры с отломанными концами, а также с плохо смачивающейся внутренней поверхностью стенок.
Малые количества жидких лекарственных средств (менее 1 мл или 1 г) дозируют каплями. При отсутствии стандартного каплемера (ГФ) последний может быть заменен эмпирическим каплемером — пипеткой, откалиброванной путем пятикратного взвешивания 20 капель соответствующего жидкого лекарственного средства.
На этикетке штангласа (флакона) с прикрепленным каплемером следует указать наименование лекарственного средства, число капель в 1 мл или 1 г и соответствие 1 капли стандартного каплемера числу капель нестандартного.
4.2. Аптечные пипетки
Аптечные пипетки предназначены для отмеривания небольших объемов жидкости — от 1 до 15 мл.
Выпускаются вместимостью 3, 6, 10 и 15 мл.
Штангласы к ним — 100 и 250 мл и резиновые баллончики — 7,5; 15 и 30 мл.
Таблица 2
Устройство аптечной пипетки
Пипетка состоит из:
— стеклянной градуированной трубки, суженной книзу;
— стеклянного шара с двумя тубусами (верхним и боковым);
— резинового баллончика, надетого на верхний тубус стеклянного шара;
— резиновой трубки с бусинкой или пробкой, надетой на боковой тубус.
Пипетка крепится в горловине штангласа с помощью прокладки (резинового кольца) и не должна доходить до дна штангласа на 3 — 5 мм.
Для наполнения пипетку слегка приподнимают над штангласом и сжимают резиновый баллончик.
Не допускается попадание жидкости в баллончик во избежание загрязнения.
Для установления мениска на необходимом уровне пользуются боковым тубусом, нажимая резиновую трубку у бусинки.
Жидкость из пипетки выливают сплошной струей, сжимая резиновый баллончик, опустив кончик пипетки в горлышко флакона для отпуска.
4.3. Аптечные бюретки с 2-ходовым краном и бюреточные
установки с механическим приводом
Аптечные бюретки выпускаются вместимостью 10, 25, 60, 100, 200 мл.
Бюретки монтируются на специальных установках — вертушках (на 20, 16 и 8 бюреток) или на специальных штативах.
При сборке и эксплуатации бюреточных установок следует руководствоваться инструкцией, прилагаемой к ним.
Высота всех бюреток независимо от вместимости — 450 мм при соответственно различном диаметре (12 — 32 мм), в этом случае середина шкалы бюреток, смонтированных на вертушке, находится на уровне глаз фармацевта, работающего сидя, что позволяет уменьшить ошибку при дозировании.
Жидкие лекарственные средства отмеривают, контролируя требуемый объем визуально по шкале бюретки.
4.3.1. Бюретки с 2-ходовым краном выпускаются в 4 наборах. Комплекты N 1 — 3 могут быть использованы для фасовки жидкостей. Набор N 4 используется для дозирования воды.
Бюретки с 2-ходовым краном монтируются на специальном штативе и через питающую трубку соединяются с питающим сосудом. Нулевая отметка бюретки находится на уровне крана. Проходные отверстия в штоке крана расположены под углом 90° C.
Открытую верхнюю часть бюретки закрывают стеклянным колпачком, а баллон с водой — стеклянной пробкой.
Для наполнения бюретки 2-ходовой кран ставят в положение наполнения бюретки (окрашенным концом ручки крана вверх). Для слива отмеренного объема жидкости кран переводят в положение слива из бюретки (окрашенным концом ручки крана вниз).
Если жидкость подтекает через закрытый кран бюретки, следует произвести его шлифовку.
Материалом для шлифовки служат: очень тонкий наждак (грубый наждак может дать царапины), цинка оксид, тонко размолотый алюминия оксид.
Перед шлифовкой пробку крана и муфту очищают, смачивая водой или 10% раствором камфоры в скипидаре и покрывают одним из указанных порошков для шлифовки. Пробку крана вставляют в муфту и быстро вращают то в одну, то в другую сторону, вынимая и снова вставляя. При остановке вращения пробку из муфты обязательно вынимают.
Хорошо притертый шлиф не мутный, а почти прозрачный.
Для кранов используют летнюю и зимнюю смазки следующего состава (в частях):
Смазку изготавливают, сплавляя составные части в выпарительной чашке на водяной бане, процеживают через двойной слой марли в банку с плотно навинчивающейся крышкой.
4.3.2. Бюреточная установка с механическим приводом
Установка состоит из металлической вертушки на опорной стойке в виде треноги. По окружности вертушки размещено 16 полиэтиленовых питающих сосудов вместимостью 1 л, стеклянных соединительных трубок и градуированных бюреток.
Каждая бюретка и питающая трубка крепятся в гнездах соответствующего крана с помощью резиновых уплотнительных колечек (втулок) и резьбовых колпачков (штуцеров). Каждый кран имеет два диафрагменных клапана — заполняющий и сливной.
Клапанами управляют с помощью двух механических тросиковых приводов с пружинными захватами, нажимая на клавиши «наполнение» или «слив», смонтированные на основании треноги вертушки.
Бюреточную установку на рабочем месте располагают таким образом, чтобы клавиши управления располагались справа.
При работе вертушку поворачивают и фиксируют с помощью специального фиксатора так, чтобы штоки клапанов диафрагменного крана соответствующей бюретки расположились напротив пружинных захватов рычажно-тросиковых приводов.
При нажатии на клавишу «наполнение» один из пружинных захватов оттягивает шток клапана наполнения. Шток оттягивает диафрагму, открывая сообщение между бюреткой и питающей трубкой. Бюретка заполняется жидкостью до необходимого объема.
При нажатии на клавишу «слив» другой пружинный захват тросикового привода оттягивает шток диафрагмы сливного клапана. Диафрагма оттягивается. Жидкость сливается во флакон.
Диафрагма клапана наполнения в это время плотно закрывает сообщение бюретки с питающей трубкой.
Перед эксплуатацией бюреточную установку вытирают от пыли и антикоррозийного покрытия, проверяют работу фиксатора. Вертушка должна двигаться плавно и хорошо фиксироваться при попадании шарика в отверстие. При необходимости регулирования используют гайку фиксатора.
Проверяют работу системы управления кранами. Винты на кранах при вращении вертушки должны свободно проходить через скобы пружинных захватов системы управления. В фиксированном положении между винтами и скобами должен быть просвет 1 — 3 мм.
В зафиксированном положении винты кранов должны останавливаться строго против соответствующих скоб пружинного захвата системы управления. Нарушение совпадения оси винта крана с осью скобы захвата регулируют с помощью болта закрепления кронштейна.
Открытие кранов производится при помощи тросиков, натяжением ручек управления. В рабочем режиме тросик должен находиться в натянутом положении и плавно двигаться в блоках при нажатии ручки управления. Необходимая степень натяжения тросика регулируется с помощью специального винта и гайки.
Если перемещение ручки системы управления до конца не обеспечивает полного открытия крана, о чем свидетельствует медленное наполнение бюретки и выливание жидкости из крана, необходимо завинтить опорную планку или дополнительно натянуть тросик.
Для надежной работы бюреточной установки и ее длительной эксплуатации необходимо периодически при сборке бюреточной установки после мойки закапывать вазелиновое масло на концы штоков клапанов кранов, куда ввернуты винты с полиэтиленовыми головками. При выполнении этой операции следует нажимать на клавиши механического привода для того, чтобы концы штоков вышли из отверстий корпуса крана. Смазка предохраняет штоки от коррозии и кристаллизации остатков лекарственных средств на концах штоков.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 1
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
ЗНАЧЕНИЯ ПЛОТНОСТИ НЕКОТОРЫХ ЖИДКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 2
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
СООТНОШЕНИЕ
МЕЖДУ ПЛОТНОСТЬЮ И КОНЦЕНТРАЦИЕЙ ВОДОРОДА ПЕРЕКИСИ
В РАСТВОРЕ
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 3
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
ПЕРЕЧЕНЬ
СТАНДАРТНЫХ СПИРТОВЫХ РАСТВОРОВ, РАЗРЕШЕННЫХ К ИЗГОТОВЛЕНИЮ
В АПТЕКЕ В СООТВЕТСТВИИ С ДЕЙСТВУЮЩЕЙ
НОРМАТИВНОЙ ДОКУМЕНТАЦИЕЙ
———————————
<*> Здесь и далее указана новая нормативная документация.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 4
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
СПИСОК
КОНЦЕНТРИРОВАННЫХ РАСТВОРОВ И ЖИДКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ,
РЕКОМЕНДУЕМЫХ ДЛЯ ОТМЕРИВАНИЯ ИЗ БЮРЕТОК
———————————
<*> Хранить в защищенном от света месте.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 5
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
СПИСОК
РАСТВОРОВ И ЖИДКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ, РЕКОМЕНДУЕМЫХ
ДЛЯ ОТМЕРИВАНИЯ ИЗ АПТЕЧНЫХ ПИПЕТОК
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 6
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
СПИСОК
КОНЦЕНТРИРОВАННЫХ РАСТВОРОВ, РЕКОМЕНДУЕМЫХ ДЛЯ ИЗГОТОВЛЕНИЯ
ГЛАЗНЫХ КАПЕЛЬ
Примечание. Вскрытые флаконы с концентратами для глазных капель должны быть использованы в течение суток.
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 7
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
ДАННЫЕ
ДЛЯ ИЗГОТОВЛЕНИЯ 1 Л КОНЦЕНТРИРОВАННОГО РАСТВОРА НЕКОТОРЫХ
ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 8
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
СОДЕРЖАНИЕ
СПИРТА В НЕКОТОРЫХ ЖИДКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВАХ
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 9
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
КОЭФФИЦИЕНТЫ УВЕЛИЧЕНИЯ ОБЪЕМА (КУО)
———————————
<*> Суспензия в 30% спирте.
<**> Суспензия в 70, 90, 96% спирте.
Примечание. КУО — коэффициент увеличения объема (КУО) показывает увеличение объема раствора в мл при растворении 1 г лекарственного или вспомогательного вещества при 20° C (мл/г).
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 10
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
КОЛИЧЕСТВА
ВОДЫ ОЧИЩЕННОЙ И СПИРТА ЭТИЛОВОГО КОНЦЕНТРАЦИИ 96,1 — 96,9%
В ГРАММАХ (Г), КОТОРЫЕ НЕОБХОДИМО СМЕШАТЬ ПРИ 20° C, ЧТОБЫ
ПОЛУЧИТЬ 1000 Г ЭТИЛОВОГО СПИРТА КОНЦЕНТРАЦИИ:
30, 40, 50, 60, 70, 80, 90, 95, 96%
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 11
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
КОЛИЧЕСТВА
ВОДЫ ОЧИЩЕННОЙ И СПИРТА ЭТИЛОВОГО КОНЦЕНТРАЦИИ 95,1 — 96,5%
В МИЛЛИЛИТРАХ (МЛ), КОТОРЫЕ НЕОБХОДИМО СМЕШАТЬ ПРИ 20° C,
ЧТОБЫ ПОЛУЧИТЬ 1000 МЛ СПИРТА КОНЦЕНТРАЦИИ:
30, 40, 50, 60, 70, 80, 90, 95%
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 12
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
Таблица 1
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 95% СПИРТА 20° C
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Таблица 2
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96% СПИРТА 20° C
Таблица 3
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,1% СПИРТА 20° C
Таблица 4
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,2% СПИРТА 20° C
Таблица 5
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,3% СПИРТА 20° C
Таблица 6
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,4% СПИРТА 20° C
Таблица 7
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,5% СПИРТА 20° C
Таблица 8
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,6% СПИРТА 20° C
Таблица 9
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,7% СПИРТА 20° C
Таблица 10
СООТНОШЕНИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,8% СПИРТА 20° C
Таблица 11
СООТВЕТСТВИЕ ОБЪЕМОВ (МЛ) СПИРТА ЭТИЛОВОГО РАЗЛИЧНОЙ
КОНЦЕНТРАЦИИ МАССЕ (Г) 96,9% СПИРТА 20° C
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 13
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
КОЭФФИЦИЕНТЫ
ВОДОПОГЛОЩЕНИЯ ЛЕКАРСТВЕННОГО РАСТИТЕЛЬНОГО СЫРЬЯ
Примечания. 1. Коэффициент водопоглощения соответствует количеству жидкости (мл), удерживаемому 1,0 г лекарственного растительного сырья после его отжатия в перфорированном стакане инфундирки.
2. Если коэффициент водопоглощения для сырья отсутствует, рекомендуется использовать следующие значения:
3. Расходный коэффициент, используемый при изготовлении настоя корней алтея, показывает, во сколько раз следует увеличить массу сырья и объем экстрагента, чтобы получить заданный объем извлечения необходимой концентрации.
4. Расходные коэффициенты для изготовления настоя корней алтея различной концентрации:
1% — 1,05
2% — 1,10
3% — 1,15
4% — 1,20
5% — 1,30
5. Для настоя корней алтея концентраций более 5% расходный коэффициент рассчитывают по формуле:
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 14
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
ОСОБЕННОСТИ ИЗГОТОВЛЕНИЯ НЕКОТОРЫХ ЖИДКИХ ПРЕПАРАТОВ
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Приложение 15
к Инструкции
по изготовлению в аптеках
жидких лекарственных форм
СОСТАВ ЭМУЛЬСИИ БЕНЗИЛБЕНЗОАТА
Изготовление эмульсии
Прописи 1, 2, 3. В ступке смешивают мыло калийное с соответствующим количеством горячей воды очищенной (I). Постепенно добавляют бензилбензоат, тщательно эмульгируя. Первичную эмульсию разбавляют остальным количеством горячей воды (II). Готовую эмульсию фильтруют через двойной слой марли и после охлаждения массу эмульсии доводят водой до 100,0 г.
Прописи 4, 5. Отдельно в ступке изготавливают раствор мыла калийного с 5,5 мл (10% эмульсия) или 10,5 мл (20% эмульсия) горячей воды очищенной. В фарфоровой чашке расплавляют 1,0 эмульгатора Т-2 и смешивают с 10 мл горячей воды. Оба эмульгатора смешивают в ступке и эмульгируют соответствующее количество бензилбензоата, добавляют оставшееся количество горячей воды очищенной (II) и далее поступают как описано выше (Прописи 1, 2, 3).
Прописи 6,7. Стружку 2 г мыла хозяйственного заливают 18 мл горячей воды (I). Полученным 10% раствором мыла эмульгируют соответствующее количество бензилбензоата и далее поступают, как описано выше (Прописи 1, 2, 3).
Начальник Управления организации
обеспечения лекарствами
и медицинской техникой
Т.Г.КИРСАНОВА
Зарегистрировано в Минюсте России 29 мая 2023 г. N 73564
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРИКАЗ
от 22 мая 2023 г. N 249н
ОБ УТВЕРЖДЕНИИ ПРАВИЛ ИЗГОТОВЛЕНИЯ И ОТПУСКА ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ АПТЕЧНЫМИ ОРГАНИЗАЦИЯМИ, ИМЕЮЩИМИ ЛИЦЕНЗИЮ НА ФАРМАЦЕВТИЧЕСКУЮ ДЕЯТЕЛЬНОСТЬ
В соответствии с частью 1 статьи 56 Федерального закона от 12 апреля 2010 г. N 61-ФЗ «Об обращении лекарственных средств» и подпунктом 5.2.170 пункта 5 Положения о Министерстве здравоохранения Российской Федерации, утвержденного постановлением Правительства Российской Федерации от 19 июня 2012 г. N 608, приказываю:
1. Утвердить прилагаемые правила изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность.
2. Признать утратившим силу приказ Министерства здравоохранения Российской Федерации от 26 октября 2015 г. N 751н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность» (зарегистрирован Министерством юстиции Российской Федерации 21 апреля 2016 г., регистрационный N 41897).
3. Настоящий приказ вступает в силу с 1 сентября 2023 г. и действует до 1 сентября 2029 г.
Министр
М.А. МУРАШКО
УТВЕРЖДЕНЫ
приказом Министерства
здравоохранения
Российской Федерации
от 22 мая 2023 г. N 249н
ПРАВИЛА ИЗГОТОВЛЕНИЯ И ОТПУСКА ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ АПТЕЧНЫМИ ОРГАНИЗАЦИЯМИ, ИМЕЮЩИМИ ЛИЦЕНЗИЮ НА ФАРМАЦЕВТИЧЕСКУЮ ДЕЯТЕЛЬНОСТЬ
I. Общие положения
1. Настоящие правила распространяются на изготовление и отпуск лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность, в том числе по рецептам на лекарственные препараты и по требованиям медицинских организаций (далее соответственно — лекарственные препараты, рецепт, требование).
2. При изготовлении лекарственных препаратов аптечными организациями используются лекарственные препараты и (или) фармацевтические субстанции, включенные в государственный реестр лекарственных средств для медицинского применения <1>, единый реестр зарегистрированных лекарственных средств Евразийского экономического союза <2>.
<1> Статья 33 Федерального закона от 12 апреля 2010 г. N 61-ФЗ «Об обращении лекарственных средств».
<2> Порядок формирования и ведения единого реестра зарегистрированных лекарственных средств Евразийского экономического союза, утвержденный Решением Совета Евразийской экономической комиссии от 3 ноября 2016 г. N 84 «О порядках формирования и ведения единого реестра зарегистрированных лекарственных средств Евразийского экономического союза и информационных баз данных в сфере обращения лекарственных средств», официальный сайт Евразийского экономического союза http://www.eaeunion.org/, 21 ноября 2016 г., вступило в силу 6 мая 2017 г., которое является обязательным для Российской Федерации в соответствии с Договором о Евразийском экономическом союзе от 29 мая 2014 г., ратифицированным Федеральным законом от 3 октября 2014 г. N 279-ФЗ «О ратификации Договора о Евразийском экономическом союзе» (Договор вступил в силу для Российской Федерации 1 января 2015 г.).
3. Изготовление лекарственных препаратов осуществляется в условиях, отвечающих санитарно-эпидемиологическим требованиям <3>.
<3> Санитарные правила СП 2.1.3678-20 «Санитарно-эпидемиологические требования к эксплуатации помещений, зданий, сооружений, оборудования и транспорта, а также условиям деятельности хозяйствующих субъектов, осуществляющих продажу товаров, выполнение работ или оказание услуг», утвержденные постановлением Главного государственного санитарного врача Российской Федерации от 24 декабря 2020 г. N 44 (зарегистрировано Министерством юстиции Российской Федерации 30 декабря 2020 г., регистрационный N 61953), с изменением, внесенным постановлением Главного государственного санитарного врача Российской Федерации от 14 апреля 2022 г. N 12 (зарегистрировано Министерством юстиции Российской Федерации 15 апреля 2022 г., регистрационный N 68213), действующие до 1 января 2027 г.
4. Упаковка изготовленных лекарственных препаратов осуществляется в зависимости от формы и способа применения лекарственного препарата в соответствии с требованиями общей фармакопейной статьи «Упаковка, маркировка и транспортирование лекарственных средств».
II. Система качества изготовления лекарственных препаратов
5. Изготовление лекарственных препаратов надлежащего качества в аптечной организации осуществляется посредством реализации комплекса мероприятий, направленных на соблюдение требований настоящих Правил (далее — система качества) и включающих в том числе:
а) установление последовательности и взаимодействия процессов, необходимых для обеспечения системы качества, в зависимости от их влияния на безопасность, эффективность и рациональность при изготовлении лекарственных препаратов;
б) определение критериев и методов, отражающих достижение результатов, как при осуществлении процессов, необходимых для обеспечения системы качества, так и при управлении ими с учетом требований законодательства Российской Федерации об обращении лекарственных средств;
в) определение количественных и качественных параметров, в том числе материальных, финансовых, информационных, трудовых, необходимых для поддержания процессов системы качества и их мониторинга;
г) обеспечение населения качественными, безопасными и эффективными лекарственными препаратами;
д) принятие мер, необходимых для достижения запланированных результатов и постоянного улучшения качества изготовления лекарственных препаратов и повышения персональной ответственности работников аптечной организации.
6. С целью организации системы качества изготовления лекарственных препаратов руководитель аптечной организации утверждает:
а) приказы и распоряжения руководителя аптечной организации по основной деятельности;
б) документы, регламентирующие исполнение процедур, в которых описан порядок выполнения производственных операций (далее — стандартные операционные процедуры);
в) документы, содержащие требования и методы определения качества изготовленного лекарственного препарата (далее — документы в области контроля качества).
7. Стандартные операционные процедуры разрабатываются в соответствии с требованиями фармакопейных статей и общих фармакопейных статей.
Стандартные операционные процедуры регламентируют последовательность действий фармацевтического работника при осуществлении изготовления, в том числе в виде внутриаптечной заготовки, упаковке и фасовке лекарственных препаратов, очистки и дезинфекции оборудования, стерилизации лабораторной посуды, уборки и дезинфекции помещений, проведении проверки при обнаружении недоброкачественных, контрафактных и фальсифицированных лекарственных средств, при ведении записей, отчетов и их хранения.
Руководителем аптечной организации назначается работник аптечной организации, ответственный за внедрение и обеспечение системы качества, который осуществляет мониторинг эффективности системы качества и актуализацию стандартных операционных процедур, подтверждение качества изготовленных лекарственных препаратов, а также гарантирует, что лекарственные препараты изготовлены согласно стандартным операционным процедурам (далее — Ответственный работник аптечной организации).
Ответственный работник аптечной организации осуществляет подтверждение соответствия каждого изготовленного лекарственного препарата установленным требованиям до их отпуска.
8. Качество изготовленного лекарственного препарата определяется его соответствием требованиям фармакопейной статьи и общих фармакопейных статей, либо в случае их отсутствия — документам в области контроля качества.
9. Руководитель аптечной организации утверждает план-график проведения первичного и последующих инструктажей работников на знание стандартных операционных процедур, проводимых не реже 1 раза в год.
10. В целях исключения загрязнения изготавливаемых лекарственных препаратов:
а) не допускается осуществлять прием пищи, употребление жидкостей, курение в зоне изготовления лекарственных препаратов;
б) работник аптечной организации, непосредственно участвующий в изготовлении лекарственных препаратов, обязан уведомить Ответственного работника аптечной организации либо, в случае его отсутствия, руководителя аптечной организации или лицо, исполняющее его обязанности, о наличии у него инфекционных заболеваний и повреждений на открытых участках тела. Ответственный работник аптечной организации (руководитель аптечной организации или лицо, исполняющее его обязанности) не допускает данного работника аптечной организации к осуществлению деятельности по изготовлению лекарственных препаратов;
в) в отношении лекарственных препаратов, представляющих повышенный риск микробиологической контаминации, применяются защитные меры (дезинфекция рук, ношение масок), предусмотренные стандартными операционными процедурами.
11. Аптечные организации должны иметь помещения и (или) зоны, в которых осуществляется изготовление лекарственных препаратов в соответствии с требованиями настоящих Правил.
Изготовление лекарственных препаратов осуществляется в помещениях и зонах, доступных только для работников аптечной организации, перечень которых определяется руководителем аптечной организации.
Лекарственные препараты разных лекарственных форм лекарственных препаратов (далее — лекарственная форма) изготавливаются в разных зонах. В случае невозможности разделения зон под конкретные лекарственные формы, необходимо принять предусмотренные стандартной операционной процедурой меры, минимизирующие риск загрязнения лекарственного препарата, в том числе перекрестного.
12. Технологическое оборудование, а также измерительные приборы проектируются, размещаются, используются и обслуживаются в соответствии с их целевым назначением и руководством по эксплуатации производителя.
Совокупность документов, в которых фиксируются факты, имеющие отношение к качеству изготавливаемого лекарственного препарата, в том числе стандартные операционные процедуры, инструкции, должны обеспечивать прослеживаемость процесса изготовления лекарственного препарата.
13. В отношении каждого нарушения требований, установленных настоящими Правилами, стандартными операционными процедурами, проводится внутренняя проверка с устранением выявленных нарушений.
III. Особенности изготовления лекарственных препаратов из фармацевтических субстанций
14. Лекарственная форма «порошки» (далее — порошок) подразделяется на:
а) простые (состоящие из одного ингредиента);
б) сложные (состоящие из двух и более ингредиентов);
в) дозированные (разделенные на отдельные дозы);
г) недозированные (неразделенные на отдельные дозы).
15. Смесь для изготовления порошков разделяется на дозы с использованием весов или дозаторов в соответствии с массой одного порошка и их количеством, указанным в рецепте или требовании.
16. Изготовление порошков осуществляется следующими способами:
а) разделительным способом — лекарственные вещества и/или лекарственные препараты выписаны на все дозы, указано, на сколько доз следует разделить массу порошка;
б) распределительным способом — лекарственные вещества выписаны на одну дозу, указано количество доз.
17. К жидким лекарственным формам относятся растворы на водных и неводных растворителях, микстуры, водные извлечения из лекарственного растительного сырья, растворы высокомолекулярных веществ, растворы защищенных коллоидов, капли, суспензии, эмульсии.
Жидкие лекарственные формы изготавливаются массо-объемным методом, методом по массе или методом по объему.
18. Массо-объемным методом изготавливаются водные и водно-спиртовые растворы порошкообразных лекарственных средств.
19. Методом по массе изготавливаются растворы порошкообразных и жидких лекарственных средств в вязких и летучих растворителях, дозируемых по массе, а также эмульсии, суспензии независимо от их концентрации.
По массе дозируются жирные и минеральные масла, глицерин, димексид, полиэтиленгликоли (полиэтиленоксиды), силиконовые жидкости, эфир, хлороформ, бензилбензоат, валидол, винилин (бальзам Шостаковского), деготь березовый, ихтиол, кислота молочная, масла эфирные, скипидар, метилсалицилат, нитроглицерин, пергидроль.
20. Методом по объему изготавливаются растворы спирта этилового различной концентрации, растворы жидких стандартных фармакопейных растворов (кроме пергидроля).
По объему также дозируются вода очищенная и вода для инъекций, водные растворы лекарственных средств, галеновые и новогаленовые лекарственные средства.
21. При указании в рецепте или требовании в качестве компонента, подлежащего изготовлению, лекарственного препарата «вода» используется вода очищенная, «спирт» — спирт этиловый, «эфир» — эфир диэтиловый (медицинский), «глицерин» — глицерин медицинский, содержащий 10 — 16% воды, с плотностью 1,223 — 1,233 грамм на кубический сантиметр.
Если в рецепте или требовании не указан растворитель, используется вода очищенная.
22. Концентрированные растворы изготавливаются массо-объемным методом в мерной посуде в асептических условиях с использованием свежеполученной очищенной воды.
23. Растворы на вязких и летучих растворителях (кроме спиртовых растворов) изготавливаются по массе. Общая масса определяется суммированием ингредиентов, входящих в лекарственный препарат.
24. При изготовлении растворов на вязких и летучих растворителях непосредственно в сухой флакон для отпуска дозируются все ингредиенты, затем отвешивается или отмеряется растворитель.
25. При использовании вязких растворителей допускается применять нагревание с учетом физико-химических свойств ингредиентов.
26. Спиртовые растворы изготавливаются массо-объемным методом. В рецепте или требовании указывается количество этилового спирта, соответствующее объемным единицам измерения. При отсутствии в рецепте или требовании указания о концентрации этилового спирта используется этиловый спирт 90%.
27. Если в рецепте или требовании указан раствор, имеющий несколько стандартных концентраций, без указания концентрации, отпускается раствор наименьшей концентрации.
28. Растворы высокомолекулярных веществ изготавливаются массо-объемным методом (растворы пепсина, желатина, крахмала и другие) или по массе (растворы эфиров целлюлозы и другие).
Для растворения ограниченно набухающих высокомолекулярных веществ используются технологические приемы набухания и нагревания (растворы желатина, крахмала и другие) или охлаждения (раствор метилцеллюлозы и другие).
29. Водные извлечения (настои, отвары и иные) изготавливаются экстракцией лекарственного растительного сырья водой очищенной, а также растворением сухих или жидких экстрактов, стандартизованных в рассчитанном объеме воды очищенной.
При изготовлении водных извлечений не допускается замена лекарственного растительного сырья настойками, эфирными маслами и экстрактами, не предназначенными для изготовления водных извлечений.
Хранение водных извлечений осуществляется в упаковке, обеспечивающей сохранение их качества.
30. При изготовлении водных извлечений из лекарственного сырья не допускается использование концентрированных растворов лекарственных средств.
31. При изготовлении водных извлечений используются стандартизованные сухие и жидкие экстракты.
32. Растворы защищенных коллоидов протаргола, колларгола, ихтиола изготавливаются массо-объемным методом.
Растворы протаргола изготавливаются путем рассыпания его на поверхность воды очищенной и оставления до полного растворения.
Растворы колларгола изготавливаются с предварительным его измельчением и смешиванием с водой очищенной.
Коллоидные растворы фильтруются через обеззоленные бумажные или стеклянные фильтры.
33. Суспензии и эмульсии независимо от концентрации изготавливаются методом по массе.
При изготовлении суспензий и эмульсий в смесителях все ингредиенты перемешиваются до получения однородной массы. Время смешивания определяется свойствами лекарственных средств. Суспензии не подлежат фильтрации.
34. При изготовлении эмульсий используются эмульгаторы, выбор которых обусловлен их технологическими и физико-химическими свойствами, количеством масляной фазы и назначением эмульсии.
Эмульсии изготавливаются через стадию первичной эмульсии с расчетом количества ее ингредиентов с последующим разбавлением дисперсионной средой.
Способ введения лекарственных средств в эмульсии определяется их физико-химическими свойствами.
35. По типу дисперсных систем мази подразделяются на гомогенные (сплавы, растворы), гетерогенные (суспензионные и эмульсионные) и комбинированные.
В зависимости от консистентных свойств мази подразделяются на мази, гели, кремы, пасты и линименты.
Мази изготавливаются методом по массе.
36. Для изготовления мазей используются вспомогательные вещества: мазевые основы, консерванты, антиоксиданты, активаторы всасывания.
Мазевая основа обеспечивает проявление специфической активности мази, не нарушает функции кожи, не вызывает аллергических реакций, иных побочных действий.
Глазные мази и мази, вводимые в полости тела, наносимые на обширные раны и ожоговые поверхности, изготавливаются в асептических условиях.
37. К гомогенным мазям относятся мази-сплавы и мази-растворы.
Мази-сплавы на липофильных основах получаются сплавлением ингредиентов с учетом их температуры плавления.
Мази-растворы на липофильных основах получаются растворением жирорастворимых лекарственных средств в расплавленной основе.
Мази-растворы на гидрофильных основах получаются при растворении водорастворимых лекарственных средств в воде или других жидкостях с учетом растворимости, затем смешиваются с основой или растворяются в ней.
38. При изготовлении суспензионных мазей фармацевтические субстанции и лекарственные препараты измельчаются, затем диспергируются с оптимальным количеством жидкости.
При содержании твердой фазы в составе мази менее 5% лекарственные средства измельчаются с дополнительно вводимой жидкостью, родственной основе, в количестве примерно равном половине массы измельчаемых лекарственных средств.
При содержании в составе мази твердой фазы от 5% до 25% лекарственные средства измельчаются с частью расплавленной основы, равной половине от массы лекарственных средств, остальное количество основы берется в нерасплавленном виде.
При содержании в составе мази твердой фазы 25% и более используется расплавленная основа для диспергирования и разбавления концентрата.
39. Эмульсионные мази на липофильных и дифильных основах содержат водные или спиртовые растворы лекарственных средств. Эмульсионные мази на гидрофильных основах содержат гидрофобные жидкости.
В эмульсионные мази в виде водных растворов вводятся протаргол, колларгол, сухие экстракты и другие водорастворимые лекарственные средства. Полученные растворы эмульгируются и смешиваются с оставшимся количеством основы.
Жидкие лекарственные формы эмульгируются основой.
40. При изготовлении комбинированных мазей лекарственные средства вводятся в основу мази с учетом физико-химических свойств лекарственных средств. Технологические приемы, используемые при изготовлении комбинированных мазей, предупреждают нежелательные взаимодействия лекарственных средств друг с другом или расслоение мази в процессе изготовления и хранения, обеспечивают получение однородной массы.
41. Изготовленные растворы для инъекций и инфузий должны быть стерильны, стабильны, выдерживать испытание на пирогенность или бактериальные эндотоксины. В изготовленных растворах для инъекций и инфузий должны отсутствовать видимые механические включения. Дополнительными требованиями для изготовленных растворов для инъекций и инфузий являются их изотоничность, изогидричность, изоионичность, изовязкость.
Раствор для инъекций и инфузий изготавливается в асептических условиях массо-объемным методом на воде для инъекций.
42. Не допускается одновременное изготовление на одном рабочем месте нескольких растворов для инъекций и инфузий, содержащих лекарственные средства с различными наименованиями или лекарственные средства одного наименования в разных концентрациях.
Не допускается изготавливать инъекционные и инфузионные растворы при отсутствии данных о химической совместимости входящих в них лекарственных средств, технологии и режиме стерилизации, а также при отсутствии методов контроля качества, установленных фармакопейной статьей, общей фармакопейной статьей либо в случае ее отсутствия — документами в области контроля качества.
43. Растворы для инъекций и инфузий фильтруются с использованием фильтровальных материалов и установок. Фильтрование раствора сочетается с одновременным розливом его в подготовленные стерильные флаконы, которые укупориваются стерильными пробками.
Не допускается превышение 3-х часов от начала изготовления растворов для инъекций и инфузий до их стерилизации.
44. Лекарственные препараты для лечения офтальмологических заболеваний изготавливаются в следующих формах: глазные капли, растворы для орошения, глазные мази, глазные примочки.
Для изготовления лекарственных препаратов для лечения офтальмологических заболеваний применяются лекарственные средства и вспомогательные вещества (растворители, мазевые основы, стабилизаторы, буферные растворы, изотонирующие вещества, консерванты, пролонгаторы).
При изготовлении жидких лекарственных форм допускается использование стерильных готовых лекарственных препаратов в жидких и твердых лекарственных формах (порошки, лиофилизаты), предназначенных для приготовления растворов для инъекций и инфузий. При изготовлении лекарственных препаратов для лечения офтальмологических заболеваний допускается использование стерильных готовых лекарственных препаратов в твердых (порошки, лиофилизаты для приготовления растворов инъекций и инфузий), жидких и мягких формах.
45. Водные глазные жидкие лекарственные формы должны быть стерильны и изотоничны, если нет других указаний в фармакопейных статьях, иметь оптимальное значение pH и соответствовать значению pH слезной жидкости — 7,4 (допускаются значения pH от 3,5 до 8,5), должны быть стабильны при хранении и соответствовать требованиям фармакопейной статьи, общей фармакопейной статьи или документов в области контроля качества на видимые механические включения.
46. Глазные капли и растворы изготавливаются в асептических условиях массо-объемным методом на воде очищенной.
В глазных каплях и растворах определяется отсутствие механических включений до и после их стерилизации.
47. Растворы лекарственных средств, требующих защиты от воздействия повышенной температуры, готовятся в асептических условиях на стерильной воде очищенной без последующей стерилизации или с использованием стерилизации фильтрованием.
48. Глазные капли, содержащие наркотические средства, психотропные, ядовитые, сильнодействующие вещества, подвергаются химическому контролю в объеме, установленном пунктом 72 настоящих Правил.
49. Глазные мази изготавливаются в асептических условиях на стерильной мазевой основе.
Мазевая основа не должна содержать примесей, должна быть нейтральна, стерильна и равномерно распределяться по слизистой оболочке глаза.
Глазные мази изготавливаются методом по массе.
При отсутствии в рецепте или требовании указаний о составе мазевой основы используется сплав вазелина, не содержащего восстанавливающих веществ, и ланолина безводного в соотношении 9:1.
50. Лекарственные средства вводятся в основу глазной мази по типу раствора, эмульсии, суспензии.
Мазь-раствор изготавливается растворением лекарственных средств в стерильной мазевой основе.
Мазь-эмульсия на абсорбционной основе изготавливается растворением водорастворимых лекарственных средств (в том числе, резорцина и цинка сульфата) в минимальном количестве стерильной воды очищенной и смешиванием с мазевой основой.
В мазь-суспензию лекарственные средства вводятся в виде мельчайших порошков после тщательного диспергирования с небольшим количеством стерильной вспомогательной жидкости (при содержании лекарственных средств до 5%) или части расплавленной основы (при содержании лекарственных средств 5% и более).
51. Глазные мази, содержащие наркотические средства, психотропные, ядовитые, сильнодействующие вещества, подвергаются химическому контролю в объеме, установленном пунктом 72 настоящих Правил.
52. Лекарственные формы, предназначенные для лечения новорожденных и детей до 1 года, готовятся в асептических условиях по правилам изготовления лекарственных форм, установленных настоящими Правилами.
53. Лекарственные формы, предназначенные для лечения новорожденных и детей до 1 года, в том числе растворы для внутреннего и наружного применения, в зависимости от природы лекарственных средств, входящих в их состав, и технологического процесса изготовления, делятся на две группы: растворы, которые стерилизуются в конечной упаковке, и растворы, изготавливаемые в асептических условиях на стерильном растворителе без последующей термической стерилизации.
IV. Особенности изготовления лекарственных препаратов из готовых лекарственных препаратов
54. Изготовление порошков из готовых лекарственных препаратов осуществляется по указанному врачом составу изготавливаемого лекарственного препарата и вспомогательному веществу (при необходимости) в рецепте или требовании.
Допускается изготовление порошков из лекарственных форм (таблеток, капсул), обеспечивающих немедленное высвобождение лекарственных средств. Не допускается изготовление порошков из лекарственных форм (таблеток, капсул) пролонгированного действия и покрытых кишечнорастворимой оболочкой.
При изготовлении порошков из таблеток ее измельчают. Если в состав таблетки входят наркотические средства, психотропные вещества, сильнодействующие лекарственные средства, то предварительно измельчают индифферентное вспомогательное вещество.
55. При изготовлении порошков из капсул их содержимое вводят в порошки по правилам изготовления лекарственных препаратов в форме порошков с учетом физико-химических свойств ингредиентов.
Масса одного порошка, приготовленного из лекарственных форм (таблеток, капсул), составляет не менее 0,1 грамма. При отсутствии указаний в рецепте и (или) требовании на вспомогательные вещества используют индифферентное вспомогательное вещество, входящее в состав данных таблеток (капсул).
56. Изготовление растворов для инъекций и инфузий из готовых лекарственных препаратов не допускается.
V. Контроль качества лекарственных препаратов
57. Контроль качества изготавливаемых и изготовленных лекарственных препаратов осуществляется посредством:
а) приемочного контроля;
б) письменного контроля;
в) опросного контроля;
г) органолептического контроля;
д) физического контроля;
е) химического контроля;
ж) контроля при отпуске лекарственных препаратов.
Все изготовленные лекарственные препараты подлежат обязательному письменному, органолептическому контролю при отпуске.
58. Результаты органолептического, физического и химического контроля изготовленных лекарственных препаратов, в том числе в виде внутриаптечной заготовки и фасовки, концентрированных растворов, тритураций, спирта этилового регистрируются в журнале регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам, требованиям и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств.
В данном журнале указываются следующие сведения:
а) дата осуществления контроля и номер по порядку;
б) номер рецепта, требования, наименование медицинской организации, выдавшей их (при наличии);
в) номер серии лекарственного средства промышленного производства;
г) состав лекарственного средства: определяемое вещество или ион (указывается при физическом или химическом контроле лекарственных форм, изготовленных по рецептам);
д) результаты физического, органолептического, качественного контроля (каждый по шкале: положительный или отрицательный), химического контроля (качественное и количественное определение);
е) фамилия, имя, отчество (при наличии) лица, изготовившего, расфасовавшего лекарственный препарат;
ж) подпись лица, проверившего изготовленный лекарственный препарат;
з) заключение по результатам письменного контроля: удовлетворительно или неудовлетворительно.
59. Журнал регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам, требованиям и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств нумеруется, прошнуровывается и скрепляется подписью руководителя аптечной организации и печатью (при наличии). Допускается ведение указанного журнала в электронном виде.
60. При изготовлении концентрированных растворов, полуфабрикатов, лекарственных препаратов в виде внутриаптечной заготовки и фасовке лекарственных препаратов все записи производятся в журнале лабораторных и фасовочных работ, оформляемом на бумажном носителе или в электронном виде. Нумерация записей в журнале лабораторных и фасовочных работ осуществляется в течение календарного года в порядке возрастания номеров.
В журнале лабораторных и фасовочных работ указываются следующие сведения:
а) дата и порядковый номер проведения контроля выданного в работу лекарственного средства (сырья);
б) номер серии;
в) наименование лекарственного средства (сырья), единица измерения, количество, розничная цена, сумма розничная (в том числе стоимость посуды);
г) порядковый номер расфасованной продукции, единица измерения, количество, розничная цена, сумма розничная, в том числе для лекарственных препаратов в форме таблеток, лекарственных препаратов в форме порошков, дозированных жидких лекарственных форм, отклонение;
д) подпись лица, расфасовавшего лекарственное средство (сырье);
е) подпись лица, проверившего расфасованное лекарственное средство (сырье), дата и номер анализа.
Журнал лабораторных и фасовочных работ нумеруется, прошнуровывается и скрепляется подписью руководителя аптечной организации и печатью (при наличии).
61. Приемочный контроль организуется с целью предупреждения поступления в аптечную организацию недоброкачественных лекарственных средств, используемых для изготовления лекарственных препаратов, а также некачественных упаковочных материалов.
Все поступающие лекарственные средства (независимо от источника их поступления) подвергаются приемочному контролю.
62. Приемочный контроль заключается в проверке поступающих лекарственных средств на соответствие требованиям по показателям: «Описание», «Упаковка», «Маркировка», а также в проверке правильности оформления сопроводительных документов.
В контроль по показателю «Описание» включается проверка внешнего вида, агрегатного состояния, цвета, запаха лекарственного средства. В случае возникновения сомнений в качестве лекарственных средств образцы направляются в аккредитованную испытательную лабораторию (центр) для проведения дополнительных испытаний. Лекарственные средства с обозначением «Забраковано при приемочном контроле» хранятся в карантинной зоне помещения хранения изолированно от других лекарственных средств.
При контроле по показателю «Упаковка» оценивается целостность упаковки лекарственного средства и ее соответствие физико-химическим свойствам лекарственных средств.
При контроле по показателю «Маркировка» проверяется соответствие маркировки первичной, вторичной упаковки лекарственного средства требованиям статьи 46 Федерального закона от 12 апреля 2010 г. N 61-ФЗ «Об обращении лекарственных средств», наличие листка-вкладыша на русском языке в упаковке (или отдельно в пачке на все количество готовых лекарственных препаратов).
63. При изготовлении лекарственных препаратов, в том числе по рецептам и требованиям, а также в виде внутриаптечной заготовки, заполняется паспорт письменного контроля, в котором указываются:
а) дата изготовления лекарственного препарата;
б) номер рецепта или требования;
в) наименование медицинской организации, название отделения (при наличии); номер серии, количество в серии — для лекарственных препаратов в виде внутриаптечной заготовки;
г) наименования взятых лекарственных средств, вспомогательных веществ и их количества, степень взятых гомеопатических разведений или гомеопатических субстанций, число доз, подписи лиц, изготовившего, расфасовавшего и проверившего лекарственную форму.
Паспорт письменного контроля заполняется сразу после изготовления лекарственного препарата, с указанием лекарственных средств на латинском языке в именительном падеже или на русском языке в родительном падеже, в соответствии с последовательностью технологических операций, серия лекарственного препарата, из которого изготовили порошки. Допускается ведение указанного паспорта письменного контроля в электронном виде.
Паспорта письменного контроля хранятся в течение двух месяцев со дня изготовления лекарственных препаратов.
При изготовлении порошков, ториев указываются фактическое значение общей массы (при взвешивании), количество и масса отдельных доз.
Общая суппозиторная масса, концентрация и объем (или масса) изотонирующего вещества, добавленного в глазные капли, растворы для инъекций и инфузий, указываются не только в паспортах письменного контроля, но и на оборотной стороне рецепта на лекарственный препарат.
В случае использования концентрированных растворов в паспорте письменного контроля указываются их состав, концентрация и взятый объем.
64. Все расчеты для изготовления лекарственного препарата производятся до изготовления лекарственного препарата и записываются в паспорте письменного контроля.
Если в состав лекарственного препарата входят наркотические средства, психотропные, ядовитые и сильнодействующие вещества, а также другие лекарственные средства, подлежащие предметно-количественному учету, их количество указывается на оборотной стороне рецепта.
65. В случае, если лекарственные препараты изготавливаются и отпускаются одним и тем же лицом, паспорт письменного контроля заполняется в процессе изготовления лекарственного препарата.
66. Изготовленные лекарственные препараты, рецепты и требования, по которым изготовлены лекарственные препараты, заполненные паспорта письменного контроля передаются на проверку провизору-аналитику, выполняющему контрольные функции при изготовлении и отпуске лекарственных препаратов.
Контроль заключается в проверке соответствия записей в паспорте письменного контроля назначениям в рецепте или требовании, правильности произведенных расчетов.
Если провизором-аналитиком проведен химический контроль качества изготовленного лекарственного препарата, то на паспорте письменного контроля проставляется номер химического анализа и подпись провизора-аналитика.
67. Опросный контроль осуществляется выборочно и проводится после изготовления фармацевтом (провизором) не более пяти лекарственных форм.
При проведении опросного контроля провизором, осуществляющим контрольную функцию, называется первое входящее в состав лекарственного препарата лекарственное средство, а в лекарственных препаратах сложного состава указывается также его количество, после чего фармацевтом (провизором) указываются все иные используемые лекарственные средства и их количество. При использовании концентрированных растворов фармацевтом (провизором) указывается также их состав и концентрация.
68. Органолептический контроль является обязательным видом контроля и заключается в проверке лекарственного препарата по внешнему виду, запаху, однородности смешивания, отсутствию механических включений в жидких лекарственных формах. На вкус проверяются выборочно лекарственные формы, предназначенные для детей.
Однородность порошков, тритураций гомеопатических, масел, сиропов, мазей, суппозиториев проверяется выборочно у каждого фармацевта (провизора) в течение рабочего дня с учетом видов изготовленных лекарственных форм.
Результаты органолептического контроля регистрируются в журнале регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам на лекарственные препараты, требованиям медицинских организаций и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств.
69. Физический контроль заключается в проверке массы или объема лекарственного препарата, количества и массы отдельных доз (не менее трех доз), входящих в лекарственный препарат, количества гранул в одном грамме лекарственного препарата в форме гомеопатических гранул (далее — гомеопатические гранулы), распадаемости гомеопатических гранул.
В рамках физического контроля проверяется также качество укупорки изготовленного лекарственного препарата.
Лекарственные препараты, изготовленные по рецептам, требованиям, подлежат физическому контролю выборочно в течение рабочего дня с учетом всех видов изготовленных лекарственных форм, но не менее 3% от их количества за день.
Лекарственные препараты, изготовленные в виде внутриаптечной заготовки, подлежат физическому контролю в количестве не менее трех упаковок каждой серии (в том числе фасовка промышленной продукции и гомеопатических лекарственных средств). Физический контроль осуществляется в отношении лекарственных препаратов, предназначенных для применения у детей в возрасте до 1 года, содержащих ядовитые, наркотические средства, психотропные и сильнодействующие вещества, лекарственные препараты, требующие стерилизации, суппозиториев, инъекционных гомеопатических растворов, настоек гомеопатических матричных.
70. Контролю количества гранул в одном грамме подлежат гранулы сахарные, как вспомогательное вещество, при поступлении в аптечную организацию.
Взвешивается 1 грамм гранул с точностью 0,01 грамма и подсчитывается количество гранул. Проводится не менее двух определений.
Гранулы гомеопатические, изготовленные в виде внутриаптечной заготовки, подвергаются контролю распадаемости выборочно, но не менее 10% от общего числа изготовленных за месяц серий.
10 гранул помещаются в коническую колбу вместимостью 100 мл, прибавляется 50 мл воды очищенной, имеющей температуру 37 °C ± 2 °C. Колба медленно покачивается 1 — 2 раза в секунду. Проводится не менее трех определений. Гранулы должны распадаться в течение не более 5 минут.
71. Результаты физического контроля фиксируются в журнале регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам, требованиям и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств.
72. Химический контроль заключается в оценке качества изготовления лекарственных препаратов по показателям:
а) качественный анализ: подлинность лекарственных средств;
б) количественный анализ: количественное определение лекарственных средств.
Для проведения химического контроля оборудуется рабочее место, оснащенное специальным оборудованием, приборами и реактивами, обеспеченное документами в области контроля качества и справочной литературой.
Результаты качественного анализа регистрируются в журнале регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам, требованиям и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств, а также в журнале регистрации результатов контроля лекарственных средств на подлинность.
73. Качественному анализу подвергаются:
а) очищенная вода и вода для инъекций ежедневно из каждого баллона, а при подаче воды по трубопроводу — на каждом рабочем месте на отсутствие хлоридов, сульфатов и солей кальция и магния, также производится контроль значения pH. Вода, предназначенная для изготовления стерильных растворов, проверяется на отсутствие восстанавливающих веществ, солей аммония и углерода диоксида;
б) все лекарственные средства и концентрированные растворы (в том числе настойки гомеопатические матричные, тритурации гомеопатические первого десятичного разведения, растворы гомеопатические первого десятичного разведения), поступающие из помещений для хранения в помещения для изготовления лекарственных препаратов;
в) лекарственные средства, поступившие в аптечную организацию в случае возникновения сомнения в их качестве;
г) концентрированные растворы, жидкие лекарственные средства в бюреточной установке и в штангласах с пипетками, находящиеся в помещении изготовления лекарственных препаратов, при их заполнении;
д) расфасованные лекарственные средства промышленного производства;
е) гомеопатические лекарственные препараты в виде внутриаптечной заготовки. Качество лекарственного препарата оценивают по вспомогательным веществам.
Вода очищенная и вода для инъекций ежеквартально подвергаются полному качественному и количественному анализу.
74. При проведении химического контроля очищенной воды и воды для инъекций в журнале регистрации результатов контроля воды очищенной, воды для инъекций указываются:
а) дата получения (отгонки) воды;
б) дата контроля воды;
в) номер проведенного химического анализа воды;
г) номер баллона или бюретки, из которых взята на анализ вода;
д) результаты контроля на отсутствие примесей в воде;
е) значения электропроводности воды;
ж) заключение о результатах анализа воды (удовлетворяет или не удовлетворяет);
з) подпись лица, проводившего анализ воды.
Журнал регистрации результатов контроля воды очищенной, воды для инъекций нумеруется, прошнуровывается и скрепляется подписью руководителя аптечной организации и печатью (при наличии). Допускается ведение указанного журнала в электронном виде.
75. Качественному анализу подвергаются выборочно лекарственные препараты различных лекарственных форм, изготовленные фармацевтом (провизором) в течение рабочего дня, но не менее 10% от общего количества изготовленных каждым фармацевтом лекарственных препаратов, кроме гомеопатических.
Гомеопатические лекарственные препараты в виде внутриаптечной заготовки изготавливают под наблюдением провизора-аналитика или провизора-технолога. В тритурациях гомеопатических и гомеопатических гранулах качество лекарственного препарата дополнительно оценивают по вспомогательным веществам.
76. При проведении химического контроля подлинности лекарственных средств в журнале регистрации результатов контроля лекарственных средств на подлинность указываются следующие сведения:
а) дата заполнения бюреточной установки, штангласа;
б) порядковый номер химического анализа;
в) наименование лекарственного средства;
г) номер серии или номер анализа лекарственного средства производителя лекарственных средств;
д) номер заполняемого штангласа;
е) определяемое вещество (ион);
ж) результаты контроля по шкале «плюс» или «минус»;
з) подписи лиц, заполнивших и проверивших заполнение.
Журнал результатов контроля лекарственных средств на подлинность нумеруется, прошнуровывается и скрепляется подписью руководителя аптечной организации и печатью (при наличии).
77. Качественному и количественному анализу подвергаются:
а) растворы для инъекций и инфузий после стерилизации проверяются по значению pH, подлинности и количественном содержанию веществ; изотонирующие и стабилизирующие вещества после стерилизации проверяются лишь в случае, предусмотренном документами в области контроля качества;
б) 10% лекарственных препаратов каждой серии, изготовленных в виде внутриаптечной заготовки, в том числе растворы для инъекций и инфузий, кроме гомеопатических лекарственных препаратов;
в) стерильные растворы для наружного применения (офтальмологические растворы для орошений, растворы для лечения ожоговых поверхностей и открытых ран, для интравагинального введения и иные стерильные растворы);
г) глазные капли и мази, содержащие ядовитые, наркотические средства, психотропные, сильнодействующие вещества. При анализе глазных капель содержание в них изотонирующих и стабилизирующих веществ определяется до стерилизации;
д) все лекарственные формы, предназначенные для лечения новорожденных и детей до 1 года;
е) растворы атропина сульфата и кислоты хлористоводородной (для внутреннего применения), растворы серебра нитрата;
ж) все концентрированные растворы, тритурации, кроме гомеопатических тритураций;
з) стабилизаторы, применяемые при изготовлении растворов для инъекций и инфузий, буферные растворы, применяемые при изготовлении глазных капель;
и) концентрация спирта этилового при разведении, а также в случае возникновения сомнений в качестве спирта этилового при его поступлении в аптечную организацию;
к) инъекционные гомеопатические растворы;
л) лекарственные формы, изготовленные по рецептам и требованиям, в количестве не менее трех лекарственных форм при работе в одну смену с учетом различных видов лекарственных форм, в том числе лекарственные формы для детей, применяемые в офтальмологической практике, содержащие ядовитые вещества, наркотические средства, психотропные вещества, сильнодействующие вещества, растворы для лечебных клизм.
78. Изготовление и контроль качества стерильных растворов осуществляются в соответствии с настоящими Правилами, требованиями соответствующих фармакопейных статей и общих фармакопейных статей или документов в области контроля качества.
79. Микробиологический контроль растворов, за исключением растворов индивидуального изготовления, на стерильность и испытание на пирогенность или бактериальные эндотоксины растворов для инъекций и инфузий проводится в соответствии с требованиями соответствующих фармакопейных статей и общих фармакопейных статей или документов в области контроля качества.
80. До и после стерилизации стерильных растворов выполняется их контроль на механические включения.
Механическими включениями являются посторонние подвижные нерастворимые вещества, кроме пузырьков газа, случайно присутствующих в растворах лекарственных препаратов.
Одновременно проверяется объем растворов в емкостях и качество их укупорки.
81. В процессе изготовления стерильных растворов осуществляется первичный и вторичный контроль на механические включения.
Первичный контроль осуществляется после фильтрования и фасовки изготовленного раствора.
При обнаружении механических включений раствор повторно фильтруется, вновь просматривается, укупоривается, маркируется и стерилизуется.
Растворы, изготовленные асептически, просматриваются один раз после фасовки или стерилизующего фильтрования.
Первичному и вторичному контролю подлежат 100% емкостей с растворами.
82. Контроль растворов на отсутствие механических включений осуществляется провизором — технологом с соблюдением условий и техники контроля.
Для просмотра емкостей оборудуется рабочее место, защищенное от попадания прямых солнечных лучей. Допускается применение черно-белого экрана и специальных устройств.
В зависимости от объема емкости просматриваются одновременно от одной до пяти штук.
VI. Сроки годности на изготавливаемые лекарственные препараты
83. Сроки годности лекарственных препаратов, изготовленных аптечными организациями, составляют:
а) для нестерильных твердых лекарственных форм и мазей, линиментов — 14 суток;
б) для нестерильных твердых желатиновых капсул — 45 суток;
в) для нестерильных жидких лекарственных форм, за исключением, настоек капель, эмульсий и суспензий — 14 суток;
г) для глазных капель — не более 2 суток;
д) для настоев, отваров, слизей — не более 2 суток;
е) для растворов инъекций и инфузий — не более 2 суток;
ж) для эмульсий, суспензий с использованием стабилизаторов — не более 7 суток, без стабилизаторов — 2 суток;
з) для твердых желатиновых капсул, содержащих порошки, изготовленные в асептических условиях из стерильных ингредиентов — 90 суток;
и) для остальных лекарственных форм — не более 10 суток.
84. Аптечная организация вправе устанавливать иные сроки годности, изготавливаемых лекарственных препаратов, если они предусмотрены общими фармакопейными статьями.
VII. Правила отпуска и маркировки лекарственных препаратов
85. Лекарственные препараты, изготовленные и расфасованные в аптечной организации, оформляются соответствующими этикетками.
Этикетки для оформления лекарственных препаратов в зависимости от способа их применения подразделяются на:
а) этикетки для лекарственных препаратов внутреннего применения с надписью «Внутреннее»;
б) этикетки для лекарственных препаратов наружного применения с надписью «Наружное»;
в) этикетки для лекарственных препаратов местного применения с надписью «Для местного применения»;
г) этикетки на лекарственные препараты для парентерального введения с надписью «Для инъекций», «Для инфузий»;
д) этикетки на глазные лекарственные препараты с надписью «Глазные капли», «Глазная мазь», «Растворы для орошения»;
е) для гомеопатических лекарственных препаратов с надписью «Гомеопатический» или «Гомеопатическое лекарственное средство».
86. На этикетках для оформления изготовленных лекарственных препаратов печатаются предупредительные надписи, соответствующие лекарственной форме:
а) для микстур — «Хранить в прохладном и защищенном от света месте», «Перед употреблением взбалтывать»;
б) для мазей, глазных мазей и глазных капель — «Хранить в прохладном и защищенном от света месте», для гомеопатических мазей «Хранить в защищенном от света месте при температуре от 5 до 15°C»;
в) для капель внутреннего применения — «Хранить в защищенном от света месте»; для гомеопатических капель — «Хранить в защищенном от света месте, при температуре не выше 25°C»; для гранул гомеопатических — «Хранить в сухом, защищенном от света месте, при температуре не выше 25°C»;
г) для инъекций и инфузий и других стерильных лекарственных форм — «Стерильно».
87. Все этикетки должны содержать предупредительную надпись «Хранить в недоступном для детей месте».
88. Для лекарственных препаратов, требующих особых условий хранения, обращения и применения, на этикетках печатаются или наклеиваются предупредительные надписи.
89. Размеры этикеток определяются в соответствии с размерами посуды или другой упаковки, в которой отпускаются изготовленные лекарственные препараты.
90. Лекарственные препараты в зависимости от лекарственной формы и назначения оформляются соответствующими видами этикеток.
91. На этикетках для оформления лекарственных препаратов, изготовленных для населения, указывается следующее:
а) наименование аптечной организации;
б) местонахождение аптечной организации;
в) номер рецепта (присваивается в аптеке);
г) фамилия, имя, отчество (при наличии) пациента;
д) наименование или состав лекарственного препарата;
е) способ применения лекарственного препарата, вид лекарственной формы;
ж) режим дозирования;
з) дата изготовления лекарственного препарата;
и) срок годности лекарственного препарата («Годен до _____»);
к) цена лекарственного препарата;
л) предостережение «Хранить в недоступном для детей месте».
92. На этикетках для оформления лекарственных препаратов, изготовленных для медицинских организаций, указывается следующее:
а) наименование медицинской организации и ее структурное подразделение (при необходимости);
б) наименование аптечной организации;
в) местонахождение аптечной организации;
г) фамилия, имя, отчество (при наличии) пациента, для которого индивидуально изготовлен лекарственный препарат (при необходимости);
д) способ применения лекарственного препарата, вид лекарственной формы;
е) дата изготовления лекарственного препарата;
ж) срок годности лекарственного препарата («Годен до _____»);
з) подписи изготовившего, проверившего и отпустившего лекарственный препарат работников аптечной организации («Изготовил ______, проверил ______, отпустил ______»);
и) номер анализа проверки лекарственного препарата;
к) состав лекарственного препарата (предусматривается пустое место для указания состава). На этикетках лекарственных препаратов для инъекций и инфузий указывается способ применения лекарственного препарата: «Внутривенно», «Внутривенно (капельно)», «Внутримышечно».
93. Текст этикеток печатается типографским способом или с использованием печатающих устройств на русском языке. Состав лекарственного препарата пишется от руки или наносится штампом. Наименования лекарственных препаратов, часто встречающихся в рецептуре, или изготовляемых в виде внутриаптечной заготовки, допускается напечатать типографским способом или с использованием печатающих устройств.
94. На этикетках для оформления гомеопатических лекарственных препаратов, изготовленных как внутриаптечная заготовка, указывается:
а) наименование аптечной организации;
б) адрес местонахождения аптечной организации;
в) наименование монокомпонентного гомеопатического лекарственного препарата на русском языке (транслитерация);
г) наименование комплексного гомеопатического лекарственного препарата на русском языке;
д) состав для монокомпонентных и комплексных гомеопатических лекарственных препаратов (активные компоненты — на латинском языке, вспомогательные компоненты — на русском языке);
е) масса гомеопатического лекарственного препарата;
ж) способ применения гомеопатического лекарственного препарата;
з) вид лекарственной формы (гранулы гомеопатические, капли гомеопатические, мазь гомеопатическая, тритурация гомеопатическая);
и) дата изготовления гомеопатического лекарственного препарата;
к) срок годности гомеопатического лекарственного препарата («Годен до _____»);
л) серия;
м) цена гомеопатического лекарственного препарата;
н) штрих-код (при наличии);
о) предостережение «Хранить в недоступном для детей месте», условия хранения.
95. Маркировка изготовленных радиофармацевтических лекарственных препаратов осуществляется в зависимости от лекарственной формы и способа применения лекарственного препарата в соответствии с требованиями общей фармакопейной статьи «Радиофармацевтические лекарственные препараты».
VIII. Контроль при отпуске лекарственных препаратов
96. Контролю при отпуске лекарственных препаратов подвергаются все изготовленные лекарственные препараты, в рамках которого проверяется соответствие:
а) упаковки лекарственного препарата физико-химическим свойствам, входящих в него лекарственных средств;
б) указанных в рецепте или требовании доз наркотических средств, психотропных веществ, сильнодействующих веществ возрасту пациента;
в) реквизитов рецепта, требования сведениям, указанным на упаковке изготовленного лекарственного препарата;
г) маркировки лекарственного препарата требованиям главы VII настоящих Правил.
В рамках контроля при отпуске проверяется наличие информации о подтверждении Ответственным работником аптечной организации соответствия изготовленных лекарственных препаратов требованиям, установленным настоящими Правилами (далее — подтверждающая информация).
При выявлении одного из указанных в подпунктах «а» — «г» настоящего пункта несоответствий и (или) отсутствии подтверждающей информации, изготовленный лекарственный препарат не подлежит отпуску.
IX. Особенности изготовления гомеопатических лекарственных препаратов
97. Лекарственный препарат в форме тритурации гомеопатической изготавливается в виде порошка, состоящего из одного или нескольких измельченных активных компонентов и (или) их разведений со вспомогательным веществом. В качестве вспомогательного вещества используется лактозы моногидрат (если в рецепте или требовании не указано иное).
98. Изготовление тритураций гомеопатических осуществляется следующими способами:
а) изготовление тритурации гомеопатической из твердых лекарственных средств;
б) изготовление тритурации гомеопатической из настоек гомеопатических матричных, растворов гомеопатических и жидких гомеопатических разведений.
Изготовление тритураций гомеопатических производится методом по массе с использованием массовых частей.
99. В тритурациях гомеопатических размер полученных частиц исходного вещества в первом десятичном или первом сотенном разведении не превышает 100 микрометров.
100. Гомеопатические гранулы изготавливаются в виде сфер для приема внутрь одинакового диаметра, содержащую активный компонент (активные компоненты) в разведениях гомеопатических.
101. Гомеопатические гранулы изготавливаются путем насыщения или нанесения жидкого гомеопатического разведения одного или нескольких активных компонентов на вспомогательный компонент — гранулы, получаемые из сахарозы, лактозы или других подходящих сахаров, разрешенных к медицинскому применению.
Для обеспечения равномерного распределения жидких гомеопатических разведений применяются гомеопатические гранулы одинакового размера.
Размеры гомеопатических гранул различаются по номерам от 1 до 12 в зависимости от их диаметра, если не применяются иные.
Гомеопатические гранулы классифицируются по количеству гранул в 1 грамме. Количество гомеопатических гранул подсчитывается в двух параллельных пробах в навеске, взвешенной с точностью до 0,01 г.
102. Изготовление гомеопатических гранул осуществляется следующими способами:
а) насыщение гранул сахарных жидким гомеопатическим разведением или смесью разведений;
б) наслаивание на гранулы сахарные жидкого гомеопатического разведения.
103. Растворы гомеопатические и разведения гомеопатические изготавливаются по массе и используются в качестве субстанций для изготовления гомеопатических лекарственных препаратов или в качестве лекарственных препаратов для внутреннего, наружного и местного применения.
Разведения гомеопатические получаются путем ступенчатого разбавления, сопровождающегося встряхиванием растворов гомеопатических, тритураций гомеопатических, настоек гомеопатических матричных.
В качестве растворителей применяются вода очищенная, вода для инъекций, раствор натрия хлорида изотонический, глицерин, спирт этиловый или другой растворитель, указанный в фармакопейной статье или в случае ее отсутствия в документах в области контроля качества.
Водные разведения гомеопатические используются для изготовления растворов инъекционных гомеопатических, мазей, суппозиториев, капель глазных гомеопатических.
Водные разведения гомеопатические, предназначенные для получения мазей и суппозиториев, изготавливаются на воде очищенной.
104. Для получения разведений гомеопатических (растворов гомеопатических) используются методы Ганемана, Корсакова и LM-метод.
105. Гомеопатические смеси изготавливаются в виде смесей тритураций гомеопатических, настоек гомеопатических матричных, растворов гомеопатических или разведений гомеопатических с различными вспомогательными веществами и предназначаются для получения лекарственных средств.
Степень разведения активных компонентов в гомеопатических смесях получается путем их последовательного ступенчатого разбавления (потенцирования) с применением вспомогательного вещества (например, растворитель, носитель), которое добавляется в соотношении 1:10, 1:100 или в ином соотношении, указанном в рецепте или требовании.
Степень разведения активных компонентов в гомеопатических смесях соответствует числу ступеней их разведения при получении гомеопатических смесей.
106. Гомеопатические смеси получаются следующими способами:
а) каждый активный компонент, входящий в состав гомеопатической смеси, предварительно потенцируется до необходимой степени разведения, и затем смешивается предписанное количество (по массе) каждого полученного разведения.
б) смешиваются предписанное количество (по массе) каждого активного компонента, взятого в разведении на ряд ступеней ниже конечного, и совместно потенцируются до необходимой степени их разведения в смеси.
107. Совместно потенцируются:
а) гомеопатические смеси, содержащие только жидкие гомеопатические разведения, при получении которых в качестве растворителя (или экстрагента) используется спирт этиловый различной концентрации при соблюдении соотношения 1:10 или 1:100.
б) тритурации гомеопатические и жидкие гомеопатические разведения, полученные с использованием воды, водно-солевых или водно-глицериновых растворов в качестве растворителя (или экстрагента).
в) гомеопатические смеси, содержащие только тритурации гомеопатические, изготовленные из порошков, гомеопатических матричных настоек, растворов гомеопатических и (или) их разведений.
108. Гомеопатические капли изготавливаются в виде жидкой лекарственной формы, содержащей один или несколько активных компонентов в соответствующих гомеопатических разведениях.
Гомеопатические капли готовятся по массе и могут содержать один или более активных компонентов.
В качестве активных компонентов при изготовлении гомеопатических капель используются гомеопатические матричные настойки, их гомеопатические разведения, растворы гомеопатические, жидкие гомеопатические разведения. Последнее десятичное или сотенное разведение активного компонента потенцируется с применением растворителя, предусмотренного в составе гомеопатических капель.
В качестве растворителей при изготовлении гомеопатических капель используются очищенная вода, глицерин, спирт, жирные и минеральные масла, иной растворитель, указанный в фармакопейной статье, общей фармакопейной статье или документах в области обеспечения качества.
109. Изготовленные гомеопатические капли расфасовываются с использованием мерной посуды или различных дозаторов в соответствии с объемом гомеопатических капель.
110. Гомеопатический сироп изготавливается в виде сиропа, содержащего один или несколько активных компонентов в соответствующих гомеопатических разведениях.
Гомеопатический сироп изготавливается посредством растворения сиропообразующего компонента в кипящей очищенной воде. Полученный сироп фильтруется в горячем виде в стерильную емкость. Концентрация сахара в гомеопатическом сиропе не может быть более 72%.
В остывший сироп вводятся гомеопатические матричные настойки или их гомеопатические разведения, растворы гомеопатические и жидкие гомеопатические разведения, тритурации гомеопатические и (или) их гомеопатические разведения.
В качестве консерванта для изготовления гомеопатического сиропа используется спирт, применение других консервантов недопустимо.
Полученный гомеопатический сироп процеживается через плотную ткань или другой подходящий материал. Концентрация сахара в лекарственном препарате не менее 64%.
111. Настойки гомеопатические матричные изготавливаются в виде жидких извлечений из высушенного растительного сырья, смеси сока растений с этанолом.
Высушенное растительное сырье, предназначенное для получения гомеопатических матричных ферментированных настоек, измельчается до размера частиц, проходящих сквозь сито с отверстиями размером не более 0,5 миллиметров.
При изготовлении ферментированных гомеопатических настоек соблюдается температурный режим, значение pH среды, продолжительность настаивания и режим перемешивания. Температурный режим (нагревание) поддерживается с помощью термостатов. Процесс экстракции интенсифицируется тщательным перемешиванием мацератов дважды в день.
112. Настойки гомеопатические матричные получаются способами перколяции или мацерации этанолом соответствующей концентрации, мацерации очищенной свежеприготовленной водой с добавлением меда или смеси меда с лактозой, мацерации глицерином в присутствии или без натрия хлорида.
113. Гомеопатические мази состоят из основы и равномерно распределенных в ней одного или нескольких активных компонентов гомеопатических разведений.
По консистенции и составу основы мази гомеопатические подразделяются на:
а) гомеопатические мази (мягкая лекарственная форма, состоящая из основы и равномерно распределенных в ней одного или нескольких активных компонентов гомеопатических разведений);
б) гомеопатические оподельдоки (мыльный линимент, состоящий из смеси активных компонентов гомеопатических разведений и основы).
114. При изготовлении гомеопатической мази активные компоненты вводятся в виде гомеопатических матричных настоек и (или) их разведений, тритураций гомеопатических, растворов гомеопатических и жидких гомеопатических разведений, субстанций синтетического, минерального и природного происхождения или иного происхождения.
115. Гомеопатическое масло изготавливается в виде экстракта или раствора для наружного применения, состоящую из гомеопатических лекарственных средств и растительного или минерального масла.
Гомеопатическое масло изготавливается:
а) мацерацией высушенного растительного сырья растительным или минеральным маслом;
б) смешиванием эфирных масел и растительных или минеральных масел;
в) иным способом, обеспечивающим получение стабильной лекарственной формы.
Гомеопатическое масло содержит один или более ингредиентов.
116. Гомеопатическое масло изготавливается по массе в соотношении: (1:10) или (1:20) или в иных соотношениях.
В качестве масел используются оливковое, арахисовое, подсолнечное, косточковые и другие растительные масла или минеральные масла, разрешенные для медицинского применения.
Лекарственные препараты на основе масел делятся на монокомпонентные и комплексные. Комплексные лекарственные препараты на основе масел изготавливаются смешиванием монокомпонентных масел, потенцированной основы и других возможных ингредиентов с маслами или без них.
117. Гомеопатические суппозитории содержат один или несколько активных компонентов в соответствующих гомеопатических разведениях.
Гомеопатические суппозитории содержат активные компоненты в гомеопатических разведениях, равномерно распределенные в суппозиторной основе.
В качестве активных компонентов используются настойки гомеопатические матричные и (или) гомеопатические разведения и (или) их смеси, тритурации гомеопатические.
118. Инъекционные гомеопатические растворы изготавливаются в виде стерильной жидкой лекарственной формы, содержащей один или несколько активных компонентов в соответствующих гомеопатических разведениях.
Условия и правила изготовления гомеопатических инъекционных растворов должны соответствовать условиям и правилам изготовления растворов для инъекций и инфузий.
Для изготовления инъекционных гомеопатических растворов в качестве растворителя используется вода для инъекций.
Для изотонирования применяется натрия хлорид. Использование других вспомогательных веществ, за исключением веществ для изотонирования и поддержания постоянства значения pH, не допускается.
119. Глазные гомеопатические капли содержат один или несколько активных компонентов в соответствующих гомеопатических разведениях.
Глазные гомеопатические капли изготавливаются по массе в асептических условиях. В качестве растворителей применяются вода очищенная свежеприготовленная, изотонический раствор натрия хлорида или буферные растворы.
X. Порядок изготовления радиофармацевтических лекарственных препаратов
120. Изготовление радиофармацевтических лекарственных препаратов осуществляется с учетом особенностей, установленных законодательством Российской Федерации в области обеспечения радиационной безопасности.
Требования настоящей главы распространяются на изготовление радиофармацевтических лекарственных препаратов, содержащих в готовой для использования форме один радионуклид или несколько радионуклидов (радиоактивных изотопов) в качестве действующего вещества или в составе действующего вещества, диагностического или терапевтического назначения, в том числе для позитронно-эмиссионной томографии, полученных с использованием радионуклидных генераторов, циклотронов, наборов реагентов, растворов радионуклидов, радиоактивных (радионуклидных) предшественников радиофармацевтических лекарственных препаратов.
Требования настоящего раздела не распространяются на деятельность по производству радиофармацевтических лекарственных средств.
121. Изготовление радиофармацевтических лекарственных препаратов осуществляется по требованиям.
При изготовлении радиофармацевтических лекарственных препаратов используются лекарственные препараты и (или) фармацевтические субстанции, включенные соответственно в государственный реестр лекарственных средств для медицинского применения, единый реестр зарегистрированных лекарственных средств Евразийского экономического союза в установленном порядке.
Допускается изготовление радиофармацевтических лекарственных препаратов из химических предшественников и радионуклидных предшественников, в соответствии с требованиями общей фармакопейной статьи «Радиофармацевтические лекарственные препараты».
122. Качество изготовленного радиофармацевтического лекарственного препарата определяется работником аптечной организации его соответствием требованиям фармакопейной статьи, общей фармакопейной статьи, либо в случае их отсутствия — документов в области контроля качества.
123. Изготовление радиофармацевтических лекарственных препаратов осуществляется в контролируемых зонах (помещениях), отвечающих требованиям санитарно-эпидемиологических правил и гигиенических нормативов в области обеспечения радиационной безопасности.
Не допускается, чтобы поверхности оборудования, используемых материалов рабочих зон, соприкасающиеся с радиофармацевтическим лекарственным препаратом или веществами, входящими в его состав, вступали с ними в химическую реакцию, выделяли или абсорбировали вещества, чтобы не изменить качество радиофармацевтического лекарственного препарата.
Не допускается одновременное изготовление различных радиофармацевтических лекарственных препаратов в одной рабочей зоне (ламинарной зоне или защитном шкафу) с целью исключения перекрестного загрязнения радиоактивными веществами или перекрестной контаминации.
124. При изготовлении радиофармацевтических лекарственных препаратов соблюдаются:
а) меры по предотвращению перекрестной контаминации;
б) меры по защите зоны изготовления от радиоактивного загрязнения.
125. Аптечная организация разрабатывает и утверждает требования к системе документации по изготовлению радиофармацевтических лекарственных препаратов, а также документацию по изготовлению, контролю и обеспечению качества радиофармацевтических лекарственных препаратов, в которой с учетом требований соответствующих фармакопейных статей и общих фармакопейных статей последовательно (поэтапно) описываются требования к исходному сырью, упаковочным материалам, материалам для маркировки, критическим для качества радиофармацевтических лекарственных препаратов промежуточным материалам и готовым радиофармацевтическим лекарственным препаратам, технология изготовления радиофармацевтических лекарственных препаратов, устанавливаются предельные значения изменений характеристик радиофармацевтических лекарственных препаратов, срок годности, требования к упаковке и маркировке, контролю качества, а также требования к проведению операций, связанных с очисткой, дезактивацией, дезинфекцией (стерилизацией) оборудования.
126. Документация по изготовлению и обеспечению качества аптечной организации, осуществляющей изготовление радиофармацевтических лекарственных препаратов, оформляется в виде утвержденных руководителем аптечной организации процедур, в которых описывается порядок выполнения производственных операций, включая:
а) поступление, идентификацию, маркировку, обработку, отбор проб, использование, хранение и уничтожение/утилизацию изготавливаемых радиофармацевтических лекарственных препаратов;
б) обслуживание и поверку измерительных приборов и оборудования для контроля окружающей среды;
в) приготовление исходных веществ;
г) ведение записей, отчетов и их хранение;
д) обслуживание приборов, оборудования и помещений, в которых осуществляется изготовление радиофармацевтических лекарственных препаратов;
е) прием, размещение, хранение, описание, идентификацию исходного сырья и материалов;
ж) ведение записей, связанных с изготовлением и контролем качества изготавливаемых радиофармацевтических лекарственных препаратов.
127. Аптечной организацией разрабатываются и утверждаются:
а) документы, в которых указываются требования к качеству исходных и упаковочных материалов, используемых при изготовлении радиофармацевтических лекарственных препаратов;
б) порядок контроля исходных и упаковочных материалов;
в) допустимые предельные значения изменений характеристик радиофармацевтических лекарственных препаратов, включая требования к выпуску и сроку хранения (в том числе радиохимической чистоты, объемной активности, радионуклидной чистоты и удельной активности);
г) письменные инструкции на все операции, связанные с очисткой, дезактивацией, дезинфекцией (стерилизацией), техническим обслуживанием оборудования.
128. Записи по использованию, очистке, дезинфекции или стерилизации, техническому обслуживанию основного оборудования подписываются работником аптечной организации, выполнившим работу, с указанием даты, времени выполнения операции, наименования радиофармацевтического препарата и номера требования.
129. Изготовление и оценка качества лекарственных препаратов в твердых формах в виде капсул, содержащих радиофармацевтический лекарственный препарат, осуществляются в соответствии с требованиями фармакопейных статей на данные лекарственные препараты, общих фармакопейных статей «Радиофармацевтические лекарственные препараты» и «Лекарственные формы».
Изготовление и оценка качества радиофармацевтических жидких лекарственных форм из концентрированных растворов радионуклидов, полученных из радионуклидных генераторов (элюатов радионуклидных генераторов), осуществляются в соответствии с требованиями общей фармакопейной статьи «Радиофармацевтические лекарственные препараты».
130. К изготовлению лекарственных форм в асептических условиях предъявляются требования в соответствии с Руководством по асептическим процессам в фармацевтическом производстве, предусмотренным приложением к Рекомендациям Коллегии Евразийской экономической комиссии от 1 марта 2021 г. N 6 «О Руководстве по асептическим процессам в фармацевтическом производстве» <4>.
<4> Официальный сайт Евразийского экономического союза http://www.eaeunion.org/, 4 марта 2021 г., вступили в силу 4 сентября 2021 г., которые являются обязательными для Российской Федерации в соответствии с Договором о Евразийском экономическом союзе от 29 мая 2014 г., ратифицированным Федеральным законом от 3 октября 2014 г. N 279-ФЗ «О ратификации Договора о Евразийском экономическом союзе» (Договор вступил в силу для Российской Федерации 1 января 2015 г.).
Доступ в зону асептического изготовления радиофармацевтического лекарственного препарата ограничивается для работников аптечной организации, не прошедших соответствующее обучение.
131. Изготовленные инъекционные растворы радиофармацевтических лекарственных препаратов должны быть стерильны, стабильны и выдерживать испытание на пирогенность.
Для флаконов, содержащих радиофармацевтические лекарственные препараты, наполняемых в асептических условиях, осуществляется контроль целостности мембранных фильтров, с учетом необходимости обеспечения радиационной безопасности и сохранения стерильности фильтров.
Инъекционные растворы радиофармацевтических лекарственных препаратов изготавливаются в асептических условиях с использованием воды для инъекций и (или) физиологического раствора, в качестве растворителей конечной лекарственной формы.
132. Запрещается изготавливать инъекционные растворы радиофармацевтических лекарственных препаратов при отсутствии данных о химической совместимости входящих в него химических соединений, технологии и режиме стерилизации, а также при отсутствии методов контроля качества, установленных фармакопейной статьей, общей фармакопейной статьей либо в случае ее отсутствия — документами в области контроля качества, разработанными непосредственно в аптечной организации.
133. Упаковка изготовленных радиофармацевтических лекарственных препаратов осуществляется в зависимости от лекарственной формы и способа применения лекарственного препарата.
134. Срок годности изготовленного радиофармацевтического лекарственного препарата устанавливается на основании следующих факторов:
а) стабильности состава радиофармацевтических лекарственных препаратов;
б) уменьшения активности радионуклида с течением времени по закону радиоактивного распада;
в) возрастания относительного содержания долгоживущих радионуклидных примесей, имеющих периоды полураспада большие, чем основной радионуклид.
135. Каждая серия изготовленного радиофармацевтического лекарственного препарата проверяется по показателям качества в соответствии с документами в области контроля качества.
136. Изготовленные радиофармацевтические лекарственные препараты подвергаются контролю работником аптечной организации, при котором проверяются:
а) упаковка радиофармацевтического лекарственного препарата на соответствие требованиям документов в области контроля качества;
б) реквизиты требования медицинской организации на изготовление радиофармацевтических лекарственных препаратов, на соответствие сведениям, указанным на упаковке изготовленного радиофармацевтического лекарственного препарата;
в) маркировка радиофармацевтического лекарственного препарата на соответствие требованиям общей фармакопейной статьи «Радиофармацевтические лекарственные препараты».
При выявлении несоответствия указанным требованиям изготовленный радиофармацевтический лекарственный препарат не подлежит отпуску.
137. Допускается отпускать изготовленные радиофармацевтические лекарственные препараты до завершения полного цикла испытаний контроля качества, установленного документами в области контроля качества. В этом случае определяется порядок отпуска, включая ответственность работников аптечной организации и оценку эффективности радиофармацевтического лекарственного препарата.
138. Радиофармацевтические лекарственные препараты хранятся в закрытой зоне, предназначенной для данных целей, с установлением ограничений и порядка доступа работников аптечной организации, в которой обеспечены условия хранения с учетом специфических свойств радиофармацевтического лекарственного препарата и необходимости сохранения его качества, предусмотренные требованиями соответствующих фармакопейных статей и общих фармакопейных статей.
