Рекомендации по применению
Внутримышечно (в/м) или внутривенно (в/в) (струйно или капельно). При инфузионном способе введения препарат следует разводить в 0,9% растворе натрия хлорида.
Струйно Нейрокс® вводят медленно в течение 5-7 мин, капельно — со скоростью 40-60 капель в минуту. Максимальная суточная доза не должна превышать 1200 мг.
При острых нарушениях мозгового кровообращения Нейрокс® применяют в комплексной терапии в первые 10-14 дней — в/в капельно по 200-500 мг 2-4 раза в сутки, затем — в/м по 200-250 мг 2-3 раза в сутки в течение 2 недель.
При черепно-мозговой травме и последствиях черепно-мозговых травм Нейрокс® применяют в течение 10-15 дней в/в капельно по 200-500 мг 2-4 раза в сутки.
При дисциркуляторной энцефалопатии в фазе декомпенсации Нейрокс® следует назначать в/в струйно или капельно в дозе 200-500 мг 1-2 раза в сутки в течение 14 дней. Затем — в/м по 100-250 мг/сут в течение последующих 2 недель.
Для курсовой профилактики дисциркуляторной энцефалопатии Нейрокс® вводят в/м в дозе 200-250 мг 2 раза в сутки в течение 10-14 дней.
При нейроциркуляторной дистонии, невротических и неврозоподобных состояниях препарат вводят в/м по 50-400 мг в сутки в течение 14 дней.
При легких когнитивных нарушениях у больных пожилого возраста и при тревожных расстройствах препарат применяют в/м в дозе 100-300 мг в сутки в течение 14-30 дней.
При остром инфаркте миокарда в составе комплексной терапии Нейрокс® вводят в/в или в/м в течение 14 суток, на фоне традиционной терапии инфаркта миокарда (включающей нитраты, бета-адреноблокаторы, ингибиторы ангиотензинпревращающего фермента (АПФ), тромболитики, антикоагулянтные и антиагрегантные препараты, а также симптоматические средства по показаниям).
В первые 5 суток, для достижения максимального эффекта, Нейрокс® вводят внутривенно, в последующие 9 суток препарат может вводиться внутримышечно.
Внутривенное введение препарата производят путем капельной инфузии медленно, (во избежание побочных эффектов) в течение 30-90 минут (в 100-150 мл 0,9% раствора натрия хлорида или 5% раствора декстрозы (глюкозы)), при необходимости возможно медленное струйное в/в введение препарата, продолжительностью не менее 5 минут.
Введение препарата (в/в или в/м) осуществляют 3 раза в сутки, через каждые 8 часов, Суточная доза составляет 6-9 мг/кг массы тела, разовая доза — 2-3 мг/кг массы тела. Максимальная суточная доза не должна превышать 800 мг, разовая — 250 мг.
При открытоугольной глаукоме различных стадий в составе комплексной терапии Нейрокс® вводят в/м по 100-300 мг/сутки, 1- 3 раза в сутки в течение 14 дней.
При абстинентном алкогольном синдроме Нейрокс® вводят в/м или в/в капельно в дозе 200-500 мг 2-3 раза в сутки в течение 5-7 дней.
При острой интоксикации антипсихотическими лекарственными препаратами препарат вводят в/в в дозе 200-500 мг/сут в течение 7- 14 дней.
При острых гнойно-воспалиительных процессах брюшной полости (острый некротический панкреатит, перитонит) Нейрокс® назначают в первые сутки как в предоперационном, так и в послеоперационном периоде. Вводимые дозы зависят от формы и тяжести заболевания, распространенности процесса, вариантов клинического течения. Отмена препарата должна производиться постепенно только после устойчивого положительного клиниколабораторного эффекта.
При остром отечном (интерстициальном) панкреатите Нейрокс® назначают по 200- 500 мг 3 раза в день, в/в капельно (в 0,9 % растворе натрия хлорида) и в/м. Легкая степень тяжести некротического панкреатита- по 100-200 мг 3 раза в день капельно (в 0,9 % растворе натрия хлорида) и в/м. Средняя степень тяжести — по 200 мг 3 раза в день, в/в капельно (в 0,9 % растворе натрия хлорида). Тяжелое течение — в пульсдозировке 800 мг в первые сутки, при двукратном режиме введения; далее по 200-500 мг 2 раза в день с постепенным снижением суточной дозы. Крайне тяжелое течение — в начальной дозировке 800 мг/сут до стойкого купирования проявлений панкреатогенноrо шока, по стабилизации состояния по 300-500 мг 2 раза в день в/в капельно (в 0,9 % растворе натрия хлорида) с постепенным снижением суточной дозировки.
Изучение влияния этилметилгидроксипиридина сукцината на эффективность нестероидных противовоспалительных препаратов при висцеральной и соматической боли в эксперименте на мышах и крысах
Статьи
Е.А. Иванова, А.Г. Васильчук, А.И. Матюшкин, Т.А. Воронина
ФГБНУ «НИИ фармакологии им. В.В. Закусова», Москва, Россия
Резюме
Цель исследования. Изучить влияние этилметилгидроксипиридина сукцината (ЭМГПС) на противоболевой эффект неселективного ингибитора циклооксигеназы (ЦОГ) диклофенака натрия и селективного ингибитора ЦОГ-2 эторикоксиба на моделях острой висцеральной и соматической боли и оценить возможность применения ЭМГПС в комбинации с ингибиторами ЦОГ для снижения их доз с сохранением противоболевой эффективности.
Материал и методы. Изучено влияние ЭМГПС при однократном пероральном введении на противоболевые эффекты нестероидных противовоспалительных препаратов (НПВП): неселективного ингибитора ЦОГ диклофенака натрия и селективного ингибитора ЦОГ-2 эторикоксиба — на моделях острой висцеральной (тест «уксусные корчи») и соматической боли (формалиновый тест и тест механической гипералгезии при воспалении) в эксперименте на мышах и крысах.
Результаты. На модели острой висцеральной боли у мышей ЭМГПС (25—100 мг/кг) не оказывает значимого влияния на ее выраженность, но усиливает противоболевой эффект диклофенака натрия (0,5 мг/кг) и эторикоксиба (1 мг/кг). В формалиновом тесте у крыс, моделирующем боль при операционных разрезах (травма), ЭМГПС (25 мг/кг) повышает выраженность противоболевого действия ингибиторов ЦОГ (1 мг/кг) прежде всего за счет снижения боли в острую фазу, обусловленную действием формалина на афферентные нейроны. На модели механической гипералгезии у крыс, вызванной экссудативным воспалением после инъекции раствора каррагинана в лапу, ЭМГПС усиливает в большей степени эффект диклофенака, чем эторикоксиба.
Заключение. Полученные данные свидетельствуют о целесообразности клинического исследования применения ЭМГПС в комбинации с НПВП при висцеральной и соматической боли с целью оценки его способности повышать лечебный эффект НПВП.
Ключевые слова: этилметилгидроксипиридина сукцинат, нестероидные противовоспалительные препараты, висцеральная боль, соматическая боль, мыши, крысы.
Информация об авторах:
Иванова Е.А. — https://orcid.org/0000-0003-4961-2051
Васильчук А.Г. — https://orcid.org/0000-0002-9079-1322
Матюшкин А.И. — https://orcid.org/0000-0001-7640-0551
Воронина Т.А. — https://orcid.org/0000-0001-7065-469X
Автор, ответственный за переписку: Иванова Е.А. — e-mail: iwanowaea@yandex.ru
Как цитировать: Иванова Е.А., Васильчук А.Г., Матюшкин А.И., Воронина Т.А. Изучение влияния этилметилгидроксипиридина сукцината на эффективность нестероидных противовоспалительных препаратов при висцеральной и соматической боли в эксперименте на мышах и крысах. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(12):1—9. doi.org/10.17116/jnevro20231231211
Одними из основных средств фармакотерапии острой боли при широком спектре патологических состояний являются нестероидные противовоспалительные препараты (НПВП), общий механизм действия которых — ингибирование циклооксигеназы (ЦОГ) с последующим снижением повышенного при воспалении или повреждении ткани уровня простагландинов, за счет чего НПВП оказывают обезболивающий, противовоспалительный и жаропонижающий эффекты. Однако их прием сопровождается нежелательными явлениями (НЯ), обусловленными периферическим действием препаратов. Прежде всего это НЯ со стороны желудочно-кишечного тракта (ЖКТ), сердечно-сосудистой системы, НПВП-ассоциированные нефропатии, гепатотоксичность [1]. НПВП способны ускорить дегенерацию хряща, поэтому, облегчая хроническую ноцицептивную боль при остеоартрите, они могут негативно влиять на течение заболевания [2]. Высокий риск НПВП-ассоциированных НЯ применения НПВП ограничивает их долгосрочное использование [3].
Для уменьшения доз НПВП и повышения безопасности их применения возможно комбинирование НПВП со средствами, механизм действия которых исключает выраженное ингибирование фосфолипазы A2 и ЦОГ и направлен на иные звенья патогенеза боли. Такими средствами могут быть препараты с антиоксидантным действием, так как в каскаде арахидоновой кислоты образуются активные формы кислорода (АФК) [4], которые являются одними из альгогенов при воспалительной гипералгезии, и перехватчики АФК или соединения, имитирующие активность супе-роксиддисмутазы, которые уменьшают гипералгезию [5, 6]. АФК способны усиливать глутамат-зависимую трансдукцию: могут окислять сульфгидрильные группы транспортеров глутамата и, таким образом, инактивировать их, вследствие чего снижается захват глутамата из синаптической щели и его перенос в клетку [7—9].
Использование антиоксидантных препаратов совместно с НПВП целесообразно и с целью уменьшения вызываемых ими НЯ. С одной стороны, механизм побочного действия НПВП на слизистую оболочку ЖКТ является следствием их прооксидантного действия [10]. С другой стороны, при приеме НПВП существенно увеличен риск гибели пациентов, перенесших инфаркт миокарда [11]. Вследствие ишемии миокарда при инфаркте миокарда, нестабильной стенокардии и ишемической болезни активируется перекисное окисление липидов (ПОЛ) и повышается образование АФК, повреждающих клеточные мембраны и оказывающих цитотоксическое действие [12]. Поэтому применение в комбинации с НПВП средств, проявляющих антиоксидантные свойства, обосновано не только с целью усиления основного действия НПВП, но и для снижения риска развития НЯ со стороны ЖКТ, сердечнососудистой и других систем.
В настоящем исследовании для комбинации с НПВП был выбран антиоксидант этилметилгидроксипиридина сукцинат (ЭМГПС), который обладает мультимодальным механизмом действия, включающим его способность ингибировать ПОЛ и модифицировать фосфолипидный состав мембран [13—15], повышать активность Se-зависимой глутатионпероксидазы, снижать активность индуцибель-ной NO-синтазы, связывать супероксидный анион-ради-кал, уменьшать глутаматную эксайтотоксичность [16], улучшать энергетический статус клетки и влиять на процессы в цикле Кребса [17, 18].
Цель исследования — изучить влияние ЭМГПС на противоболевой эффект неселективного ингибитора ЦОГ диклофенака натрия и селективного ингибитора ЦОГ-2 это-рикоксиба на моделях острой висцеральной и соматической боли и оценить возможность применения ЭМГПС в комбинации с ингибиторами ЦОГ для снижения их доз с сохранением противоболевой эффективности.
Материал и методы
В работе использовали половозрелых беспородных белых мышей-самцов массой 24—29 г и крыс-самцов массой 240—280 г. из питомника филиала «Столбовая» ФГБУН «Научный центр биомедицинских технологий ФМБА России». Организацию и проведение работ осуществляли в соответствии с ГОСТ 33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами», ГОСТ 33215-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур» и Директивой 2010/63/EU Европейского Парламента и Совета Европейского Союза от 22.09.2010 по охране животных, используемых в научных целях. Проведение опытов одобрено Комиссией по биомедицинской этике НИИ фармакологии им. В.В. Закусо-ва (протокол №01 от 28.01.2021).
Использовали диклофенак натрия (Вольтарен, раствор для внутримышечного введения 75 мг/3 мл; «Novartis Pharma Stein AG», Швейцария); эторикоксиб (Аркоксия, таблетки, покрытые пленочной оболочкой; «Merck sharp & Dohme B.V.», Нидерланды); ЭМГПС (Мексидол, раствор для в/в введения 50 мг/мл; ООО «НПК «ФАРМАСОФТ», Россия); в качестве растворителя применяли физиологический раствор (Натрия хлорид, раствор для инфузий 0,9%; ОАО НПК «ЭСКОМ», Россия).
Висцеральную боль у мышей вызывали внутрибрюшинным введением 0,9% раствора уксусной кислоты из расчета 0,1 мл на 10 г массы тела (тест «уксусные корчи», ТУК). Введение раствора уксусной кислоты приводит к раздражению серозных оболочек, что вызывает сокращение абдоминальной мускулатуры и проявляется специфическими болевыми движениями — корчами, количество которых подсчитывали на протяжении 15 мин сразу после введения раствора уксусной кислоты [19]. О противоболевом действии препаратов судили по снижению количества корчей после их введения относительно количества корчей в контрольной группе мышей, которым вводили растворитель.
Изучение влияния ЭМГПС на выраженность противоболевого действия НПВП на модели висцеральной боли у мышей проводили в трех опытах. В первом оценивали влияние ЭМГПС на действие диклофенака натрия, во втором — на действие эторикоксиба, в третьем — на висцеральную боль per se. С целью выбора доз НПВП для применения в комбинации с ЭМГПС оценивали дозозави-симость их противоболевого эффекта: для диклофенака натрия в диапазоне доз от 0,5 до 10 мг/кг, для эторикокси-ба — от 1 до 20 мг/кг. Дозы ЭМГПС в комбинации с НПВП составляли от 12,5 до 100 мг/кг, влияние ЭМГПС per se изучали при его введении в дозах 25, 50 и 100 мг/кг. Препараты или физиологический раствор (контрольная группа) мышам вводили перорально за 1 ч до внутрибрюшинного введения 0,9% раствора уксусной кислоты.
Формалиновый тест, моделирующий боль при операционных разрезах (травмах). В заднюю лапу крыс вводили 0,1 мл 2% раствора формалина [19]. Каждые 5 мин в баллах регистрировали 4 типа поведенческих реакций: 0 — отсутствие реакции; 1 — лапа остается на горизонтальной поверхности, но животное на нее не опирается; 2 — лапа поднята; 3 — лапа облизывается, грызется или встряхивается. Подсчитывали сумму баллов в острую (0—5 мин), тоническую (20—60 мин) фазу боли и интерфазу (5—20 мин). Критерием анальгетического эффекта считали уменьшение болевых реакций в группах крыс, получавших препараты, относительно контрольной группы животных, которым вводили физиологический раствор. Изучаемые НПВП эторикоксиб и диклофенак натрия в дозах 1 и 10 мг/кг соответственно, ЭМГПС в дозе 25 мг/кг, комбинации этих НПВП (1 мг/кг) с ЭМГПС (25 мг/кг) и физиологический раствор вводили перорально за 1 ч до введения 2% раствора формалина.
При проведении теста механической гипералгезии при воспалении гипералгезию регистрировали у крыс с воспалением, вызванным введением в заднюю лапу 0,1 мл 1% раствора каррагинана [20]. О гипералгезии судили по снижению порога тактильной чувствительности, которую фиксировали через 3 и 24 ч после введения раствора каррагинана с помощью волосков фон Фрея весом от 0,06 до 23,96 г («Aesthesio Ugo Basile», Италия). Крыс помещали по отдельности в пластиковые камеры (20x10x14 см) на возвышенной решетчатой платформе с перфорациями и в течение 15 мин адаптировали в условиях покоя. Нити фон Фрея предъявляли перпендикулярно в разных местах подошвенной поверхности задних лап животных, исключая области пальцев и скакательного сустава. Для каждого волоска фон Фрея тестирование проводили 5 раз с интервалом 3 с. Определяли порог реакции, вызывающий отдергивание лапы. Эторикоксиб и диклофенак натрия в дозах 1 и 10 мг/кг, ЭМГПС в дозе 25 мг/кг, комбинации этих НПВП (1 мг/кг) с ЭМГПС (25 мг/кг) вводили перорально дважды через 2 и 23 ч после введения раствора каррагинана. Группе крыс без воспаления лапы (контрольная группа) и группе крыс «Каррагинан» (животным с отеком лапы, которым не вводили препараты) перорально в эти же сроки вводили физиологический раствор.
Статистическую обработку результатов осуществляли с помощью программы Statistica 10.0. Нормальность распределения данных проверяли критерием Шапиро— Уилка с последующей оценкой межгруппового равенства дисперсий критерием Левена. При нормальном распределении в группах и соблюдении межгруппового равенства дисперсий дальнейшую статистическую обработку проводили путем однофакторного дисперсионного анализа с последующим сравнением групп с помощью критерия Ньюмана—Кейлса и t -критерия Стьюдента. При отсутствии нормального распределения использовали критерий Кра-скела—Уоллиса. При обнаружении статистически значимых различий между группами с помощью критерия Кра-скела—Уоллиса далее проводили статистический анализ методом сравнения средних рангов для всех групп. Различия между группами считали статистически значимыми при p <0,05. Результаты представляли на рисунках, выполненных с помощью программы GraphPad Prism V. 8.4.3: при применении параметрической статистики — как среднее значение±стандартное отклонение (M±SD), непараметрической — в виде боксплотов.
Результаты
Рис. 1. Влияние диклофенака натрия (а), эторикоксиба (б), ЭМГПС (в) и их комбинаций (а, б) при однократном пероральном введении на выраженность острой висцеральной боли в тесте ТУК у мышей (M±SD).
Fig. 1. Effect of diclofenac sodium (a), etoricoxib (b), EMGPS (c) and their combinations (a, b) with a single oral administration on the severity of acute visceral pain in the TUC test in mice (M±SD).
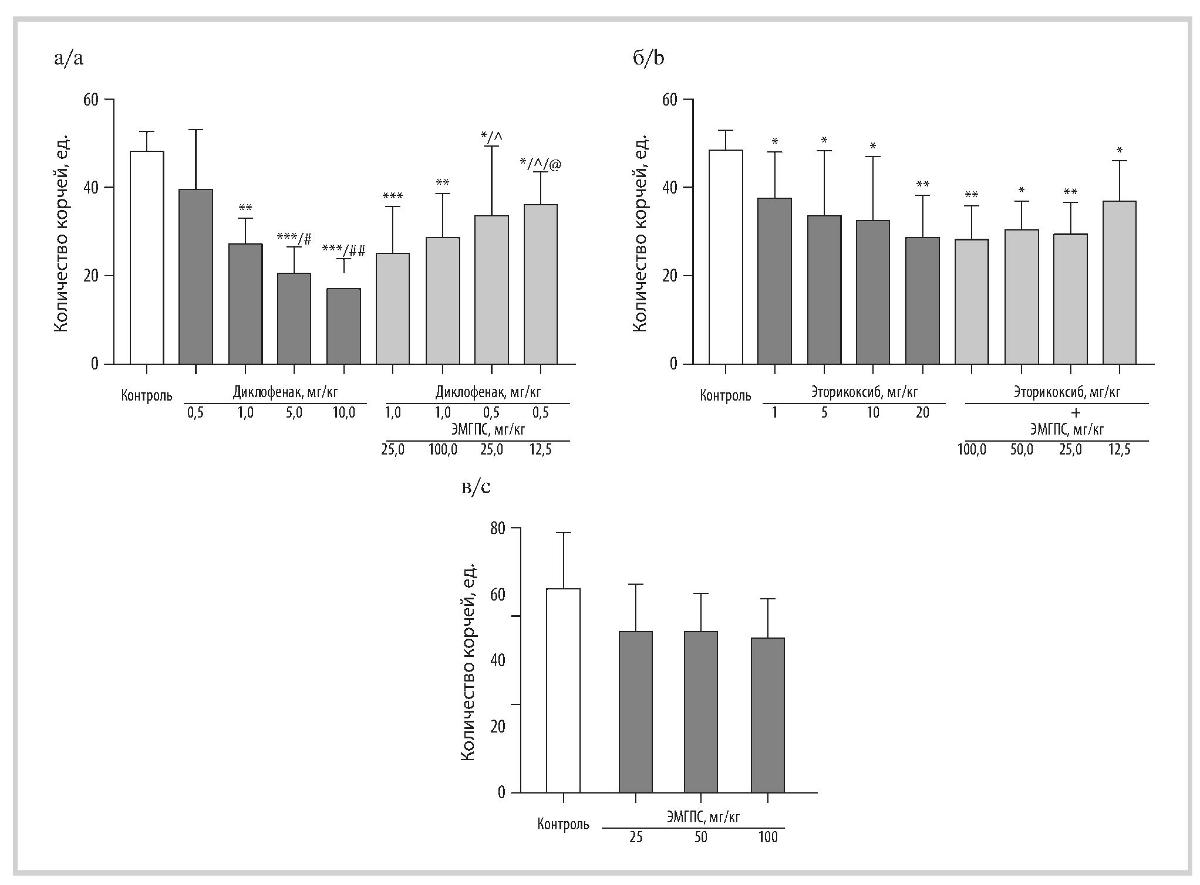
* — p<0,05,** — p<0,005, *** — p<0,0005 по сравнению с контролем; для рис. 1а: # — p<0,05, ## — p<0,005 по сравнению с группой «Диклофенак 0,5 мг/кг»; А — p <0,05 по сравнению с группой «Диклофенак 5 мг/кг»; @ — p <0,05 по сравнению с группой «Диклофенак 10 мг/кг, критерий Ньюмена—Кейлса».
* — p<0.05, ** — p<0.005, *** — p<0.0005 compared to control; for fig. 1a: # — p<0.05, ## — p<0.005 compared with the «Diclofenac 0.5 mg/kg» group; A — p<0.05 compared with the «Diclofenac 5 mg/kg» group; @ — p<0.05 compared with the «Diclofenac 10 mg/kg group, Newman—Keuls test».
Влияние препаратов на висцеральную боль в ТУК у мышей. Висцеральная боль у мышей после внутрибрюшинного введения им 0,9% раствора уксусной кислоты проявлялась специфическими болевыми движениями — корчами, количество которых в контрольных группах варьировало от 48,3 до 62,0 (рис. 1). Диклофенак натрия оказывал дозозависимое противоболевое действие и значимо снижал болевую реакцию животных при однократном пероральном введении в дозах от 1 до 10 мг/кг, но не в дозе 0,5 мг/кг. Противоболевой эффект препарата в дозе 1 мг/кг соответствовал 43,6%, в дозе 5 мг/кг — 57,0%, в дозе 10 мг/кг — 64,6%. При этом уменьшение интенсивности висцеральной боли при введении мышам диклофенака натрия в дозах 5 и 10 мг/кг было значимо соответственно на 47,7 и 57,0% более выражено, чем в группе животных, которым его вводили в дозе 0,5 мг/кг (рис. 1, а). Применение диклофенака натрия в дозе 1 мг/кг и это-рикоксиба с ЭМГПС в дозе 25 мг/кг приводило к значимому снижению боли на 47,7%; использование этого НПВП совместно с ЭМГПС в дозе 100 мг/кг подавляло боль на 40,3%. Применение диклофенака натрия в дозе 0,5 мг/кг, в которой препарат не оказывал значимого влияния на висцеральную боль, совместно с ЭМГПС в дозах 25 и 12,5 мг/кг приводило к появлению значимого противоболевого эффекта. Комбинация диклофенака натрия в дозе 0,5 мг/кг с ЭМГПС в дозе 25 мг/кг снижала боль на 29,8%, с ЭМГПС в дозе 12,5 мг/кг — на 25,1% (см. рис. 1, а).
Эторикоксиб при однократном пероральном введении в диапазоне доз 1—20 мг/кг дозозависимо подавлял висцеральную боль у мышей. Препарат в дозе 1 мг/кг значимо снижал количество корчей на 22,5%, в дозе 5 мг/кг — на 33,9%, в дозе 10 мг/кг — на 36,4%, в дозе 20 мг/кг — на 43,2%. Применение эторикоксиба в дозе 1 мг/кг совместно с ЭМГПС в дозах 25—100 мг/кг усиливало выраженность противоболевого эффекта НПВП и приводило к подавлению боли на 40,1—44,2%, что было сопоставимо с эффектом эторикоксиба в дозе 20 мг/кг. Хотя при статистическом анализе с помощью критерия Ньюмена—Кейлса различий между группами комбинаций эторикоксиба (1 мг/кг) и ЭМГПС (25—100 мг/кг) не было, при попарном сравнении с помощью t-критерия Стьюдента зарегистрировано значимое (p<0,05) повышение эффективности этих комбинаций на 22,6—28,0% по сравнению с введением только эторикоксиба. Однако при применении этори-коксиба (1 мг/кг) в комбинации с ЭМГПС в дозе 12,5 мг/кг количество корчей практически не отличалось от показателя в группе мышей, которым вводили только эторикоксиб в дозе 1 мг/кг (см. рис. 1, б). ЭМГПС при однократном пероральном введении в дозах 25—100 мг/кг значимо не влиял на выраженность висцеральной боли у мышей. Вместе с тем при его применении в дозах 50 и 100 мг/кг наблюдалась тенденция к снижению количества корчей (соответственно на 19,8%, p=0,07, и 23,4%, p=0,075, t -критерий Стьюдента) (см. рис. 1, в).
Таким образом, на модели острой висцеральной боли у мышей ЭМГПС при однократном пероральном введении в дозах 25—100 мг/кг не оказывал значимого влияния на ее выраженность, но усиливал противоболевой эффект диклофенака натрия и эторикоксиба при их однократном пероральном введении в дозах 0,5 и 1 мг/кг.
Влияние препаратов на соматическую боль в формалиновом тесте у крыс. В формалиновом тесте спонтанное болевое поведение крыс после введения им 0,1 мл 2% раствора формалина характеризовалось двухфазной реакцией (рис. 2). Первая фаза, которая длилась в течение 5 мин, обусловлена действием формалина на ионный канал TRPA1 афферентных нейронов, вторая фаза начиналась с 20 мин наблюдения, и ее механизм связывают с развивающейся воспалительной реакцией и центральной сенсити-зацией [21]. Регистрируемое с 5-й по 20-ю мин снижение болевой реакции — интерфаза — объясняют результатом гиперполяризации и временной инактивации нейронов, повышение возбудимости которых и центробежное распространение формалина в коже вызывают вторую фазу болевой реакции [22].
Рис. 2. Влияние диклофенака натрия (а, б), эторикоксиба (в, г) и их комбинаций с ЭМГПС при однократном пероральном введении на формалиновую боль у крыс в острую и тоническую фазу.
Fig. 2. Effect of diclofenac sodium (a, b), etoricoxib (c, d) and their combinations with EMGPS with a single oral administration on formaldehyde pain in rats in the acute and tonic phase.
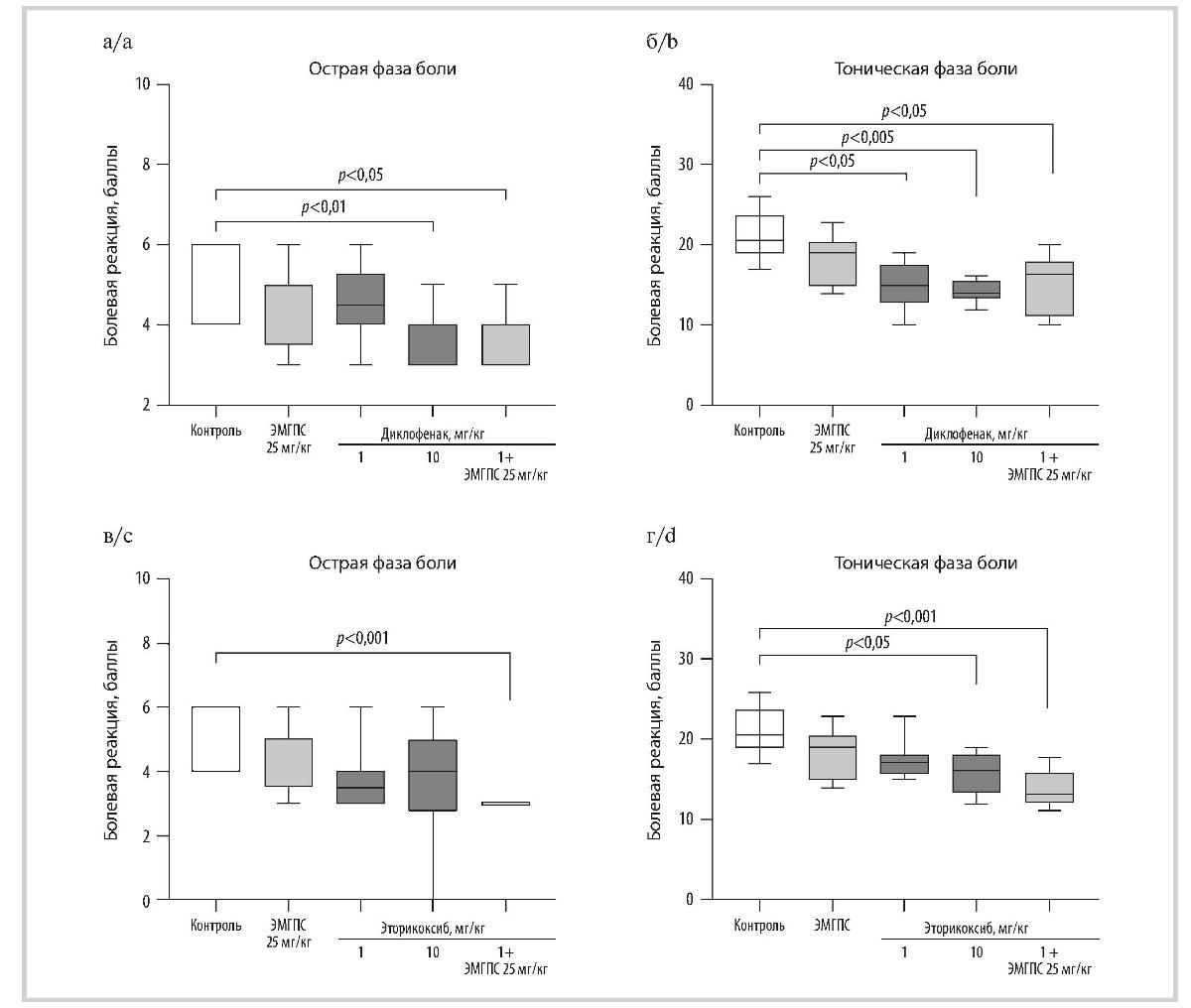
Данные представлены в виде боксплотов; статистическую обработку данных проводили с помощью критерия Краскела—Уоллиса с последующим статистическим анализом данных методом сравнения средних рангов для всех групп.
Data are presented as boxplots; Statistical processing of the data was carried out using the Kruskal—Wallis test, followed by statistical analysis of the data by comparing average ranks for all groups.
Диклофенак натрия оказывал дозозависимое противоболевое действие в формалиновом тесте у крыс. В дозе 10 мг/кг он значимо снижал количество свидетельствующих о боли спонтанных реакций крыс на 50,0% в острую фазу боли и на 31,7% в тоническую. Введение животным диклофенака натрия в меньшей дозе (1 мг/кг) приводило к значимому подавлению боли (на 26,8%) только в тоническую фазу (см. рис. 2, а, б). Эторикоксиб оказывал значимое противоболевое действие только в дозе 10 мг/кг и на 17,1% снижал количество свидетельствующих о боли спонтанных реакций крыс в тоническую фазу. На острую фазу боли препарат влияния не оказывал (см. рис. 2, в, г).
ЭМГПС при однократном пероральном введении в дозе 25 мг/кг не оказывал значимого влияния на болевое поведение крыс в формалиновом тесте. Однако его применение совместно с диклофенаком натрия или эторикоксибом в дозе 1 мг/кг усиливало выраженность противоболевого действия НПВП за счет появления у комбинаций препаратов способности снижать боль (на 50,0%) в острую фазу. Эффект комбинаций препаратов и диклофенака натрия в дозе 10 мг/кг в острую фазу формалиновой боли развивался за счет уменьшения ее длительности; болевые реакции крыс сразу после введения раствора формалина во всех опытных группах практически не различались. Применение ЭМГПС в дозе 25 мг/кг совместно с эторикоксибом в дозе 1 мг/кг еще и значимо на 23,5% усиливало противоболевой эффект НПВП в тоническую фазу боли (см. рис. 2). Значимых различий в поведении животных опытных групп во время интерфазы выявлено не было.
Влияние препаратов на соматическую боль в тесте механической гипералгезии при воспалении у крыс. При экссудативном воспалении лапы у крыс, вызванном инъекцией раствора каррагинана, развивается гипералгезия, которую регистрировали с помощью нитей фон Фрея через 3 и 24 ч после его индукции. При тактильной стимуляции порог чувствительности животных с каррагинановым отеком, которым вводили растворитель, через 3 ч после введения каррагинана составил 5 г, через 24 ч — 8 г против порога чувствительности, равного 60 г, у крыс, которым раствор каррагинана не вводили.
Диклофенак натрия в тесте механической гиперал-гезии при воспалении проявлял дозозависимый противоболевой эффект. Через 3 ч после индукции воспаления диклофенак натрия значимо увеличивал порог чувствительности животных по сравнению с группой, которой вводили раствор каррагинана и растворитель, только при введении в дозе 10 мг/кг (порог чувствительности составил 26 г). Через 24 ч порог чувствительности крыс, которым вводили диклофенак натрия в обеих изучаемых дозах (1 и 10 мг/кг), повышался до значения группы животных без отека лапы (рис. 3, а, б).
У крыс с каррагинановым отеком, которым вводили эторикоксиб в дозах 1 и 10 мг/кг, порог чувствительности при тактильной стимуляции поврежденной лапы был значимо выше по сравнению с группой животных с отеком лапы, которым вводили только растворитель, и через 3 и 24 ч после индукции воспаления составил 26 г (см. рис. 3, в, г).
ЭМГПС в дозе 25 мг/кг не влиял на порог чувствительности поврежденной лапы крыс с каррагинановым отеком при ее тактильной стимуляции. Однако его введение совместно с диклофенаком натрия в дозе 1 мг/кг приводило к повышению порога чувствительности животных по сравнению с введением только диклофенака натрия в дозе 1 мг/кг, который не оказывал на него значимого влияния. Порог чувствительности крыс, которым вводили диклофенак натрия в дозе 1 мг/кг с ЭМГПС в дозе 25 мг/кг, через 3 ч после введения флогогена составил 43 г, т.е. был в 8,6 раз выше, чем в группе крыс с отеком лапы, которым вводили только растворитель. Через 24 ч после индукции воспаления при тактильной стимуляции порог чувствительности крыс с отеком лапы, которым вводили комбинацию диклофенака натрия (1 мг/кг) с ЭМГПС (25 мг/кг), не отличался от порога чувствительности животных, которым вводили диклофенак натрия в обеих изучаемых дозах (см. рис. 3, а, б). На эффект эторикоксиба ЭМГПС (25 мг/кг) оказывал меньшее влияние. Порог чувствительности крыс, которым перорально вводили комбинацию эторикоксиба (1 мг/кг) и ЭМГПС (25 мг/кг), через 3 и 24 ч после индукции воспаления был незначимо повышен по сравнению с соответствующими значениями в группе животных, которым вводили только эторикоксиб (1 мг/кг), и составлял соответственно 43 и 60 г (см. рис. 3, в, г).
Обсуждение
Результаты проведенного экспериментального исследования свидетельствуют о том, что ЭМГПС в дозе 25 мг/кг усиливает противоболевое действие ингибиторов ЦОГ диклофенака натрия и эторикоксиба, используемых в малой дозе (1 мг/кг). Острая висцеральная боль у мышей, тоническая фаза формалиновой боли и механическая гипералгезия у крыс с отеком лапы возникают на фоне развития острого экссудативного воспаления, при котором повышено образование АФК, поэтому зарегистрированное влияние ЭМГПС на противоболевой эффект НПВП можно связать с его антиоксидантными свойствами. Острая фаза формалиновой боли обусловлена действием формалина на ионный канал TRPA1 афферентных нейронов. Ионный канал TRPA1 коэкспрес-сируется с ионным каналом TRPV1 [22], и антагонисты ионного канала TRPV1 способны снижать выраженность болевого поведения крыс в острую фазу индуцированной формалином боли [23]. Диклофенак натрия при пероральном введении в дозе 10 мг/кг, но не 1 мг/кг, подавляет формалиновую боль у крыс в острую фазу за счет влияния на ионные каналы TRPV1, так как известно, что этот НПВП снижает выраженность механической и тепловой гипералгезии, вызванной активацией этих каналов [24]. Применение ЭМГПС в дозе 25 мг/кг при введении совместно с диклофенаком натрия и эторикоксибом в дозе 1 мг/кг приводит к появлению значимого анальгетического эффекта в острую фазу формалиновой боли, что в первую очередь обусловлено его мембранотропными свойствами.
В проведенных нами ранее экспериментах показано, что на модели каррагинанового отека у мышей и крыс анти-экссудативный эффект комбинаций ЭМГПС в дозе 25 мг/кг и диклофенака натрия или эторикоксиба в дозе 1 мг/кг при однократном пероральном введении не уступает эффекту этих НПВП в дозе 10 мг/кг [25]. ЭМГПС в дозе 100 мг/кг усиливает антиэкссудативное и анальгетическое действия диклофенака натрия в дозе 5 мг/кг при однократном внутрибрюшинном введении препаратов крысам [26]. Однако при превентивном 10-дневном пероральном введении
Рис. 3. Влияние диклофенака натрия (а, б), эторикоксиба (в, г) и их комбинаций с ЭМГПС при однократном пероральном введении в тесте механической гипералгезии при воспалении у крыс через 3 (а, в) и 24 (б, г) ч после введения раствора каррагинана.
Fig. 3. The effect of diclofenac sodium (a, b), etoricoxib (c, d) and their combinations with EMGPS after a single oral administration in a test of mechanical hyperalgesia during inflammation in rats 3 (a, c) and 24 (b, d) hours after injection of carrageenan solution.
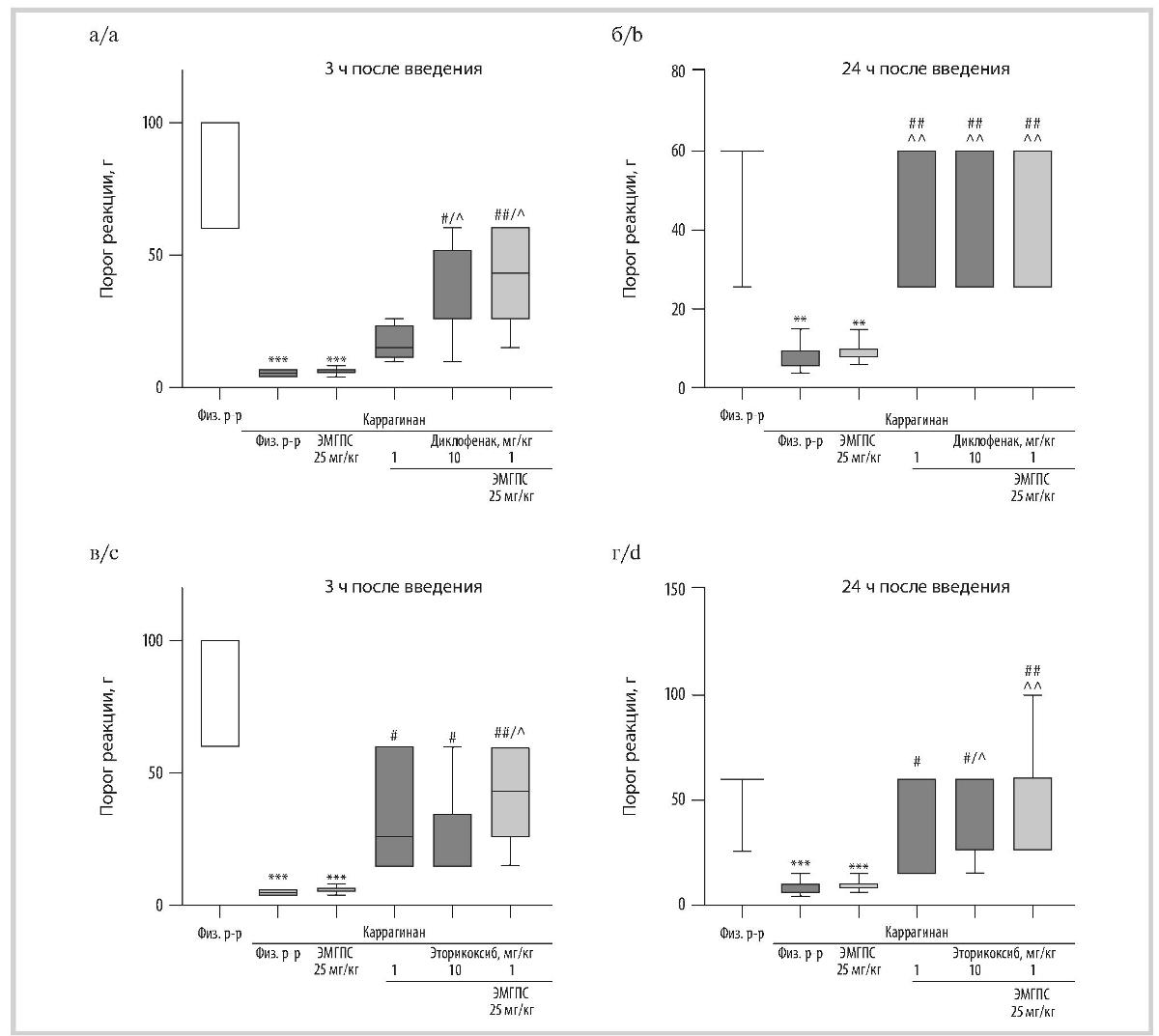
По оси ординат — порог болевой реакции в граммах (г). Данные представлены в виде боксплотов; ** — p<0,005, *** — p<0,0005 по сравнению с группой «Физиолоический раствор»; ## — p <0,005 по сравнению с группой «Каррагинан + физиологический раствор»; a — p <0,05, АА — p <0,005 по сравнению с группой «Каррагинан + ЭМГПС 25 мг/кг»; критерий Краскела—Уоллиса с последующим статистическим анализом данных методом сравнения средних рангов для всех групп.
On the ordinate — the threshold of pain reaction in grams (g). Data are presented as boxplots; ** — p<0.005, *** — p<0.0005 compared with the «Physiological solu-tion» group; ## — p<0.005 compared to the «Carrageenan + saline solution» group; A — p<0.05, AA — p<0.005 compared with the «Carrageenan + EMGPS 25 mg/kg» group; Kruskal—Wallis test followed by statistical analysis of data by comparing average ranks for all groups.
ЭМГПС в дозе 100 мг/кг в комбинации с диклофенаком натрия в дозе 5 мг/кг усиление противовоспалительного эффекта НПВП не превышает эффект однократного сочетанного введения этих препаратов при внутрибрюшинном введении [27]. В исследованиях in vitro установлено, что диклофенак натрия оказывает дозозависимый проок-сидантный эффект в реакции Фентона, зарегистрированный хемилюминесцентным методом, а ЭМГПС в концентрации 250 или 25 мкМ совместно с диклофенаком натрия в концентрациях соответственно 50, 100 или 10 мкМ уменьшает пик хемилюминесценции, который пропорционален скорости свободнорадикальных реакций, по сравнению с использованием только НПВП, но при этом увеличивает длительность и квантовый выход хемилюминесценции [28]. Значимых изменений кинетики хемилюминесценции не происходит при применении ЭМГПС в концентрации 25 мкМ с диклофенаком натрия в концентрации 1 мкМ, что подтверждает целесообразность применения препаратов в малых дозах [28].
Полученные данные согласуются с результатами клинических исследований. Так, применение ЭМГПС в комбинированной терапии совместно с НПВП, вазоактивными препаратами, миорелаксантами, витаминами группы B ускоряет темп снижения боли при пояснично-крестцовых радикулопатиях [29, 30, 31], остеохондрозе разных отделов позвоночника и радикулоишемии [32, 33, 34].
Заключение
Установлено, что на моделях острой висцеральной и соматической боли у мышей и крыс ЭМГПС при однократном пероральном введении в малой дозе 25 мг/кг усиливает противоболевой эффект диклофенака натрия и этори-коксиба, используемых в малой дозе 1 мг/кг. Полученные данные свидетельствуют о целесообразности клинического исследования применения ЭМГПС в комбинации с НПВП при висцеральной и соматической боли с целью оценки его способности повышать лечебный эффект НПВП.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Литература / References
1. Каратеев А.Е., Насонов Е.Л., Ивашкин В.Т. и др. Рациональное использование нестероидных противовоспалительных препаратов. Клинические рекомендации. Научно-практическая ревматология. 2018;56(1):1-29. Karateev AE, Nasonov EL, Ivashkin VT, et al. Clinical guidelines. NauchnoPrakticheskaja Revmatologija. 2018;56(1):1-29. (In Russ.). https://doi.org/10.14412/1995-4484-2018-1-29
2. Ross A, Hauser MD. Wonder why? The Acceleration of Articular Cartilage Degeneration in Osteoarthritis by Nonsteroidal Anti-inflammatory Drugs. J Prolother. 2010;2(1):305-322.
3. O’Neil CK, Hanlon JT, Marcum ZA. Adverse effects of analgesics commonly used by older adults with osteoarthritis: Focus on non-opioid and opioid analgesics. Am J Geriat Pharmacother. 2012;10(6):331-342. https://doi.org/10.1016/j.amjopharm.2012.09.004
4. Eling TE, Curtis JF. Xenobiotic metabolism by prostaglandin H synthase. Pharmacol Ther. 1992;53(2):261-273. https://doi.org/10.1016/0163-7258(92)90012-o
5. Wang ZQ, Porreca F, Cuzzocrea S, et al. A newly identified role for superoxide in inflammatory pain. J Pharmacol Exp Ther. 2004;309(3):869-878. https://doi.org/10.1124/jpet.103.064154
6. Khattab MM. TEMPOL, a membrane-permeable radical scavenger, attenuates peroxynitriteand superoxide anion-enhanced carrageenan-induced paw edema and hyperalgesia: a key role for superoxide anion. Eur J Pharmacol. 2006;548(1-3):167-173. https://doi.org/10.1016/j.ejphar.2006.08.007
7. Trotti D, Danbolt NC, Volterra A. Glutamate transporters are oxidant vulnerable: A molecular link between oxidative and excitotoxic neurodegeneration? Trends Pharm Sci. 1998;19(8):328-334. https://doi.org/10.1016/s0165-6147(98)01230-9
8. Maher P, Schubert D. Signaling by reactive oxygen species in the nervous system. Cell Mol Life Sci. 2000;57(8):1287-1305. https://doi.org/10.1007/pl00000766
9. Foran E, Trotti D. Glutamate transporters and the excitotoxic path to motor neuron degeneration in amyotrophic lateral sclerosis. Antioxidants & Redox Signaling. 2009;11(7):1587-1602. https://doi.org/10.1089/ars.2009.2444
10. Sandoval-Acuña C, Lopez-Alarcón C, Aliaga ME, Speisky H. Inhibition of mitochondrial complex I by various non-steroidal anti-inflammatory drugs and its protection by quercetin via a coenzyme Q-like action. Chem Biol Interact. 2012;199(1):18-28. https://doi.org/10.1016/j.cbi.2012.05.006
11. Gislason GH, Jacobsen S, Rasmussen JN, et al. Risk of death or reinfarction associated with the use of selective cyclooxygenase-2 inhibitors and nonselective nonsteroidal antiinflammatory drugs after acute myocardial infarction. Circulation. 2006;113(25):2906-2913. https://doi.org/10.1161/circulationaha.106.616219
12. Никольская И.Н., Хромова О.М., Ирхина И.С. и др. Сравнительная оценка клинической эффективности и безопасности препарата мексидол у больных с острым коронарным синдромом при включении в стандартную схему терапии. Кардиология и сердечно-сосудистая хирургия. 2013;6(3):37-42. Nikol’skaia IN, Khromova OM, Irkhina IS, et al. Comparative evaluation of clinical efficacy and safety of mexidol in patients with acute coronary syndrome in addition to standart regimen of treatment. Kardiologiya i Serdechno-Sosudistaya Khirurgiya. 2013;6(3):37-42. (In Russ.).
13. Воронина Т.А. Мексидол: Основные нейропсихотропные эффекты и механизм действия. Фарматека. 2009;6(180):35-38. Voronina TA. Mexidol: main neuropsychotropic effects and mechanisms of action. Farmateka. 2009;6(180):35-38. (In Russ.).
14. Дюмаев К.М., Воронина Т.А., Смирнов Л.Д. Антиоксиданты в профилактике и терапии патологий ЦНС. М.: Издательство Института биомедицинской химии; 1995. Dumaev KM, Voronina TA, Smirnov LD. Antioxidants in the prevention and therapy of Central nervous system pathologies. M.: Publishing House of the Institute of Biomedical Chemistry; 1995. (In Russ.).
15. Бурлакова Е.Б., Кайране Ч.Б., Молочкина Е.М., Хохлов А.П. Модификация липидов наружной мембраны митохондрий печени мышей и кинетических параметров мембраносвязанной моноаминоксидазы in vivo и in vitro. Вопросы медицинской химии. 1984;30(1):66-72. Burlakova EB, Kairane ChB, Molochkina EM, Khokhlov AP. Membranemodulating effects of 3-hydroxypyridine derivatives. Voprosy Meditsinskoi Khimii. 1984;30(1):66-72. (In Russ.).
16. Щулькин А.В. Влияние мексидола на развитие феномена эксайтотоксичности нейронов in vitro. Журнал неврологии и психиатрии им. С.С. Корсакова. 2012;112(2):35-39. Shchulkin AV. Effect of mexidol on the development of the phenomenon of the neuronal excitotoxicity in vitro. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2012;112(2):35-39. (In Russ.).
17. Лукьянова Л.Д. Современные проблемы адаптации к гипоксии. Сигнальные механизмы и их роль в системной регуляции. Патологическая физиология и экспериментальная терапия. 2011;(1):3-19. Lukyanova LD. Current issues of adaptation to hypoxia. signal mechanisms and their role in system regulation. Patologicheskaya Fiziologiya i Ehksperimental’naya Terapiya. 2011;(1):3-19. (In Russ.).
18. Лукьянова Л.Д. Сигнальные механизмы гипоксии. М.: РАН; 2019. Lukyanova LD. Signal’nye Mekhanizmy Gipoksii. M.: RAS; 2019. (In Russ.).
19. Воронина Т.А., Гузеватых Л.С. Методические рекомендации по изучению анальгетической активности лекарственных средств. М.: Гриф и К; 2012. Voronina TA, Guzevatykh LS. Metodicheskie rekomendatsii po izucheniyu anal’geticheskoi aktivnosti lekarstvennykh sredstv. M.: Grif and K; 2012. (In Russ.).
20. McNamara CR, Mandel-Brehm J, Bautista DM, et al. TRPA1 mediates formalin-induced pain. Proc Nat Acad Sci. 2007;104(33):13525-13530. https://doi.org/10.1073/pnas.0705924104
21. Fisher M, Carli G, Raboisson P, Reeh P. The interphase of the formalin test. Pain. 2014;155(3):511-521. https://doi.org/10.1016/j.pain.2013.11.015
22. Gouin O, L’Herondelle K, Lebonvallet N, et al. TRPV1 and TRPA1 in cutaneous neurogenic and chronic inflammation: pro-inflammatory response induced by their activation and their sensitization. Protein & Cell. 2017;8(9):644-661. https://doi.org/10.1007/s13238-017-0395-5
23. Kanai Y, Hara T, Imai A. Participation of the spinal TRPV1 receptors in formalin-evoked pain transduction: a study using a selective TRPV1 antagonist, iodoresiniferatoxin. J Pharm Pharmacol. 2006;58(4):489-493. https://doi.org/10.1211/jpp.58.4.0008
24. Nozadze I, Tsiklauri N, Gurtskaia G, Tsagareli MG. NSAIDs attenuate hyperalgesia induced by TRP channel activation. Data in Brief. 2016;6:668-673. https://doi.org/10.1016/j.dib.2015.12.055
25. Иванова Е.А., Матюшкин А.И., Васильчук А.Г., Воронина Т.А. Способность мексидола усиливать антиэкссудативное действие диклофенака натрия и эторикоксиба на модели каррагенанового отека у крыс и мышей. Вестник Московского университета. Биология. 2021;76(2):61-66. Ivanova EA, Matyushkin AI, Vasilchuk AG, Voronina TA. Ability of mexidol to enhance antiexudative effect of diclofenac sodium and etoricoxib in rats and mice with carrageenan-induced edema. Moscow University Biological Sciences Bulletin. 2021;76(2):61-66. (In Russ.). https://doi.org/10.3103/S0096392521020024
26. Иванова Е.А., Васильчук А.Г., Матюшкин А.И., Воронина Т.А. Усиление противовоспалительного и анальгетического эффекта диклофенака натрия при его применении в комбинации с мексидолом в эксперименте на грызунах. Экспериментальная и клиническая фармакология. 2020;83(7):22-26. Ivanova EA, Vasil’chuk AG, Matyushkin AI, Voronina TA. Enhancement of the anti-inflammatory and analgesic effect of diclofenac sodium in combination with mexidol. Ehksperimental’naya i Klinicheskaya Farmakologiya. 2020;83(7):22-26. (In Russ.). https://doi.org/10.30906/0869-2092-2020-83-7-22-26
27. Иванова Е.А., Васильчук А.Г., Матюшкин А.И., Воронина Т.А. Влияние комбинированного применения мексидола с диклофенаком натрия на выраженность экссудативного воспаления у крыс при превентивном десятидневном пероральном введении. Фармакокинетика и фармакодинамика. 2022;(1):14-19. Ivanova EA, Vasil’chuk AG, Matyushkin AI, Voronina TA. Effect of the combination of mexidol and diclofenac sodium on exudative inflammation in rats after ten-day preventive oral administration. Farmakokinetika i Farmakodinamika. 2022;(1):14-19. (In Russ.). https://doi.org/10.37489/2587-7836-2022-1-14-19
28. Иванова Е.А., Дмитриева С.А., Золотов Н.Н., Воронина Т.А. Влияние диклофенака натрия и его комбинаций с мексидолом на Fe2+индуцированную хемилюминесценцию. Химико-фармацевтический журнал. 2023;57(5):9-13. Ivanova EA, Dmitrieva SA, Zolotov NN, Voronina TA. The effect of diclofenac sodium and its combinations with mexidol on Fe2+-induced chemiluminescence. Pharmaceutical Chemistry Journal. 2023;57(5):9-13. (In Russ.). https://doi.org/10.30906/0023-1134-2023-57-5-9-13
29. Шатрова В.П., Месхи К.Т. Применение антиоксидантов в комплексном лечении вертеброгенных нейрососудистых синдромов. Журнал неврологии и психиатрии им. С.С. Корсакова. 2008;108(7):79-81. Shatrova VP, Meskhi KT. The use of antioxidants in the complex treatment of vertebrogenic neurovascular syndromes. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2008;108(7):79-81. (In Russ.).
30. Лихачева Е.Б. Мексидол в консервативном лечении пояснично-крестцовых радикулопатий. Фарматека. 2012;6(239):83-87. Likhacheva EB. Mexidol in the conservative treatment of lumbosacral radiculopathy. Farmateka. 2012;6(239):83-87. (In Russ.).
31. Лихачева Е.Б., Шоломов И.И. Динамика клинико-иммунологических показателей в оценке эффективности применения Мексидола при пояснично-крестцовой радикулопатии. Журнал неврологии и психиатрии им. С.С. Корсакова. 2006;106(10):52-57. Likhacheva EB, Sholomov II. Clinical and immunological assessment of efficacy of mexidol in the treatment of lumbosacral radiculopathy. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2006;106(10):52-57. (In Russ.).
32. Хужахметова Д.Х. Применение Мексидола по стандартизированной схеме введения в лечении остеохондрозов позвоночника. Бюллетень экспериментальной биологии и медицины. 2012;1:219-225. Khuzhakhmetova DH. The use of Mexidol in a standardized regimen for the treatment of osteochondrosis of the spine. Byulleten’ Ehksperimental’noi Biologii i Meditsiny. 2012;1:219-225. (In Russ.).
33. Синченко О.Г. Использование антигипоксантных и нейрометаболических свойств Мексидола в лечении вертеброгенного радикулоишемического синдрома. Бюллетень экспериментальной биологии и медицины. 2012;1:60-62. Sinchenko OG. The use of antihypoxant and neurometabolic properties of Mexidol in the treatment of vertebrogenic radiculoishemic syndrome. Byulleten’ Ehksperimental’noi Biologii i Meditsiny. 2012;1:60-62. (In Russ.).
34. Андреев В.В. Комплексное лечение спондилогенных радикулоишемий с применением Мексидола. Бюллетень экспериментальной биологии и медицины. 2012;S1:63-68. Andreev VV. Complex treatment of spondylo genic radiculo-ischemia with the use of Mexidol. Byulleten’ Ehksperimental’noi Biologii i meditsiny. 2012;S1:63-68. (In Russ.).
Investigation of the effect of ethylmethylhydroxypyridine succinate on the effectiveness of non-steroidal anti-inflammatory drugs for visceral and somatic pain in mice and rats
E.A. Ivanova, A.G. Vasilchuk, A.I. Matyushkin, T.A. Voronina
Zakusov Institute of Pharmacology, Moscow, Russia
Abstract
Objective. To study the effect of ethylmethylhydroxypyridine succinate (EMHPS) on the analgesic effect of the non-selective cyclooxygenase (COX) inhibitor diclofenac sodium and the selective COX-2 inhibitor etoricoxib in models of acute visceral and somatic pain and to evaluate the possibility of using EMHPS in combination with COX inhibitors to reduce their doses while maintaining analgesic efficiency.
Material and methods. We studied the effect of EMHPS with a single oral administration on the analgesic effects of non-steroidal anti-inflammatory drugs (NSAIDs): the non-selective COX inhibitor diclofenac sodium and the selective COX-2 inhibitor etoricox-ib — on models of acute visceral (vinegar writhing test) and somatic pain (formalin test and mechanical hyperalgesia during inflammation) in an experiment on mice and rats.
Results. In a model of acute visceral pain in mice, EMGPS (25—100 mg/kg) does not have a significant effect on its severity, but enhances the analgesic effect of diclofenac sodium (0.5 mg/kg) and etoricoxib (1 mg/kg). In the formalin test in rats, which simulates pain during surgical incisions (trauma), EMGPS (25 mg/kg) increases the severity of the analgesic effect of COX inhibitors (1 mg/kg), primarily by reducing pain in the acute phase caused by the effect of formalin on afferent neurons. In a model of mechanical hyperalgesia in rats caused by exudative inflammation after injection of a carrageenan solution into the paw, EMHPS enhances the effect of diclofenac to a greater extent than etoricoxib.
Conclusion. The data obtained indicate the feasibility of a clinical study of the use of EMGPS in combination with NSAIDs for visceral and somatic pain in order to assess its ability to increase the therapeutic effect of NSAIDs.
Keywords: ethylmethylhydroxypyridine succinate, non-steroidal anti-inflammatory drugs, visceral pain, somatic pain, mice, rats.
Information about the authors:
Ivanova E.A. — https://orcid.org/0000-0003-4961-2051
Vasilchuk A.G. — https://orcid.org/0000-0002-9079-1322
Matyushkin A.I. — https://orcid.org/0000-0001-7640-0551
Voronina T.A. — https://orcid.org/0000-0001-7065-469X
Corresponding author: Ivanova E.A. — e-mail: iwanowaea@yandex.ru
To cite this article: Ivanova EA, Vasilchuk AG, Matyushkin AI, Voronina TA. Investigation of the effect of ethylmethylhydroxypyridine succinate on the effectiveness of non-steroidal anti-inflammatory drugs for visceral and somatic pain in mice and rats. S.S. Korsakov Journal of Neurology and Psychiatry = Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2023;123(12):1—9. (In Russ.). doi.org/10.17116/jnevro20231231211
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Описание препарата Нейрокс® (раствор для внутривенного и внутримышечного введения, 50 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2021 году
Дата согласования: 26.04.2021
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Нейрокс®
- Заказ в аптеках Москвы
Фотографии упаковок

26.04.2021
Действующее вещество
ATX
Фармакологическая группа
Нозологическая классификация (МКБ-10)
Список кодов МКБ-10
- F06.7 Легкое когнитивное расстройство
- F10.3 Абстинентное состояние
- F41.9 Тревожное расстройство неуточненное
- F48 Другие невротические расстройства
- F48.9 Невротическое расстройство неуточненное
- G90 Расстройства вегетативной [автономной] нервной системы
- G93.4 Энцефалопатия неуточненная
- H40.1 Первичная открытоугольная глаукома
- I21 Острый инфаркт миокарда
- I67.2 Церебральный атеросклероз
- I67.9 Цереброваскулярная болезнь неуточненная
- K65.0 Острый перитонит
- K85 Острый панкреатит
- S06 Внутричерепная травма
- S09 Другие и неуточненные травмы головы
- T43.3 Антипсихотическими и нейролептическими препаратами
- T90 Последствия травм головы
Состав
| Раствор для внутривенного и внутримышечного введения | 1 амп. (2/5 мл) |
| действующее вещество: | |
| этилметилгидроксипиридина сукцинат | 100/250 мг |
| вспомогательные вещества: натрия дисульфит; вода для инъекций |
Описание лекарственной формы
Раствор: бесцветная или слегка желтоватая прозрачная жидкость.
Фармакологическое действие
Фармакодинамика
Этилметилгидроксипиридина сукцинат (ЭМГПС) является ингибитором свободнорадикальных процессов, мембранопротектором, обладающим антигипоксическим, стрессопротективным, ноотропным, противосудорожным и анксиолитическим действием. Относится к классу 3-оксипиридинов. Механизм действия обусловлен антиоксидантным и мембранопротекторным свойствами. Подавляет перекисное окисление липидов, повышает активность супероксиддисмутазы, повышает соотношение липид-белок, улучшает структуру и функцию мембраны клеток. Модулирует активность мембраносвязанных ферментов, рецепторных комплексов, что способствует их связыванию с лигандами, сохранению структурно-функциональной организации биомембран и транспорта нейромедиаторов, улучшению синаптической передачи. Повышает концентрацию в головном мозге дофамина. Усиливает компенсаторную активацию аэробного гликолиза и снижает степень угнетения окислительных процессов в цикле Кребса в условиях гипоксии с увеличением уровня АТФ и креатинфосфата, активирует энергосинтезирующую функцию митохондрий. Повышает резистентность организма к воздействию различных повреждающих факторов при патологических состояниях (шок, гипоксия и ишемия, нарушение мозгового кровообращения, интоксикация этанолом и антипсихотическими ЛС). Улучшает метаболизм и кровоснабжение головного мозга, микроциркуляцию и реологические свойства крови, уменьшает агрегацию тромбоцитов. Стабилизирует мембраны клеток крови (эритроциты и тромбоциты), снижая вероятность развития гемолиза. Обладает гиполипидемическим действием, уменьшает содержание общего Хс и ЛПНП.
Нормализует метаболические процессы в ишемизированном миокарде, уменьшает зону некроза, восстанавливает и/или улучшает электрическую активность и сократимость миокарда, а также увеличивает коронарный кровоток в зоне ишемии, повышает антиангинальную активность нитропрепаратов, уменьшает последствия реперфузионного синдрома при острой коронарной недостаточности.
Стрессопротекторное действие проявляется в нормализации постстрессового поведения, соматовегетативных нарушений, восстановлении циклов «сон-бодрствование», нарушенных процессов обучения и памяти, снижении дистрофических изменений в различных структурах головного мозга.
ЭМГПС обладает выраженным антитоксическим действием при абстинентном синдроме, устраняет неврологические и нейротоксические проявления острой алкогольной интоксикации, корректирует поведенческие и когнитивные нарушения. Под влиянием ЭМГПС усиливается действие транквилизирующих, нейролептических, антидепрессивных, снотворных и противосудорожных средств, что позволяет снизить их дозы и уменьшить побочные эффекты.
Фармакокинетика
При в/м введении препарат определяется в плазме крови на протяжении 4 ч после введения. Tmax при в/м введении — 0,3–0,58 ч. Cmax при в/м введении в дозе 400–500 мг — 2,5–4 мкг/мл. ЭМГПС быстро переходит из кровяного русла в органы и ткани и быстро выводится из организма. Среднее время удержания препарата в организме при в/м введении — 0,7–1,3 ч.
Метаболизируется в печени путем глюкуронирования. Быстро выводится с мочой, в основном в виде метаболитов (50% за 12 ч) и в незначительном количестве — в неизмененном виде (0,3% за 12 ч). Наиболее интенсивно выводится в течение первых 4 ч после приема препарата. Показатели выведения с мочой неизмененного препарата и метаболитов имеют значительную индивидуальную вариабельность.
Показания
- острые нарушения мозгового кровообращения (в составе комплексной терапии);
- черепно-мозговая травма, последствия черепно-мозговых травм;
- дисциркуляторная энцефалопатия;
- синдром вегетативной (нейроциркуляторная) дистонии;
- легкие когнитивные расстройства атеросклеротического генеза;
- тревожные расстройства при невротических и неврозоподобных состояниях;
- острый инфаркт миокарда (с первых суток) в составе комплексной терапии;
- первичная открытоугольная глаукома различных стадий, в составе комплексной терапии;
- купирование абстинентного синдрома при алкоголизме с преобладанием неврозоподобных и вегетативно-сосудистых расстройств;
- острая интоксикация антипсихотическими ЛС;
- острые гнойно-воспалительные процессы брюшной полости (острый некротический панкреатит, перитонит — в составе комплексной терапии).
Противопоказания
- повышенная индивидуальная чувствительность к препарату или его компонентам;
- острая почечная недостаточность;
- острая печеночная недостаточность;
- беременность;
- грудное вскармливание;
- детский возраст.
С осторожностью: аллергические заболевания и реакции в анамнезе.
Способ применения и дозы
В/м или в/в (струйно или капельно). При инфузионном способе введения препарат следует разводить в 0,9% растворе натрия хлорида.
Струйно Нейрокс® вводят медленно, в течение 5–7 мин, капельно — со скоростью 40–60 капель в минуту.
Максимальная суточная доза не должна превышать 1200 мг.
При острых нарушениях мозгового кровообращения Нейрокс® применяют в комплексной терапии в первые 10–14 дней — в/в капельно по 200–500 мг 2–4 раза в сутки, затем — в/м по 200–250 мг 2–3 раза в сутки в течение 2 нед.
При ЧМТ и последствиях ЧМТ Нейрокс® применяют в течение 10–15 дней в/в капельно по 200–500 мг 2–4 раза в сутки.
При дисциркуляторной энцефалопатии в фазе декомпенсации Нейрокс® следует назначать в/в струйно или капельно в дозе 200–500 мг 1–2 раза в сутки в течение 14 дней. Затем — в/м по 100–250 мг/сут в течение последующих 2 нед.
Для курсовой профилактики дисциркуляторной энцефалопатии Нейрокс® вводят в/м в дозе 200–250 мг 2 раза в сутки в течение 10–14 дней.
При нейроциркуляторной дистонии, невротических и неврозоподобных состояниях препарат вводят в/м по 50–400 мг/сут в течение 14 дней.
При легких когнитивных нарушениях у больных пожилого возраста и при тревожных расстройствах препарат применяют в/м в дозе 100–300 мг/сут в течение 14–30 дней.
При остром инфаркте миокарда в составе комплексной терапии Нейрокс® вводят в/в или в/м в течение 14 сут, на фоне традиционной терапии инфаркта миокарда (включающей нитраты, β-адреноблокаторы, ингибиторы АПФ, тромболитики, антикоагулянтные и антиагрегантные препараты, а также симптоматические средства по показаниям). В первые 5 сут Нейрокс® вводят в/в, в последующие 9 сут препарат может вводиться в/м. В/в введение препарата производят путем капельной инфузии медленно (во избежание побочных эффектов), в течение 30–90 мин (в 100–150 мл 0,9% раствора натрия хлорида или 5% раствора декстрозы (глюкозы), при необходимости возможно медленное струйное в/в введение препарата, продолжительностью не менее 5 мин. Введение препарата (в/в или в/м) осуществляют 3 раза в сутки, через каждые 8 ч. Суточная доза составляет 6–9 мг/кг, разовая доза — 2–3 мг/кг. Максимальная суточная доза не должна превышать 800 мг, разовая — 250 мг.
При открытоугольной глаукоме различных стадий в составе комплексной терапии Нейрокс® вводят в/м по 100–300 мг/сут, 1–3 раза в сутки в течение 14 дней.
При абстинентном алкогольном синдроме Нейрокс® вводят в/м или в/в капельно в дозе 200–500 мг 2–3 раза в сутки в течение 5–7 дней.
При острой интоксикации антипсихотическими лекарственными препаратами Нейрокс® вводят в/в в дозе 200–500 мг/сут в течение 7–14 дней.
При острых гнойно-воспалительных процессах брюшной полости (острый некротический панкреатит, перитонит) Нейрокс® назначают в первые сутки как в предоперационном, так и в послеоперационном периоде. Вводимые дозы зависят от формы и тяжести заболевания, распространенности процесса, вариантов клинического течения. Отмена препарата должна производиться постепенно, только после устойчивого положительного клинико-лабораторного эффекта.
При остром отечном (интерстициальном) панкреатите Нейрокс® назначают по 200–500 мг 3 раза в день, в/в капельно (в 0,9% растворе натрия хлорида) и в/м. Легкая степень тяжести некротического панкреатита — по 100–200 мг 3 раза в день капельно (в 0,9% растворе натрия хлорида) и в/м. Средняя степень тяжести — по 200 мг 3 раза в день, в/в капельно (в 0,9% растворе натрия хлорида). Тяжелое течение — в пульс-дозировке 800 мг в первые сутки, при двукратном режиме введения; далее по 200–500 мг 2 раза в день с постепенным снижением суточной дозы. Крайне тяжелое течение — в начальной дозировке 800 мг/сут до стойкого купирования проявлений панкреатогенного шока, до стабилизации состояния по 300–500 мг 2 раза в день в/в капельно (в 0,9% растворе натрия хлорида) с постепенным снижением суточной дозировки.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
При парентеральном введении (особенно в/в струйно): сухость, металлический привкус во рту, ощущение разливающегося тепла во всем теле, першение в горле и дискомфорт в грудной клетке, ощущение нехватки воздуха (как правило, связаны с чрезмерно высокой скоростью введения и носят кратковременный характер).
При длительном применении — тошнота, метеоризм, нарушение сна (сонливость или нарушение засыпания).
Аллергические реакции.
Взаимодействие
Усиливает действие бензодиазепиновых анксиолитиков, противоэпилептических (карбамазепин), противопаркинсонических (леводопа) ЛС, нитратов. Уменьшает токсические эффекты этанола.
Передозировка
Симптомы: нарушение сна (бессонница, в некоторых случаях — сонливость); при в/в введении — незначительное и кратковременное (до 1,5–2 ч) повышение АД.
Лечение: как правило, не требуется — симптомы исчезают самостоятельно в течение суток. В тяжелых случаях при бессоннице — нитразепам 10 мг, оксазепам 10 мг или диазепам 5 мг. При чрезмерном повышении АД — гипотензивные ЛС под контролем АД.
Особые указания
В период лечения необходимо соблюдать осторожность при вождении автотранспорта и занятии другими потенциально опасными видами деятельности, требующими концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Раствор для внутривенного и внутримышечного введения, 50 мг/мл.
По 2 мл в ампулах светозащитного стекла с цветным кольцом разлома или цветной точкой и насечкой. На ампулы дополнительно наносят 1, 2 или 3 цветных кольца и/или двухмерный штрихкод, и/или буквенно-цифровую кодировку, или без дополнительных цветных колец, двухмерного штрихкода, буквенно-цифровой кодировки.
По 5 амп. в контурной ячейковой упаковке из пленки ПВХ и пленки полимерной или без нее. По 1, 2, 4 или 10 контурных ячейковых упаковок вместе с инструкцией по применению в пачке из картона.
По 5 мл в ампулах светозащитного стекла с цветным кольцом разлома или цветной точкой и насечкой. На ампулы дополнительно наносят 1, 2 или 3 цветных кольца и/или двухмерный штрихкод, и/или буквенно-цифровую кодировку, или без дополнительных цветных колец, двухмерного штрихкода, буквенно-цифровой кодировки.
По 5 амп. в контурной ячейковой упаковке из пленки ПВХ и пленки полимерной или без нее. По 1, 2, 4 контурные ячейковые упаковки вместе с инструкцией по применению в пачке из картона.
Производитель
ЗАО «ФармФирма «Сотекс».
141345, Московская обл., Сергиево-Посадский муниципальный р-н, сельское поселение Березняковское, пос. Беликово, 10, 11, 12.
Юридическое лицо, на имя которого выдано регистрационное удостоверение, и организация, принимающая претензии от потребителей. ЗАО «ФармФирма «Сотекс». 141345, Московская обл., Сергиево-Посадский муниципальный р-н, сельское поселение Березняковское, пос. Беликово, 11.
Тел./факс: (495) 956-29-30.
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
5 лет.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
В состав препарата в качестве основных действующих веществ входят этилметилгидроксипиридина сукцинат и витамин В6. В качестве вспомогательного компонента в препарате МексиВ 6® есть Магния лактата дигидрат в достаточном количестве (327, 6 мг) для оказания терапевтического эффекта.
Компоненты препарата МексиВ 6® обладают хорошо изученными эффектами, действуют синергично, дополняя и усиливая действия друг друга.
ЭМГПС (этилметилгидроксипирина сукцинат) история создания
Этилметилгидроксипиридина сукцинат (ЭМГПС) был синтезирован в начале 1980-х годов в ГУ НИИ Фармакологии РАМН под руководством академика РАМН Артура Викторовича Вальдмана фармакологами Л. Д. Смирновым и В. И. Кузьминым, там же были выявлены его фармакологические эффекты, проведено изучение механизма действия, выполнены доклинические исследования по токсикологии и фармакокинетике, проведены первые клинические испытания. В течение 16 лет ЭМГПС активно изучался в клинике при лечении различных нозологий в качестве ноотропного и церебропротекторного средства.
В 1996 году ЭМГПС был зарегистрирован под торговым названием «Мексидол®» как антиоксидантное средство. На российском рынке на данный момент существует несколько дженериков.
Этилметилгидроксипиридина сукцинат – производное янтарной кислоты и оксипиридина.
Янтарная кислота – один из важнейших компонентов цикла Кребса. Ее роль в организме заключается в том, что она:
- быстро повышает уровень макроэргических фосфатов (АТФ, АДФ);
- ускоряет оборот в клетке восстановительных ферментов;
- поддерживает транспорт кальция.
Важно подчеркнуть, что янтарная кислота легко окисляется даже в условиях гипоксии. Более того, при гипоксии активируется именно сукцинат-зависимое дыхание митохондрий, что способствует стимуляции образования АТФ. При этом энергетическая мощность процесса синтеза АТФ при окислении янтарной кислоты существенно выше, чем при окислении любого другого субстрата. В целом, можно сказать, что янтарная кислота выполняет роль универсального адаптогена, способствующего активации процессов восстановления организма, в первую очередь головного мозга, в условиях стрессового воздействия, примером которого может служить ишемия и гипоксия.
Вместе с тем в условиях длительной ишемии неизбежно проявляется феномен «срыва адаптации», когда сукцинат-зависимые процессы уже не в состоянии поддерживаться на должном уровне за счет внутренних резервов организма, что ведет к усугублению энергодефицита клеток, активации перекисного окисления липидов и, в частности, мембранных фосфолипидов. Результатом этого служат нарушения естественной транспортно-защитной функции биологических мембран, повышение их микровязкости, изменения их проницаемости для различных ионов и, в результате, изменения в жизнедеятельности нейрона, а в дальнейшем – его деструкция и гибель.
Особо опасны свободные радикалы для митохондрий, в частности для митохондриальной ДНК (мтДНК). Поскольку митохондрии используют 85-99% всего кислорода, потребляемого клетками, то самые большие количества супероксидрадикала образуются именно в митохондриях. В результате отмечается окислительное повреждение молекулы мтДНК и, соответственно, повышение вероятности развития мутаций и процессов апоптоза.
В клиническом плане повышенная продукция свободных радикалов является одной из существенных причин:
- длительного спазма церебральных сосудов;
- прогрессирования постишемического отека;
- дегенерации нейронов за счет нарушения целостности мембран;
т.е. важным механизмом развития неврологического и когнитивного дефицита.
Все вышесказанное обуславливает целесообразность направленной фармакологической коррекции уровня сукцината в ЦНС в условиях ишемии с помощью препаратов янтарной кислоты.
Другой химический компонент оксипиридин является одним из мощных «скавенджеров» – ловушкой свободных радикалов, обладающего способностью нейтрализовать образовавшийся радикал ОН-, причем именно в условиях ишемии, поскольку он реализуется даже при недостатке кислорода (в отличие от большинства других препаратов-антиоксидантов).
Таким образом, для этилметилгидроксипиридина сукцината характерен в полной мере комплексный антиоксидантный эффект, несвойственный многим препаратам-антиоксидантам, применяющимся в неврологической практике. В итоге реализуется важнейшее в плане нейропротекции действие этилметилгидроксипиридина сукцината – мембранопротекторное – как в отношении внешних, так и внутренних – митохондриальных мембран, обеспечивается нормализация кальциевого тока, содержания липидных фракций и соотношения холестерин/фосфолипиды.
Кроме того, этилметилгидроксипиридина сукцинат за счет своего влияния на конформационное состояние рецепторных структур обладает неспецифическим модулирующим эффектом в отношении различных нейромедиаторных систем (ГАМК, дофамин, ацетилхолин), что в клиническом плане определяет его ноотропное, противотревожное и противосудорожное действие.

Пиридоксин (витамин В6) входит в состав ферментов, участвующих в метаболизме аминокислот (триптофан, метионин, цистеин, глутаминовая кислота и др.), которые входят в состав белков, в первую очередь, клеток нервной ткани.
Магний является жизненно важным элементом, который находится во всех тканях организма и необходим для нормального функционирования клеток, участвует в большинстве реакций обмена веществ. В частности, он участвует в регуляции передачи нервных импульсов и в сокращении мышц. Организм получает магний вместе с пищей. Недостаток магния в организме может наблюдаться при нарушении режима питания (диета) или при увеличении потребности в магнии (при повышенной физической и умственной нагрузке, стрессе, применении диуретиков).
Итак, основные свойства (механизм действия) Мекси В6®:
- антиоксидантные свойства и способность стабилизировать мембраны клеток;
- способность активировать энергосинтезирующие функции митохондрий;
- способность модулировать работу рецепторных комплексов и прохождение ионных токов;
- способность улучшать синаптическую передачу и взаимосвязь структур мозга.
Благодаря этому механизму действия, МексиВ 6® оказывает влияние на ключевые базисные звенья патогенеза различных заболеваний, имеет большой спектр клинических эффектов, реализующихся, по крайней мере, на двух уровнях — нейрональном и сосудистом.
Основные эффекты МексиВ 6®:
Антигипоксический эффект.
МексиВ 6® оказывает отчетливое антигипоксическое и противоишемическое действие, что выражается в способности препарата увеличивать продолжительность жизни и число выживших животных в условия различных гипоксических состояний: гипобарической гипоксии, гипоксии с гиперкапнией в гермообъеме и гемической гипоксии. Механизм реализации этого эффекта связан с влиянием на эндогенное дыхание митохондрий, с активацией энергосинтезирующей функции митохондрий, а также – тем, что сукцинат в условиях гипоксии способен напрямую окисляться дыхательной цепью.
Нейропротекторный эффект.
МексиВ 6® вызывает изменение функциональной активности биологической мембраны, которое приводит к конформационным изменениям белковых макромолекул синаптических мембран, вследствие чего препарат оказывает модулирующее влияние на активность мембраносвязанных ферментов, ионных каналов и рецепторных комплексов, в частности, бензодиазепиновый, ГАМК, ацетилхолиновый, усиливая их способность к связыванию с лигандами, повышая активность нейромедиаторов и активацию синаптических процессов.
Антистрессорный эффект.
МексиВ 6® выражается в нормализации постагрессового поведения, соматовегетативных показателей, восстановлении циклов сон-бодрствование и нарушенных процессов обучения и памяти, уменьшении язв желудка, снижении дистрофических, морфологических изменений, возникающих после стресса в различных структурах мозга и в миокарде.
Ноотропный эффект.
МексиВ 6® выражается в способности улучшать обучение и память, способствовать сохранению памятного следа и противодействовать процессу угасания привитых навыков и рефлексов. МексиВ 6® оказывает выраженное антиамнестическое действие, устраняя нарушения памяти, вызванные различными воздействиями (электрошок, травма головного мозга, депривация сна, введение скополамина, этанола, бензодиазепинов и др.).
Противотревожный эффект.
МексиВ 6® обладает выраженным транквилизирующим действием, способностью устранять тревогу, страх, напряжение, беспокойство, в частности в конфликтных ситуациях. При парентеральном введении он имеет сходный по глубине эффект с диазепамом (седуксеном) и алпразоламом (ксанакс).
Противосудорожный эффект.
МексиВ 6® оказывает влияние как на первично-генерализованные судороги, вызванные прежде всего введением ГАМК-ергических веществ, так и на эпилептиформную активность мозга с хроническим эпилептогенным очагом.
Вегетотропный эффект.
МексиВ 6® эффективен при вегето-сосудистых дистониях, особенно протекающих по пароксизмальному типу. Он обладает вегетонормализующим и отчетливо выраженным транквилизирующим действием при невротических и неврозоподобных состояниях.
Антиалкогольный эффект.
МексиВ 6® проявляется в устранении неврологических и нейротоксических проявлений острой алкогольной интоксикации, вызванной однократным введением высоких доз этанола. Также он восстанавливает нарушения поведения вегетативного и эмоционального статуса, ухудшение когнитивных функций, процессов обучения и памяти, вызванные длительным (5 месяцев) введением этанола и его отменой.
Антиатерогенный эффект.
МексиВ 6® снижает содержание атерогенных липопротеидов и триглицеридов, повышает уровень антиатерогенных липопротеидов высокой плотности в сыворотке крови.
Геропротективный эффект.
МексиВ 6® оказывает отчетливое корригирующее влияние на нарушенные при старении процессы обучения и памяти, улучшая процесс фиксации, сохранения и воспроизведения информации, способствует восстановлению эмоционального и вегетативного статуса, уменьшает проявления неврологического дефицита, снижает уровень в мозге и крови маркеров старения -липофусцина, малонового альдегида, холестерина.

МексиВ 6® повышает резистентность организма к действию различных экстремальных повреждающих факторов, таких как:
- нарушение сна;
- конфликтные ситуации;
- стресс;
- травмы головного мозга;
- электрошок;
- физические нагрузки;
- гипоксия;
- ишемия;
- различные интоксикации, в том числе этанолом.
Также он обладает способностью потенцировать действие других центральнодействующих веществ, в особенности тех, которые реализуют свое действие как прямые агонисты рецепторов (нейролептики, антидепрессанты, снотворные, противосудорожные, противопаркинсонические). Это позволяет уменьшить их дозы и снять большинство побочных эффектов.
Показания к применению
В составе комбинированной терапии:
- Дисциркуляторной энцефалопатии;
- Синдрома вегетативной дистонии;
- Тревожных состояниях при невротических и неврозоподобных состояниях;
- Абстинентного синдрома при алкоголизме с преобладанием неврохоподобных и вегетативно-сосудистых расстройств;
- Ишемической болезни сердца (профилактика приступов);
- Состояния после острой интоксикации антипсихотическими средствами;
- Астенического состояния, а также для профилактики развития соматических заболеваний под воздействием экстремальных факторов и нагрузок.
Противопоказания
Гиперчувствительность;
Острая печеночная и/или почечная недостаточность;
Беременность;
Лактация;
Детский возраст.
С осторожностью
- Язвенная болезнь желудка и 12-перстной кишки
Способ применения и дозы
Внутрь, по 1 таблетке 3 раза в сутки. Максимальная суточная доза 6 таб/сут.
Длительность лечения – 2-8 недель.
При необходимости возможно проведение повторных курсов.
Побочное действие
Тошнота, сухость во рту, диарея, сонливость, аллергические реакции, гиперсекреция соляной кислоты, онемение, появление чувства сдавления в конечностях – симптом «чулок» и «перчаток», снижение лактации (иногда это используют как лечебный эффект.
МексиВ 6 — лекарственный препарат, который должен быть выписан специалистом*
*А.Н. БОГОЛЕПОВА, С.Г. БУРД, Я.Е. ФРИС Возможности использования комбинированной терапии у больных с хронической ишемией мозга «ЖНиП им. Корсакова» № 8 – 2018.
Состав
В составе 1 мл раствора для внутривенного и внутримышечного введения содержится 50 мг действующего вещества этилметилгидроксипиридина сукцината и вспомогательные вещества: 1 мг натрия дисульфита и до 1 мл воды для инъекций.
Форма выпуска
- 1 ампула (2 мл) по 5, 10, 20 и 50 штук в картонной упаковке;
- 1 ампула (5 мл) по 5, 10 и 20 штук в картонной упаковке.
Фармакологическое действие
- препарат защищает мембраны клеток головного мозга (нейронов) от любых воздействий (мембранопротективное действие);
- улучшает кровообращение в области головного мозга и снижает потребность нейронов в кислороде (антигипоксическое действие);
- оказывает прямое активирующее влияние на умственную деятельность (ноотропное действие);
- снимает чувство тревоги, страха и напряжения;
- повышает стрессоустойчивость (анксиолитическое действие);
- подавляет развитие судорог (противосудорожное действие).
Фармакодинамика и фармакокинетика
Активное действующее вещество Нейрокса этилметилгидроксипиридина сукцинат (ЭМГПС) — подавляет токсическое действие свободных радикалов, образующихся в процессе обмена веществ в организме человека и разрушающих клетки и ткани. Он защищает мембраны (оболочки) клеток головного мозга от любых воздействий, улучшает их строение и функцию (в том числе транспортировку кислорода и нейромедиаторов – веществ, с помощью которых передается информация в клетках головного мозга).
Под действием Нейрокса повышается концентрация в головном мозге дофамина, который называют гормоном удовольствия. Все это приводит к повышению стрессоустойчивости и умственных способностей, снижению тревожности и судорожной готовности. Нейрокс оказывает антитоксическое воздействие при острой и хронической алкогольной интоксикации, при абстинентном синдроме (интоксикации, развивающейся на фоне отрыва от алкоголя у больных хроническим алкоголизмом) и при передозировке средств, влияющих на центральную нервную систему.
Длительность действия Нейрокса при внутримышечном введении — до 4 часов. Максимальная концентрация в плазме крови наступает через 20 – 40 минут после введения. Действующее вещество быстро переходит из кровеносных сосудов в органы и ткани и также быстро выводится из организма с мочой, предварительно метаболизируясь (разлагаясь на продукты обмена – метаболиты) в печени.
Показания к применению Нейрокса
Показания к применению Нейрокса:
- острые нарушения мозгового кровообращения, в том числе ишемические инсульты;
- заболевания, связанные с нарушением обменных процессов в клетках головного мозга (энцефалопатии);
- состояния после перенесенных черепно-мозговых травм;
- легкие умственные нарушения на фоне атеросклероза;
- тревожные состояния на фоне неврозов и психических заболеваний;
- инфаркт миокарда (в составе комплексного лечения).
Показания к применению Нейрокса включают в себя также алкогольную интоксикацию, абстинентный синдром на фоне хронического алкоголизма и острую интоксикацию антипсихотическими лекарственными средствами (нейролептиками).
Противопоказания для применения Нейрокса
Нейрокс нельзя применять при следующих заболеваниях и состояниях:
- тяжелых заболеваниях, сопровождающихся острыми нарушениями функции почек или печени (острой почечной и печеночной недостаточностью);
- беременности и кормлении ребенка грудью;
- повышенной чувствительности организма к компонентам препарата;
- детям любого возраста.
С осторожностью Нейрокс применяют при аллергических заболеваниях и реакциях, которые были у пациента в прошлом. Во время лечения следует соблюдать осторожность при вождении автомобиля и выполнении других работ, требующих повышенной концентрации внимания и быстроты ответных реакций.
Побочные эффекты Нейрокса
На фоне быстрого введения препарата (особенно при внутривенном струйном введении) возможно появление сухости и металлического привкуса во рту, прилива тепла, першения в горле и чувства нехватки воздуха. Возможны также аллергические реакции.
Если применять препарат курсами, превышающими по длительности рекомендованные, то нельзя исключить появления тошноты, повышенного газообразования в кишечнике и кишечных колик, сонливости или нарушения засыпания.
Нейрокс, инструкция по применению (Способ и дозировка)
Нейрокс вводится внутримышечно или внутривенно (струйно или капельно). При капельном введении препарат разводится физраствором (0,9% хлористым натрием). Дозировки Нейрокса чаще всего подбираются индивидуально врачом с учетом заболевания, состояния пациента и рекомендаций производителя.
Инструкция по применению Нейрокса рекомендует начинать лечение с суточной дозы 50-300 мг. Дозу более 50 мг лучше распределять на 2 – 3 введения. Постепенно дозу увеличивают до получения терапевтического эффекта. Максимальная суточная доза — 800 мг. Курс лечения в зависимости от состояния больного и дозировки может колебаться от 5 до 30 дней.
Внутривенно струйно лекарство вводят очень медленно в течение не менее 5 минут, капельно — со скоростью 40-60 капель в минуту.
Возможна ли передозировка Нейроксом?
При передозировке возможно появление бессонницы или, напротив, сонливости. Если препарат вводится внутривенно, возможен некоторый подъем артериального давления (АД) в течение 90 – 120 минут после введения. После этого времени симптомы АД приходит в норму самостоятельно, самочувствие восстанавливается в течение суток.
При бессоннице иногда назначаются лекарственные препараты из группы транквилизаторов (Диазепам) в минимальной дозировке.
Взаимодействие Нейрокса с другими лекарственными препаратами
Нейрокс потенцирует (усиливает) действие бензодиазепиновых транквилизаторов (Диазепам), противоэпилептических (Карбамазепин), противопаркинсонических (Леводопа) лекарственных препаратов и нитратов (Нитроглицерин).
Уменьшает токсическое действие алкоголя.
Условия продажи
В аптеке Нейрокс можно приобрести только по рецепту врача.
Условия хранения
Ампулы Нейрокс должны храниться в недоступном для детей, сухом, защищенном от света месте при температуре не выше 25 °С.
Срок годности
Препарат хранится 3 года при соблюдении вышеуказанных условий.
Аналоги Нейрокса
Совпадения по коду АТХ 4-го уровня:
Аналоги — это препараты разных лекарственных групп, которые используются для лечения одних и тех же заболеваний. Аналоги Нейрокса:
- препараты из группы ноотропов: Пирацетам, Фенибут;
- препараты из группы бензодиазепиновых транквилизаторов: Нозепам, Сибазон;
- препараты из группы противоэпилептических средств: Карбамазепин;
- препараты, улучшающие мозговое кровообращение: Винпоцетин;
- препараты из группы антиоксидантов: витамины С и Е.
Алкоголь и Нейрокс
Нейрокс снижает токсическое действие алкоголя.
Отзывы о Нейроксе
Отзывы о Нейроксе разные, приблизительно половина из них положительная, половина – отрицательная. В положительных отзывах отмечается в основном эффект от комплексного лечения различных неврологических расстройств, в состав которого входил в том числе и Нейрокс.
Отрицательные отзывы о Нейроксе связаны с отсутствием лечебного эффекта после проведенного курса лечения. Очевидно, во многом эффективность этого препарата связана с правильностью его назначения и подобранной дозировкой.
Цена Нейрокса, где купить
Цена Нейрокса в Москве зависит от дозировки препарата в одной ампуле и от количества ампул в упаковке:
- 10 ампул по 2 мл — около 300 рублей;
- 50 ампул по 2 мл – около 1200 рублей;
- 5 ампул по 5 мл – около 300 рублей.
Цена уколов Нейрокса будет зависеть от подобранной врачом дозы и длительности курса лечения.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Нейрокс таблетки п/о плен. 125мг 30штРафарма АО
-
Нейрокс раствор для в/в и в/м введ. 50мг/мл 2мл 10штФармФирма Сотекс ЗАО
-
Нейрокс раствор для в/в и в/м введ. 50мг/мл 5мл 5штФармФирма Сотекс ЗАО
-
Нейрокс таблетки п/о плен. 125мг 50штРафарма АО
-
Нейрокс раствор для в/в и в/м введ. 50мг/мл 2мл 50штФармФирма Сотекс ЗАО
показать еще
