Сулема, или дихлорид ртути осаждает белок, обладает сильным дезинфицирующим и антибактериальным действием.
Дихлорид ртути применяется для целей наружной дезинфекции как антисептическое средство в растворах (1:1000–2:1000) для дезинфекции кожи, белья, одежды, предметов ухода за больными, для обмывания стен.
Местно препараты сулемы и других солей ртути применяются для лечения заболеваний кожи в виде мазей.
Сертификат анализа сулемы 98%
Наименование: сулемы 98%
Молекулярная формула: HgCl2
Вес: 271,50
Art NO: AL2460
Batch No: AL2460 — MERC
| Sr Нет | тесты | Характеристики | Результаты |
| 1 | Описание | Белый кристаллический порошок | Белый кристаллический порошок |
| 2 | Анализ (мин.) | 98,0% | 99,73% |
| 3 | Кальций (Ca) | <0,005% | 0,0006% |
| 4 | Магний (Mg) | <0,005% | 0,0006% |
| 5 | Калий (K) | <0,005% | <0,005% |
| 6 | Натрий (Na) | <0,005% | <0,005% |
Результаты: Вышеуказанный продукт соответствует LR класса
Сертификат анализа сулемы AR 99,5%Наименование: сулемы AR 99,5%
Молекулярная формула: HgCl2 Вес: 271,50 Art NO: AL2463 Batch No: AL2463 — MERC Производство Дата: Август 2011 Дата окончания действия: август 2016
| Sr Нет | тесты | Характеристики | Результаты |
| 1 | Описание | Белый кристаллический порошок | Белый кристаллический порошок |
| 2 | Анализ (мин.) | 99,5% | 99,73% |
| 3 | Эфир нерастворимые вещества | <0,01% | 0,008% |
| 4 | Вода нерастворимого вещества | <0,01% | 0,006% |
| 5 | Нелетучих веществ | <0,02% | 0,01% |
| 6 | Остаток после восстановления с помощью муравьиной кислоты, | <0,02% | 0,01% |
| 7 | Нитраты (NO 3) | <0,001% | 0,0008% |
| 8 | Кальций (Ca) | <0,001% | 0,0006% |
| 9 | Медь (Cu) | <0,0005% | <0,0005% |
| 10 | Железо (Fe) | <0,001% | 0,0006% |
| 11 | Свинец (Pb) | <0,0005% | <0,0005% |
| 12 | Магний (Mg) | <0,001% | 0,0006% |
| 13 | Калий (K) | <0,005% | <0,005% |
| 14 | Натрий (Na) | <0,005% | <0,005% |
Результаты: Вышеуказанный продукт соответствует требованиям класса AR
1. Продукт идентификации
Синонимы: Mercury двухлорный; сулема; хлорид ртути (II); ртути перхлорида
CAS No: 7487-94-7
Молекулярный вес: 271,52
Химическая формула:HgCl2
Коды продукта: AL24632.
Состав / информация о компонентахКомпонент № КАС Процент опасных ———— ———— ———— —— ——- сулемы 7487-94-7 98 — 100% Да
Чтобы сформулировать диапазон в соответствии со стандартами для лабораторий, наша Mercury Chloride. апробированных нашими квалифицированными тестерами качества по различным стандартам качества , таких как чистота и качество. ,
хлорид ртути (II) , или хлорид ртути (архаически, сулема) является химическое соединение ртути и хлора с формулой HgCl2. Это белое кристаллическое вещество представляет собой лабораторный реагент и молекулярное соединение. Как только используется в качестве средства для лечения сифилиса, он больше не используется в лечебных целях из — за токсичности ртути и наличие превосходных процедур.
Наиболее важными солями ртути являются хлорид ртути, оксид ртути, нитрат ртути, сульфат ртути.
В Альфа CHEMIKA мы производим и продавать сулемы онлайн.
хлорид ртути является химическое соединение с формулой Hg2Cl2. Также известный как каломели (минеральной форме, редко встречается в природе) или хлорид ртути, этого плотного белого или желтовато-белого цвета, без запаха твердое вещество является главным примером соединения ртути. Сулемы для продажи в Альфа CHEMIKA, которая является ведущим производителем хлорида ртути в Индии.
Особые указания
Сулема — сильный яд.
Применяя растворы дихлорида ртути следует соблюдать осторожность, так как даже при местном применении препаратов сулемы возможно отравление вследствие их всасывания.
Для дезинфекции металлических инструментов растворы сулемы не применяются, так как они вызывают коррозию металлов.
Отравление сулемой
Картину отравления сулемой делят на три стадии:
- В первой преобладают симптомы поражения пищевого канала — жгучая боль по ходу пищевода и желудка, тошнота, рвота, металлический вкус во рту, слизистая оболочка рта набухает, серого цвета, часто покрывается налетом.
- Вторая стадия характеризуется ослаблением деятельности сердца.
- В третьей стадии поражаются органы, выделяющие ртуть, особенно почки, толстые кишки и слюнные железы, развивается ртутный стоматит, ртутный колит, «сулемовая» почка.
Смертельная доза сулемы 0,2–0,3 г.
На вскрытии местные явления выражены разнообразно — от покраснения и набухания слизистой оболочки до некроза в виде плотного серого струпа. Особенно выражены изменения в почках и толстых кишках. Почки увеличены, корковое вещество утолщено, желтовато-серого цвета с полосчатыми кровоизлияниями, пирамиды темно-красные. В извитых канальцах отложения солей кальция. В толстом кишечнике — сулемовая дизентерия: от серозного воспаления до дифтеритического некротического поражения с изъязвлениями. Зернистая дистрофия печени, миокарда и желез не имеющих протоков. Диагностика отравления сулемой сложная.
Состав и форма выпуска
Рецепт на сулему
| Rp.: | Hydrargyri dichloridi | 0,5 |
| D. t. d. N 10 in tabul. | ||
| S. |
Дихлорид ртути — таблетки розоватого или красновато-розового цвета по 0,5 и 1 г для приготовления растворов для наружного применения, состоящих из равных частей сулемы и натрия хлорида с прибавлением эозина для придания растворам предупреждающей окраски.
Срок годности и условия хранения
Хранить в хорошо закупоренных стеклянных банках. Срок годности сулемы не ограничен.
Свойства
Сулема (Hydrargyri dichloridum, Hydrargyrum dichloratum, Hydrargyrum bichloratum corrosivum s. Sublimate) —HgCl2 — тяжёлый белый кристаллический порошок или белые кристаллы, растворимые 16 частях воды (лучше растворим в кипящей) и в этиловом спирте.
Сулема HgCl2 — получается сухим путем и мокрым; последний — проще. В первом случае подвергают перегонке смесь сернокислой ртути и поваренной соли. С. образуется по ур.:
HgSO4 + 2NaCl = HgCl2 + Na2SO4.
Для предупреждения образования каломели HgCl (так как HgSO 4 обыкновенно содержит соль закиси ртути) к смеси NaCl и HgSO 4 прибавляют немного перекиси марганца или перегонку ведут в атмосфере хлористого водорода.Перегонка ведется в железных или стеклянных ретортах, и задача заключается в том, чтобы постепенно поднять температуру и поддерживать ее на известной точке. Сернокислую соль ртути готовят, нагревая почти до кипения 2 частицы серной кислоты с 1 част. ртути:
H2SO4 +Hg = HgSO4 + SO2 + 2Н 2O
пока проба соляной кислотой не покажет отсутствия соли закиси ртути. Иногда для получения С. ртуть растворяют в царской водке, раствор выпаривают и полученную массу перегоняют, смешав ее с песком. Для получения С. мокрым путем к нагретому раствору HgSO 4 прибавляют поваренной соли или соляной кислоты и выделившуюся при осаждении С. перекристаллизовывают. Иногда берут окись ртути и, растворяя ее в соляной кислоте, получают С. О свойствах С. и о применении в медицине см. Ртуть.
Для получения кристаллической С. в лаборатории сперва растворяют ртуть в небольшом избытке разбавленной азотной кислоты (тяга!). Затем осаждают оксид едким натром; осадок на фильтре несколько раз промывают водой и сушат. К взвешенному HgO добавляют эквимолярное количество концентрированной соляной кислоты. Профильтрованный раствор выпаривают (тяга!); кристаллы растирают, взвешивают и пакуют. Выход близок к теоретическому.
Сулема немного летуча, работать с ней желательно в вытяжном шкафу. Работать с растворимыми солями ртути (в т.ч. С. и особенно азотнокислой ртутью) следует в перчатках и маске; при попадании растворов на кожу, слизистые или в глаза надо возможно скорее промыть пораженное место большим количеством воды.
Дихлорид ртути или сулема – главная составляющая часть лекарства при терапевтическом лечении рака головного мозга: в крайних случаях необходимо прибегать к крайним средствам.
Дихлорид ртути от позднелабинского sublimatum – сулема HgCl2 (буквально – высоко поднятое, вознесенное, то есть добытое возгонкой) – бесцветные кристаллы ромбической формы. Плотность сулемы 5,44 г/см3, температура плавления 277 0 С, температура кипения 304°С. Растворима в холодной воде (1:18,5), легко растворима в кипящей воде (1:3) и спирте (1:4), растворима в эфире, ацетоне, легко возгоняется. Водные растворы имеют кислую реакцию.
Сулема – сильный яд. Смертельная доза сулемы – 0,5 г.
Получают растворением ртути в концентрированной серной кислоте с последующим нагреванием сухого сульфата ртути с хлоридом натрия или прямым хлорированием ртути при нагревании.
Применяют для получения других солей ртути, как дезинфицирующие средства в медицине, в фармацевтической промышленности, для протравливания семян, пропитки дерева и др. Сулему используют в качестве катализатора в органическом синтезе.
Регистрация препарата ртути дихлорид (сулема) для медицинских целей в России аннулирована в 1999 году.
В настоящее время соли ртути используются только в гомеопатии в разведении 10 в минус 6 степени.
Ранее применялись водные растворы сулемы 0,1-0,2% концентрации (1:1000 – 2:1000) для дезинфекции белья, одежды, предметов ухода за больными, для дезинфекции помещений и др.
Сулема выпускается в порошке и таблетках (по 0,5 и 1 г.), состоящих из равных частей дихлорида ртути и хлорида натрия. Таблетки окрашиваются 1% раствором эозина в розовый или красно-розовый цвет и дают опалесцирующий раствор такого же цвета. Таблетки предназначаются только для наружного применения (для приготовления растворов).
Сулема – лучшее средство при таких тяжелых опухолях, как рак головного мозга, рак предстательной железы, рак мочевого пузыря, рак гортани и полости рта, саркома кости, наружные новообразования, а также рак желудка, рак пищевода и рак кишечника.
При лечении опухолей и метастатических поражениях головного мозга Кемеровским консультационным центром «Алькахест» сулема рекомендуется в простых и сложных рецептах.
В первом случае достаточно растворить 0,5 г. сулемы в 1000 мл. дистиллированной воды и принимать разведение по одной столовой ложке, три раза в день за час до еды в 50 мл. воды. Этот рецепт рекомендуется при опухолях головного мозга. Выходить на максимальную дозу надо постепенно, начиная с чайной ложки на 50 мл. воды и далее по самочувствию.
При метастических поражениях и опухолях головного мозга, сулема принимается одновременно с антимитотическими ядами таких ядовитых растений, как вёх ядовитый, болиголов крапчатый и борец белоустый. Используются не настойки, а вытяжки из этих растений. Применяя метод перколяции, строго соблюдая сроки сбора растений, вытяжки оптимальной концентрации готовятся из только что заготовленного сырья.
Механизм противоопухолевого действия цикутоксина, кониина и аконитина, объясняется их способностью блокировать митоз клеток на стадии метафазы, в самом начале кариокинеза (деления ядра клетки).
Схема лечения вытяжками трав.
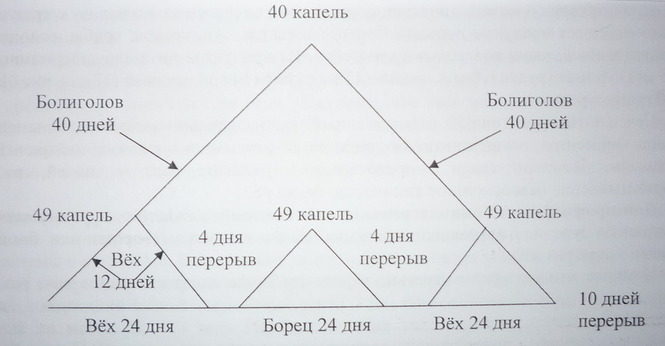
Применение вытяжек из этих трав при метастатических поражениях головного мозга целесообразно независимо от локализации и вида опухоли.
Рекомендации по приему лекарственных трав следующие:
1. Вытяжка болиголова – в ОБЕД за 30 мин до еды в 50 мл. воды по капельной схеме «горкой» с 1 до 40 капель и обратно (до 15 капель можно принимать без воды).
2. Вытяжка вёха ядовитого – УТРОМ и ВЕЧЕРОМ за 30 мин до еды в 50 мл. воды по следующей схеме:
Схема приема вытяжки вёха ядовитого
| Дни приема | Количество капель | Дни приема | Количество капель |
| Утром Вечером | Утром Вечером | ||
|
1 2 3 4 5 6 7 8 9 10 11 12 |
2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |
13 14 15 16 17 18 19 20 21 22 23 24 |
24 23 22 21 20 19 18 17 16 15 14 13 12 11 10 9 8 7 6 5 4 3 2 1 |
Вытяжка борца белоустого – УТРОМ и ВЕЧЕРОМ за 30 мин. до еды в 50 мл воды. Схема приема аналогична вышеприведенной по вёху.
Курс лечения вытяжками ядовитых трав рассчитан на 3 месяца. При переносимости лекарств курсы повторяются.
В период лечения вытяжками трав исключить из рациона больного:
1. Кофе. 2. Молоко. 3. Крепкий черный чай.
Ограничить поступление глюкозы, кальция и соли до 5 — 6 г.
Селен – один из самых важных элементов, участвующих в защите организма от раковых клеток.
По данным Всемирной Организации Здравоохранения для поддержания здоровья нам нужно совсем немного селена: мужчине – 70мкг в сутки, женщине – 55 мкг, ребенку 1 мкг на 1 кг веса ребенка. Селен препятствует развитию некоторых хронических заболеваний, злокачественных и доброкачественных опухолей, болезней сердца и даже алкоголизма, регулирует работу щитовидной железы и укрепляет иммунную систему.
При опухолях и метастатических поражениях головного мозга наряду с травами – адаптогенами, рекомендуются продукты и травы, богатые селеном: лук, чеснок, грибы, солодка, душица, донник лекарственный, хвощ полевой и др.растения. Из продуктов питания, содержащих селен – говядина (35 мг),куриная грудка (20 мг), лапша (17 мг), яйцо (14 мг), овсянка (12 мг), рис (10 мг),хлеб (5мг) на 100 грамм продукта.
Селен активирует ген р53, ответственный за окислительно-восстановительные реакции, входит в состав ферментов, осуществляющих реакции детоксикации в клетках, нейтрализующих свободные радикалы. Наконец, селен предотвращает развитие рака у людей, в клетках которых вырабатывается недостаточное количество белка р53.
Для профилактики онкологических заболеваний, каждому здоровому человеку необходимо проходить курс противоракового лечения вёхом ядовитым, борцем или болиголовом не реже одного — двух раз в год.
Сулема (от позднелат. sublimatum — сулема, буквально — высоко поднятое, вознесённое, то есть добытоевозгонкой), хлорид ртути (II), HgCl2, бесцветные кристаллы ромбической системы; плотность 5,44 г/см3, tпл.277 °С; tkип 304 °С; легко сублимируется. Растворима в спирте, эфире, уксусной кислоте; в 100 г водырастворяется 7,4 г сулемы при 20 °С и 55 г при 100 °С. Образует комплексные соединения. Получаютрастворением ртути в концентрированной серной кислоте с последующим нагреванием сухого сульфатартути с хлоридом натрия или прямым хлорированием ртути при нагревании. Сулема служит для получения других соединений ртути, например каломели. Сулему используют в качестве катализатора в органическом синтезе.
Растворы сулемы применяют в медицине для обеззараживания кожных покровов, одежды и т. п. Сулемасильно ядовита.
Свойства
Хлорид ртути — бесцветное, кристаллическое, плохорастворимое[1] в воде и очень ядовитое соединение. Плотность 5,44 г/см³, tпл. 277°С; tkип 304°С. Растворимость в воде 7,4 г на 100 г при 20 °С и 55г при 100 °С. Растворим также в спирте, эфире, ацетоне; легко возгоняется.
Получение
Получают растворением ртути в концентрированной серной кислоте с последующим нагреванием сухого сульфата ртути с хлоридом натрия или прямым хлорированием ртути при нагревании.
Применение
Применяют для получения других солей ртути, как дезинфицирующее средство в медицине (чаще в разведении 1:1000), для протравливания семян, в фармацевтической промышленности, для пропитки дерева и др. Сулему используют в качестве катализатора в органическом синтезе.
Для ртути (II) известны оксид HgO, галогениды HgГ2 (где Г – галоген) и соли.
Оксид ртути (II) HgO существует в двух формах – красной и желтой, обе формы имеют одинаковую структуру, кристаллизуются в ромбической сингонии, цвет зависит от размера кристаллов: при размерах до 4 мкм цвет оксида желтый, выше 8 мкм – красный. Красная форма образуется при осторожном нагревании нитрата ртути (II) при 350 °С:
2Hg(NO3)2 = 2HgO + 4NO2 + O2.
Желтая – при добавлении щелочей к раствору соли Hg (II) :
Hg(NO3)2 + 2NaOH = HgO + 2NaNO3 + H2O.
Оксид ртути (II) обладает только основными свойствами, растворяется в кислотах:
HgO + 2HNO3 = Hg(NO3)2 + H2O.
Гидроксид ртути (II) Hg(OH)2 не выделен, он разлагается в момент образования на оксид и воду.
Хлорид ртути (II) HgCl2 – сулема – образуется при нагревании смеси сульфата ртути (II) с хлоридом натрия:
HgSO4 + 2NaCl = HgCl2 + Na2SO4.
Сулема – бесцветное кристаллическое вещество, плотность 5,44 г/см3, температура плавления 277°С, плохорастворима в воде.
Одно из широко используемых соединений ртути (II) – фульмиат ртути (II) Hg(CNO)2, соль гремучей кислоты, его называют гремучей ртутью. Это первое взрывчатое вещество, при ударе мгновенно разлагается:
Hg(CNO)2 = Hg + N2 + 2CO.
Общие Физические свойства Термические свойства Химические свойства Классификация Безопасность
| Хлорид ртути(II) | ||||||||||||||||||||||||||||||||||||||||
| Систематическое наименование |
Хлорид ртути(II) | |||||||||||||||||||||||||||||||||||||||
| Традиционные названия | Сулема | |||||||||||||||||||||||||||||||||||||||
| Хим. формула | HgCl2 | |||||||||||||||||||||||||||||||||||||||
| Состояние | твёрдое | |||||||||||||||||||||||||||||||||||||||
| Молярная масса | 271,52 г/моль | |||||||||||||||||||||||||||||||||||||||
| Плотность | 5,43 г/см³ | |||||||||||||||||||||||||||||||||||||||
| Т. плав. | 276 °C | |||||||||||||||||||||||||||||||||||||||
| Т. кип. | 304 °C °C | |||||||||||||||||||||||||||||||||||||||
| Растворимостьв воде | 7,4 г/100 мл | |||||||||||||||||||||||||||||||||||||||
| Рег. номер CAS | 7487-94-7 | |||||||||||||||||||||||||||||||||||||||
| PubChem | 24085 | |||||||||||||||||||||||||||||||||||||||
| 231-299-8 | ||||||||||||||||||||||||||||||||||||||||
| SMILES | Cl[Hg]Cl, [Cl-].[Cl-].[Hg+2] | |||||||||||||||||||||||||||||||||||||||
| RTECS | OV9100000 | |||||||||||||||||||||||||||||||||||||||
| Номер ООН | 1624 | |||||||||||||||||||||||||||||||||||||||
| ChemSpider | 22517 | |||||||||||||||||||||||||||||||||||||||
| NFPA 704 | 0 4 0 | |||||||||||||||||||||||||||||||||||||||
|
Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. ОПАСНОСТЬ! МОЖЕТ БЫТЬ Смертельно при проглатывании. ВРЕДНО ПРИ ВДЫХАНИИ ИЛИ Проникает через кожу.Вызывает сильное раздражение глаз, кожи и дыхательных путей; Может привести к ожогам. Может вызывать аллергическую КОЖИ РЕАКЦИЯ. Ртутных соединений ВЛИЯЕТ почкам и центральной нервной системы. Врожденный дефект ОПАСНОСТИ. МОЖЕТ ПРИВЕСТИ К врожденным дефектам.SAF-T-DATA (TM) Рейтинги (При условии, здесь для вашего удобства)
Оценка: 4 — Экстремальные (Яд) Возможные последствия для здоровья———————————- Вдыхание: Вызывает раздражение дыхательных путей. Симптомы включают боль в горле, кашель, боль, стеснение в груди, затрудненное дыхание, одышка и головные боли. Пневмониту может развиваться. Может быть поглощено при вдыхании с симптомами , чтобы параллельно проглатывания. Vapor ингаляции может сжечь слизистую оболочку носа и горла. Проглатывание: высокотоксичных! Средняя смертельная доза для неорганических солей ртути составляет около 1 грамма. Может вызвать жжение во рту и глотке, боли в животе, рвота, коррозионных язв, кровавый понос.Может сопровождаться быстрым и слабый пульс, поверхностное дыхание, бледность, истощение, центральной нервной системы , проблемы, тремор и коллапсу. Задержка может наступить смерть от почечной недостаточности. При контакте с кожей: Вызывает irritaton и ожоги кожи. Симптомы включают покраснение и боль. Может вызвать аллергию кожи и сенсибилизацию. Может проникать через кожу с симптомами , чтобы параллельно проглатывания. Припопадании в глаза: Вызывает раздражение и ожоги глаз. Симптомы включают покраснение, боль, затуманенное зрение; может привести к серьезным и необратимые повреждения глаз. Хроническое воздействие: Хроническое воздействие через любой маршрут может производить повреждения центральной нервной системы. Может вызвать мышечный тремор, личность и поведение изменений, потеря памяти, металлический привкус во рту, разрыхление зубов, нарушения пищеварения, кожные высыпания, повреждения головного мозга и почек. Может вызвать аллергию кожи и накапливается в организме. Повторный контакт с кожей может привести к коже , чтобы включить в серый цвет. Teratogen: может повредить развитию плода и снижение фертильности у самцов и самок. Обострение ранее существовавших условий: Лица с нервными расстройствами или нарушением функции почек или дыхательной функции, или история аллергии или известной сенсибилизация к ртути могут быть более восприимчивы к воздействие вещества.4.Меры первой помощи Привдыхании: Вынести на свежий воздух. Если нет дыхания проведите искусственную вентиляцию легких. Если дыхание затруднено, дайте кислород.Обратиться к врачу немедленно. При попадании внутрь: Побудить сразу рвота по указанию медицинского персонала. Никогда не давайте ничего в рот человеку , потерявшему сознание. Обратиться к врачу немедленно. Контакт с кожей: Немедленно промыть кожу большим количеством воды в течение не менее 15 минут, сняв загрязненную одежду и обувь. Обратиться к врачу немедленно. Стирайте одежду перед повторным использованием. Тщательно очистите обувь перед повторным использованием. При попадании в глаза: Немедленно промойте глаза большим количеством воды в течение не менее 15 минут, поднимая нижний и верхние веки иногда. Обратиться к врачу немедленно.5.Меры пожарной безопасностиОгонь: . Не считается пожароопасным Взрыв: . Взрывчатые создаются условия за счет трения, тепла или удара фосфора, сурьмы, мышьяка, солей серебра, сульфиды, ацетилен, аммиак и щавелевая кислота Пожаротушению: Вода , сухие химикалии, пену или диоксид углерода. Не использовать поток воды, так как поток будет растечься и огонь. Не допускайте попадания воды стоки попадания в канализацию или водные артерии. Специальная информация: В случае пожара, носить полную защитную одежду и NIOSH-одобренный автономный дыхательный аппарат с полной маской , работающий в требовании давления или другом режиме положительного давления.6.МерыпопредотвращениюиликвидациичрезвычайныхПроветрить зону утечки или разлива. Методы очистки персонала требуют защитную одежду и средства защиты органов дыхания от пыли. Разливы: Встреча и место в подходящий контейнер для утилизации или захоронения в способе , который не приводит к образованию пыли. Посыпать область с серой или полисульфида кальция , чтобы подавить ртуть. Положение США (СЕРКЛА) требуют отчетов проливов и выбросов в почву, воду и воздух в избытке регистрируемых величин. Бесплатный номер для Национального центра береговой охраны США по реагированию (800) 424-8802.7.Обработка и хранениеХранить в плотно закрытой таре, хранить в прохладном, сухом, проветриваемом помещении. Защита от физических повреждений и прямых солнечных лучей. Изолировать от несовместимых веществ. Соблюдать строгие гигиенические практики. Контейнеры этого материала могут быть опасными , когда пусто , так как они сохраняют остатки продукта (пыль, твердые частицы); соблюдать все предупреждения и меры предосторожности , перечисленные для продукта.8.Контроль воздействия / Средстваиндивидуальной защитыБортовые Пределы воздействия: — OSHA Приемлемый потолка Концентрация: ртуть и ее соединения: 0,1 мг / м3 (TWA), кожа — ACGIH Пороговое предельное значение (ТДЗ): неорганические и металлическая ртуть, а Hg: 0,025 мг / м3 (TWA) кожи, A4 не классифицируемый как канцероген длячеловека. — ACGIH показателям биологического воздействия: общая неорганической ртути в моче (предсменные): 35 мкг / г креатинина, общего неорганического ртути в крови ( в конце смены): 15 мкг / л. система вентиляции: система местного и / или основной вентиляции рекомендуется держать экспозиции сотрудника ниже предельных значений воздействия ВДВ. Местная вытяжная вентиляция , как правило , предпочтительнее , поскольку он может контролировать выбросы загрязняющего вещества на его источнике, предотвращения его распространения в рабочей зоне. Пожалуйста , обратитесь к АКГЭПГ документу, Промышленная вентиляция, Руководство по рекомендуемой практикой, последнее издание, для деталей. Личные Респираторы (NIOSH Утвержденный): Если предел воздействия превышен и технические средства контроля не представляется возможным, респиратора частиц в условиях полного лицевой маски (NIOSH тип N100 фильтры) можно носить до 50 раз предельно допустимую или максимальной концентрации использования , установленного соответствующим регулирующим органом или респиратора поставщика, в зависимости от того самый низкий. Если частицы масла (например , смазки, смазочно — охлаждающие жидкости. Глицерин и т.д.) присутствуют, используйте тип R NIOSH или P фильтр. В экстренных случаях или когда уровень воздействия не известен, используйте полный лицевой маски положительного давления, дыхательным аппаратом. ВНИМАНИЕ:. Воздушные респираторы не защищают рабочих в атмосфере с недостатком кислорода Защита кожи: Носить непроницаемую защитную одежду, включая ботинки, перчатки, плащи, фартуки, в случае необходимости, для предотвращения контакта с кожей. Защита глаз: Использование химической безопасности очки и / или маску на лицо , где напыление или разбрызгивание растворов возможно. Поддержание промывки глаз и быстро мочить в рабочей зоне.9.Физические и химические свойстваВнешний вид: Белые кристаллы или порошок. Запах: . Без запаха Растворимость: 7,4 г в 100 г воды. Удельный вес: 5,4 рН: 3,2 (0,2 М раствор) % Летучие по объему @ 21C (70F): 0 Точка кипения: . 302С (576F) сублимируется Точка плавления: . 276C (529F) сублимируется Плотность паров (воздух = 1): 8.7Давление паров (мм рт.ст.): 1 @ 136.2C (277F) Скорость испарения (BuAc = 1): Нет информации.10.Стабильность и химическая активностьСтабильность: Продукт стабилен при нормальных условиях использования и хранения. Медленно разлагается с образованием металлической ртути в присутствии органического вещества и солнечного света, и становится летучим при 300C (572F). Опасные продукты разложения: Оксиды содержащегося металла и галогена, возможно , также свободно, или ионной галогена. Опасная полимеризация: Не происходит. Несовместимость: Реагирует бурно с калия и натрия. Несовместимые со многими соединениями: формиаты, сульфиты, фосфаты, альбумин, аммиак, желатин, карбонаты, гипофосфиты, сульфиды, щелочам, алкалоид соли, известковой воды, сурьмы и мышьяка, бромиды, буру, восстановленное железо, медь, железо, свинец, дубильной кислоты . и растительные вяжущие условия , которых следует избегать: Высокая температура, удара, трения, несоединимое.11.Токсикологическая информацияТоксикологические данные: Oral крысы LD50: 1 мг / кг. Раздражение, Стандартный Дрейза, кролик: Кожа, 500 мг / 24H, тяжелая; Глаз, 50 мкг / 24H, тяжелая. Исследовал как tumorigen, мутагены, репродуктивный эффекторной. Репродуктивной токсичности: Все формы ртути могут проникать через плаценту к плоду, но большинство из того , что известно было изучено из экспериментальных животных. См. Хроническая Опасность для здоровьяканцерогенность: EPA / IRIS Классификация: Группа C — Возможный канцероген для человека.
12. Экологическая информацияЭкологическая Судьба: Химическая инвентаризации Статус — Часть 1
Химическая инвентаризации Статус — Часть 2
Федеральные, государственные и международные правила — Часть 1
Федеральные, государственные и международные правила — Часть 2 |
- Главная
- Съезд хирургов 2019
- Рубрики для тезисов 2019
- Возможности лечения перитонита и нефропатии, вызванной введением сулемы в эксперименте
>
>
>
Известное соединение сулема (хлорид ртути, HgCl2) используется в экспериментальной хирургии для моделирования нефротоксических эффектов. При введении в брюшную полость помимо этого развивается токсический перитонит, степень тяжести которого зависит от введенной дозы токсиканта.
В опытах на 96 крысах (по 8 животных в группе) изучали возможности коррекции метаболических нарушений посредством различных комбинаций лекарственных средств, которые вводили внутрибрюшинно. Использовали антиоксидантный препарат «Рексод» (рекомбинантная супероксиддисмутаза человека) в дозах 10тыс.Ед./кг. Рецепторный антагонист интерлейкина — 1β) и «БТШ» применяли в 20 мг/кг (рекомбинантный) внутрибрюшинно в двух вариантах: за 30 минут до введения токсиканта (профилактическое введение) и спустя 1 час (лечебное) применение.
Спустя 48 часов животных выводили из опыта (эвтаназия). Проводили расчет массовых коэффициентов органов (легкие, почки, надпочечники, селезенку, печень), отбирали сыворотку крови для проведения биохимического анализа (общий белок, глюкоза, мочевина, протромбин, билирубин).
Установили, что применение супероксиддисмутазы в виде монотерапии и в сочетании с БТШ и, особенно, с рецепторным антогнистом интерлейкина -1 в значительной степени снизило выраженность токсического эффекта. В на статистически значимом уровне (p<0,009-0,016) меньшей степени были выражены биохимические отклонения. Морфологических изменений в почках были менее выражены. Отмечена тенденция к уменьшению объема воспалительного выпота в брюшной полости.
JOURNAL OF NEW MEDICAL TECHNOLOGIES — 2016 — V. 23, № 2 — P. 90-95
УДК: 616.61-099-546.49 — 616-008.9 — 577.17.049.001.6 DOI: 10.12737/20431
ВЛИЯНИЕ СУЛЕМЫ НА ФУНКЦИИ ПОЧЕК НА ФОНЕ ГИПОКАЛЬЦИЕМИИ ВЫЗВАННОЙ ДВУСТОРОННЕЙ ПАРАТИРЕОИДЭКТОМИЕЙ
В .Б. БРИН*, Р.И. КОКАЕВ**
*ГБОУ ВПО СОГМА Минздрава РФ, Владикавказ, ул. Пушкинская, 40, г. Владикавказ, РСО-Алания, 362025 **ФГБУН Институт биомедицинских исследований ВНЦ РАН и Правительства РСО-Алания, ул. Пушкинская, 47, г. Владикавказ, РСО-Алания, 362025, e-mail: [email protected]
Аннотация. Влияние тяжелых металлов на обмен веществ и гомеосгаз электролитов, делают необходимым изучение их взаимовлияния на уровне главного аппарата поддержания этого постоянства — почки. В работе исследованы некоторые особенности изменения водо-электролитовыделительной функции почек под влиянием хлорида ртути (сулемы) в условиях гипокальциемии, вызванной гипо-паратиреозом. Работа проведена на 60 крысах-самцах линии Вистар, разделённых на три группы, одну опытную и две контрольные: одна с изолированным введением хлорида ртути, вторая с моделью гипокальциемии, вызванной двусторонней паратиреоидэктомией. Опытную группу составили крысы с сочетанной моделью гипопаратиреоза с ртутной интоксикацией. У всех групп животных было отмечено увеличение диуреза, в основном за счет снижения канальцевой реабсорбции, что в большей степени проявилось у животных с введением хлорида ртути, как изолированным, так и сочетанным. Также паратиреоидэктомия, как и ртутная интоксикация, приводят к увеличению экскреции кальция с мочой вследствие нарушения его канальцевой реабсорбции, что выражено больше в сочетанной модели гипопаратиреоза с введением хлорида ртути. Схожие изменения отмечены в почечной обработке натрия. Повреждающее влияние гипокальциемии и избытка ртути, проявляющееся в протеи-нурии, также более выражено в сочетанной модели эксперимента. Потенцирование токсических эффектов хлорида ртути гипокальциемией подтверждает возможную роль кальция в механизмах токсичности тяжелого металла.
Ключевые слова: тяжелые металлы, хлорид ртути, почки, гипокальциемия, паратиреоидэктомия.
MERCURIC CHLORIDE EFFECTS ON RENAL EXCRETORY FUNCTIONS UNDER THE HYPOCALCEMIA CAUSED BY PARATHYROIDECTOMY
V.B. BRIN*, R.I. KOKAEV**
*North Ossetia State Medical Academy, Pushkinskaya st., 40, Vladikavkaz, North Ossetia-Alania, 362025 **Biomedical Research of Vladikavkaz Scientific Center of the Russian Academy of Sciences and the Government of the Republic of North Ossetia-Alania, Pushkinskaya st. 47, Vladikavkaz, North Ossetia-Alania, 362025,
e-mail: [email protected]
Abstract. The influence of heavy metals on metabolism and homeostasis of electrolytes causes the necessity to study their interaction on the level of the main unit which is maintaining this constancy — the kidneys. This research is devoted to the features of water-electrolyte changes of renal excretory function under the mercury chloride effects in a hypocalcemia caused by hypoparathyroidism. The study was conducted on 60 male rats Wistar, divided into three groups. The first group was experimental and the other two groups were control; one group — with the introduction of isolated mercury chloride, the second — with the model hypocalcemia caused by bilateral parathyroidectomy. Test group of rats was with a combined model hypo-parathyroidism with mercury intoxication. All groups of animals showed an increase in urine output, mainly due to the decrease in tubular reabsorption, which is more evident in animals with mercuric chloride administration, both alone and together. The parathyroidectomy and mercury intoxication lead to increased calcium excretion in the urine due to the violation of its tubular reabsorption, it is expressed more in hypo-parathyroidism model with mercuric chloride administration. Similar changes are observed in the renal sodium handling. The damaging impact of hypocalcemia and overage of mercury manifested in proteinuria, is more pronounced in the combined experimental model. The potentiation of the toxic effects of mercury chloride hypocalcemia suggests a possible role of calcium in the mechanisms of heavy metal toxicity.
Key words: heavy metals, mercury chloride, kidney, hypocalcemia, parathyroidectomy.
В современной литературе есть множество данных о последствиях тотальной тиреоидэк-томии, в результате которой у больных развивается дефицит гормона паращитовидных желёз [13,18,22] и, как следствие, стойкая гипо-кальциемия [6,14,17]. Описаны случаи вторичного гипопаратиреоза у беременных, сопровождающегося гипокальциемией [8,10], как и случаи идиопатического гипопаратиреоза [11]. Изменение метаболизма кальция может происходить в течение жизни человека в связи с рядом перестроек, при беременности и лактации, также с возрастом, когда баланс Са становится отрицательным. Нарушение в системе регуляторных механизмов поддержания гомео-стаза электролитов, на сегодняшний день, может усугубляться влиянием агрессивных факторов внешней среды, таких как тяжелые металлы и независимо от причины изменения кальциевого гомеостза наблюдается тесная взаимосвязь между этими нарушениями и патогенезом токсического влияния тяжелых металлов. В серии наших предыдущих исследований было показано влияние тяжелых металлов на ряд показателей водо-электролитовыделительной функции почек на фоне изменения кальциевого го-меостаза в моделях с гипер- и гипокальциемией [3,4]. Неоднократно была отмечена значимость сочетанного влияния измененного гомео-стаза кальция и ряда тяжелых металлов (свинца, кобальта, никеля и др.) [1,2,5]. Одним из высокотоксичных, с большим спектром вариантов повреждающего действия, тяжелых металлов относится ртуть. Обсуждаемым вопросом является роль ртути в кальций-опосредованном нарушении работы клеточных систем. Известно, что увеличение цитозольного кальция может модулировать дестабилизацию лизосомальных мембран через активацию Ся2+-зависимой фос-фолипазы А2 [9], а в работе В. ЫатсЫ (2004) показано, что микромолярные концентрации ртути приводят к дестабилизации лизосомаль-ных мембран, за счет значительного роста внутриклеточной концентрации катиона, чего не происходит в среде, освобожденной от кальция, а также после предварительного воздействия на клетки блокаторами кальциевых каналов [16]. Отсюда можно предположить вероятность проявлений взаимного влияния избытков тяжелого металла и нарушенной регуляции кальциевого гомеостаза на различных уровнях и системах организма, в том числе и в одной из
основных систем поддержания электролитного гомеостазиса — системе выделения.
Цель исследования — изучение особенности изменения водо-электролитовыделительной функции почек под влиянием хлорида ртути (сулемы) в условиях гипокальциемии, вызванной гипопаратиреозом.
Материалы и методы исследования. Работа проведена на 60 крысах-самцах линии Вистар, массой 200-300 грамм. В проведении экспериментов руководствовались статьёй 11-й Хельсинской декларации Всемирной медицинской ассоциации (1964), «Международными рекомендациями по проведению медико-биологических исследований с использованием животных» (1985) и Правилами лабораторной практики в Российской Федерации (приказ МЗ РФ от 19.06.2003 № 267).
В эксперименте животные были разделены на 4 группы:
1-я группа — интактные животные (Фон);
2-я группа — контрольные животные с двусторонней паратиреоидэктомией (гипопарати-реозом — ГПТ);
3-я группа — контрольные животные с внут-рижелудочным введением хлорида ртути в дозировке 0,1 мг/кг (в пересчёте на металл) в течение 30 дней ежедневно 1 раз в сутки (И^);
4-я группа — животные с введением хлорида ртути на фоне гипопаратиреоза в те же сроки н + ГПТ).
Модель экспериментального гипопаратире-оза создавали оперативным путем, у предварительно наркотизированных крыс, удаляя у них паращитовидные железы выжиганием электротермокаутером. Исследуемые показатели у всех групп животных определяли через 1 месяц.
Для сбора мочи животные помещались в обменные клетки на 6 часов. После этого в условиях спонтанного диуреза определялись объём диуреза, скорость клубочковой фильтрации по клиренсу эндогенного креатинина, каналь-цевая реабсорбция воды. Концентрацию белка (по методу Лоури), креатинина и кальция в биологических жидкостях (моче и плазме крови) определяли с помощью спектрофотометра (Аре1 Р0-303), концентрацию натрия и калия -методом пламенной фотометрии (ФПА-2). Ос-молярность мочи определялась криоскопиче-ским методом (0втота^030) Статистическая обработка результатов исследования, учитывая нормальное распределение рядов сравнения, проводилась с применением критерия «Ы
10ШМАЬ ОБ ШШ МБЭТСАЬ ТБСНМОШСТББ — 2016 — V. 23, № 2 — Р. 90-95
Стьюдента с использованием программы СтарНРай Рт1хш 6.1. Об отсутствии значимых различий и факторных влияний судили при критическом уровне достоверности (р) меньшем или равном 0,05.
Результаты и их обсуждение. У всех экспериментальных животных с паратиреоидэк-томией (ГПТ) исследование водовыделительной функции выявило значительное увеличение шестичасового диуреза (р<0,001), что было обусловлено, как повышением (р<0,01) скорости клубочковой ультрафильтрации (СКФ), так и слабовыраженным, но достоверным (р<0,02) снижением канальцевой реабсорбции воды (табл.). У групп животных с ведение хлорида ртути, как изолированно (Н£), так и на фоне гипопаратиреоза (Д^+ГПТ) также было отмечено более выраженное увеличение диуреза (р<0,001), однако обусловлено это было значительным снижением канальцевой реабсорбции (р<0,001), при уменьшении скорости клубочко-вой ультрафильтации (р<0,01).
В состоянии кальциевого гомеостаза и его почечной обработке у животных с удаленными паращитовидными железами отмечались соответствующие изменения (рис. 1), приводящие к снижению уровня кальция в плазме крови (р<0,001), что согласуется с данными подобных исследований [7]. Так, на фоне значительного, более чем в два раза, увеличения экскреции катиона с мочой (р<0,001), было отмечено достоверное уменьшение его в плазме крови, что, при неизменённом уровне фильрационного заряда, было связано со значительным снижением его канальцевой реабсорбции (р<0,001). В данной серии эксперимента, у животных с ГПТ отсутствие достоверного снижения фильтаци-онного заряда кальция при его сниженной концентрации в плазме крови было обусловлено с увеличением скорости клубочковой ульт-рафильрации плазмы. Вероятное при этом повышение скорости тока первичной мочи могло стать причиной некоторого снижения осмо-лярности конечной мочи (р<0,01) у крыс с пара-тиреоидэктомией (табл.).
Токсическое влияние ртути (И£) проявляется в увеличении экскреции кальция с мочой (р<0,01) вследствие снижения его канальцевой реабсорб-ции (р<0,01), при слабовыраженном снижении фильтрационного заряда (р<0,05), обусловленного низким уровнем СКФ плазмы. При этом отмечено увеличение (р<0,01) концентрации кальция в плазме крови, вероятно связанное с угнетающим действием ртути на активность щелочной фосфа-
тазы в костной ткани и повышением выведения кальция из костей [12,19,21].
Данные проявления токсического действия сулемы значительно усиливаются у животных с гипокальциемией, вызванной паратиреоидэк-томией (Цд+ГПТ). В большей степени увеличиваются потери кальция с мочой (р<0,001), что обусловлено значительным снижением его ка-нальцевой реабсорбции (р<0,001). При этом сниженный уровень фильтрационного заряда катиона (р<0,001) обусловлен, как снижением общей СКФ, так и уменьшением концентрации катиона в крови относительно интактных животных (р<0,01).
Рис. 1. Изменение почечной обработки кальция на фоне гипокальциемии и введения хлорида ртут
Рис. 2. Изменение почечной обработки натрия на фоне гипокальциемии и введения хлорида ртути
Эффекты ГПТ на обмен натрия у животных (рис. 2) проявились в некотором повышении экскреции катиона с мочой (р<0,05) на фоне увеличения его фильтрационного заряда (р<0,001), что, очевидно, связано с увеличением СКФ. Отмечено, также, небольшое снижение концентрации натрия в плазме крови (р<0,05), вероятно, обусловленное его потерями с мочой.
У животных других групп, как с изолированным введением хлорида ртути, так и в сочетании с паратириновой депривацией, выявлены однонаправленные изменения изучаемых процессов поддержания натриевого гомеоста-
зиса. Отмечено значительное увеличение экскреции натрия с мочой (р<0,001) вследствие снижения его канальциевой реабсорбции (р<0,001), несмотря на уменьшение фильтрационного заряда катиона (р<0,001). В результате выраженных потерь натрия с мочой, его концентрация в плазме крови была достоверно сниженной (р<0,001). Все отмеченные изменения проявлялись в большей степени у животных с введением сулемы на фоне гипопарати-реоза (р<0,001 относительно фона).
Таблица
Влияние сулемы на фоне гипокальциемии,
вызываемой двусторонней паратиреоидэктомией, на функции почек
Примечание: I — достоверное отличие от фона; А -достоверное отличие от контроля с гипопаратирео-зом; * — достоверное отличие от контроля с введением хлорида ртути
В балансе другого жизненно-важного электролита — калия, тоже были отмечены изменения (табл.). В модели с гипопаратиреозом достоверного изменения концентрации калия в плазме крови не отмечалось. При этом была незначительно снижена его экскреция с мочой (р<0,05), на фоне увеличения фильтрационного заряда катиона (р<0,02), что может быть объяснено увеличенной скоростью клубочковой ультрафильтрации.
У крыс с ртутной интоксикацией, как изолированной, так и сочетанной с паратиреоидэк-томией, при неизмененном фильтрационном заряде калия, отмечено увеличение концентрации его в плазме крови (р<0,01), и достоверное увеличение его потерь с мочой (р<0,01). Вероятной причиной гиперкалиемии является токсическое разрушение эритроцитов, что приводит к компенсаторному увеличению секреции катиона, и объясняет увеличение его экскреции при сниженном уровне СКФ.
При введении ртути, как изолированно, так и на фоне гипопаратиреоза, отмечена выраженная протеинурия (р<0,001), свидетельствующая о токсическом действии сулемы (рис. 3), как на фильтрационный барьер нефро-нов, так и на их канальцевый аппарат. Более выраженная протеинурия при действии ртути на фоне паратиреоидэктомии позволяет считать, наряду с вышеприведенными различиями, более интенсивное повреждающее действие ртути на фоне гипокальциемии.
Экскреция белка
Рис. 3. Протеинурия на фоне гипопаратиреоза и введения хлорида ртути.
Прямое повреждающее действие ртути на клетки эпителия канальцев, нарушение работы энергозависимых транспортных систем мембран клеток, связанное с токсическим действием на ферментные системы энергообеспечения, нарушение эффектов альдостерона, как и ряд других патогенетических механизмов, описанных в литературе [15,16], приводят выявленному катионному дисбалансу.
В условиях токсического поражения нефронов ртутью, проявляющегося в повреждении, как фильтрационного барьера клубочков, так и канальцев, почки теряют способность к осмотическому концентрированию мочи, что и проявляется (табл.) в выведении гипоосмотич-
Показатель Стат. п-ли Группы животных
Фон (п-15) ГПТ (п-15) Hg (п-15) Hg + ГПТ (п-15)
Диурез мл/час/100 г M±m 0,0643±0,002 0,138±0,008 0,218±0,011 0,221±0,006
Р X XA XA
Фильтр ация, мл/час/100 г M±m 15,3±0,22 18,17±0,33 12,71±0,25 12,18±0,23
Р X XA XA
К воды, о/ /о M±m 99,58±0,016 99,24±0,007 98,28±0,026 98,19±0,04
Р X XA XA
С калия в плазме крови, M±m 4,11±0,085 4,25±0,054 4,92±0,071 5,23±0,083
Р — XA XA*
Экскреция калия, мкмоль/час/100 M±m 6,618±0,203 5,32±0,062 7,25±0,081 7,87±0,059
Р X XA XA
ФЗ калия, мкмоль/час/100 г M±m 59,63±1,26 73,36±1,13 59,41±0,93 60,52±1,27
Р X — —
Осмолярность мочи, огм/л M±m 2,15±0,017 1,94±0,048 1,78±0,031 1,85±0,052
Р X XA XA
Экскреция белка, мг/час/100 г M±m 0,121±0,005 0,199±0,014 2,414±0,022 2,58±0,053
Р X XA XA
JOURNAL OF NEW MEDICAL TECHNOLOGIES — 2016 — V. 23, № 2 — P. 90-95
ной мочи у крыс в группах с введением хлорида ртути (р<0,01).
Заключение. Многие годы в литературе обсуждается вопрос о большой вероятности того, что токсические эффекты тяжелых металлов опосредуются через изменение Ca2+ гомео-стаза [20]. Так ртуть, обладающая большой афинностью к SH-группам, может блокировать активность всех SH-содержащих ферментных
Литература
1. Брин В.Б., Митциев А.К., Митциев К.Г. Способ коррекции нефротоксического действия кадмия в эксперименте // Вестник новых медицинских технологий. 2011. Т. 17, №2. С. 194-195.
2. Брин В.Б., Митциев К.Г., Митциев А.К., Кабисов О.Т. Влияние экспериментальной гиперкальцие-мии на кардиоваскулярные проявления хронической медной интоксикации // Вестник новых медицинских технологий. 2014. Т. 21, №2. С. 83-86.
3. Брин В.Б., Бузоева М.Р. Сравнительное изучение ре-нальных эффектов хлорида кобальта в условиях измененного гомеостазиса кальция // Вестник новых медицинских технологий. 2010. Т.17, №7. С. 88-90.
4. Бузоева М.Р., Брин В.Б. Почечные эффекты хлорида кобальта на фоне хронического гипопаратиреоза // Вестник новых медицинских технологий. 2009. Т.16, №4. С. 75-76.
5. Митциев К.Г., Брин В.Б., Митциев А.К., Кабисов О.Т. Влияние гиперкальциемии, вызванной каль-цитриолом, на функциональное состояние сердечно-сосудистой системы // Владикавказский медико-биологический вестник. 2012. Т. X1V, №22. С. 120123.
6. Agarwal P., Prakash M., Singhal M., Bhadada S.K., Gupta Y., Khandelwal N. To assess vascular calcification in the patients of hypoparathyroidism using mul-tidetector computed tomography scan // Indian J Endocrinol Metab. 2015. 19(6). P. 785-790.
7. Ayusheeva A.V., Lepekhova S.A., Goldberg O.A., Il’iche-va E.A., Andaeva T.M., Koryakina L.B., Kurganskii I.S., Zaritskaya L.V. Parathyroidectomy in Rats Using Microsurgery and Medical Adhesive Sulfacrylate. Vestn Ross Akad Med Nauk. 2015. №3. P. 320-327.
8. Bakas P., Chados N., Hassiakos D., Creatsa M., Liapis A, Creatsas G. Secondary hypoparathyroidism during pregnancy — case report and review of the literature // Clin Exp Obstet Gynecol. 2015. Vol. 42(6). P. 825-826.
9. Burlando B., Marchi B., Panfoli I., Viarengo A. Essential role of Ca2+-dependent phospholipase A2 in estradiol-induced lysosome activation // Am. J. Physiol. Cell Physiol. 2002. Vol. 283. P.1461-1468.
10. Callies F., Arlt W., Scholz H.J., Reincke M., Allolio B. Management of hypoparathyroidism during pregnan-cy—report of twelve cases // Eur J Endocrinol. 1998. Vol. 139(3). P. 284-289.
11. Jeong Y.S., Ju H.S., Younghee C., Hannah S., Tae-Seo S.
систем, таких как Ca/Mg АТФ-аза, изменяя внутриклеточный баланс Ca2+, нарушать работу митохондрий и вызывать оксидативный стресс. В нашем варианте эксперимента показано потенцирование токсических эффектов хлорида ртути в сочетанной модели с измененным кальциевым гомеостазом, что может подтверждать возможную роль катиона в проявлениях токсичности ртути.
References
Brin VB, Mittsiev AK, Mittsiev KG. Sposob korrektsii nefrotoksicheskogo deystviya kadmiya v eksperimente. Vestnik novykh meditsinskikh tekhnologiy. 2011;17(2):194-5. Russian.
Brin VB, Mittsiev KG, Mittsiev AK, Kabisov OT. Vliyanie eksperimental’noy giperkal’tsiemii na kardiovaskulyar-nye proyavleniya khronicheskoy mednoy intoksikatsii. Vestnik novykh meditsinskikh tekhnologiy. 2014;21(2):83-6. Russian.
Brin VB, Buzoeva MR. Sravnitel’noe izuchenie renal’nykh effektov khlorida kobal’ta v usloviyakh izmenennogo go-meostazisa kal’tsiya. Vestnik novykh meditsinskikh tekhno-logiy. 2010;17(7):88-90. Russian.
Buzoeva MR, Brin VB. Pochechnye effekty khlorida kobal’ta na fone khronicheskogo gipoparatireoza. Vestnik novykh meditsinskikh tekhnologiy. 2009;16(4):75-6. Russian.
Mittsiev KG, Brin VB, Mittsiev AK, Kabisov OT. Vliyanie giperkal’tsiemii, vyzvannoy kal’tsitriolom, na funktsion-al’noe sostoyanie serdechno-sosudistoy sistemy. Vladi-kavkazskiy mediko-biologicheskiy vestnik.
2012;X1V(22):120-3. Russian.
Agarwal P, Prakash M, Singhal M, Bhadada SK, Gupta Y, Khandelwal N. To assess vascular calcification in the patients of hypoparathyroidism using multidetector computed tomography scan. Indian J Endocrinol Metab. 2015;19(6):785-90.
Ayusheeva AV, Lepekhova SA, Goldberg OA, Il’icheva EA, Andaeva TM, Koryakina LB, Kurganskii IS, Zaritskaya LV. Parathyroidectomy in Rats Using Microsurgery and Medical Adhesive Sulfacrylate. Vestn Ross Akad Med Nauk. 2015;3:320-7.
Bakas P, Chados N, Hassiakos D, Creatsa M, Liapis A, Creatsas G. Secondary hypoparathyroidism during pregnancy — case report and review of the literature. Clin Exp Obstet Gynecol. 2015;42(6):825-6. Burlando B, Marchi B, Panfoli I, Viarengo A. Essential role of Ca2+-dependent phospholipase A2 in estradiol-induced lysosome activation. Am. J. Physiol. Cell Phy-
siol. 2002;283:1461-8.
Callies F, Arlt W, Scholz HJ, Reincke M, Allolio B. Management of hypoparathyroidism during pregnancy-report of twelve cases. Eur J Endocrinol. 1998;139(3):284-9.
Jeong YS, Ju HS, Younghee C, Hannah S, Tae-Seo S.
Widespread intracranial calcifications in a patient with hypoparathyroidism // Korean J Intern Med 2016; Published online: January 29, 2016.
12. Jin GB, Inoue S, Urano T, Cho S, Ouchi Y, Cyong JC. Induction of anti-metallothionein antibody and mercury treatment decreases bone mineral density in mice. Toxicol Appl Pharmacol. 2002. Vol. 185, №2. P. 98-110.
13. Khan M.I., Waguespack S.G., Hu M.I. Medical management of postsurgical hypoparathyroidism // Endocr Pract. 2011. Suppl 1: P.18-25.
14. Liu L., Yang J. The changes of parathyroid hormone and serum calcium after total thyroidectomy // Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2015. Vol. 29(11). P. 984-987.
15. Marchi B., Burlando B., Moorec M.N., Viarengo A. Mercury- and copper-induced lysosomal membrane destabilization depends on [Ca2+]i dependent phos-pholipase A2 activation // Aquatic Toxicology. 2004. Vol. 66. P. 197-204.
16. Masato O., Atsushi M., Mitsuya S. Heavy metal chelator TPEN attenuates fura-2 fluorescence changes induced by cadmium, mercury and methylmercury // The Journal of Veterinary Medical Science Advance Publication 15 Jan 2016.
17. Sikjaer T., Moser E., Rolighed L., Underbjerg L., Bis-lev L.S., Mosekilde L., Rejnmark L. Concurrent Hypo-parathyroidism Is Associated with Impaired Physical Function and Quality of Life in Hypothyroidism // J Bone Miner Res. 2016 Feb 10. doi: 10.1002.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
18. Suwannasarn M., Jongjaroenprasert W., Chayangsu P., Suvikapakornkul R., Sriphrapradang P. Single measurement of intact parathyroid hormone after thyroi-dectomy can predict transient and permanenthypopa-rathyroidism: a prospective study // Asian J Surg. 2016 Jan 9. pii: S1015-9584(15). P.00150-5.
19. Suzuki N., Yamamoto M., Watanabe K., Kambegawa A., Hattori A. Both mercury and cadmium directly influence calcium homeostasis resulting from the suppression of scale bonecells: the scale is a good model for the evaluation of heavy metals in bone metabolism // J Bone Miner Metab. 2004. Vol. 22, №5. P. 439-446.
20. Viarengo A., Nicotera P. Possible role of Ca2+ in heavy metal cytotoxicity.Comparative Biochemistry and Physiology // Comparative Pharmacology and Toxicology. 1991. 100(1-2). P. 81-84.
21. Yachiguchi K., Sekiguchi T., Nakano M., Hattori A., Yamamoto M., Kitamura K., Maeda M., Tabuchi Y., Kondo T., Kamauchi H., Nakabayashi H., Srivastav A.K., Hayakawa K., Sakamoto T., Suzuki N. Effects of inorganic mercury and methylmercury on osteoclasts and osteoblasts in the scales of the marine teleost as a model system of bone // Zoolog Sci. 2014. 31(5). P.330-337.
22. Youngwirth L., Benavidez J., Sippel R., Chen H. Parathyroid hormone deficiency after total thyroidectomy: incidence and time // J Surg Res. 2010. 163(1). P. 69-71.
Widespread intracranial calcifications in a patient with hypoparathyroidism. Korean J Intern Med 2016; Published online: January 29, 2016.
Jin GB, Inoue S, Urano T, Cho S, Ouchi Y, Cyong JC. Induction of anti-metallothionein antibody and mercury treatment decreases bone mineral density in mice. Toxicol Appl Pharmacol. 2002;185(2):98-110. Khan MI, Waguespack SG, Hu MI. Medical management of postsurgical hypoparathyroidism. Endocr Pract. 2011. Suppl 1:18-25.
Liu L, Yang J. The changes of parathyroid hormone and serum calcium after total thyroidectomy. Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2015;29(11):984-7.
Marchi B, Burlando B, Moorec MN, Viarengo A. Mercury- and copper-induced lysosomal membrane destabi-lization depends on [Ca2+]i dependent phospholipase A2 activation. Aquatic Toxicology. 2004;66:197-204.
Masato O, Atsushi M, Mitsuya S. Heavy metal chelator TPEN attenuates fura-2 fluorescence changes induced by cadmium, mercury and methylmercury. The Journal of Veterinary Medical Science Advance Publication 15 Jan 2016.
Sikjaer T, Moser E, Rolighed L, Underbjerg L, Bislev LS, Mosekilde L, Rejnmark L. Concurrent Hypoparathyroidism Is Associated with Impaired Physical Function and Quality of Life in Hypothyroidisms J Bone Miner Res. 2016 Feb 10. doi: 10.1002.
Suwannasarn M, Jongjaroenprasert W, Chayangsu P, Suvikapakornkul R, Sriphrapradang P. Single measurement of intact parathyroid hormone after thyroidectomy can predict transient and permanenthypoparathyroid-ism: a prospective study. Asian J Surg. 2016 Jan 9. pii: S1015-9584(15). P.00150-5.
Suzuki N, Yamamoto M, Watanabe K, Kambegawa A, Hattori A. Both mercury and cadmium directly influence calcium homeostasis resulting from the suppression of scale bonecells: the scale is a good model for the evaluation of heavy metals in bone metabolism. J Bone Miner Metab. 2004;22(5):439-46.
Viarengo A, Nicotera P. Possible role of Ca2+ in heavy metal cytotoxicity.Comparative Biochemistry and Physiology. Comparative Pharmacology and Toxicology. 1991;100(1-2):81-4.
Yachiguchi K, Sekiguchi T, Nakano M, Hattori A, Ya-mamoto M, Kitamura K, Maeda M, Tabuchi Y, Kondo T, Kamauchi H, Nakabayashi H, Srivastav AK, Hayakawa K, Sakamoto T, Suzuki N. Effects of inorganic mercury and methylmercury on osteoclasts and osteoblasts in the scales of the marine teleost as a model system of bone. Zoolog Sci. 2014;31(5):330-7.
Youngwirth L, Benavidez J, Sippel R, Chen H. Parathyroid hormone deficiency after total thyroidectomy: incidence and time. J Surg Res. 2010;163(1):69-71.
Тубокурарина хлорид
Тубокураринхлорид (d-Тубокураринхлорид) — алкалоид из группы изохинолиновых алкалоидов[нем.] растительного происхождения, обладающий миорелаксантным физиологическим действием и, благодаря наличию у него такой биологической активности, применяемый в медицине как мышечный релаксант в виде препарата тубокурарин-хлорида (Tubocurarini chloridum). Является одним из действующих веществ яда кураре и химически представляет собой производное бис-бензилизохинолина (входит в группу из примерно 400 соединений близкого строения, встречающихся в различных видах растений)[1].
| Тубокурарина хлорид | |
|---|---|
| Тубарин в ампулах |
|
| Химическое соединение | |
| Брутто-формула | C37H41N2O6⁺ |
| CAS | 57-95-4 |
| PubChem | 6000 |
| DrugBank | DB01199 |
| Состав | |
| Классификация | |
| АТХ | M03AA02 |
| Способы введения | |
| внутривенное вливание | |
| Другие названия | |
| Тубокурарин-хлорид, Тубокурарин, (+)-тубокурарин | |
| Медиафайлы на Викискладе |
Синонимы: Amelizol, Curadetensin, Curarin, Delacurarine, Myostatine, Myricin, Tubadil, Tubaril, Tubarine, Tubocuran, Курарин-аста, Интоксотрин и др.
В медицинской практике используется с 40-х годов XX века. В настоящее время уже редко применяется в медицине (его синтетические аналоги гораздо доступнее и более безопасны в применении).
История открытия и изучения
править
Издревле использовался (в виде кураре) южно-американскими индейцами, проживавшими в бассейнах Ориноко и Амазонки, в качестве яда для стрел. Европейцы знали о своеобразном действии кураре ещё с XVI века, но первые серьёзные научные исследования кураре были проведены только в конце XIX века (Р. Бём, 1895 г.). Гарольд Кинг в 1935 г. выделил этот алкалоид из кураре в чистом виде, в 1937 г. установил природный источник этого алкалоида (хондродендрон войлочный), а в 1948 г. им же было установлено строение молекулы данного соединения[2] (впоследствии выяснилось, что не вполне точно). Окончательно строение тубокурарина было установлено только к 1970 г. исследованиями нескольких учёных (А. Дж. Эверетт, Л.А. Лоу, С. Вилкинсон)[3][4].
Попытки осуществить полный химический синтез этого соединения предпринимались ещё до установления его точного строения. В 1979 г. была предложена полусинтетическая схема синтеза тубокурарина (в качестве исходного соединения использовался один из его предшественников в биосинтезе). В 2016 г. немецкие учёные из Университета им. Иоганна Гутенберга сообщили о разработке ими успешной схемы синтеза тубокурарина, включающей в себя 15 стадий и использующей ванилин в качестве исходного соединения[1].
Механизм действия и физиологические эффекты
править
Является конкурентным ингибитором н-холинорецепторов мионевральных синапсов, снижающим или полностью устраняющим их чувствительность к ацетилхолину, что препятствует возбуждению мышечных волокон под действием нервных импульсов (прямая возбудимость мышц при этом сохраняется). Физиологически это проявляется в полной миорелаксации, имеющей временный и обратимый характер. Действие развивается постепенно, обычно релаксация мышц начинается через 1-1,5 мин, а максимум действия наступает через 3-4 мин[3][5].
Подвергается биотрансформации в организме (преимущественно в мышцах).
В небольших и умеренных дозах не оказывает влияния на сознание, органы чувств и биоэлектрическую активность мозга. В больших дозах уже блокирует н-холинорецепторы вегетативных нервных узлов, каротидной зоны и мозгового вещества надпочечников.
Мышцы под воздействием тубокурарина расслабляются в следующей последовательности: мышцы пальцев рук — глаз — ног — шеи — спины, потом межреберные мышцы и диафрагма.
При приеме малых доз остановка дыхания может не произойти (если не блокирована нервная передача к межреберным мышцам и диафрагме), однако при увеличении дозы происходит остановка дыхания; если же производится искусственная вентиляция легких, действие d-тубокурарина постепенно проходит и восстанавливается естественное дыхание.
При этом восстановление функции мышц происходит в последовательности, обратной их расслаблению. При адекватной искусственной вентиляции легких d-тубокурарин не вызывает нарушений основных функций организма.
На сердечно-сосудистую систему d-тубокурарин выраженного непосредственного влияния не оказывает, однако в связи с ганглиоблокирующим действием может вызывать понижение артериального давления (обычно на 15—20 мм рт. ст.). На ЦНС d-тубокурарин в обычных дозах существенного влияния не оказывает. Следует учитывать, что d-тубокурарин способствует освобождению из тканей гистамина и может иногда вызывать спазм мышц бронхов и гортани[5].
Плохо всасывается в ЖКТ. Не проникает через гематоэнцефалический барьер и плаценту. Максимальная концентрация в крови достигается в пределах 5-7 мин. после введения. Полная миорелаксация скелетных мышц и апноэ у большинства людей наблюдается при концентрации тубокурарина в плазме крови от 4 до 10 мг/мл.
Период полувыведения у человека — 13 мин. До 40% от введённого количества выводится из организма (с мочой) в неизменном виде. За несколько часов после введения, из организма выводится до 70% от исходного количества, попавшего в организм (особенно интенсивно выводится в первые 25-30 мин. после введения). Практически полностью выводится из организма за 24 ч.
Если требуется более длительное действие, вводят d-тубокурарин повторно, при этом в связи со способностью к кумуляции каждая последующая доза должна быть в 1,5-2 раза меньше предыдущей. Обычно для операции, продолжающейся 2-2,5 ч, расходуется 40-45 мг препарата[5].
Используется как миорелаксант при острых спастических состояниях (судорогах) скелетных мышц (например, при отравлении стрихнином, столбняке, некоторых психических заболеваниях) и как вспомогательное средство при хирургическом наркозе в травматологии и торокальной и абдоминальной хирургии (значительно улучшает протекание как самого наркоза, так и посленаркозного периода).
Вводят внутривенно.
Средняя доза для взрослого человека составляет 15—25 мг, при этом релаксация длится 20—25 мин. Однако дозы d-тубокурарина, так же как и других миорелаксантов, зависят от применяемого наркоза. При комбинированной общей анестезии с применением закиси азота внутривенное введение d-тубокурарина в дозе 0,4—0,5 мг/кг вызывает полное мышечное расслабление и апноэ продолжительностью 20—25 мин. Удовлетворительное расслабление мышц брюшного пресса и конечностей продолжается в течение 20—30 мин.
Если требуется более длительное действие, вводят тубокурарин повторно, при этом в связи со способностью к кумуляции каждая последующая доза должна быть в 1,5—2 раза меньше предыдущей. Обычно для операции, продолжающейся 2—2,5 ч, расходуется 40—45 мг препарата.
При использовании мощных наркотических средств (фторотан, эфир, пентран и др.) дозу снижают на 30-50%. При эфирном наркозе первоначальная доза d-тубокурарина составляет 0,25—0,4 мг/кг.
Тубокурарин применяют только после перевода пациентов на искусственную вентиляцию легких[5].
Лекарственная аллергия на тубокурарин и другие алкалоиды группы кураре, тяжёлая миастения, заболевания лёгких; заболевания, нарушающие электролитный баланс и вызывающие гипокалиемию (поражения печени и почек, кишечная непроходимость).
С осторожностью назначают пожилым пациентам[5].
Взаимодействие с другими лекарственными средствами
править
Антагонистами тубокурарина являются антихолинэстеразные средства (прозерин, галантамин и др.).
Усиливают его действие некоторые другие миорелаксанты (диплацин, анатруксоний, диоксоний)[5].
Форма выпуска: 1% раствор в ампулах по 1,5 мл (15 мг в 1,5 мл)[5].
Хранение: список А.
Синтетическими аналогами тубокурарина являются дитилин (имеет самую короткую продолжительность миорелаксирующего эффекта — 5-10 мин.), диплацин и павулон (20-40 мин.), а также анатруксоний. Как для тубокурарина, так и для его синтетических аналогов, характерно наличие в молекуле двух катионных центров на расстоянии в 1,5 нм (именно такая особенность строения их молекул позволяет им конкурировать с ацетилхолином в молекулярно-биохимических процессах передачи нервно-мышечного возбуждения)[3].
- ↑ 1 2 Nicola Otto, Dorota Ferenc, Till Opatz. A Modular Access to (±)-Tubocurine and (±)-Curine — Formal Total Synthesis of Tubocurarine // The Journal of Organic Chemistry. — 2017-01-20. — Т. 82, вып. 2. — С. 1205–1217. — ISSN 0022-3263. — doi:10.1021/acs.joc.6b02647.
- ↑ Harold King. 64. Curare alkaloids. Part VII. Constitution of dextrotubocurarine chloride (англ.) // Journal of the Chemical Society (Resumed). — 1948-01-01. — Iss. 0. — P. 265–266. — ISSN 0368-1769. — doi:10.1039/JR9480000265. Архивировано 4 июня 2018 года.
- ↑ 1 2 3 Ю.А. Овчинников. Биоорганическая химия. — Москва: Просвещение, 1987. — С. 651-652. — 815 с.
- ↑ A. J. Everett, L. A. Lowe, S. Wilkinson. Revision of the structures of (+)-tubocurarine chloride and (+)-chondrocurine (англ.) // Journal of the Chemical Society D: Chemical Communications. — 1970-01-01. — Iss. 16. — P. 1020–1021. — ISSN 0577-6171. — doi:10.1039/C29700001020. Архивировано 9 июня 2018 года.
- ↑ 1 2 3 4 5 6 7 Чекман И.С., Пелещук А.П., Пятак О.А. и др. Справочник по клинической фармакологии и фармакотерапии / И.С. Чекман. — Киев: Здоров’я, 1987. — С. 285-286. — 736 с.
Сулема, или дихлорид ртути осаждает белок, обладает сильным дезинфицирующим и антибактериальным действием.
Дихлорид ртути применяется для целей наружной дезинфекции как антисептическое средство в растворах (1:1000–2:1000) для дезинфекции кожи, белья, одежды, предметов ухода за больными, для обмывания стен.
Сертификат анализа сулемы:
Наименование: сулемы 98%
Молекулярная формула: HgCl2
Вес: 271,50
Art NO: AL2460
Batch No: AL2460 — MERC
Sr Нет
3 Кальций (Ca)
4 Магний (Mg)
6 Натрий (Na)
Результаты: Вышеуказанный продукт соответствует LR класса
Сертификат анализа сулемы AR 99,5%
Наименование: сулемы AR 99,5%
Молекулярная формула: HgCl2
Вес: 271,50
Art NO: AL2463
Batch No: AL2463 — MERC
Sr Нет
7 Нитраты (NO 3)
8 Кальций (Ca)
9 Медь (Cu)
10 Железо (Fe)
11 Свинец (Pb)
12 Магний (Mg)
14 Натрий (Na)
Особые указания
Сулема — сильный яд.
Применяя растворы дихлорида ртути следует соблюдать осторожность, так как даже при местном применении препаратов сулемы возможно отравление вследствие их всасывания.
Для дезинфекции металлических инструментов растворы сулемы не применяются, так как они вызывают коррозию металлов.
Отравление сулемой
Картину отравления сулемой делят на три стадии:
В первой преобладают симптомы поражения пищевого канала — жгучая боль по ходу пищевода и желудка, тошнота, рвота, металлический вкус во рту, слизистая оболочка рта набухает, серого цвета, часто покрывается налетом.
Вторая стадия характеризуется ослаблением деятельности сердца.
В третьей стадии поражаются органы, выделяющие ртуть, особенно почки, толстые кишки и слюнные железы, развивается ртутный стоматит, ртутный колит, «сулемовая» почка.
Смертельная доза сулемы 0,2–0,3 г.
