Форма выпуска, упаковка и состав
препарата Стрензик®
Раствор для п/к введения в виде бесцветной или желтоватой, прозрачной, слегка опалесцирующей или опалесцирующей жидкости, возможно наличие нескольких небольших полупрозрачных или белых частиц.
Вспомогательные вещества: натрия хлорид, натрия гидрофосфата гептагидрат, натрия дигидрофосфата моногидрат, вода д/и.
0.8 мл — флаконы стеклянные вместимостью 2 мл (1) — пачки картонные с этикеткой контроля первого вскрытия.
0.8 мл — флаконы стеклянные вместимостью 2 мл (12) — пачки картонные с этикеткой контроля первого вскрытия.
0.8 мл — флаконы стеклянные вместимостью 3 мл (1) — пачки картонные с этикеткой контроля первого вскрытия.
0.8 мл — флаконы стеклянные вместимостью 3 мл (12) — пачки картонные с этикеткой контроля первого вскрытия.
* Производится с использованием технологии рекомбинантной ДНК с использованием клеток яичника китайского хомяка (СНО) млекопитающих.
Фармакологическое действие
Фармакологическая активность средства определяется активностью фермента асфотаза альфа.
Асфотаза альфа, человеческий рекомбинантный тканенеспецифический гибридный Fc-дека-аспартатный белок ЩФ с ферментативной активностью, улучшает минерализацию скелета у пациентов с гипофосфатазией.
Биологическое действие асфотазы альфа обеспечивается за счет растворимой части рекомбинантного человеческого неспецифического тканевого изофермента ЩФ. Неспецифический тканевой изофермент ЩФ представляет собой металлофермент, который катализирует гидролиз фосфомоноэфиров с образованием неорганического фосфата и спирта, за счет чего обеспечивается физиологический процесс минерализации костей.
Фармакокинетика
На основании результатов популяционного фармакокинетического анализа был сделан вывод, что асфотаза альфа характеризуется линейным фармакокинетическим профилем при п/к введении доз вплоть до 28 мг/кг/нед. В качестве фактора, оказывающего влияние на клиренс и Vd асфотазы альфа, выступала масса тела. Ожидается, что уровень фармакокинетического воздействия будет возрастать с увеличением массы тела. Влияние иммуногенности на фармакокинетику асфотазы альфа варьировало с течением времени, что связано с варьирующей природой иммуногенности. В целом, было показано, что иммуногенность снижает уровень фармакокинетического воздействия менее чем на 20%.
Показания активных веществ препарата
Стрензик®
Длительная заместительная ферментная терапия пациентов с гипофосфатазией с началом в детском возрасте с целью купирования проявлений заболевания со стороны костей.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Устанавливают индивидуально.
Лечение должно быть начато врачом, имеющим опыт в области ведения пациентов с метаболическими расстройствами или заболеваниями костей.
Рекомендованная схема применения асфотазы альфа — 2 мг/кг массы тела путем п/к инъекции 3 раза/нед., либо 1 мг/кг массы тела путем п/к инъекции 6 раз/нед.
Побочное действие
Со стороны системы кроветворения: часто — повышенная склонность к образованию кровоподтеков.
Со стороны иммунной системы: часто — анафилактоидные реакции, реакции гиперчувствительности.
Со стороны нервной системы: очень часто — головная боль.
Со стороны сердечно-сосудистой системы: часто — приливы.
Со стороны пищеварительной системы: часто — гипестезия полости рта, тошнота.
Со стороны кожи и подкожных тканей: очень часто — эритема; часто — липогипертрофия (образование плотных участков измененной подкожно-жировой клетчатки, возникающее в связи с многократным повторным использованием одного места введения), генерализованный эластолиз, обесцвечивание кожи, включая гипопигментацию, нарушения со стороны кожи (стрии).
Со стороны костно-мышечной системы: очень часто — боль в конечности, часто — миалгия.
Общие реакции: очень часто — лихорадка, раздражительность, часто — озноб.
Местные реакции: очень часто — гематома, реакции со стороны места инъекции (включая эритему, обесцвечивание, боль, зуд, макулу, отек, кровоподтек, гипертрофию, уплотнение, реакцию в месте введения, атрофию, узелок, сыпь, папулу, гематому, воспаление, уртикарную сыпь, местную гипертермию, кровоизлияние, воспаление подкожных тканей и объемное образование в области места проведения инъекции); часто — постинъекционный целлюлит, рубец.
Противопоказания к применению
Повышенная чувствительность к компонентам средства.
С осторожностью следует применять средство у пациентов с нарушением функции печени и почек, а также у пожилых пациентов, в связи с недостаточностью данных; у пациентов с гипофосфатазией в возрасте от 0 до 5 лет с выявленным краниосиностозом, поскольку, несмотря на применение асфотазы альфа, возможно прогрессирование краниосиностоза с повышением внутричерепного давления.
Применение при беременности и кормлении грудью
Применение асфотазы альфа не рекомендуется во время беременности, а также женщинам детородного возраста не использующим средства контрацепции.
Во время терапии асфотазой альфа следует прекратить грудное вскармливание.
Применение при нарушениях функции печени
С осторожностью следует применять средство у пациентов с нарушением функции печени.
Применение при нарушениях функции почек
С осторожностью следует применять средство у пациентов с нарушением функции почек.
Применение у детей
Разрешено применение средства у детей.
Применение у пожилых пациентов
С осторожностью следует применять средство у пожилых пациентов.
Особые указания
Асфотаза альфа содержит каталитический домен тканенеспецифической ЩФ. При введении асфотазы альфа определение активности ЩФ рутинными лабораторными методами не представляется возможным в связи с многократно завышенными результатами. Активность асфотазы альфа не следует интерпретировать по значениям активности ЩФ, поскольку активность ЩФ характеризуется различиями ферментных характеристик.
Сообщалось о реакциях гиперчувствительности, включая признаки и симптомы, согласующиеся с анафилаксией у пациентов, получавших асфотазу альфа. Реакции возникают через несколько мин после п/к введения средства и могут возникать у пациентов, получавших лечение более 1 года. При возникновении реакций гиперчувствительности, необходимо немедленное прекращение лечения и назначение соответствующей медикаментозной терапии. Следует соблюдать принятые в настоящее время стандарты оказания неотложной помощи.
При необходимости повторного введения средства пациенту после серьезной реакции гиперчувствительности, следует оценить потенциальный риск и ожидаемую пользу от применения средства, принимая во внимание другие факторы, которые могут влиять на развитие реакции гиперчувствительности, такие как одновременная инфекция и/или использование антибиотиков. Если принято решение о повторном применении средства, повторное введение должно производиться под наблюдением врача, при использовании превентивных мер по предотвращению реакций гиперчувствительности.
Применение асфотазы альфа может вызвать развитие реакций в месте инъекции (включая, но не ограничиваясь, эритему, сыпь, обесцвечивание, зуд, боль, папулу, узелок, атрофию), которые определены в качестве связанных с терапией нежелательных явлений, возникающих во время проведения инъекции или до конца дня, в который проведена инъекция. Чередование областей проведения инъекций обычно способствует эффективному контролю возникновения данных реакций. Как правило, данные реакции расцениваются в качестве несерьезных, легких или умеренных по степени тяжести и самоограничивающихся.
Имеются сообщения о нежелательных явлениях краниосиностоза (связанного с повышенным внутричерепным давлением), включая ухудшение уже имеющегося краниосиностоза, у пациентов с гипофосфатазией в возрасте < 5 лет. Связи между терапией асфотазой альфа и прогрессированием краниосиностоза выявлено не было в связи с недостаточностью данных. Краниосиностоз, в качестве проявления гипофосфатазии — явление, указанное в опубликованной литературе и возникающее у 61,3 % пациентов в возрасте от момента рождения до 5 лет при естественном течении гипофосфатазии с началом в младенческом возрасте при отсутствии лечения. Краниосиностоз может привести к повышенному внутричерепному давлению.
Пациентам с гипофосфатазией в возрасте до 5 лет рекомендуется периодическое наблюдение (включая исследование глазного дна на предмет проявлений отека диска зрительного нерва) и незамедлительное вмешательство при повышенном внутричерепном давлении.
У пациентов с гипофосфатазией были выявлены отложения солей кальция в области глаз (конъюнктивальные и роговичные), а также нефрокальциноз Связи между терапией асфотазой альфа и ухудшением эктопической кальцификации выявлено не было в связи с недостаточностью данных.
Отложения солей кальция в области глаз (конъюнктивальные и роговичные) и нефрокальциноз указаны в опубликованной литературе в качестве проявлений гипофосфатазии. Нефрокальциноз возникает у 51.6 % пациентов в возрасте от момента рождения до 5 лет при естественном течении гипофосфатазии с началом в младенческом возрасте при отсутствии лечения. Пациентам с гипофосфатазией рекомендовано периодическое офтальмологическое обследование и УЗИ почек.
У пациентов с гипофосфатазией при применении асфотазы альфа может увеличиваться концентрация паратгормона в сыворотке крови, особенно на протяжении первых 12 недель терапии. У пациентов, получающих терапию асфотазой альфа, рекомендуется контролировать содержание паратгормона и кальция в сыворотке крови. Может понадобиться дополнительное применение препаратов кальция и перорального витамина D.
У пациентов, получающих терапию асфотазой альфа, может иметь место диспропорциональный прирост массы тела.
Рекомендуется диетологический контроль.
Стрензик — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005666
Торговое наименование:
Стрензик
Международное непатентованное наименование:
асфотаза альфа
Лекарственная форма:
раствор для подкожного введения
Состав на 1 мл
40 мг/мл
действующее вещество: асфотаза альфа 40 мг,
вспомогательные вещества:
натрия хлорид 8,76 мг, натрия гидрофосфата гептагидрат 5,5 мг, натрия дигидрофосфата моногидрат 0,62 мг, вода для инъекций до 1 мл;
100 мг/мл
действующее вещество: асфотаза альфа 100 мг,
вспомогательные вещества:
натрия хлорид 8,76 мг, натрия гидрофосфата гептагидрат 5,5 мг, натрия дигидрофосфата моногидрат 0,62 мг, вода для инъекций до 1 мл.
Описание
Бесцветная или желтоватая, прозрачная, слегка опалесцирующая или опалесцирующая жидкость, возможно наличие нескольких небольших полупрозрачных или белых частиц.
Фармакотерапевтическая группа:
Ферментное средство
Код ATX:
А16АВ13
Фармакологические свойства
Характеристика препарата
Асфотаза альфа представляет собой человеческий рекомбинантный тканенеспецифический химерный Fc-дека-аспартатный гликопротеин щелочной фосфатазы, экспрессирующийся в модифицированной культуре клеток яичника китайского хомячка. Асфотаза альфа – растворимый гликопротеин из двух цепочек по 726 аминокислот, включающий в себя: (1) каталитический домен человеческой тканенеспецифической щелочной фосфатазы; (2) Fc-домен человеческого иммуноглобулина G1; (3) дека-аспартатный пептидный домен (D10).
Очищается с помощью аффинной хроматографии и хроматографии гидрофобного взаимодействия, в процессе производства субстанции проводится инактивация и удаление вирусов.
Фармакодинамика
Фармакологическая активность препарата определяется активностью фермента асфотаза альфа.
Биологическое действие асфотазы альфа обеспечивается за счет растворимой части рекомбинантного человеческого неспецифического тканевого изофермента щелочной фосфатазы. Неспецифический тканевой изофермент щелочной фосфатазы представляет собой металлофермент, который катализирует гидролиз фосфомоноэфиров с образованием неорганического фосфата и спирта, за счет чего обеспечивается физиологический процесс минерализации костей.
Гипофосфатазия – редкое тяжелое прогрессирующее потенциально смертельное наследственное заболевание, обусловленное дефицитом щелочной фосфатазы, который возникает из-за мутации в гене ALPL, кодирующем неспецифический тканевой изофермент щелочной фосфатазы. Дефицит активности щелочной фосфатазы ведет к нарушениям регуляции обмена фосфата и кальция, гипоминерализации костей, нарушениям со стороны скелета (деформация и разрушение костей), и полиорганным осложнениям. Клиническими проявлениями также могут быть боль и выраженная мышечная слабость, дыхательная недостаточность, судороги, нарушение функции почек, нарушение двигательной функции, а также заболевания зубов.
Асфотаза альфа применяется как патогенетическое лечение гипофосфатазии в качестве длительной заместительной ферментной терапии. Устранение дефицита активности щелочной фосфатазы за счет замещения дефектного фермента предотвращает нарушения минерализации скелета и способствует восстановлению этого процесса.
Было продемонстрировано, что по сравнению с исходными значениями, лечение асфотазой альфа приводит к положительным изменениям у пациентов по таким признакам как уровни биохимических субстратов тканенеспецифической щелочной фосфатазы (неорганического пирофосфата и пиридоксаль-5′-фосфата), минерализация костной ткани, структура костей, рост, мышечная сила, физическая функция, способность передвигаться и инвалидность.
Механизм действия
Асфотаза альфа, человеческий рекомбинантный тканенеспецифический гибридный Fc-дека-аспартатный белок щелочной фосфатазы с ферментативной активностью, улучшает минерализацию скелета у пациентов с гипофосфатазией.
Клиническая эффективность и безопасность
Результаты клинических исследований асфотазы альфа получены в открытых не рандомизированных исследованиях с участием не менее 69 пациентов в основном с детской и инфантильной формами гипофосфатазии. В исследовании ENB-006-09/ ENB-008-10 у пациентов на фоне лечения асфотазой альфа по сравнению с группой контроля (исторический контроль с включением пациентов, не получавших терапию), отмечалась положительная рентгенологическая динамика по шкале общего впечатления о рентгенологических изменениях (RGI-C) на протяжении первых 6 месяцев терапии. По данным биопсии кости отмечена положительная динамика показателей минерализации костной ткани: толщина остеоида, отношение объема остеоида и объема костной ткани и время задержки минерализации костной ткани. У 9 из 13 пациентов получающих асфотазу альфа в этом исследовании наблюдалось увеличение показателя роста приближающегося к возрастной норме.
У пациентов с инфантильной формой гипофосфатазии в исследовании ENB-002-08/ ENB-003-08 при оценке по шкале общего впечатления о рентгенологических изменениях (RGI-C) зафиксировано: значительное улучшение отмечено у 7 из 11 пациентов; нарастающие темпы роста у 5 из 11 детей.
В исследовании ENB-009-10 на пациентах от 13 до 66 лет продемонстрирована положительная динамика минерализации костной ткани по результатам биопсии, отмечено улучшение показателей: толщина остеоида, отношение объема остеоида и объема костной ткани и время задержки минерализации костной ткани.
Фармакокинетика
После внутривенной инфузии дозы 3 мг/кг на протяжении 1,08 часа в исследуемых когортах медиана времени (Тmax) варьировала от 1,25 до 1,50 часов а среднее значение максимальной концентрации в плазме (Сmax) – от 42694 (8443) до 46890 (6635) ЕД/л. Абсолютная биодоступность после первой и третьей подкожной дозы варьировала от 45,8 до 98,4% с медианой Тmax от 24,2 до 48,1 часов.
Абсолютная биодоступность и скорость абсорбции после подкожного введения составляет 0,602 (95% доверительный интервал – ДИ: 0,567, 0,638) или 60,2% и 0,572 (95% ДИ: 0,338, 0,967)/сутки, соответственно. Центральные и периферические объемы распределения в пересчете на пациента с массой 70 кг (и 95% ДИ) составляли 5,66 (2,76, 11,6) л и 44,8 (33,2, 60,5) л, соответственно. Значения центрального и периферического клиренса в пересчете на пациента с массой 70 кг (и 95% ДИ) составляли 15,8 (13,2, 18,9) л/сутки и 51,9 (44,0, 61,2) л/сутки, соответственно. Среднее значение периода полувыведения после подкожного введения составляло 2,28 ± 0,58 суток.
Линейность/нелинейность
На основании результатов популяционного фармакокинетического анализа был сделан вывод, что асфотаза альфа характеризуется линейным фармакокинетическим профилем при подкожном введении доз вплоть до 28 мг/кг/неделю. В качестве фактора, оказывающего влияние на клиренс и объем распределения асфотазы альфа, выступала масса тела. Ожидается, что уровень фармакокинетического воздействия будет возрастать с увеличением массы тела. Влияние иммуногенности на фармакокинетику асфотазы альфа варьировало с течением времени, что связано с варьирующей природой иммуногенности. В целом, было показано, что иммуногенность снижает уровень фармакокинетического воздействия менее чем на 20%.
Показания к применению
Препарат Стрензик показан для длительной заместительной ферментной терапии пациентов с гипофосфатазией с началом в детском возрасте с целью купирования проявлений заболевания со стороны костей.
Противопоказания
Гиперчувствительность к действующему веществу (асфотазе альфа) или любому из вспомогательных веществ (компонентам препарата).
С осторожностью
В связи с недостаточностью данных препарат следует применять с осторожностью у пациентов с нарушением функции печени и почек, а также у пожилых пациентов.
У пациентов с гипофосфатазией в возрасте от 0 до 5 лет с выявленным краниосиностозом, так как, несмотря на применение асфотазы альфа, возможно прогрессирование краниосиностоза с повышением внутричерепного давления (см. раздел «Особые указания»).
Применение при беременности и в период грудного вскармливания
Беременность
Какие-либо данные в отношении применения асфотазы альфа беременными женщинами отсутствуют. После повторных подкожных введений асфотазы альфа беременным мышам в диапазоне терапевтической дозы (>0,5 мг/кг) уровни препарата определялись количественно в организме плода при всех исследованных дозах, что свидетельствует о трансплацентарном переносе асфотазы альфа. В отношении репродуктивной токсичности исследований на животных недостаточно. Применение асфотазы альфа не рекомендуется во время беременности, а также женщинам детородного возраста не использующим средства контрацепции.
Кормление грудью
В отношении выделения асфотазы альфа с грудным молоком у человека данных недостаточно. Не может быть исключен риск для новорожденного/ребенка, находящегося на грудном вскармливании. На время терапии асфотазой альфа следует прекратить грудное вскармливание.
Фертильность
В доклинических исследованиях фертильности не было выявлено какого-либо эффекта на фертильность и эмбриофетальное развитие.
Способ применения и дозы
Лечение должно быть начато врачом, имеющим опыт в области ведения пациентов с метаболическими расстройствами или заболеваниями костей.
Рекомендованная схема применения асфотазы альфа – 2 мг/кг массы тела путем подкожной инъекции три раза в неделю, либо 1 мг/кг массы тела путем подкожной инъекции шесть раз в неделю.
Более подробная информация представлена в таблице дозирования ниже.
| Масса тела (кг) |
При введении 3 раза в неделю | При введении 6 раз в неделю | ||||
| Вводимая доза |
Вводимый объем |
Используемый флакон с объемом препарата |
Вводимая доза |
Вводимый объем |
Используемый флакон с объемом препарата |
|
| 3 | 6 мг | 0,15 мл | 0,30 мл | |||
| 4 | 8 мг | 0,20 мл | 0,30 мл | |||
| 5 | 10 мг | 0,25 мл | 0,30 мл | |||
| 6 | 12 мг | 0,30 мл | 0,30 мл | 6 мг | 0,15 мл | 0,30 мл |
| 7 | 14 мг | 0,35 мл | 0,45 мл | 7 мг | 0,18 мл | 0,30 мл |
| 8 | 16 мг | 0,40 мл | 0,45 мл | 8 мг | 0,20 мл | 0,30 мл |
| 9 | 18 мг | 0,45 мл | 0,45 мл | 9 мг | 0,23 мл | 0,30 мл |
| 10 | 20 мг | 0,50 мл | 0,70 мл | 10 мг | 0,25 мл | 0,30 мл |
| 11 | 22 мг | 0,55 мл | 0,70 мл | 11 мг | 0,28 мл | 0,30 мл |
| 12 | 24 мг | 0,60 мл | 0,70 мл | 12 мг | 0,30 мл | 0,30 мл |
| 13 | 26 мг | 0,65 мл | 0,70 мл | 13 мг | 0,33 мл | 0,45 мл |
| 14 | 28 мг | 0,70 мл | 0,70 мл | 14 мг | 0,35 мл | 0,45 мл |
| 15 | 30 мг | 0,75 мл | 1,00 мл | 15 мг | 0,38 мл | 0,45 мл |
| 16 | 32 мг | 0,80 мл | 1,00 мл | 16 мг | 0,40 мл | 0,45 мл |
| 17 | 34 мг | 0,85 мл | 1,00 мл | 17 мг | 0,43 мл | 0,45 мл |
| 18 | 36 мг | 0,90 мл | 1,00 мл | 18 мг | 0,45 мл | 0,45 мл |
| 19 | 38 мг | 0,95 мл | 1,00 мл | 19 мг | 0,48 мл | 0,70 мл |
| 20 | 40 мг | 1,00 мл | 1,00 мл | 20 мг | 0,50 мл | 0,70 мл |
| 25 | 50 мг | 0,50 мл | 0,80 мл* | 25 мг | 0,63 мл | 0,70 мл |
| 30 | 60 мг | 0,60 мл | 0,80 мл* | 30 мг | 0,75 мл | 1,00 мл |
| 35 | 70 мг | 0,70 мл | 0,80 мл* | 35 мг | 0,88 мл | 1,00 мл |
| 40 | 80 мг | 0,80 мл | 0,80 мл* | 40 мг | 1,00 мл | 1,00 мл |
| 50 | 50 мг | 0,50 мл | 0,80 мл* | |||
| 60 | 60 мг | 0,60 мл | 0,80 мл* | |||
| 70 | 70 мг | 0,70 мл | 0,80 мл* | |||
| 80 | 80 мг | 0,80 мл | 0,80 мл* | |||
| 90 | 90 мг | 0,90 мл | 0,80 мл* (х2) | |||
| 100 | 100 мг | 1,00 мл | 0,80 мл* (х2) |
* используется препарат концентрации 100 мг/мл (80 мг/0,8 мл)
Пациенты с нарушением функции почек и печени
Безопасность и эффективность препарата Стрензик у пациентов с нарушением функции почек или печени не изучалась, и для данных пациентов не может быть рекомендована какая-либо особая схема применения препарата.
Пациенты взрослого возраста
Имеется ограниченное количество данных по эффективности и безопасности у пациентов с гипофосфатазией в возрасте старше 18 лет.
Лица пожилого возраста
Данные об опыте применения препарата Стрензик у пациентов пожилого возраста отсутствуют. При применении препарата пациентами пожилого возраста особых указаний нет.
Способ применения
Стрензик предназначен исключительно для подкожного введения. Не предназначен для внутривенного и внутримышечного введения. Максимальный объем вводимого за одну инъекцию лекарственного препарата не должен превышать 1 мл. При необходимости введения большего объема за один раз делают несколько инъекций в разные места введения.
Шприцы должны иметь достаточно малый объем, позволяющий в достаточной степени точно набрать предписанную дозу из флакона.
Места введения инъекций следует чередовать и тщательно контролировать на предмет возникновения проявлений потенциальных реакций.
Пациенты могут самостоятельно осуществлять инъекции только в том случае, если они прошли соответствующую подготовку по процедурам введения препарата.
Подготовка и проведение инъекции.
Соблюдайте правила антисептики. Вначале снимите с флакона защитную крышку, чтобы обнажить стерильную резиновую прокладку. Снимите пластиковый колпачок с иглы шприца и выбросьте его в контейнер для острых предметов. Потяните поршень, чтобы набрать в шприц воздух в объеме, эквивалентном необходимой дозе препарата. Держа шприц и флакон под углом 45°, введите иглу через стерильную резиновую прокладку. Теперь полностью задвиньте поршень, чтобы воздух попал во флакон. Переверните флакон и шприц, и следя за тем, чтобы игла находилась в растворе, потяните за поршень и наберите в шприц правильную дозу. Перед тем, как вынуть иглу из флакона, проверьте шприц на наличие пузырьков воздуха. При их наличии слегка постучите по стенке шприца, пока пузырьки не поднимутся вверх. Когда все пузырьки окажутся вверху, аккуратно нажмите на поршень, чтобы они попали обратно во флакон. Теперь проверьте дозу лекарственного препарата в шприце, чтобы убедиться, что набрано правильное количество.
Извлеките иглу из флакона, следя за тем, чтобы она ничего не касалась.
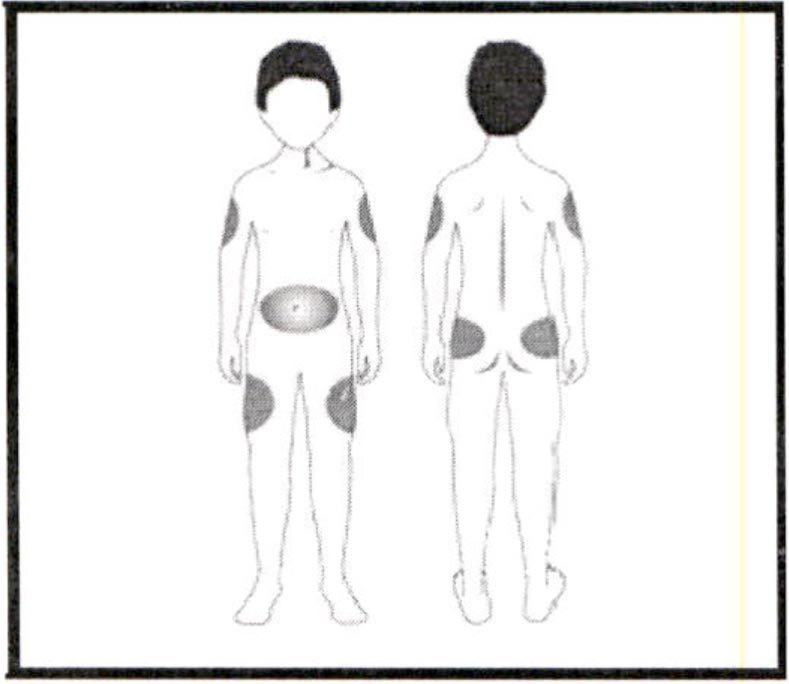
Выберите место для подкожной инъекции (бедра, живот, руки, ягодицы). Наиболее подходящие области для инъекции отмечены серым цветом на рисунке. Не используйте те участки, на которых имеются неприятные ощущения или патологические образования.
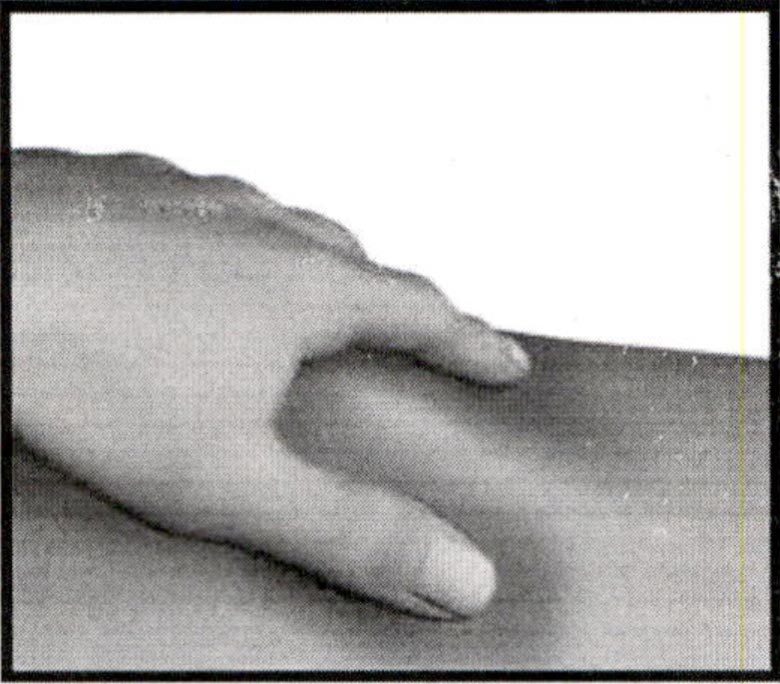
Аккуратно захватите кожу большим и указательным пальцами в месте инъекции.
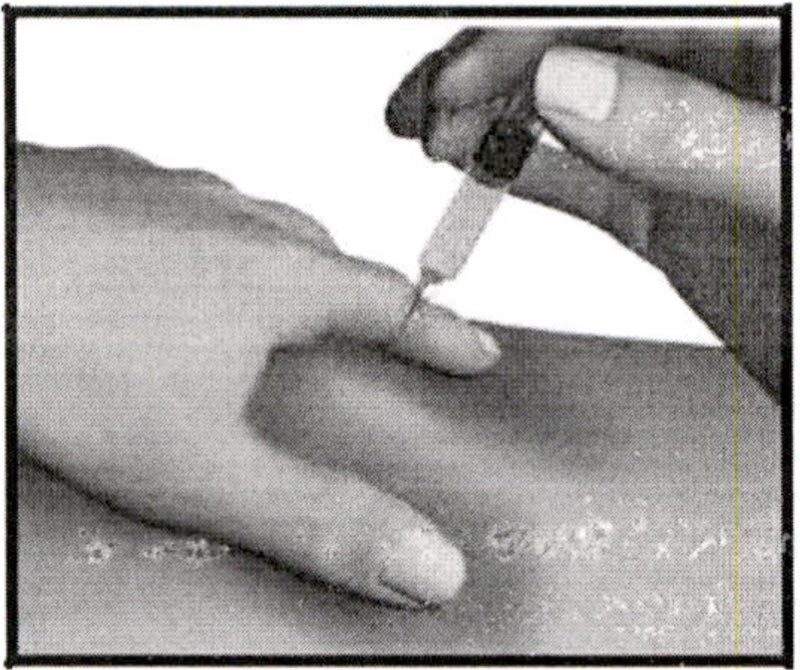
Держа шприц так же, как карандаш или дротик, введите иглу в приподнятую кожу под углом между 45° и 90° к поверхности кожи. Для маленьких детей с небольшим количеством подкожного жира или тонкой кожей предпочтителен угол 45°.
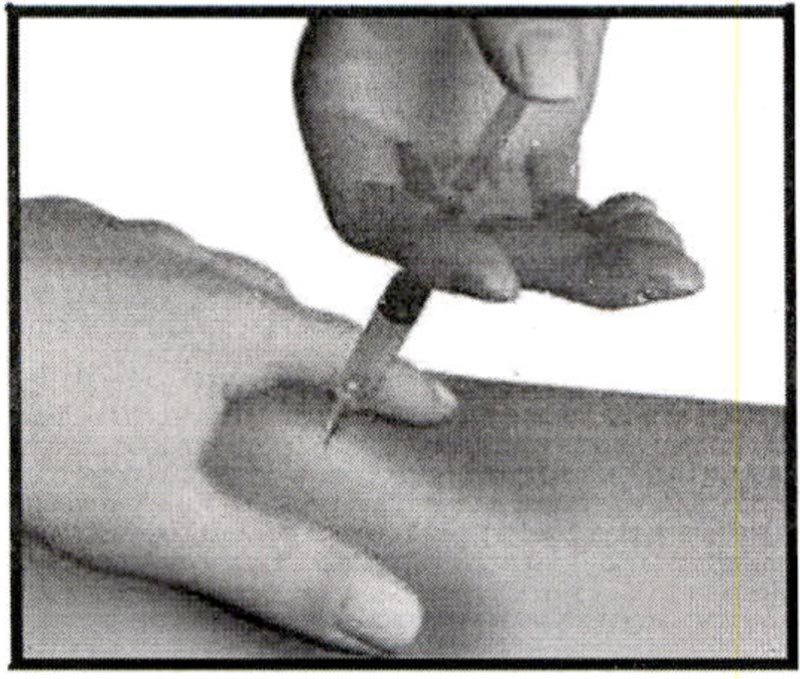
Продолжайте удерживать кожу и вводите препарат, надавливая на поршень и медленно считая до 10.
Извлеките иглу, отпустите кожную складку и аккуратно приложите кусочек ваты или марли к месту инъекции на несколько секунд. При необходимости наложите небольшую повязку или пластырь на место инъекции.
Побочное действие
В качестве наиболее часто наблюдаемых нежелательных явлений выступали местные нежелательные реакции, связанные с введением препарата. Большинство этих реакций были несерьезными и легкими или умеренными по степени тяжести. Серьезные нежелательные явления, связанные с инъекцией, были выявлены у 2 пациентов и не привели к прекращению терапии асфотазой альфа: у одного пациента с гипофосфатазией с началом в младенческом возрасте развились лихорадка и озноб, а у другого пациента с гипофосфатазией с началом в детском возрасте – гипестезия полости рта, боль в конечности, озноб и головная боль.
Ниже представлены данные о нежелательных реакциях при применении асфотазы альфа, наблюдавшиеся в рамках клинических исследований у 71 пациента (в возрасте от 1 дня до 66 лет), в соответствии с поражением органов и систем органов (MedDRA) и классификацией ВОЗ по частоте встречаемости: «очень часто» (≥1/10), «часто» (≥1/100 – <1/10), «нечасто» (≥1/1,000 – <1/100), «редко» (≥1/10000 – <1/1000), «очень редко» (<1/10000) и «частота неизвестна» (частота не может быть определена, основываясь на доступных данных). В пределах каждой группы частоты нежелательные реакции указаны в порядке убывания серьезности.
Таблица 1. Нежелательные реакции, выявленные в клинических исследованиях у пациентов с гипофосфатазией (в возрасте от 1 дня до 66 лет)
| Класс по поражению органов и систем органов | Категория частоты | Нежелательная реакция |
| Инфекционные и паразитарные заболевания | Часто | Постинъекционный целлюлит |
| Гематологические нарушения и нарушения со стороны лимфатической системы | Часто | Повышенная склонность к образованию кровоподтеков |
| Нарушения со стороны иммунной системы | Часто | Анафилактоидные реакции, гиперчувствительность2 |
| Нарушения со стороны нервной системы | Очень часто | Головная боль |
| Сосудистые нарушения | Часто | Приливы |
| Нарушения со стороны желудочно-кишечного тракта | Часто | Гипестезия полости рта Тошнота |
| Нарушения со стороны кожи и подкожных тканей | Очень часто | Эритема |
| Часто | Липогипертрофия (образование плотных участков измененной подкожно-жировой клетчатки, возникающее в связи с многократным повторным использованием одного места введения) Генерализованный эластолиз Обесцвечивание кожи, включая гипопигментацию Нарушение со стороны кожи («стрии») |
|
| Заболевания опорно-двигательного аппарата и соединительной ткани | Очень часто | Боль в конечности |
| Часто | Миалгия | |
| Общие расстройства и нарушения в месте введения препарата | Очень часто | Реакции со стороны места инъекции1 Лихорадка Раздражительность |
| Часто | Озноб | |
| Травмы, отравления и осложнения процедур | Очень часто | Гематома |
| Часто | Рубец |
1 Предпочтительные термины, рассматриваемые в качестве реакции со стороны места инъекции, представлены в разделе ниже.
2 Предпочтительные термины, рассматриваемые как гиперчувствительность, представлены в разделе ниже.
Реакции со стороны места инъекции
Реакции со стороны места инъекции (включая эритему, обесцвечивание, боль, зуд, макулу, отек, кровоподтек, гипертрофию, уплотнение, реакцию в месте введения, атрофию, узелок, сыпь, папулу, гематому, воспаление, уртикарную сыпь, местную гипертермию, кровоизлияние, воспаление подкожных тканей и объемное образование в области места проведения инъекции) являются наиболее частыми нежелательными реакциями, наблюдаемыми приблизительно у 73% пациентов в рамках клинических исследований. Частота возникновения реакции со стороны места инъекции была выше у пациентов с гипофосфатазией с началом в детском возрасте, а также у пациентов, получавших инъекции с частотой 6 раз в неделю (по сравнению с частотой 3 раза в неделю). Большинство реакций со стороны места инъекции были легкими и самоограничивающимися. Ни одна из данных реакций не расценивалась в качестве серьезного нежелательного явления. V двух пациентов наблюдалось возникновение реакций со стороны места инъекции, что вызвало необходимость уменьшения дозы асфотазы альфа.
Из 71 пациента, получавшего лечение в рамках клинических исследований, у одного пациента развилась тяжелая реакция со стороны места инъекции, проявляющаяся в виде обесцвечивания кожи и приведшая к отмене терапии.
Гиперчувствительность
Реакции гиперчувствительности включают эритему/покраснение, гипертермию/ лихорадку, раздражительность, тошноту, боль, дрожь/озноб, гипестезию полости рта, головную боль, приливы, признаки и симптомы, соответствующие анафилаксии.
Иммуногенность
Существует потенциальная возможность иммуногенного воздействия. Из 69 пациентов с гипофосфатазией, включенных в клинические исследования и по которым имеются данные в динамике, у 56 (81,2%) пациентов через некоторое время после применения препарата Стрензик было выявлено наличие антител к лекарственному препарату. Среди данных 56 пациентов у 25 (44,6%) также было выявлено наличие нейтрализующих антител. Гуморальный ответ (с наличием или без наличия нейтрализующих антител) по своей природе был переменным по времени. Образование антител не оказывало влияния на клиническую эффективность или безопасность препарата.
Каких-либо тенденций со стороны нежелательных явлений основанных на статусе наличия антител, в клинических исследованиях выявлено не было. Более того, у пациентов с наличием антител после подкожного введения асфотазы альфа не было выявлено проявлений гиперчувствительности или тахифилаксии.
Передозировка
Данные в отношении передозировки асфотазы альфа отсутствуют.
Взаимодействие с другими лекарственными средствами
Исследований взаимодействий с асфотазой альфа не проводилось. Основываясь на структуре и фармакокинетике, влияние асфотазы альфа на метаболизм, связанный с системой цитохрома Р-450, является маловероятным.
Фармацевтическое
Препарат не следует смешивать с другими лекарственными препаратами, так как исследования совместимости не проводились.
Особые указания
Исследований по оценке генотоксического и канцерогенного потенциала асфотазы альфа не проводилось.
Асфотаза альфа содержит каталитический домен тканенеспецифической щелочной фосфатазы. При введении асфотазы альфа определение активности щелочной фосфатазы рутинными лабораторными методами не представляется возможным в связи с многократно завышенными результатами. Активность асфотазы альфа не следует интерпретировать по значениям активности щелочной фосфатазы, поскольку активность щелочной фосфатазы характеризуется различиями ферментных характеристик.
Гиперчувствительность
Сообщалось о реакциях гиперчувствительности, включая признаки и симптомы, согласующиеся с анафилаксией у пациентов, получавших асфотазу альфа. Реакции возникают через несколько минут после подкожного введения препарата и могут возникать у пациентов, получавших лечение более одного года. При возникновении реакции гиперчувствительности, рекомендуется немедленное прекращение лечения, и назначение соответствующей медикаментозной терапии. Следует соблюдать принятые в настоящее время стандарты оказания неотложной помощи.
При необходимости повторного введения препарата пациенту после серьезной реакции гиперчувствительности, врач должен оценить риск и пользу от применения препарата, принимая во внимание другие факторы, которые могут влиять на развитие реакции гиперчувствительности, такие как одновременная инфекция и/или использование антибиотиков. Если принято решение о повторном применении препарата, повторное введение должно производиться под наблюдением врача, и при использовании превентивных мер по предотвращению гиперчувствительности. Пациента и его лечащего врача следует предупредить о возможности повторения признаков и симптомов тяжелой реакции гиперчувствительности. Необходимо наблюдение за последующими введениями препарата и необходимо информировать о мерах экстренного лечения при применении препарата на дому терапией, назначенной лечащим врачом.
Реакция на инъекцию
Применение асфотазы альфа может вызвать развитие локальных реакций со стороны места инъекции (включая, но не ограничиваясь, эритему, сыпь, обесцвечивание, зуд, боль, папулу, узелок, атрофию), которые определены в качестве связанных с терапией нежелательных явлений, возникающих во время проведения инъекции или до конца дня, в который проведена инъекция. Чередование областей проведения инъекций обычно способствует эффективному контролю возникновения данных реакций. Как правило, данные реакции расцениваются в качестве несерьезных, легких или умеренных по степени тяжести и самоограничивающихся.
При возникновении у любого из пациентов тяжелой инъекционной реакции применение препарата Стрензик должно быть прекращено и назначена соответствующая терапия.
Краниосиностоз
В клинических исследованиях асфотазы альфа нежелательные явления краниосиностоза (связанного с повышенным внутричерепным давлением), включая ухудшение уже имеющегося краниосиностоза, было выявлено у пациентов с гипофосфатазией в возрасте <5 лет. Связи между терапией асфотазой альфа и прогрессированием краниосиностоза выявлено не было в связи с недостаточностью данных. Краниосиностоз, в качестве проявления гипофосфатазии, – явление, указанное в опубликованной литературе и возникающее у 61,3% пациентов в возрасте от момента рождения до 5 лет при естественном течении гипофосфатазии с началом в младенческом возрасте при отсутствии лечения. Краниосиностоз может привести к повышенному внутричерепному давлению. Пациентам с гипофосфатазией в возрасте до 5 лет рекомендуется периодическое наблюдение (включая исследование глазного дна на предмет проявлений отека диска зрительного нерва) и незамедлительное вмешательство при повышенном внутричерепном давлении.
Эктопическая кальцификация
У пациентов с гипофосфатазией и клинических исследованиях асфотазы альфа были выявлены отложения солей кальция в области глаз (конъюнктивальные и роговичные), а также нефрокальциноз. Связи между терапией асфотазой альфа и ухудшением эктопической кальцификации выявлено не было в связи с недостаточностью данных. Отложения солей кальция в области глаз (конъюнктивальные и роговичные) и нефрокальциноз указаны в опубликованной литературе в качестве проявлений гипофосфатазии. Нефрокальциноз возникает у 51,6% пациентов в возрасте от момента рождения до 5 лет при естественном течении гипофосфатазии с началом в младенческом возрасте при отсутствии лечения. Пациентам с гипофосфатазией рекомендовано периодическое офтальмологическое обследование и ультразвуковое исследование почек.
Содержание паратгормона и кальция в сыворотке крови
У пациентов с гипофосфатазией при применении асфотазы альфа может увеличиваться концентрация паратгормона в сыворотке крови, особенно на протяжении первых 12 недель терапии. У пациентов, получающих терапию асфотазой альфа, рекомендуется контролировать содержание паратгормона и кальция в сыворотке крови. Может понадобиться дополнительное применение препаратов кальция и перорального витамина D.
Диспропорциональный прирост массы тела
У пациентов может иметь место диспропорциональный прирост массы тела. Рекомендуется диетологический контроль.
Вспомогательные вещества
Данный лекарственный препарат содержит менее I ммоль натрия (23 мг) на флакон.
Особые меры предосторожности при утилизации и прочем обращении
Каждый флакон предназначен исключительно для однократного применения и может быть проколот лишь один раз.
Используемые шприцы должны иметь достаточно малый объем, позволяющий в достаточной степени точно набрать предписанную дозу из флакона.
Не использованный в течение 1 ч препарат следует выбросить.
Влияние на способность управления транспортными средствами и работу с механизмами
Препарат Стрензик не оказывает или оказывает незначительное влияние на способность управления транспортными средствами и работу с механизмами.
Форма выпуска
Раствор для подкожного введения 40 мг/мл, 100 мг/мл.
По 12 мг/0,3 мл; 18 мг/0,45 мл; 28 мг/0,7 мл; 40 мг/1,0 мл в стеклянный флакон гидролитического класса I вместимостью 2 или 3 мл, укупоренный бутил каучуковой пробкой и алюминиевой крышкой с полипропиленовым откидным колпачком.
По 1 или 12 флаконов с инструкцией по применению в пачку картонную.
По 80 мг/0,8 мл в стеклянный флакон гидролитического класса 1 вместимостью 2 или 3 мл, укупоренный бутил каучуковой пробкой и алюминиевой крышкой с полипропиленовым откидным колпачком.
По 1 или 12 флаконов с инструкцией по применению в пачку картонную.
Условия хранения
В защищенном от света месте, при температуре 2-8 °С.
Не замораживать!
Хранить в оригинальной упаковке для защиты от света.
Хранить в недоступном для детей месте.
Срок годности
2 года. Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
Алексион Фарма ГмбХ, Швейцария
Гиссхюбельштрассе 30, СН-8045, Цюрих, Швейцария
Giesshubelstrasse 30, СН-8045 Zurich, Switzerland
Производитель
Производство готовой лекарственной формы и фасовка (первичная упаковка):
Алексион Фарма Интернешнл Оперейшнс Анлимитед Компани. Ирландия
Монксленд Индастриал Эстейт, Атлон, Роскоммон N37 DH79, Ирландия
Monksland Industrial Estate, Athlone, Roscommon N3/ DH79, Ireland
Выпускающий контроль качества:
Алексион Фарма Интернешнл Оперейшнс Анлимитед Компани, Ирландия
Коллеж Бизнес энд Текнолоджи парк, Бланчардстаун Род Норт, Дублин, 15, Ирландия
College Business and Technology Park, Blanchardstown, Dublin 15, Ireland
Получить дополнительную информацию о препарате, а также направить свои претензии и информацию о нежелательных явлениях можно по следующему адресу в России:
ООО «Алексион Фарма»
143421 Московская область. Красногорский район, 26 км автодороги Балтия Бизнес центр Рига Лэнд, Блок Б этаж 2.
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Фармакологическая активность препарата определяется активностью фермента асфотаза альфа.
Гипофосфатазия — редкое тяжелое потенциально смертельное наследственное заболевание, причиной которого является одна или несколько мутаций с утратой функции гена, кодирующего неспецифический тканевой изофермент щелочной фосфатазы. Для гипофосфатазии характерен широкий спектр проявлений в костной ткани, в том числе рахит/остеомаляция, изменение метаболизма кальция и фосфата, нарушение роста и подвижности, дыхательная недостаточность, требующая искусственной вентиляции легких, а также витамин В6-зависимые судороги.
Асфотаза альфа применяется как патогенетическое лечение гипофосфатазии в качестве длительной заместительной ферментной терапии Устранение дефицита активности щелочной фосфатазы за счет замещения дефектного фермента предотвращает нарушения минерализации скелета и способствует восстановлению этого процесса.
Было продемонстрировано, что по сравнению с исходными значениями, лечение асфотазой альфа приводит к положительным изменениям у пациентов по таким признакам как уровни биохимических субстратов тканенеспецифической щелочной фосфатазы (неорганического пирофосфата и пиридоксаль-5′-фосфата), минерализация костной ткани, структура костей, рост, мышечная сила, физическая функция, способность передвигаться и инвалидность.
Клиническая эффективность и безопасность
Исследование ENB-006-09/ENB-008-10
Исследование ENB-006-09/ENB-008-10 было открытым и рандомизированным, в котором участвовали 13 пациентов. К моменту завершения исследования медиана длительности лечения пациентов превышала 76 месяцев (6,3 лет; от 1 до 79 месяцев). У 5 исследуемых пациентов симптомы гипофосфатазии были впервые выявлены в возрасте до 6 месяцев, а у 8 — после 6 месяцев. Возраст на момент включения в исследование составлял от 6 до 12 лет, по завершении исследования — от 10 до 18 лет; 9 пациентам к моменту окончания исследования исполнилось от 13 до 17 лет.
Действие асфотазы альфа на результаты рентгеновского исследования
Выявленные отклонения рентгенограммы от исходных значений оценивали с применением шкалы общей оценки рентгенографических изменений, по следующим баллам: -3 = тяжелое ухудшение, -2 = умеренное ухудшение, -1 = минимальное ухудшение, 0 = без изменений, +1 = минимальное излечение, +2 = значительное излечение, +3 = (практически) полное излечение. Большинство пациентов, получавших асфотазу альфа, в течение первых 6 месяцев лечения достигли баллов +2 и +3, и в ходе последующего лечения эти значения оставались стабильными. Значения у исторических контрольных пациентов с течением времени не изменялись.
Биопсия костной ткани
Перед взятием биоптата костной ткани пациентам вводили тетрациклин в качестве метки для костной ткани в виде двух 3-дневных курсов (с интервалом в 14 дней). Биоптат костной ткани из подвздошного гребня получали с применением стандартной методики. У 10 пациентов в популяции согласно протоколу (за исключением пациентов, получавших перорально витамин D от исходной временной точки до недели 24), прошедших биопсию из подвздошного гребня до и после введения асфотазы альфа:
- среднее (SD) значение толщины остеоида составило 12,8 (3,5) мкм в исходной временной точке и 9,5 (5,1) мкм к неделе 24;
- среднее (SD) значение отношения объема остеоида / объема костной ткани составило 11,8 (5,9) % в исходной временной точке и 8,6 (7,2) % к неделе 24;
- среднее (SD) значение времени задержки минерализации составило 93 (70) дней в исходной временной точке и 119 (225) дней к неделе 24.
Рост
Из пациентов, получавших асфотазу альфа, у 11 из 13 наблюдали устойчивое и явное догоняющее увеличение темпов роста, у 1 из 13 не наблюдали явного догоняющего увеличения темпов роста, а у 1 пациента не было собрано достаточно данных для определенного заключения.
За временной период наблюдения исторических контрольных пациентов у 1 из 16 наблюдали явное догоняющее увеличение роста, у 12 из 16 не наблюдали явного догоняющего увеличения роста, а данные 3 из 16 пациентов не позволяли сделать окончательного вывода.
Некоторым пациентам в ходе исследования требовался витамин D для приема внутрь.
Исследование ENB-002-08/ENB-003-08
Исследование ENB-002-08/EN В-003-08 было открытым, нерандомизированным и неконтролируемым. В исходном исследовании участвовали 11 пациентов; 10 были включены в дополнительное исследование, 9 из них завершили дополнительное исследование. К моменту завершения исследования медиана длительности лечения пациентов превышала 79 месяцев (6,6 лет; от 1 до > 84 месяцев). Гипофосфатазия у всех пациентов началась в возрасте до 6 месяцев. Возраст начала лечения в исследовании — от 0,5 месяцев до 35 месяцев.
При полном анализе данных у 7 из 11 пациентов изменение балла по шкале общей оценки рентгенографических изменений составило +2 на неделе 24 в сравнении с исходными рентгенограммами. Снижение тяжести рахита (по шкале общей оценки рентгенографических изменений) сохранялось в течение, как минимум, 72 месяцев последующего лечения (в том числе, как минимум, 84 месяцев у 4 пациентов).
У 5 из 11 пациентов отмечали явное догоняющее увеличение темпов роста. На момент последней оценки (n = 10, 9 получали лечение, как минимум, в течение 72 месяцев) медианные улучшения Z-оценки относительно исходного значения составили 1,93 для роста и 2,43 для массы тела. Отмечались колебания в увеличении темпов роста пациентов, что может указывать на более высокую тяжесть заболевания и более высокую степень нарушений у этих пациентов в младшем возрасте.
Исследование ENB-010-10
Исследование ENB-010-10 было открытым и контролируемым; в нем участвовали 69 пациентов возрастом от 1 дня до 72 месяцев с перинатальной/инфантильной гипофосфатазией. Средний возраст на момент появления симптомов заболевания: 1,49 месяца. Пациенты получали препарат Стрензик® в дозе 6 мг/кг в неделю в течение первых 4 недель. Начальная доза асфотазы альфа у всех пациентов, участвовавших в исследовании, составила 6 мг/кг в неделю. Дозу асфотазы альфа увеличивали в ходе исследования у 11 пациентов. У 9 из этих 11 пациентов дозы увеличивали непосредственно для улучшения клинического ответа. Тридцать восемь пациентов получали лечение, как минимум, в течение 2 лет (24 месяцев), а 6 — как минимум, в течение 5 лет (60 месяцев).
При полном анализе данных у 50 из 69 пациентов (72,5 %) балл по шкале общей оценки рентгенографических изменений составил ≥2 к неделе 48, и пациенты были признаны ответившими на лечение. Улучшения медианы балла шкалы общей оценки рентгенографических изменений сохранялись в ходе всего курса лечения (от 0,9 до 302,3 недель), даже с учетом того, что после недели 96 наблюдение вели уже за меньшим количеством пациентов (после недели 96 всего наблюдали 29 пациентов, а после недели 192 уже наблюдали не более 8 пациентов).
У 24 из 69 пациентов (35 %) отмечали явное догоняющее увеличение темпов роста, а у 32 из 69 пациентов (46 %) отмечали явный догоняющий набор массы тела, что подтверждалось перемещением в более высокий перцентиль графиков роста с течением времени. У 40 из 69 пациентов не отмечали явного догоняющего увеличения темпов роста, а у 32 из 69 — явного догоняющего набора массы тела. У 4 пациентов было получено недостаточно данных для однозначного заключения о результатах лечения, а еще у 1 пациента данные невозможно было оценить с определенностью.
Исследование ENB-009-10
Исследование ENB-009-10 было открытым и рандомизированным. Всего участвовало девятнадцать пациентов, 14 из которых завершили исследование, а 5 выбыли. К моменту завершения исследования медиана длительности лечения пациентов превышала 60 месяцев (от 24 до 68 месяцев). Начало гипофосфатазии было отмечено в возрасте до 6 месяцев у 4 пациентов, в возрасте от 6 месяцев до 17 лет — у 14 пациентов, и в возрасте старше 18 лет — у одного пациента. Возраст пациентов на момент включения в исследование составлял от 13 до 66 лет; к моменту завершения исследования — от 17 до 72 лет.
У пациентов подросткового (и взрослого) возраста в этом исследовании не было отмечено явного прибавления роста.
Примерно через 48 недель всех пациентов перевели на рекомендуемую дозу 1,0 мг/кг/сут.
Искусственная вентиляция легких
В исследованиях ENB-002-08/ENB-003-08 (11 пациентов) и ENB-010-10 (69 пациентов) (оба исследования открытые, нерандомизированное и неконтролируемые) участвовали пациенты возрастом от 0,1 до 312 недель в исходный момент времени. 69 пациентов завершили исследования, а 11 — выбыли. Медиана длительности лечения пациентов составила 27,6 месяцев (от 1 дня до 90 месяцев).
В исходной временной точке 29 из 80 пациентов нуждались в ИВЛ:
- 16 пациентам в исходной временной точке требовалась инвазивная ИВЛ (интубация/трахеостомия; один из пациентов перед переводом на инвазивную ИВЛ кратковременно получал неинвазивную ИВЛ):
- 7 пациентов были переведены с инвазивной ИВЛ (длительность ИВЛ — от 12 до 168 недель), 4 пациента — на режим спонтанного дыхания, а 3 пациента — на неинвазивную ИВЛ. Балл шкалы общей оценки рентгенографических изменений у пяти из 7 пациентов достиг ≥2;
- 5 пациентов продолжали находиться на инвазивной ИВЛ, у 4 из них балл по шкале общей оценки рентгенографических изменений составил < 2;
- 3 пациента умерли, будучи на ИВЛ;
- 1 пациент отозвал согласие на участие.
- 13 пациентам в исходной временной точке требовалась неинвазивная ИВЛ:
- 10 пациентов были переведены с ИВЛ на режим спонтанного дыхания (длительность ИВЛ — от 3 до 216 недель). У 9 из 10 пациентов балл по шкале общей оценки рентгенографических изменений достиг ≥2, и только у 1 пациента балл оставался < 2.
- 2 пациентам потребовалась инвазивная ИВЛ, 1 продолжал получать неинвазивную ИВЛ; все 3 пациента умерли, балл по шкале общей оценки рентгенографических изменений на момент смерти составил < 2.
При естественном течении заболевания и отсутствии лечения у пациентов раннего возраста можно предположить высокую смертность среди пациентов, требующих проведения ИВЛ.
МНН: Асфотаза альфа
Производитель: Patheon Italia S.p.A.
Анатомо-терапевтическо-химическая классификация: Асфотаза альфа
Номер регистрации в РК:
№ РК-ЛС-5№026303
Информация о регистрации в РК:
16.10.2024 — 16.10.2029
- русский
- қазақша
- Скачать инструкцию медикамента
Торговое наименование
Стрензик
Международное непатентованное название
Асфотаза
альфа
Лекарственная
форма, дозировка
Раствор
для подкожного введения, 40 мг/мл, 100 мг/мл
Фармакотерапевтическая группа
Пищеварительный
тракт и обмен веществ. Препараты для лечения заболеваний
пищеварительного тракта и нарушения обмена веществ и другие.
Ферментные препараты. Асфотаза альфа.
Код
АТХ: A16AB13
Показания к применению
Препарат
Стрензик показан для длительной заместительной ферментной терапии у
пациентов с гипофосфатазией, с началом в детском возрасте, с целью
купирования проявлений заболевания со стороны костей.
Перечень
сведений, необходимых до начала применения
Противопоказания
—
тяжелая или опасная для жизни гиперчувствительность к действующему
веществу или к любому из вспомогательных веществ, в случае если
гиперчувствительность не поддается контролю.
Меры
предосторожности при использовании
Препарат
Стрензик применяют только по назначению врача. Сообщите
своему врачу до или во время лечения препаратом о следующих
ситуациях:
—
недавний
прием, прием в настоящее время или планируемый прием любых других
лекарственных препаратов, а также необходимость
в прохождении лабораторных исследований (кровь на анализ). Препарат
Стрензик может привести к тому, что некоторые тесты будут показывать
ошибочно более высокие или более низкие результаты. Поэтому,
возможно, потребуется использовать другой тип теста в случае приема
препарата Стрензик.
—
наличие сильной аллергии на асфотазу альфа или какой-либо другой
ингредиент этого лекарственного препарата.
—
наличие аллергических реакций, в том числе опасных для жизни,
требующих медикаментозного лечения, аналогичного анафилаксии.
Пациенты, у которых наблюдались симптомы, похожие на анафилаксию,
испытывали затруднение дыхания, ощущение удушья, тошноту, отеки
вокруг глаз и головокружение. Реакции на прием асфотазы альфа могут
возникать в течение нескольких минут после приема и даже у пациентов,
принимающих асфотазу альфа более одного года. В случае развития
каких-либо из перечисленных симптомов следует прекратить прием
препарата Стрензик и немедленно обратиться за медицинской помощью.
—
в случае возникновения анафилактической реакции или явлений с
подобными симптомами врачу следует обсудить с пациентом следующие
шаги и возможность возобновления приема Стрензик под медицинским
наблюдением. Необходимо всегда следовать инструкциям лечащего врача.
—
во время лечения препаратом Стрензик может возникнуть выработка
белков крови против вводимого препарата, также называемых
антилекарственными антителами. Следует сообщить лечащему врачу, в
случае замеченного снижения эффективности препарата Стрензик.
—
если после приема препарата Стрензик, в местах инъекций, через
несколько месяцев наблюдались жировые комки или уменьшение жировой
ткани на поверхности кожи (локализованная липодистрофия). Следует
внимательно ознакомиться с информаций, отмеченной в разделе «Способ
применения» данной инструкции, для правильного выполнения
инъекции. Чтобы снизить риск развития липодистрофии, важно чередовать
инъекции в следующих областях: область живота, бедер или дельтовидная
мышца.
—
в случае развития нарушения зрения. Сообщалось о некоторых
нежелательных явлениях, связанных с нарушением зрения (например,
накопление кальция в глазах (кальцификация конъюнктивы и роговицы)),
как у пациентов, принимавших препарат Стрензик, так и у тех, кто не
принимал данный препарат, вероятно это связано с течением заболевания
(гипофосфатазией).
—
изменение формы головы ребенка, принимающего данный препарат
(сообщалось о раннем сращении костей головы (краниосиностоз) у детей
в возрасте до 5 лет у детей с гипофосфатазией, как у пациентов,
принимавших препарат Стрензик, так и у тех, кто не принимал данный
препарат, вероятно это связано с течением заболевания
(гипофосфатазией).
—
если во время введения препарата или в течение нескольких часов после
инъекции возникла реакция в месте инъекции (боль, узелки, сыпь,
изменение цвета), следует немедленно сообщить лечащему врачу.
—
если наблюдается повышение концентрации паратиреоидного гормона в
крови и, как следствие, низкий уровень кальция, в случае
необходимости, дополнительный прием витамина D перорально может быть
назначен лечащим врачом.
—
увеличение массы тела при применении препарата Стрензик. При
необходимости дополнительные рекомендации по питанию могут быть
предоставлены лечащим врачом.
Взаимодействия
с другими лекарственными препаратами
Основываясь
на структуре и фармакокинетике, влияние асфотазы
альфа на метаболизм, связанный с системой цитохрома Р-450, является
маловероятным.
Асфотаза
альфа содержит каталитический домен тканевой неспецифической щелочной
фосфатазы. Введение асфотазы альфа влияет на результаты рутинного
измерения уровней щелочной фосфатазы (ЩФ) в сыворотке крови, что
может привести к измерению показателей активности ЩФ в сыворотке в
несколько тысяч единиц на литр. Результаты активности асфотазы альфа
не следует интерпретировать как тот же показатель, что и активность
ЩФ сыворотки, из-за различий в характеристиках ферментов.
Щелочная
фосфатаза (ЩФ) используется в качестве реагента во многих рутинных
лабораторных анализах. Если асфотаза альфа присутствует в клинических
лабораторных образцах, могут быть зарегистрированы аберрантные
значения.
Лечащий
врач должен проинформировать лабораторию о том, что пациент принимает
лекарственные препараты, влияющие на уровень ЩФ. У пациентов,
получающих препарат Стрензик могут быть рассмотрены альтернативные
методы анализа (т. е. без использования репортерной системы,
конъюгированной с ЩФ).
Препарат
не следует смешивать с другими лекарственными препаратами, так как
данных по совместимости недостаточно.
Специальные
предупреждения
Прослеживаемость
В
целях улучшения мер по прослеживаемости биологических лекарственных
препаратов название и номер серии вводимого препарата должны быть
четко зафиксированы.
Гиперчувствительность
Сообщалось
о реакциях гиперчувствительности у пациентов, получавших терапию
асфотазой альфа, включая симптомы, свойственные анафилаксии. К таким
симптомам относились
затрудненное дыхание, ощущение удушья, отеки вокруг глаз и
головокружение. Реакции могут возникать в течение нескольких минут
после подкожного введения асфотазы альфа и могут возникать у
пациентов, находящихся на лечении более одного года. Другие реакции
гиперчувствительности включали рвоту, тошноту, лихорадку, головную
боль, приливы, раздражительность, озноб, эритему кожи, сыпь, зуд и
гипестезию полости рта. При возникновении
реакции гиперчувствительности рекомендуется немедленное прекращение
лечения, и назначение соответствующей медикаментозной терапии.
Следует соблюдать принятые в настоящее время стандарты оказания
неотложной помощи.
При
необходимости повторного введения препарата пациенту после серьезной
реакции гиперчувствительности, врач должен оценить риск и пользу от
применения препарата, принимая во внимание другие факторы, которые
могут влиять на развитие реакции гиперчувствительности, такие как
сопутствующая инфекция и/или применение антибиотиков. Если принято
решение о повторном применении препарата, повторное введение должно
производиться под наблюдением врача, и при использовании превентивных
мер по предотвращению развития реакций гиперчувствительности. За
пациентом необходимо наблюдение за развитием повторного появления
симптомов тяжелой реакции гиперчувствительности. Решение о
необходимости наблюдения при последующих введениях препарата и о
необходимости оказания неотложной помощи на дому принимает лечащий
врач.
Повторное
назначение асфотазы альфа противопоказано при наличии тяжелых или
потенциально жизнеугрожающих неконтролируемых реакций
гиперчувствительности.
Реакции
в месте введения
При
введении асфотазы альфа могут возникать реакции в месте введения (в
том числе, эритема, сыпь, изменение цвета кожи, зуд, болевые
ощущения, папулезные и узелковые высыпания, атрофия); под этим
термином понимают любые нежелательные реакции, имеющие отношение к
инъекции и возникающие во время инъекции или до окончания дня, во
время которого была проведена инъекция препарата. Для снижения
частоты данных реакций следует чередовать места инъекции.
При
возникновении у любого из пациентов тяжелой инъекционной реакции
применение препарата Стрензик должно быть прекращено и назначена
соответствующая терапия.
Липодистрофия
Были
отмечены случаи локализованной липодистрофии, в том числе липоатрофии
и липогипертрофии, в местах введения спустя несколько месяцев после
начала терапии препаратом Стрензик. Пациентам рекомендуется строго
следовать технике правильного выполнения инъекций и чередовать места
введения.
Краниосиностоз
Краниосиностоз
(связанный с повышением внутричерепного давления), в том числе
ухудшение уже существующего краниосиностоза и возникновение
мальформации Арнольда-Киари, регистрировался как нежелательное
явление при гипофосфатазии у пациентов в возрасте младше 5 лет на
фоне применения препарата Стрензик. Причинно-следственная связь между
фармакологическим действием препарата Стрензик и прогрессированием
краниосиностоза не установлена. Краниосиностоз как проявление
гипофосфатазии был также отмечен у пациентов с инфантильной
гипофосфатазией в возрасте младше 5 лет, не получавших лечения.
Краниосиностоз
может привести к повышенному внутричерепному давлению. Пациентам с
гипофосфатазией в возрасте до 5 лет рекомендуется периодическое
наблюдение (включая исследование глазного дна на выявление проявлений
отека диска зрительного нерва) и незамедлительное вмешательство при
повышенном внутричерепном давлении.
Эктопическая
кальцификация
У
пациентов с гипофосфатазией отмечали кальцификацию тканей глаза
(конъюнктивы и роговицы) и нефрокальциноз. Имеется недостаточно
данных, на основании которых можно было бы установить
причинно-следственную связь между влиянием препарата Стрензик и
эктопической кальцификацией. Кальцификация тканей глаза (конъюнктивы
и роговицы) и нефрокальциноз является проявлением гипофосфатазии.
Нефрокальциноз был отмечен пациентов с инфантильной гипофосфатазией
в возрасте до 5 лет, не получавших лечения. Пациентам с
гипофосфатазией рекомендовано периодическое офтальмологическое
обследование и ультразвуковое исследование почек.
Концентрация
паратгормона и кальция в плазме крови
У
пациентов с гипофосфатазией при применении асфотазы альфа может
увеличиваться концентрация паратиреоидного гормона в плазме крови,
особенно на протяжении первых 12 недель лечения препаратом Стрензик.
У пациентов, получающих терапию асфотазой альфа, рекомендуется
контролировать концентрацию паратиреоидного гормона и кальция в
плазме крови. Может понадобиться дополнительное применение препаратов
кальция и перорального витамина D.
Непропорциональный
прирост массы тела
У
пациентов может иметь место непропорциональный прирост массы тела.
Рекомендуется назначение индивидуальной диеты.
Вспомогательные
вещества
Данный
лекарственный препарат содержит менее 1 ммоль натрия (23 мг) на
флакон.
Применение
в период беременности и лактации
Беременность
Данных
о применении асфотазы альфа у беременных женщин недостаточно.
Применение асфотазы альфа не рекомендуется во время беременности, а
также женщинам репродуктивного возраста, не использующим эффективные
средства контрацепции.
Кормление
грудью
Данных
о проникновении асфотазы альфа в грудное молоко человека
недостаточно. Не может быть исключен риск для новорожденного/ребенка,
находящегося на грудном вскармливании. Следует принять решение либо о
прекращении грудного вскармливания, либо о прекращении терапии
асфотазой альфа с учетом пользы грудного вскармливания для ребенка и
необходимости терапии для женщины.
Фертильность
Данных
о влиянии препарата на фертильность, развитие эмбриона и плода
недостаточно.
Особенности
влияния лекарственного средства на способность управлять транспортным
средством или потенциально опасными механизмами
Лекарственный
препарат Стрензик не оказывает влияния или оказывает незначительное
влияние на способность управлять автомобилем и работать с
механизмами.
Рекомендации
по применению
Режим
дозирования
Рекомендованный
режим дозирования препарата – 2 мг/кг массы тела асфотазы альфа
подкожно три раза в неделю, либо 1 мг/кг массы тела асфотазы альфа 6
раз в неделю.
Максимальная
рекомендованная доза асфотазы альфа составляет 6 мг/кг массы тела в
неделю.
Более подробная информация по дозированию представлена в
таблице ниже.
|
Масса тела (кг) |
При введении 3 раза в неделю |
При введении 6 раз в неделю |
||||
|
Вводимая |
Вводимый |
Объем |
Вводимая |
Вводимый |
Объем |
|
|
3 |
6 мг |
0.15 мл |
0.7 мл |
|||
|
4 |
8 мг |
0.20 мл |
0.7 мл |
|||
|
5 |
10 мг |
0.25 мл |
0.7 мл |
|||
|
6 |
12 мг |
0.30 мл |
0.7 мл |
6 мг |
0.15 мл |
0.7 мл |
|
7 |
14 мг |
0.35 мл |
0.7 мл |
7 мг |
0.18 мл |
0.7 мл |
|
8 |
16 мг |
0.40 мл |
0.7 мл |
8 мг |
0.20 мл |
0.7 мл |
|
9 |
18 мг |
0.45 мл |
0.7 мл |
9 мг |
0.23 мл |
0.7 мл |
|
10 |
20 мг |
0.50 мл |
0.7 мл |
10 мг |
0.25 мл |
0.7 мл |
|
11 |
22 мг |
0.55 мл |
0.7 мл |
11 мг |
0.28 мл |
0.7 мл |
|
12 |
24 мг |
0.60 мл |
0.7 мл |
12 мг |
0.30 мл |
0.7 мл |
|
13 |
26 мг |
0.65 мл |
0.7 мл |
13 мг |
0.33 мл |
0.7 мл |
|
14 |
28 мг |
0.70 мл |
0.7 мл |
14 мг |
0.35 мл |
0.7 мл |
|
15 |
30 мг |
0.75 мл |
1.0 мл |
15 мг |
0.38 мл |
0.7 мл |
|
16 |
32 мг |
0.80 мл |
1.0 мл |
16 мг |
0.40 мл |
0.7 мл |
|
17 |
34 мг |
0.85 мл |
1.0 мл |
17 мг |
0.43 мл |
0.7 мл |
|
18 |
36 мг |
0.90 мл |
1.0 мл |
18 мг |
0.45 мл |
0.7 мл |
|
19 |
38 мг |
0.95 мл |
1.0 мл |
19 мг |
0.48 мл |
0.7 мл |
|
20 |
40 мг |
1.00 мл |
1.0 мл |
20 мг |
0.50 мл |
0.7 мл |
|
25 |
50 мг |
0.50 мл |
0.8 мл |
25 мг |
0.63 мл |
0.7 мл |
|
30 |
60 мг |
0.60 мл |
0.8 мл |
30 мг |
0.75 мл |
1.0 мл |
|
35 |
70 мг |
0.70 мл |
0.8 мл |
35 мг |
0.88 мл |
1.0 мл |
|
40 |
80 мг |
0.80 мл |
0.8 мл |
40 мг |
1.00 мл |
1.0 мл |
|
50 |
50 мг |
0.50 мл |
0.8 мл |
|||
|
60 |
60 мг |
0.60 мл |
0.8 мл |
|||
|
70 |
70 мг |
0.70 мл |
0.8 мл |
|||
|
80 |
80 мг |
0.8 мл |
0.8 мл |
|||
|
90 |
90 мг |
0.90 мл |
0.8 мл (x2) |
|||
|
100 |
100 мг |
1.0 мл |
0.8 мл (x2) |
Особые
группы пациентов
Взрослые
пациенты
Коррекция
дозы для взрослых пациентов с детской гипофосфатазией (ГФ) не
требуется.
Пациенты
пожилого возраста
Безопасность и эффективность асфотазы альфа у пациентов
пожилого возраста не установлены, конкретных рекомендаций по режиму
дозирования препарата для таких пациентов нет.
Почечная
недостаточность
Безопасность
и эффективность асфотазы альфа у пациентов с почечной
недостаточностью не изучались, конкретных рекомендаций по режиму
дозирования препарата для таких пациентов нет.
Печеночная
недостаточность
Безопасность
и эффективность асфотазы альфа у пациентов с нарушением функции
печени не изучались, конкретных рекомендаций по режиму дозирования
препарата для таких пациентов нет.
Способ
применения
Препарат
Стрензик предназначен только для подкожного введения. Препарат не
предназначен для внутривенного или внутримышечного введения.
Максимальный объем лекарственного препарата на одну
инъекцию не должен превышать 1 мл. При необходимости введения более 1
мл допускается проведение нескольких инъекций
в одно и то же время в разные места введения
(бедра, живот, руки (дельтовидные мышцы), ягодицы).
Препарат
Стрензик следует вводить с помощью стерильных одноразовых шприцев и
инъекционных игл. Используемые шприцы должны иметь достаточно малый
объем, позволяющий в достаточной степени точно набрать
рекомендованную дозу препарата из флакона.
Места
инъекций следует менять и тщательно контролировать на наличие
признаков потенциальных реакций.
Пациенты
могут делать инъекции самостоятельно только в том случае, если они
должным образом обучены процедурам введения.
Каждый
флакон предназначен только для однократного использования и его
следует прокалывать только один раз. Любой неиспользованный раствор
во флаконе следует утилизировать.
Подготовка
и проведение инъекции.
Подготовка и проведение инъекции должны проходить с
соблюдение правил асептики.
Необходимо
тщательно вымыть руки водой с мылом.
Рекомендуется
извлечь неоткрытые флаконы с препаратом Стрензик из холодильника за
15-30 минут до введения, чтобы раствор достиг комнатной температуры.
Не следует нагревать препарат любым другим способом (например, в
микроволновой печи или в горячей воде). После извлечения флакона из
холодильника препарат Стрензик следует использовать в течение
максимум 3 часов.
Снимите
защитный колпачок с флакона. Снимите защитный колпачок со шприца,
который планируется к использованию.
Следует
всегда использовать новый шприц в защитной пластиковой упаковке.
Установите
ширококанальную иглу (например, 25G) с защитным пластиковым
колпачком на пустой шприц и надавите на иглу поворачивая ее по
часовой стрелке до упора.
Снимите
пластиковый колпачок с иглы шприца. Следует соблюдать осторожность
чтобы не допустить ранения иглой.
Потяните
за поршень, чтобы набрать в шприц воздух в объеме, эквивалентном
необходимой дозе препарата.
Извлечение
раствора препарата из флакона
|
1. Удерживая
2. Теперь |
|
|
3. Переверните |
|
|
4. Перед тем, как
5. Когда все |
|
|
6. После удаления |
Установка
иглы для инъекций на шприц
1. Извлеките иглу из флакона и наденьте на нее защитный
колпачок.
2. Снимите иглу большего диаметра, нажимая и поворачивая
против часовой стрелки. Утилизируйте иглу с защитным колпачком в
контейнере для острых предметов.
3. Установите иглу меньшего диаметра (например, 27 или
29G) с защитным колпачком на заполненный шприц и поверните иглу по
часовой стрелке на шприце до упора. Снимите колпачок с иглы.
4. Держите шприц иглой вверх и постучите пальцем по
цилиндру шприца, чтобы удалить пузырьки воздуха.
Следует проверить правильность объема, содержащегося в
наполненном шприце.
Объем одной инъекции не должен превышать 1 мл. В случае
необходимости введения более 1 мл, следует сделать несколько инъекций
в разные участки тела.
Проведение
инъекции препарата Стрензик
|
Выберите Не |
|
|
Аккуратно |
|
|
Держа |
|
|
Продолжая |
|
|
Извлеките |
|
|
Если необходима |
Меры, которые необходимо
принять в случае передозировки
В
случае подозрения случайного введения более высокой следует
обратиться к лечащему врачу.
Меры,
которые необходимо принять в случае пропуска дозы
Если
доза асфотазы альфа пропущена, не следует вводить двойную дозу, чтобы
компенсировать пропущенную дозу.
Рекомендуется
обратиться за консультацией к медицинскому работнику для разъяснения
способа применения лекарственного препарата.
В
случае возникновения каких-либо вопросов относительно способа
применения лекарственного препарата Стрензик пациенту рекомендуется
обратиться за консультацией к медицинскому работнику для объяснения
способа применения этого лекарственного средства.
Описание нежелательных реакций,
которые проявляются при стандартном применении лекарственного
препарата и меры, которые следует принять в этом случае
Нежелательные реакции классифицированы по частоте
развития. Категории частоты определяются в соответствии со следующими
условными обозначениями: очень часто
(≥ 1/10), часто (≥
1/100 до <1/10), нечасто
(≥1/1000 до <1/100), редко
(≥1/10000 до <1/1000), очень редко
(<1/10000), неизвестно
(исходя из известных данных, не может быть оценена).
Очень часто (≥ 1/10):
— головная
боль
— эритема
—
боль в конечности
—
реакции в месте инъекции (включая атрофию, абсцесс, эритему,
изменение цвета, боль, зуд, пятно, отек, ушиб, синяк, липодистрофию
(липоатрофию или липогипертрофию), уплотнение, реакцию, узелки, сыпь,
папулы, гематомы, воспаление, крапивницу, кальцификация, повышение
температуры, кровотечение, целлюлит, рубцы, новообразования,
экстравазация, шелушение и везикулы), повышение температуры тела,
раздражительность
—
гематомы
Часто (≥1/100 до <1/10):
— целлюлит в месте инъекции
— повышенная склонность к образованию гематом
— анафилактоидные реакции, гиперчувствительность (в том
числе эритема/покраснение, лихорадка/лихорадка, сыпь, зуд,
раздражительность, тошнота, рвота, боль, озноб/озноб, гипестезия во
рту, головная боль, приливы, тахикардия, кашель, а также признаки и
симптомы, соответствующие анафилаксии )
— гипокальциемия
— прилив
— гипестезия во рту, тошнота
— изменение цвета кожи, кожные заболевания (растянутая
кожа)
— миалгия
— мочекаменная болезнь
— бугристость кожи
— формирование шрамов/рубцов
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов.
РГП
на ПХВ «Национальный Центр экспертизы лекарственных средств и
медицинских изделий» Комитета медицинского и фармацевтического
контроля Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав лекарственного препарата
Один
мл раствора содержит
активное
вещество:
асфотаза альфа*, 40 мг или 100 мг
*
асфотаза альфа, полученная методом рекомбинантной ДНК с
использованием культуры клеток яичника китайского хомячка (CHO).
вспомогательные
вещества:
натрия хлорид, динатрия
гидрофосфат гептагидрат, натрия дигидрофосфат
моногидрат, вода для
инъекций.
Описание
внешнего вида, запаха, вкуса
Прозрачный,
слегка опалесцирующий или опалесцирующий раствор от бесцветного до
желтоватого цвета. Возможно наличие нескольких небольших
полупрозрачных или белых частиц.
Форма выпуска и упаковка
По
28 мг/0.7 мл, 40 мг/1.0 мл (для дозировки 40 мг/мл) или по 80 мг/ 0.8
мл (для дозировки 100 мг/мл) в стеклянный флакон тип I, укупоренный
бутилкаучуковой пробкой, обжатой сверху алюминиевым колпачком с
полипропиленовой крышкой («флип-офф»).
По
12 флаконов вместе с инструкцией по медицинскому применению на
казахском и русском языках помещают в коробку картонную с контролем
первого вскрытия.
Срок хранения
30 месяцев
Препарат
сохраняет химическую и физическую стабильность при использовании до
3 часов при температуре от 23 до 27 °C.
Не
применять по истечении срока годности.
Условия хранения
Хранить в
оригинальной упаковке в защищенном от света месте, при температуре
2-8 °С.
Не
замораживать!
Хранить в недоступном для детей месте!
Условия отпуска из аптек
По
рецепту
Сведения
о
производителе
1.
Alexion Pharma International Operations Limited
Monksland Industrial Estate, Athlone,
Co. Roscommon N37 DH79, Ирландия
Tel.: +353
(0) 1 254 6400
2.
Patheon Italia S.p.A
Viale
G.B. Stucchi, 110, 20900 Monza, Италия
Держатель
регистрационного удостоверения
Alexion
Europe
SAS
103-105
rue Anatole France, 92300 Levallois-Perret, Франция
Тел.: +33
(0)1 47 32 36 03
Адрес
электронной почты: adverse.events.kz@astrazeneca.com
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории Республики Казахстан, принимающей претензии
(предложения) по качеству лекарственных средств от потребителей и
ответственной за пострегистрационное
наблюдение за безопасностью лекарственного средства
Представительство
ЗАК “АстраЗенека Ю-Кей Лимитед”,
Республика
Казахстан, г. Алматы, 050000
ул.
Кунаева, д. 77, офис 101
Телефон:
+7 727 232 14 15; +7 701 0326745
e—mail:
adverse.events.kz@astrazeneca.com
или
по ссылке https://contactazmedical.astrazeneca.com
| 26._Strensiq_KZ_PIL_clean_for_subm_16July2024_rus_2_.docx | 0.37 кб |
| 27._Strensiq_KZ_PIL_clean_for_subm_16July2024_kaz_2(1)_.docx | 0.36 кб |
Отправить прикрепленные файлы на почту
СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12
от 14850.00 ₽
в наличии в 3 аптеках
Бесплатный самовывоз в Москве
Оплата наличными или картой при получении в аптеке
Формы выпуска
РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ
Характеристики
- Категория
Лекарства
- Действующее вещество (МНН)
АСФОТАЗА АЛЬФА
- Форма выпуска РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ
- Дозировка и размер 100 МГ/МЛ
- Производитель ALEXION PHARMA INTERNATIONAL SARL
- Страна производитель Ирландия
- Рецептурный препарат Да
Наличие СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12 и цены в аптеках Москвы
Инструкция по применению СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12
Показания к применению
Препарат Стрензик показан для длительной заместительной ферментной терапии пациентов с гипофосфатазией с началом в детском возрасте с целью купирования проявлений заболевания со стороны костей.
Противопоказания
Гиперчувствительность к действующему веществу (асфотазе альфа) или любому из вспомогательных веществ (компонентам препарата).
Побочные действия
В качестве наиболее часто наблюдаемых нежелательных явлений выступали местные нежелательные реакции, связанные с введением препарата. Большинство этих реакций были несерьезными и легкими или умеренными по степени тяжести. Серьезные нежелательные явления, связанные с инъекцией, были выявлены у 2 пациентов и не привели к прекращению терапии асфотазой альфа: у одного пациента с гипофосфатазией с началом в младенческом возрасте развились лихорадка и озноб, а у другого пациента с гипофосфатазией с началом в детском возрасте — гипестезия полости рта, боль в конечности, озноб и головная боль.
Ниже представлены данные о нежелательных реакциях при применении асфотазы альфа, наблюдавшиеся в рамках клинических исследований у 71 пациента (в возрасте от 1 дня до 66 лет), в соответствии с поражением органов и систем органов (MedDRA) и классификацией ВОЗ по частоте встречаемости: «очень часто» (? 1/10), «часто» (? 1/100 — < 1/10), «нечасто» (? 1/1,000 — < 1/100), «редко» (? 1/10000 — < 1/1000), «очень редко» (< 1/10000) и «частота неизвестна» (частота не может быть определена, основываясь на доступных данных). В пределах каждой группы частоты нежелательные реакции указаны в порядке убывания серьезности.
Таблица 1 Нежелательные реакции, выявленные в клинических исследованиях у пациентов с гипофосфатазией (в возрасте от 1 дня до 66 лет)
|
Класс по поражению органов и систем органов |
Категория частоты |
Нежелательная реакция |
|
Инфекционные и паразитарные заболевания |
Часто |
Постинъекционный целлюлит |
|
Гематологические нарушения и нарушения со стороны лимфатической системы |
Часто |
Повышенная склонность к образованию кровоподтеков |
|
Нарушения со стороны иммунной системы |
Часто |
Анафилактоидные реакции, Гиперчувствительность2 |
|
Нарушения со стороны нервной системы |
Очень часто |
Головная боль |
|
Сосудистые нарушения |
Часто |
Приливы |
|
Нарушения со стороны желудочно-кишечного тракта |
Часто |
Гипестезия полости рта Тошнота |
|
Нарушения со стороны кожи и подкожных тканей |
Очень часто |
Эритема |
|
Часто |
Липогипертрофия (образование плотных участков измененной подкожно-жировой клетчатки, возникающее в связи с многократным повторным использованием одного места введения) Генерализованный эластолиз Обесцвечивание кожи, включая гипопигментацию Нарушение со стороны кожи («стрии») |
|
|
Заболевания опорно-двигательного аппарата и соединительной ткани |
Очень часто |
Боль в конечности |
|
Часто |
Миалгия |
|
|
Общие расстройства и нарушения в месте введения препарата |
Очень часто |
Реакции со стороны места инъекции1 |
|
Лихорадка |
||
|
Раздражительность |
||
|
Часто |
Озноб |
|
|
Травмы, отравления и осложнения процедур |
Очень часто |
Гематома |
|
Часто |
Рубец |
1 Предпочтительные термины, рассматриваемые в качестве реакции со стороны места инъекции, представлены в разделе ниже.
2 Предпочтительные термины, рассматриваемые как гиперчувствительность, представлены в разделе ниже.
Реакции со стороны места инъекции
Реакции со стороны места инъекции (включая эритему, обесцвечивание, боль, зуд, макулу, отек, кровоподтек, гипертрофию, уплотнение, реакцию в месте введения, атрофию, узелок, сыпь, папулу, гематому, воспаление, уртикарную сыпь, местную гипертермию, кровоизлияние, воспаление подкожных тканей и объемное образование в области места проведением инъекции) являются наиболее частыми нежелательными реакциями, наблюдаемыми приблизительно у 73% пациентов в рамках клинических исследований. Частота возникновения реакции со стороны места инъекции была выше у пациентов с гипофосфатазией с началом в детском возрасте, а также у пациентов, получавших инъекции с частотой 6 раз в неделю (по сравнению с частотой 3 раза в неделю). Большинство реакций со стороны места инъекции были легкими и самоограничивающимися. Ни одна из данных реакций не расценивалась в качестве серьезного нежелательного явления. У двух пациентов наблюдалось возникновение реакций со стороны места инъекции, что вызвало необходимость уменьшения дозы асфотазы альфа.
Из 71 пациента, получавшего лечение в рамках клинических исследований, у одного пациента развилась тяжелая реакция со стороны места инъекции, проявляющаяся в виде обесцвечивания кожи и приведшая к отмене терапии.
Гиперчувствительность
Реакции гиперчувствительности включают эритему/покраснение, гипертермию/ лихорадку, раздражительность, тошноту, боль, дрожь/озноб, кинестезию полости рта, головную боль, приливы, признаки и симптомы, соответствующие анафилаксии.
Иммуногенность
Существует потенциальная возможность иммуногенного воздействия. Из 69 пациентов с гипофосфатазией, включенных в клинические исследования и по которым имеются данные в динамике, у 56 (81,2%) пациентов через некоторое время после применения препарата Стрензик было выявлено наличие антител к лекарственному препарату. Среди данных 56 пациентов у 25 (44,6%) также было выявлено наличие нейтрализующих антител. Гуморальный ответ (с наличием или без наличия нейтрализующих антител) по своей природе был переменным по времени. Образование антител не оказывало влияния на клиническую эффективность или безопасность препарата.
Каких-либо тенденций со стороны нежелательных явлений основанных на статусе наличия антител, в клинических исследованиях выявлено не было. Более того, у пациентов с наличием антител после подкожного введения асфотазы альфа не было выявлено проявлений гиперчувствительности или тахифилаксии.
С осторожностью
В связи с недостаточностью данных препарат следует применять с осторожностью у пациентов с нарушением функции печени и почек, а также у пожилых пациентов.
У пациентов с гипофосфатазией в возрасте от 0 до 5 лет с выявленным краниосиностозом, так как, несмотря на применение асфотазы альфа, возможно прогрессирование краниосиностоза с повышением внутричерепного давления (см. раздел «Особые указания»).
Особые указания
Исследований по оценке генотоксического и канцерогенного потенциала асфотазы альфа не проводилось.
Асфотаза альфа содержит каталитический домен тканенеспецифической щелочной фосфатазы. При введении асфотазы альфа определение активности щелочной фосфатазы рутинными лабораторными методами не представляется возможным в связи с многократно завышенными результатами. Активность асфотазы альфа не следует интерпретировать по значениям активности щелочной фосфатазы, поскольку активность щелочной фосфатазы характеризуется различиями ферментных характеристик.
Гиперчувствительность
Сообщалось о реакциях гиперчувствительности, включая признаки и симптомы, согласующиеся с анафилаксией у пациентов, получавших асфотазу альфа. Реакции возникают через несколько минут после подкожного введения препарата и могут возникать у пациентов, получавших лечение более одного (года. При возникновении реакции гиперчувствительности, рекомендуется немедленное прекращение лечения, и назначение соответствующей медикаментозной терапии. Следует соблюдать принятые в настоящее время стандарты оказания неотложной помощи.
При необходимости повторного введения препарата пациенту после серьезной реакции гиперчувствительности, врач должен оценить риск и пользу от применения препарата, принимая во внимание другие факторы, которые могут влиять на развитие реакции гиперчувствительности, такие как одновременная инфекция и/или использование антибиотиков. Если принято решение о повторном применении препарата, повторное введение должно производиться под наблюдением врача, и при использовании превентивных мер по предотвращению гиперчувствительности. Пациента и его лечащего врача следует предупредить о возможности повторения признаков и симптомов тяжелой реакции гиперчувствительности. Необходимо наблюдение за последующими введениями препарата и необходимо информировать о мерах экстренного лечения при применении препарата на дому терапией, назначенной лечащим врачом.
Реакция на инъекцию
Применение асфотазы альфа может вызвать развитие локальных реакций со стороны места инъекции (включая, но не ограничиваясь, эритему, сыпь, обесцвечивание, зуд, боль, папулу, узелок, атрофию), которые определены в качестве связанных с терапией нежелательных явлений, возникающих во время проведения инъекции или до конца дня, в который проведена инъекция. Чередование областей проведения инъекций обычно способствует эффективному контролю возникновения данных реакций. Как правило, данные реакции расцениваются в качестве несерьезных, легких или умеренных по степени тяжести и самоограничивающихся.
При возникновении у любого из пациентов тяжелой инъекционной реакции применение препарата Стрензик должно быть прекращено и назначена соответствующая терапия.
Краниосиностоз
В клинических исследованиях асфотазы альфа нежелательные явления краниосиностоза (связанного с повышенным внутричерепным давлением), включая ухудшение уже имеющегося краниосиностоза, было выявлено у пациентов с гипофосфатазией в возрасте < 5 лет. Связи между терапией асфотазой альфа и прогрессированием краниосиностоза выявлено не было в связи с недостаточностью данных. Краниосиностоз, в качестве проявления гипофосфатазии, — явление, указанное в опубликованной литературе и возникающее у 61,3% пациентов в возрасте от момента рождения до 5 лет при естественном течении гипофосфатазии с началом в младенческом возрасте при отсутствии лечения. Краниосиностоз может привести к повышенному внутричерепному давлению.
Пациентам с гипофосфатазией в возрасте до 5 лет рекомендуется периодическое наблюдение (включая исследование глазного дна на предмет проявлений отека диска зрительного нерва) и незамедлительное вмешательство при повышенном внутричерепном давлении.
Эктопическая кальцификация
У пациентов с гипофосфатазией в клинических исследованиях асфотазы альфа были выявлены отложения солей кальция в области глаз (конъюнктивальные и роговичные), а также нефрокальциноз Связи между терапией асфотазой альфа и ухудшением эктопической кальцификации выявлено не было в связи с недостаточностью данных. Отложения солей кальция в области глаз (конъюнктивальные и роговичные) и нефрокальциноз указаны в опубликованной литературе в качестве проявлений гипофосфатазии. Нефрокальциноз возникает у 51,6% пациентов в возрасте от момента рождения до 5 лет при естественном течении гипофосфатазии с началом в младенческом возрасте при отсутствии лечения. Пациентам с гипофосфатазией рекомендовано периодическое офтальмологическое обследование и ультразвуковое исследование почек.
Содержание паратгормона и кальция в сыворотке крови
У пациентов с гипофосфатазией при применении асфотазы альфа может увеличиваться концентрация паратгормона в сыворотке крови, особенно на протяжении первых 12 недель терапии. У пациентов, получающих терапию асфотазой альфа, рекомендуется контролировать содержание паратгормона и кальция в сыворотке крови. Может понадобиться дополнительное применение препаратов кальция и перорального витамина D.
Диспропорциональный прирост массы тела
У пациентов может иметь место диспропорциональный прирост массы тела. Рекомендуется диетологический контроль.
Вспомогательные вещества
Данный лекарственный препарат содержит менее 1 ммоль натрия (23 мг) на флакон.
Особые меры предосторожности при утилизации и прочем обращении
Каждый флакон предназначен исключительно для однократного применения и может быть проколот лишь один раз.
Используемые шприцы должны иметь достаточно малый объем, позволяющий в достаточной степени точно набрать предписанную дозу из флакона.
Не использованный в течение 1 ч препарат следует выбросить.
Способ применения
Лечение должно быть начато врачом, имеющим опыт в области ведения пациентов с метаболическими расстройствами или заболеваниями костей.
Рекомендованная схема применения асфотазы альфа — 2 мг/кг массы тела путем подкожной инъекции три раза в неделю, либо 1 мг/кг массы тела путем подкожной инъекции шесть раз в неделю.
Более подробная информация представлена в таблице дозирования ниже.
|
Масса тела (кг) |
При введении 3 раза в неделю |
При введении 6 раз в неделю |
||||
|
Вводимая доза |
Вводимый объем |
Используемый флакон с объемом препарата |
Вводимая доза |
Вводимый объем |
Используемый флакон с (объемом препарата |
|
|
3 |
6 мг |
0,15 мл |
0,30 мл |
|||
|
4 |
8 мг |
0,20 мл |
0,30 мл |
|||
|
5 |
10 мг |
0,25 мл |
0,30 мл |
|||
|
6 |
12 мг |
0,30 мл |
0,30 мл |
6 мг |
0,15 мл |
0,30 мл |
|
7 |
14 мг |
0,35 мл |
0,45 мл |
7 мг |
0,18 мл |
0,30 мл |
|
8 |
16 мг |
0,40 мл |
0,45 мл |
8 мг, |
0,20 мл |
0,30 мл |
|
9 |
18 мг |
0,45 мл |
0,45 мл |
9 мг |
0,23 мл |
0,30 мл |
|
10 |
20 мг |
0.50 мл |
0,70 мл |
10 мг |
0,25 мл |
0,30 мл |
|
11 |
22 мг |
0,55 мл |
0,70 мл |
11 мг |
0.28 мл |
0,30 мл |
|
12 |
24 мг |
0,60 мл |
0,70 мл |
12 мг |
0,30 мл |
0,30 мл |
|
13 |
26 мг |
0,65 мл |
0,70 мл |
13 мг |
0,33 мл |
0,45 мл |
|
14 |
28 мг |
0,70 мл |
0,70 мл |
14 мг |
0,35 мл |
0,45 мл |
|
15 |
30 мг |
0,75 мл |
1,00 мл |
15 мг |
0,38 мл |
0,45 мл |
|
16 |
32 мг |
0,80 мл |
1,00 мл |
16 мг |
0,40 мл |
0,45 мл |
|
17 |
34 мг |
0,85 мл |
1,00 мл |
17 мг |
0 43 мл |
0,45 мл |
|
18 |
36 мг |
0,90 мл |
1.00 мл |
118 мг |
0,45 мл |
0,45 мл |
|
19 |
38 мг |
0,95 мл |
1,00 мл |
19 мг |
0,48 мл |
0,70 мл |
|
20 |
40 мг |
1,00 мл |
1,00 мл |
20 мг |
0,50 мл |
0,70 мл |
|
25 |
50 мг |
0,50 мл |
0,80 мл* |
25 мг |
0,63 мл |
0,70 мл |
|
30 |
60 мг |
0,60 мл |
0,80 мл* |
30 мг |
0,75 мл |
1,00 мл |
|
35 |
70 мг |
0,70 мл |
0,80 мл* |
35 мг |
0,88 мл |
1,00 мл |
|
40 |
80 мг |
0,80 мл |
0,80 мл* |
40 мг |
1,00 мл |
1,00 мл |
|
50 |
50 мг |
0,50 мл |
0,80 мл* |
|||
|
60 |
60 мг |
0,60 мл |
0,80 мл* |
|||
|
70 |
70 мг |
0,70 мл |
0,80 мл* |
|||
|
80 |
80 мг |
0,80 мл |
0,80 мл* |
|||
|
90 |
90 мг |
0,90 мл |
0,80 мл* (х2) |
|||
|
100 |
100 мг |
1,00 мл |
0,80 мл* (х2) |
*используется препарат концентрации 100 м*/мл (80 мг/0,8 мл)
Пациенты с нарушением функции почек и печени
Безопасность и эффективность препарата Стрензик у пациентов с нарушением функции почек или печени не изучалась, и для данных пациентов не может быть рекомендована какая-либо особая схема применения препарата.
Пациенты взрослого возраста
Имеется ограниченное количество данных по эффективности и безопасности у пациентов с гипофосфатазией в возрасте старше 18 лег.
Лица пожилого возраста
Данные об опыте применения препарата Стрензик у пациентов пожилого возраста отсутствуют. При применении препарата пациентами пожилого возраста особых указаний нет.
Способ применения
Стрензик предназначен исключительно для подкожного введения. Не предназначен для внутривенного и внутримышечного введения.
Максимальный объем вводимого за одну инъекцию лекарственного препарата не должен превышать 1 мл. При необходимости введения большего объема за один раз делают несколько инъекций в разные места введения.
Шприцы должны иметь достаточно малый объем, позволяющий в достаточной-степени точно набрать предписанную дозу из флакона.
Места введения инъекций следует чередовать и тщательно контролировать па предмет возникновения проявлений потенциальных реакций.
Пациенты могут самостоятельно осуществлять инъекции только в том случае, если они прошли соответствующую подготовку но процедура, введения препарата.
Подготовка и проведение инъекции
Соблюдайте правила антисептики. Вначале снимите с флакона защитную крышку, чтобы обнажить стерильную резиновую прокладку. Снимите пластиковый колпачок с иглы шприца и выбросьте его в контейнер для острых предметов. Потяните за поршень, чтобы набрать в шприц воздух в объеме, эквивалентном необходимой дозе препарата. Держа шприц и флакон под углом 45°, введите иглу через стерильную резиновую прокладку. Теперь полностью задвиньте поршень, чтобы воздух попал во флакон. Переверните флакон и шприц, и следя за тем, чтобы игла находилась в растворе, потяните за поршень и наберите в шприц правильную дозу. Перед тем, как вынуть иглу из флакона, проверьте шприц на наличие пузырьков воздуха. При их наличии слегка постучите по стенке шприца, пока пузырьки не поднимутся вверх. Когда все пузырьки окажутся вверху, аккуратно нажмите на поршень, чтобы они попали обратно во флакон. Теперь проверьте дозу лекарственного препарата в шприце, чтобы убедиться, что набрано правильное количество.
Извлеките иглу из флакона, следя за тем, чтобы она ничего не касалась.
Выберите место для подкожной инъекции (бедра, живот, руки, ягодицы). Наиболее подходящие области для инъекции отмечены серым цветом на рисунке. Не используйте те участки, на которых имеются неприятные ощущения или патологические образования.
Аккуратно захватите кожу большим и указательным пальцами в месте инъекции.
Держа шприц так же, как карандаш или дротик, введите иглу в приподнятую кожу под углом между 45° и 90° к поверхности кожи. Для маленьких детей с небольшим количеством подкожного жира или тонкой кожей предпочтителен угол 45°.
Продолжайте удерживать кожу и вводить препарата, надавливая на поршень и медленно считая до 10.
Извлеките иглу, отпустите кожную складку и аккуратно приложите кусочек ваты или марли к месту инъекции на несколько секунд. При необходимости наложите небольшую повязку или пластырь на место инъекции.
Передозировка
Данные в отношении передозировки асфотазы альфа отсутствуют.
Лекарственная форма
раствор для подкожного введения
Состав
На 1 мл
40 мг/мл
действующее вещество: асфотаза альфа 40 мг;
вспомогательные вещества: натрия хлорид 8,76 мг, натрия гидрофосфата гептагидрат 5,5 мг, натрия дигидрофосфата моногидрат 0,62 мг, вода для инъекций до 1 мл;
100 мг/мл
действующее вещество:асфотаза альфа 100 мг;
вспомогательные вещества: натрия хлорид 8,76 мг, натрия гидрофосфата гептагидрат 5,5 мг, натрия дигидрофосфата моногидрат 0,62 мг, вода для инъекций до 1 мл.
Описание
Бесцветная или желтоватая, прозрачная, слегка опалесцирующая или опалесцирующая жидкость, возможно наличие нескольких небольших полупрозрачных или белых частиц.
Фармакодинамика
Характеристика препарата
Асфотаза альфа представляет собой человеческий рекомбинантный тканенеспецифический химерный Fc-дека-аспартатный гликопротеин щелочной фосфатазы, экспрессирующийся в модифицированной культуре клеток яичника китайского хомячка.
Асфотаза альфа — растворимый гликопротеин из двух цепочек по 726 аминокислот, включающий в себя: (1) каталитический домен человеческой тканенеспецифической щелочной фосфатазы; (2) Fc-домен человеческого иммуноглобулина G1; (3) дека-аспартатный пептидный домен (D10).
Очищается с помощью аффинной хроматографии и хроматографий гидрофобного взаимодействия, в процессе производства субстанции проводится инактивация и удаление вирусов.
Фармакодинамика
Фармакологическая активность препарата определяется активностью фермента асфотаза альфа.
Биологическое действие асфотазы альфа обеспечивается за счет растворимой части рекомбинантного человеческого неспецифического тканевого изофермента щелочной фосфатазы. Неспецифический тканевой изофермент щелочной фосфатазы представляет собой металлофермент, который катализирует гидролиз фосфомоноэфиров с образованием неорганического фосфата и спирта, за счет чего обеспечивается физиологический процесс минерализации костей.
Гипофосфатазия — редкое тяжелое прогрессирующее потенциально смертельное наследственное заболевание, обусловленное дефицитом щелочной фосфатазы, который возникает из-за мутации в гене ALPL, кодирующем неспецифический тканевой изофермент щелочной фосфатазы. Дефицит активности щелочной фосфатазы ведет к нарушениям регуляции обмена фосфата и кальция, гипоминерализации костей, нарушениям со стороны скелета (деформация и разрушение костей), и полиорганным осложнениям. Клиническими проявлениями также могут быть боль и выраженная мышечная слабость, дыхательная недостаточность, судороги, нарушение функции почек, нарушение двигательной функции, а также заболевания зубов.
Асфотаза альфа применяется как патогенетическое лечение гипофосфатазии в качестве длительной заместительной ферментной терапии Устранение дефицита активности щелочной фосфатазы за счет замещения дефектного фермента предотвращает нарушения минерализации скелета и способствует восстановлению этого процесса.
Было продемонстрировано, что по сравнению с исходными значениями, лечение асфотазой альфа приводит к положительным изменениям у пациентов по таким признакам как уровни биохимических субстратов тканенеспецифической щелочной фосфатазы (неорганического пирофосфата и пиридоксаль-5′-фосфата), минерализация костной ткани, структура костей, рост, мышечная сила, физическая функция, способность передвигаться и инвалидность.
Механизм действия
Асфотаза альфа, человеческий рекомбинантный тканенеспецифический гибридный Fc- дека-аспартатный белок щелочной фосфатазы с ферментативной активностью, улучшает минерализацию скелета у пациентов с гипофосфатазией.
Клиническая эффективность и безопасность
Результаты клинических исследований асфотазы альфа получены в открытых не рандомизированных исследованиях с участием не менее 69 папистов в основном с детской и инфантильной формами гипофосфагазии. В исследовании ENB-006-09/ENB-008-10 у пациентов на фоне лечения асфотазой альфа по сравнению с группой контроля (исторический контроль с включением пациентов, не получавших терапию), отмечалась положительная рентгенологическая динамика по шкале общего впечатления о рентгенологических изменениях (RGI-C) на протяжении первых 6 месяцев терапии. По данным биопсии кости отмечена положительная динамика показателей минерализации костной ткани: толщина остеоида, отношение объема остеоида и объема костной ткани и время задержки минерализации костной ткани. У 9 из 13 пациентов получающих асфотазу альфа в этом исследовании наблюдалось увеличение показателя роста приближающегося к возрастной норме.
У пациентов с инфантильной формой гипофосфатазии в исследовании ENB-002-08/ ENB-003-08 при оценке по шкале общего впечатления о рентгенологических изменениях (RGI-C) зафиксировано: значительное улучшение отмечено у 7 из 11 пациентов; нарастающие темпы роста у 5 из 11 детей.
В исследовании ENB-009-10 на пациентах от 13 до 66 лет продемонстрирована положительная динамика минерализации костной ткани по результатам биопсии, отмечено улучшение показателей: толщина остеоида, отношение объема остеоида и объема костной ткани и время задержки минерализации костной ткани.
Фармакокинетика
После внутривенной инфузии дозы 3 мг/кг на протяжении 1,08 часа в исследуемых когортах медиана времени (Тmах) варьировала от 1,25 до 1,50 часов, а среднее значение максимальной концентрации в плазме (Сmах) — oт 42694 (8443) до 46890 (6635) ЕД/л. Абсолютная биодоступность после первой и третьей подкожной дозы варьировала от 45,8 до 98,4% с медианой Тmах от 24,2 до 48,1 часов.
Абсолютная биодоступность и скорость абсорбции после подкожного введения составляет 0,602 (95% доверительный интервал — ДИ: 0,567, 0,638) или 60,2% и 0,572 (95% ДИ: 0,338, 0,967)/сутки, соответственно. Центральные и периферические объемы распределения в пересчете на пациента с массой 70 кг (и 95 % ДИ) составляли 5,66 (2,76, 11,6) л и 44,8 (33,2, 60,5) л, соответственно.
Значения центрального и периферического клиренса в пересчете на пациента с массой 70 кг (и 95% ДИ) составляли 15,8 (13,2. 18,9) л/сутки и 51,9 (44,0, 61,2) л/сутки, соответственно.
Среднее значение периода полувыведения после подкожного введения составляло 2,28 ± 0,58 суток.
Линейность/нелинейность
На основании результатов популяционного фармакокинетического анализа был сделан вывод, что асфотаза альфа характеризуется линейным фармакокинетическим профилем при подкожном введении доз вплоть до 28 мг/кг/неделю. В качестве фактора, оказывающего влияние на клиренс и объем распределения асфотазы альфа, выступала масса тела. Ожидается, что уровень фармакокинетического воздействия будет возрастать с увеличением массы тела.
Влияние иммуногенности на фармакокинетику асфотазы альфа варьировало с течением времени, что связано с варьирующей природой иммуногенности. В целом, было показано, что иммуногенность снижает уровень фармакокинетического воздействия менее чем на 20%.
Применение при беременности и кормлении грудью
Беременность
Какие-либо данные в отношении применения асфотазы альфа беременными женщинами отсутствуют. После повторных подкожных введений асфотазы альфа беременным мышам в диапазоне терапевтической дозы (> 0,5 мг/кг) уровни препарата определялись количественно в организме плода при всех исследованных дозах, что свидетельствует о трансплацентарном переносе асфотазы альфа. В отношении репродуктивной токсичности исследований на животных недостаточно. Применение асфотазы альфа не рекомендуется во время беременности, а также женщинам детородного возраста не использующим средства контрацепции.
Кормление грудью
В отношении выделения асфотазы альфа грудным молоком человека данных недостаточно. Не может быть исключен риск для новорожденного ребенка, находящегося на грудном вскармливании. На время терапии асфотазой альфа следует прекратить грудное вскармливание.
Фертильность
В доклинических исследованиях фертильности не было выявлено какого-либо эффекта на фертильность и эмбриофетальное развитие.
Взаимодействие с другими лекарственными препаратами
Исследований взаимодействий с асфогазой альфа не проводилось. Основываясь на структуре и фармакокинетике, влияние асфотазы альфа на метаболизм, связанный с системой цитохрома Р-450, является маловероятным.
Фармацевтическое
Препарат не следует смешивать с другими лекарственными препаратами, так как исследования совместимости не проводились.
Влияние на способность управлять транспортными средствами
Препарат Стрензик не оказывает или оказывает незначительное влияние на способность управления транспортными средствами и работу с механизмами.
Форма выпуска и дозировка
Раствор для подкожного введения, 40 мг/мл и 100 мг/мл.
Упаковка
По 12 мг/0,3 мл; 18 мг/0,45 мл; 28 мг/0,7 мл; 40 мг/1,0 мл в стеклянный флакон гидролитического класса I вместимостью 2 или 3 мл, укупоренный бутилкаучуковой пробкой и алюминиевой крышкой с полипропиленовым откидным колпачком.
По 1 или 12 флаконов с инструкцией по применению в пачку картонную.
По 80 мг/0,8 мл в стеклянный флакон гидролитического класса 1 вместимостью 2 или 3 мл, укупоренный бутилкаучуковой пробкой и алюминиевой крышкой с полипропиленовым откидным колпачком.
По 1 или 12 флаконов с инструкцией по применению в пачку картонную.
Условия хранения
В защищенном от света месте, при температуре 2-8 °С.
Не замораживать!
Хранить в оригинальной упаковке для защиты от света.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности.
Условия отпуска из аптек
Источники
1. Анатомо-терапевтическо-химическая классификация (ATX)
2. Официальная инструкция от производителя

Проверено специалистом
Проверено специалистом
Наталья Фесенко
Ведущий фармацевт, 12 лет стажа
Номер 104013 0001267, регистрационный номер 52
Отзывы о СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12
Я приобрел СТРЕНЗИК раствор (аналог инсулина длительного действия)для подкожного введения по рекомендации врача и был приятно удивлен его эффективностью. Применял [согласно инструкции и заметил значительное улучшение состояния. Инъекции помогли справиться с проблемой повышенного уровня сахара в крови, что очень облегчило мою повседневную жизнь. Рекомендую этот препарат тем, кто столкнулся с аналогичными проблемами.
Смотреть все отзывы
Часто задаваемые вопросы
Условия хранения СТРЕНЗИК
В защищенном от света месте, при температуре 2-8 °С.Не замораживать!Хранить в оригинальной упаковке для защиты от света.Хранить в недоступном для детей месте.
Топ товаров из категории
Купить СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12 в аптеке г. Москва и в других городах
СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12 от производителя ALEXION PHARMA INTERNATIONAL SARL доступен в Москве, а также в других городах: Подольск, Домодедово, Химки, Щелково, Жуковский, Долгопрудный, Мытищи, Балашиха, Королев, Пушкино.
Цена товара СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12 варьируется от 14850₽.
Мы рекомендуем обратить внимание и на другие товары из категории Лекарства, например:
- ХОНДРОФЕН МАЗЬ ДЛЯ НАРУЖНОГО ПРИМЕНЕНИЯ 30 Г №1
- МАГНЕВИСТ РАСТВОР ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ 469,01 МГ/МЛ 20 МЛ №10
- ПЕНТАНОВ ПЛЮС ТАБЛЕТКИ №12
- АРЕПЛИВИР ТАБЛЕТКИ ПОКРЫТЫЕ ПЛЕНОЧНОЙ ОБОЛОЧКОЙ 200 МГ №40
- ПАЛЕКСИЯ ТАБЛЕТКИ ПОКРЫТЫЕ ПЛЕНОЧНОЙ ОБОЛОЧКОЙ 100 МГ №20
а также
при необходимости выполнить поиск по действующему веществу — АСФОТАЗА АЛЬФА,
чтобы найти аналогичные товары c похожими свойствами.
Другие товары ALEXION PHARMA INTERNATIONAL SARL
Также можете ознакомиться с другими продуктами производителя ALEXION PHARMA INTERNATIONAL SARL: среди популярных товаров вы найдете и узнаете сколько стоят в аптеках:
- КАНУМА КОНЦЕНТРАТ ДЛЯ ПРИГОТОВЛЕНИЯ РАСТВОРА ДЛЯ ИНФУЗИЙ 2 МГ/МЛ 10 МЛ №1
- СОЛИРИС КОНЦЕНТРАТ ДЛЯ ПРИГОТОВЛЕНИЯ РАСТВОРА ДЛЯ ИНФУЗИЙ 10 МГ/МЛ 30 МЛ №1
- СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 40 МГ/МЛ 0,7 МЛ №12
- СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 40 МГ/МЛ 1 МЛ №12
- СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12 в Москве: цены в Москве, аналоги, инструкция по применению.
- СТРЕНЗИК РАСТВОР ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ 100 МГ/МЛ 0,8 МЛ №12 в Москве – сколько стоит в аптеках и где купить в Москве с доставкой или самовывозом – смотрите на 009.рф
- Информация носит ознакомительный характер и не является публичной офертой.
Список товаров по алфавиту
- А
- Б
- В
- Г
- Д
- Е
- Ж
- З
- И
- Й
- К
- Л
- М
- Н
- О
- П
- Р
- С
- Т
- У
- Ф
- Х
- Ц
- Ч
- Ш
- Щ
- Э
- Ю
- Я
- A-Z
- 0-9
