Трихомоноз кошек – это относительно не новая, но пока малоизученная, но очень распространенная паразитарная болезнь кошек. Заводчики кошек сталкиваются с ней чаще, чем даже ветеринарные врачи, потому что именно длительные хронические диареи у котят в питомниках кошек послужили причиной изучения трихомоноза.
Впервые трихомоноз описан был в 1922 году. Исследования в то время почти не проводились, так как считалось, что это часть комменсальной микрофлоры. Однако было исследование, когда после заражения котята развили диарею такую, что погибли в течение 10 дней после заражения. Однако большого внимания тогда трихомоносам не уделяли. Определили что есть у кошек отдельный штамм простейших, который устойчив к метронидазолу, но глубокое исследование трихомоноза кошек началось всего несколько лет назад и сейчас набирает обороты.
Активное изучение началось в начале 2000 годов, большую роль и в изучении и исследовании трихомоноза кошек занимает американский ветеринарный врач Gookin JL. Его англоязычные исследования можно найти в интернете.
Заражение происходит орально-фекальным путем, чаще всего в виде прямого контакта со свежим калом зараженного животного. Вылизывание загрязненной шерсти, друг друга, и загрязненность окружающей среды являются основными факторами заражения.
Чаще болеют породистые кошки, наиболее предрасположены бенгалы, ориенталы и персы. Беспородные болеют реже. Чаще к трихомонозу предрасполагает скученное содержание, одиночные кошки не болеют почти никогда. Если болеет «одиночка» — то чаще всего или куплен из питомника, где уже был заражен, или это отдельно живущий кот-производитель, к которому приезжали кошки и заразили.
Генетическая предрасположенность есть, болеют в основном породистые, доказана неустойчивость в этим паразитам. В большинстве исследований чистокровные породистые кошки заражались чаще.
Часто такие кошки имеют большую историю болезни, обращаются к разным врачам, прежде чем находят причину. Часто им становится лучше на лекарствах, антибиотиках, диетах, после отмены – возврат симптомов: или сразу или через некоторое время.
Часто протекают совместно с лямблиозом и кокцидиозом, клостридиозом, вызывая ко-инфекцию и трудности при лечении и диагностике, так как при обнаружении лямблий и других распространенных простейших врачи не всегда исследуют дальше, считая причину диареи установленной, а исследование на трихомоноз не является рутинным. Симптомы этих болезней очень схожи. Поэтому часто причиной якобы « очень устойчивых лямблий, не отвечающих на терапию» являются как раз недодиагностированные трихомоносы. Также ряд авторов считает, что именно наличие сопутствующих паразитозов является причиной для клинического проявления диареи.

Клинические признаки трихомоноза:
В среднем возраст наиболее часто обращающихся с проблемой пациентов — 6-12 мес, но болеют кошки всех возрастов, но чаще молодые.
Хроническая диарея, разной степени тяжести. Капли крови в жидких фекалиях в конце дефекации, примеси слизи в нем. Стул может быть мягкий или слабооформленный, иногда совсем жидкий, пенистый. Цвет чаще желтовато-зеленый, светлый. Часто описывается владельцами словом «каша». Диарея хроническая, часто других жалоб нет. Диарея может быть сильная настолько, что течет «водой». Часто из-за этого воспален анус, вплоть до пролапса( выпадения). Диарея иногда доходит до 20 раз в день. Иногда животные даже могут не добегать до лотка, пачкая пол, шерсть. Иногда же стул относительно сформирован, но есть слизь, кровь, или стул разжижен в конце.
Газы и активная перистальтика, недержание стула. Владельцы отмечают чрезвычайно неприятный, даже зловонный запах фекалий и газов, при дефекации часто звуки «журчания».
Часто протекает совместно с лямблиозом, кокцидиозом.
Заражение, носительство, тяжесть течения трихомонозом не зависит от ВЛК, ВИД и ГКС в иммуносупрессивных дозах, исследования не доказали связи. То есть, болеют не только животные с иммуносупрессией.
Диагностика.
Может не обнаруживаться в рутинных анализах, так как паразит имеет только стадию трофозоита, не выдерживает охлаждения и для большинства исследований кала используется гиперсолевой раствор, в котором они погибают и движения не видно, и анализ получается ложноотрицательный. Также нужен очень свежий мазок или смыв, ибо трихомоносы живут всего 20 минут в окружающей среде. Максимально 6 часов.
Самый точный способ – культивация на специальных средах. Не каждая клиника имеет термостат для культивации, и специальные среды, достаточно дорогие, около 1000 р., поэтому этот метод встречается редко.
ПЦР после экстракции ДНК из свежих фекалий
Флотационные методы не применяются
Нативный мазок из свежего кала –фекалии должны быть доставлены не позднее 6 часов, можно увлажить фекалии. Все равно , это метод низкой чувствительности , потому что сложно посчитать жгутики трихомонад, чтобы определить вид их – метронидазолом лечатся пентатрихомонасы, ронидазолом – тритрихомонасы.
Смыв из прямой кишки – оптимальный способ для забора. Может выполняться на приеме. Берут 20 мл физраствора , в помощью трубки вводят глубоко в кишечник ректально и тут же втягиваем раствор обратно в шприц. Можно использовать трубку от инфузионной системы. Длина ее примерно равна состоянию от ануса до холки. Смазывают самый кончик маслом или левомеколем но немного, чтобы жировые пятна не мешали потом исследованию.
Важно отличать трихомонад от лямблий – лямблии имеют движение по типу «падающего листа», они вертятся. А трихомонасы – движутся целенаправленно, движение поступательные.

Лечение:
Ронидазол 20-30 мг\кг 2 раза в день 2 недели. Единственный с доказанной эффективностью, используется в птицеводстве, для лечения трихомонад, живущих в зобу птиц. Также эффективен и у кошек.
Но есть очень большая проблема – для кошек есть нейротоксичный эффект и не все кошки могут пройти полный курс лечения из-за побочных эффектов. Иногда около 50% кошек проявляют тремор, слюнотечение, дрожь, крутятся на месте. Лечение в таких случаях прекращают, потому что оно становится опасно.
Ронидазол не сертифицирован в России для кошек, поэтому прибрести его можно только в магазинах для голубей, или на Птичьем рынке в отделах для голубей. Лучше покупать в проверенных голубятниками магазинах, по рекомендациям и отзывам, потому что подделки на рынках периодически встречаются.
Что делать, если у кошки проявились побочные эффекты на Ронидазол?
Ситуация сложная, потому что к остальным препаратам трихомонасы малоэффективны, в том числе – Орнидазол, который часто называют альтернативой….
При развитии побочных эффектов препаратом выбора является:
Тинидазол – 30 мг\кг 14 дней 1 раз в день.
Его плюс еще и в том, что Тинидазол действует также на лямблий, а часто именно сочетание этих двух паразитозов дает диарею. Однако действие на трихомонад слабее.
После проведенного лечения обычно наступает явное улучшение, стул становится обычным, сформированным, котята начинают активно набирать вес.
К сожалению, даже после полного курса лечения примерно 54% кошек рецидивируют. Даже если были получены отрицательные смывы или ПЦР. Причиной может быть реинвазия (перезаражение) или не все кошки освободились от паразита. Рецидивы обычно случается после стрессовой ситуации или смены корма.
Часто реинвазия в питомнике или приюте возникает из-за того, что лечат не все поголовье, а только тех, кто выявляет клинические признаки. А остальные кошки могут быть носителями и происходит перезаражение.
Некоторые авторы для закрепления периода ремиссии применяют препарат паромомицина 165 мг\кг 2 раза в день 5 дней. Но, к сожалению, и он обладает нейротоксичностью, и должен использоваться с осторожностью, но он делает ремиссию более устойчивой.
Прогноз
В целом благоприятный. Наблюдается самовыздоровление у 88% после достижению 2 лет. Но остаются носителями инвазии в питомнике.
Кошки с хронической диареей могут иметь длительные периоды ремиссии , рецидивы обычно начинаются на смене рациона, стрессовых ситуациях, которые вызывают изменение микробиома кишечника.
В сети ветеринарных клиник «Василек» вы можете сдать анализ на трихомоноз и методом ПЦР и смывом из кишечника, а также записаться на прием к гастрэнтерологу Невровой Елене Викторовне. Запись по телефону +7 499-110 -01-05
- Описание
- Изображения
- Отзывы
Ронидазол (Ronidazole)
Ронидазол — нитроимидазольный антибиотик, используемый с целью излечения трихомоназа у птиц, кошек, а также иных животных. Применяется в дозировке согласно курсу ветеринара или орнитолога.
Ронидазол — особенный продукт с доказанной эффективностью, используется в птицеводстве и животноводстве для лечения трихомонад, живущих в зобу птиц. Помимо этого результативен и у кошек.
Чаще всего для лечения трихомоноза используют рондиназол, утвердительные результаты появляются спустя несколько дней. В 1-ых фазах лечения многие симптомы могут сохраняться. Лекарственное средство может активизировать побочные эффекты, по этой причине назначать его должен исключительно врач. Ронидазол лишает трихомонад способности плодиться, тем самым останавливая оборот воспроизводства инфекции.
Хотя трихомониаз достаточно заразен и порождает серьёзные проблемы, он крайне хорошо лечится. Наблюдение полного излечения птиц и кошек — превосходный.
Как только лечебное средство станет функционировать, стул кошки нормализуется, запах становится обыденным. Уже после смерти последних Tritrichomonas foetus котенок полностью выздоравливает.
Масса — 50 гр
Продукт в ПОРОШКЕ !!!
Отправляем исключительно при условии 100 % оплаты за заказ.
Наложенным платежем НЕ ОТПРАВЛЯЕМ
Что известно о трихомонадной инфекции кошек?
Tritrichomonas foetus
Читать статью через ВКонтакте
Статья обновлена 14.02.2024
Tritrichomonas foetus — это одноклеточный эукариотический организм, локализуется в толстом кишечнике кошачьих и является возбудителем трихомоноза, заболевания с хронической и рецидивирующей диареей с примесью слизи и свежей крови в кале. Животные, зараженные T. foetus, зачастую не реагируют на обычное лечение. Диагностика трихомонадной инфекции проводится либо микроскопическим исследованием, либо путем выделения ДНК в кале с последующей амплификацией.
T. foetus часто ошибочно идентифицируют как другое жгутиковое простейшее: Giardia duodenalis или Pentatrichomonas hominis.
Без надлежащего лечения диарея может проходить самопроизвольно через месяцы или годы, но кошки при этом могут оставаться носителям.
Вступление
Tritrichomonas foetus — это трихомонада, которая впервые была описана как бычий венерический патоген, вызывающий бесплодие, аборты и эндометриты (FELLEISEN, 1999; STOCKDALE et al., 2006). Более десяти лет назад T. foetus был также идентифицирован в кале домашних кошек с хронической диареей (GOOKIN et al., 1999; LEVY et al., 2003). Трихомонады обнаружены как у кошек с диареей и так без нее (DA CUNHA & MUNIZ, 1922; JORDAN, 1956), но их считали комменсальными и условно-патогенными организмами (DIMSKI, 1989; BARR, 1998).
Возможно, долгое время T. foetus при микроскопии путали с Pentatrichomonas spp. [Eukaryota; Parabasalia; Trichomonadida; Trichomonadidae] или Giardia spp. [Eukaryota; Fornicata; Diplomonadida; Hexamitidae; Giardiinae] (GOOKIN et al., 1999); однако, благодаря генетической идентификации в 2003 году T. foetus был признан возбудителем трихомоноза кошек (LEVY et al., 2003).
Поскольку трихомоноз кошек был идентифицирован как заболевание желудочно-кишечного тракта, исследователи обратили свой интерес к пониманию его этиологии, эпидемиологии и патогенеза, а также к диагностике и лечению (GOOKIN et al., 1999, 2006, 2010; GREY et al., 2010).
Таксономия
Трихомонады вида Tritrichomonas foetus представляют собой анаэробные простейшие организмы отряда Trichomonadida семейства Trichomonadidae (BRUGEROLLE & LEE, 2000). Новая систематика классифицирует трихомонады как [cellular organisms; Eukaryota; Parabasalia; Tritrichomonadida; Tritrichomonadidae; Tritrichomonas].
Историческая справка
Трихомоноз был впервые описан у кошки в Бразилии Da Cunha и Muniz в 1922 году, которые назвали возбудителя Trichomonas felis. Спустя годы Brumpt (1925) выявил трихомонад с тремя-пятью передними жгутиками у собак и кошек во Франции, приняв название Trichomonas felis для обоих видов животных. Год спустя Tanabe выявил паразита, Pentatrichomonas spp. у кошки, дав ему название Pentatrichomonas felis (TANABE, 1926).
Kessel (1928) наблюдал естественный и экспериментальный трихомоноз у девяти котят. Животные страдали диареей, которая прогрессировала до дизентерии. Котята умерли в течение 10 дней после заражения.
В 1956 году молодой кошке с хронической диареей был поставлен диагноз трихомоноз, описанный как инфекция, вызванная Trichomonas spp. (JORDAN, 1956).
В период с 1956 по 1996 год исследований практически не проводили, т.к. трихомонад кошек считали непатогенным комменсальными видами, которых выявляли только при предшествующих энтеритах (DIMSKI, 1989; BARR, 1998; GOOKIN и др., 1999). В 1996 году, основываясь на микроскопическом исследовании мазков из фекалий, Romatowski (1996, 2000) установил, что Pentatrichomonas hominis вызывают мукоидную диарею у котят и взрослых кошек.
В 2001 году после молекулярного анализа гена 18S р-РНК изолятов трихомонад они были идентифицированы как Tritrichomonas foetus со сходством 99,9% (LEVY et al., 2003).
Tritrichomonas foetus также был обнаружен в репродуктивных органах кошки с пиометрой в Норвегии, хотя причиной инфекции в матке были бактерии Streptococcus spp., которые присутствовали в секреции половых органов (DAHLGREN et al., 2007).
Gray et al. (2010) исследовали репродуктивные органы 15 кошек, у которых ранее была диагностирована кишечная инфекция, вызванная T. foetus. Они использовали световую микроскопию, иммуногистохимический анализ и ПЦР анализ и не обнаружили никаких признаков паразита.
Молекулярная генетика
В нескольких исследованиях описаны возбудители крупного рогатого скота и их возможность быть источником инфекции для кошек. Однако, эпидемиологическое исследование кошек не выявило связи между инфекцией T. foetus и близостью к крупному рогатому скоту (GOOKIN et al., 2004). Исследования, связанные с перекрестным заражением, проведенные Stockdale et al. (2007, 2008), показали фенотипические различия между инфекционностью и патогенностью изолятов, выявленных у кошек и крупного рогатого скота (КРС). Молекулярные исследования показали так же и генетические различия между изолятами. Slapeta et al. (2010) предложили видоспецифические различия между генотипами T. foetus крупного рогатого скота и кошек. Другие исследователи также наблюдали немногочисленные, но постоянные генетические различия между изолятами. Sun et al. (2012) выявили отличия в цистеиновой протеазе 8 изолятов от КРС и кошек, объясняя это как возможную адаптацию к хозяину.
Новое название — Tritrichomonas blagburni было предложено для паразита кошек, чтобы отделить его от бычьего паразита (WALDEN et al., 2013). По мнению авторов, специфичность хозяина, а также морфологическая и генетическая информация должны учитываться при любой таксономической оценке. С научной точки зрения это по-прежнему считается спорным, так как данные, полученные из сравнительного анализа двух транскриптомов, не смогли подтвердить, что они являются двумя различными видами (MORIN-ADELINE et al., 2014).
Кроме того, исследования показали, что Tritrichomonas suis — трихомонада домашней свиньи, морфологически неотличима от T. foetus. Секвенирование вариабельного фрагмента ДНК и сравнение последовательностей генов не выявили различий между изолятами T.suis и T. foetus КРС. Таким образом, исследователи пришли к выводу, что T. foetus и T. suis принадлежат к одному и тому же виду, предполагая, что наименования паразитов являются синонимичными (TACHEZY et al., 2002; LUN et al., 2005).
Морфология
Простейшие T. foetus имеют только трофозоитную стадию. Это маленькие жгутиковые размером от 10 до 25 мкм в длину и от 3 до 15 мкм в ширину (GOOKIN et al., 2006). У них грушевидное тело, одно ядро, три передних жгутика и один задний жгутик (WARTON̄A & HONIGBERG, 1979). Задний жгутик проходит вдоль тела паразита, образуя волнообразную мембрану (GOOKIN et al., 2006). Аксостиль — твердая органелла, проходит по длине тела паразита (LEVINE, 1985) и выступает на заднем конце (GOOKIN et al., 2006).
Жизненный цикл
Жизненный цикл трихомонады представляет собой простой бесполый цикл, в котором трофозоит делится продольным бинарным делением. Передача возбудителя происходит при проглатывании трофозоитов, т.е. алиментарным путем (GOOKIN et al., 2017).
Нет истинной стадии цисты, но некоторые авторы описывают, что в неблагоприятных условиях окружающей среды (дефицит питательных веществ, действие лекарств или резкие изменения температуры) может происходить образование псевдоцист. В этом случае жгутики исчезают, но клетка не образует истиной цисты (PEREIRA-NEVES et al., 2003; PEREIRA-NEVES & BENCHIMOL, 2009; ROSA et al., 2015).
Факторы заражения
Передача T. foetus между кошками происходит фекально-оральным путем (GOOKIN et al., 1999, 2001). Прямого контакта со свежими испражнениями может быть достаточно для передачи паразита, так как T. foetus не попадает в виде цист в окружающую среду.
Однако Hale et al. (2009) обнаружили, что трофозоиты T. foetus более устойчивы к условиям окружающей среды, чем считалось ранее, выживая во влажных фекалиях в течение семи дней при комнатной температуре (23-20℃).
Способность паразита выживать вне хозяина может быть важным фактором в эпидемиологии заболевания, особенно в местах большого скопления кошек. Эта живучесть также позволяет предположить, что вылизывание животными друг друга и загрязнение окружающей среды фекалиями являются важными факторами в эпидемиологии заболевания (HALE et al., 2009; VAN DER SAAG et al., 2010).
Хотя теоретическая передача T. foetus между крупным рогатым скотом и кошками возможна, прямая передача не является основным источником инфекции (STOCKDALE et al., 2008). Gookin et al. (2004) не обнаружили никакой связи между инфекцией кошек и их близостью к КРС.
Факторы риска
Tritrichomonas foetus преимущественно выявляют у молодых кошек. Большинство исследований показало, что средний возраст заражения — 12 месяцев или менее; болеют же трихомонозом животные в возрасте от 4 недель до 16 лет (GOOKIN et al., 1999, 2004; BURGENER et al., 2009; FREY et al., 2009).
Во многих исследованиях зараженным кошкам был 1 год или они были моложе (FOSTER et al., 2004; GOOKIN et al., 2004; YAEGER & GOOKIN, 2005; STOCKDALE et al., 2009; ARRANZ‑SOLÍS et al., 2016).
Holliday et al. (2009) обнаружили инфицированных кошек в группе, в которой преобладали животные старше 1 года. Вероятное объяснение этого расхождения заключается в том, что инфекция, возможно, впервые попала в популяцию, а отсутствие защиты со стороны иммунной системы способствовало проявлению клинических признаков (HOLLIDAY et al., 2009).
У кошек, особенно моложе 3-х лет, инфекция может протекать бессимптомно и они могут стать источником заражения для других кошек (XENOULIS et al., 2010).
Половой предрасположенности к заражению среди кошек, инфицированных T. foetus, не описано ни в одном исследовании (GOOKIN et al., 2004; GUNN-MOORE et al., 2007; BURGENER et al., 2009; STOCKDALE et al., 2009).
В большинстве исследований чистокровные кошки заражались чаще (GUNN-MOORE и др., 2007; BURGENER и др., 2009; FREY и др., 2009; STOCKDALE и др., 2009; BELL и др., 2010; KLEIN и др., 2010). И наоборот, два исследования показали, что инфекция также распространена у кошек смешанных пород (GOOKIN et al., 1999; HOLLIDAY et al., 2009). Поскольку инфекция T. foetus чаще встречается в питомниках и приютах (GOOKIN et al., 1999; FOSTER et al., 2004), неизвестно, выявляется ли она чаще у чистокровных кошек из-за генетической предрасположенности или из-за того, что данные кошки обычно живут в местах агломерации T. foetus (HOLLIDAY et al., 2009).
Роль лечения и скученного содержания, в отличие от генетической предрасположенности, может быть ответом на более высокую распространенность инфекции среди чистокровных кошек. Это объяснение подтверждается высокой распространенностью инфекции среди кошек смешанных пород в приютах с плохими санитарными условиями (HOLLIDAY et al., 2009).
Gookin et al. (2004) не обнаружили значительной связи между инфекцией T. foetus и кошачьими туалетами, но плотность популяции кошек связана с передачей возбудителя через туалет (GOOKIN et al., 2007).
Неизвестно, влияет ли иммунный статус животного на патогенез T. foetus. С другой стороны, высокая распространенность инфекции среди молодых животных может указывать на склонность к заражению животных с незрелой иммунной системой (GOOKIN et al., 1999). Однако, в экспериментальном исследовании не было подтверждено ухудшения течения диареи при применении иммунодепрессивной дозы преднизолона (GOOKIN et al., 2001). Кроме того, по-видимому, нет никакой связи между T. foetus и иммуносупрессивными заболеваниями, такими как вирусная лейкемия кошек (FeLV) и вирусным иммунодефицитом (FIV) (GOOKIN et al., 1999; ROSADO et al., 2007).
Ко-инфекции другими энтеропатогенами можно часто наблюдать у кошек, зараженных T. foetus (GOOKIN et al., 2004). Некоторые авторы задаются вопросом, является ли T. foetus изолированной причиной диареи или сопутствующие инфекции приводят к тому, что кошки становятся более уязвимыми для паразита (STOCKDALE et al., 2009).
В некоторых исследованиях описано распространение ко-инфекции T. foetus с Giardia spp. (GOOKIN et al., 2004). Gookin et al. (2004) обнаружили ко-инфекцию T. foetus и Giardia spp. у 12% кошек, но эта связь не была значимой. Steiner et al. (2007) отметили, что большинство зараженных кошек в их исследовании также были положительными по Giardia spp. Bissett et al. (2008) сообщили, что 66% изученных кошек были ко-инфицированы.
Также часто сообщалось о ко-инфекции кокцидиями (STOCKDALE et al., 2009; GOOKIN et al., 2001, 2005; BISSETT et al., 2008). Gookin et al. (2001) экспериментально заразил восемь кошек (четыре из которых уже были заражены Cryptosporidium spp. [Eukaryota; Alveolata; Apicomplexa; Conoidasida; Coccidia; Eucoccidiorida; Eimeriorina; Cryptosporidiidae]) изолятом T. foetus. После заражения изолятом T. foetus у кошек с Cryptosporidium spp. понос появился раньше и был более тяжелым и у них было обнаружено большее количество трофозоитов, чем у кошек без кокцидий (без Cryptosporidium spp). С другой стороны, не было различий в количестве выделяемых ооцист.
Распространенность
Исследования трихомоноза кошек в нескольких странах показали, что T. foetus распространен среди домашних кошек во всем мире (STEINER et al., 2007). Глобальная распространенность T. foetus среди домашних кошек с диареей и без нее колеблется в пределах 0-81,8% в зависимости от количества проанализированных образцов, используемого метода диагностики, географического региона и образа жизни кошек.
Патогенез
Поскольку это недавно описанный паразит, патогенез T. foetus у кошек до сих пор полностью не изучен (TOLBERT & GOOKIN, 2016). Существуют лишь гипотезы о том, вызывает ли паразит клинические признаки самостоятельно или трихомоноз кошек может быть многофакторным заболеванием, связанным с кишечными ко-инфекциями и факторами, зависящими от хозяина (GOOKIN et al., 2004).
T. foetus локализуется в подвздошной, слепой и ободочной кишках кошек (GOOKIN et al., 2001; STOCKDALE et al., 2008).
Эксперименты продемонстрировали цитотоксическую и протеолитическую активность T. foetus в отношении клеток млекопитающих (BURGESS & MCDONALD, 1992). Инфекция характеризуется умеренной лимфоплазмоцитарной и нейтрофильной инфильтрацией подслизистой оболочки (YAEGER & GOOKIN, 2005). Описано истончение эпителия ободочной кишки, гипертрофия крипт, гиперплазия и повышенная митотическая активность, потеря бокаловидных клеток и микроабсцессы крипт. (SCHREY et al., 2009). Также иногда можно наблюдать эозинофелию (YAEGER & GOOKIN, 2005; SCHREY et al., 2009).
Некоторые факты наводят на мысль, что бактерии, присутствующие в ободочной кишке, являются важной частью патогенеза диареи у кошек, зараженных T. foetus. Например, диарея у этих животных обычно замедляется введением антибиотиков (GOOKIN et al., 1999, 2001). При этом не известно, уменьшают ли антибиотики бактериальный вклад в патогенез диареи или просто уменьшается количество T. foetus за счет уменьшения питательной базы (TOLBERT & GOOKIN, 2016).
Кошки с хроническим течением болезни могут демонстрировать длительные периоды клинической ремиссии; повторяющиеся эпизоды диареи могут быть вызваны диетическими изменениями или стрессовыми ситуациями, которые могут изменить микробиоту кишечника (FOSTER et al., 2004).
Клиническая картина
Клиническая картина варьируется от субклинического течения болезни до тяжелых случаев (FOSTER et al., 2004). При экспериментальном пероральном заражении клинические признаки появлялись через 2-7 дней (GOOKIN et al., 2001).
Клинические признаки включают хроническую или прерывистую диарею, желтовато-зеленые, зловонные фекалии и признаки колита: присутствие крови, слизи, недержание кала, тенезмы и/или метеоризм (GOOKIN et al., 2001; XENOULIS et al., 2013). Консистенция фекалий обычно варьируется от полуоформленной до жидкой (SCHREY et al., 2009; XENOULIS et al., 2010). При тяжелых случаях заболевания может развиться воспаление анальной области и выпадение прямой кишки (FOSTER et al., 2004; BURGENER et al., 2009).
Как и ожидалось, при заболевании, которое обычно поражает толстый кишечник, у большинства инфицированных кошек общее состояние организма хорошее, без системных нарушений (GOOKIN et al., 1999, 2001; TOLBERT & GOOKIN 2009), хотя у каждой пятой инфицированной кошки можно наблюдать анорексию, депрессию, потерю веса, рвоту и лихорадку (STOCKDALE et al., 2007).
Клинические признаки заболевания присутствуют в течение 5-24 месяцев, в среднем в течение 9 месяцев, после постановки диагноза (FOSTER et al., 2004). Степень выраженности клинических признаков варьируется от бессимптомных случаев до тяжелой диареи (FOSTER et al., 2004; GREY et al., 2010; XENOULIS et al., 2010).
Диагностика
Поскольку паразит имеет только фазу трофозоита, он не может быть идентифицирован в рутинными копропаразитологическими методами и не выдерживает охлаждения. Следовательно, диагностика инфекции T. foetus требует более специфического подхода (GOOKIN et al., 1999).
Диагноз может быть поставлен путем исследования мазка свежего кала (GOOKIN et al., 1999), высеиванием из фекалий на специфические питательные среды (GOOKIN et al., 2003) или при помощи ПЦР (GOOKIN et al., 2002); последний метод является наиболее широко используемым среди описанного в литературе. Кроме того, паразит может быть идентифицирован при помощи гистопатологического анализа биопсии кишечника (GOOKIN et al., 2001; YAEGER & GOOKIN, 2005).
| Подходящие образцы: |
| — свежий кал |
| — образцы, отобранные при помощи фекальной петли |
| — образцы, отобранные при помощи метода промывки толстой кишки, при котором приблизительно 10 мл стерильного физиологического раствора вводят через катетер в кишечник, а затем аспирируют (TOLBERT & GOOKIN, 2009; YAO & KOSTER, 2015) |
Образцы фекалий должны быть свежими, не содержать загрязняющего мусора и должны храниться без охлаждения до проведения анализа (TOLBERT & GOOKIN, 2009). Чтобы максимизировать чувствительность микроскопии и культивирования, анализ должен быть проведен в течение 6 часов после отбора материала (HALE et al., 2009).
Методы диагностики требуют наличия в кале паразитических трофозоитов. Колебания выхода трофозоитов характерны для венерического трихомоноза у крупного рогатого скота (SKIRROW et al., 1985). У кошек элиминация трофозоитов в кале, вероятно, тоже должна быть прерывистой (GOOKIN et al., 2001; STOCKDALE et al., 2008; HALE et al., 2009) и может быть снижена после терапии (GOOKIN et al., 1999; FOSTER и др., 2004; TOLBERT & GOOKIN, 2009).
Рис.1. Мазки фекалий 6-месячной кошки породы Мейн-кун с хронической диареей, окрашенные раствором Люголя (a-c) и окраской по Романовскому-Гимзе (d-f). (A), (d) — трофозоит Giardia duodenalis (Giardia lamblia); (b) и (e) — циста Giardia duodenalis (Giardia lamblia); (c) и (f) — трихомонады каплевидной формы (ув. х630) (Zanzani et al., 2016).
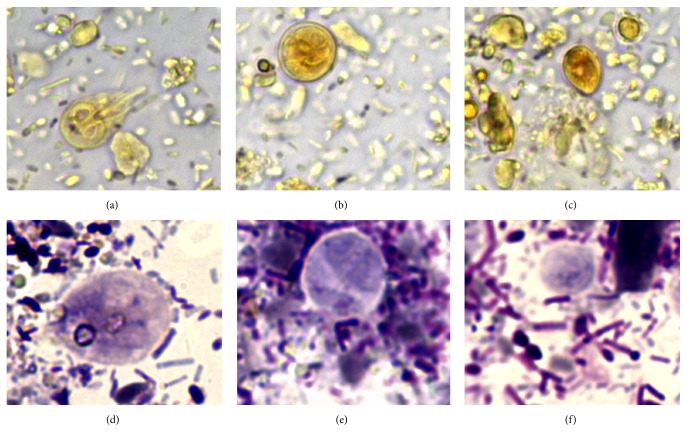
Рис.2. Трихомонады в мазках фекалий кошки, страдающей диареей. Наконечник стрелки на рис. (а) указывают на передние жгутики трофозоита, а наконечники стрелок на (b) указывает на волнистую мембрану (ув. х1000) (Zanzani et al., 2016).

Рис.3. Трихомонада в разбавленном физиологическим раствором свежем мазке фекалий кошки, страдающей диареей. Стрелки на (a) и (b) указывают на передние жгутики и волнообразную мембрану соответственно (ув. х630) (Zanzani et al., 2016).
Посев из кала — это чувствительный и специфический метод диагностики инфекции T. foetus у кошек (GOOKIN et al., 2003). Недостатком данного метода является то, что он требует жизнеспособных трофозоитов. При низких температурах и сухости среды T. foetus может умереть. Исследования показали, что фекалии, которых хранили при комнатной температуре не более 6 часов, представляют собой подходящий материал для диагностического исследования методом посева (HALE et al., 2009). Добавление физиологического раствора к фекалиям рекомендуется, если образец будет транспортироваться или храниться какое-то время до культивирования. Кроме того, в пробе фекалий не должно быть песка, т.к. он может привести к высыханию пробы и гибели паразита (GOOKIN et al., 2003).
ПЦР анализ считается специфическим и более чувствительным методом обнаружения T. foetus, поскольку он не требует жизнеспособных трофозоитов (GOOKIN et al., 2002; VERMEULEN, 2009). Gookin et al. (2004) установили чувствительность ПЦР метода в 94,4% (GOOKIN et al., 2004).
Трофозоиты T. foetus также могут быть обнаружены гистопатологическими методами, но их сохранение в образцах биопсии затруднено из-за их недолговечности. Yaeger и Gookin (2005) наблюдали паразитов в фиксированных формалином тканях ободочной кишки. Иммуногистохимия, флуоресценция и хромогенная гибридизация in situ представляют собой методы, разработанные для локализации и идентификации паразита в образцах тканей, содержащихся в формалине, но коммерчески недоступны (GOOKIN et al., 2010).
Лечение
Поиск эффективного и безопасного лечения инфекции T. foetus у кошек продолжается. Паразит продемонстрировал низкую чувствительность к нескольким противомикробным препаратам, используемых для лечения простейших, локализованных в кишечнике, и лечения трихомонозов влагалища человека, включая такие препараты как метронидазол и тинидазол (GOOKIN et al., 1999; ROMATOWSKI, 2000; GOOKIN et al., 2001; KATHER et al., 2007).
Ронидазол в настоящее время является «препаратом выбора» для лечения T. foetus (GOOKIN et al., 2006). Препарат быстро всасывается в проксимальном отделе тонкого кишечника, метаболизируется и выводится печенью и почками (ROSADO et al., 2007; LEVINE et al., 2011). Текущая рекомендуемая доза составляет 30 мг/кг один раз в день в течение 14 дней (LEVINE et al., 2011). Высокие дозы ронидазола ассоциированы с симптомами нейротоксичности; ее признаки отмечаются через три дня после начала лечения и прекращаются в течение одной-четырех недель после отмены препарата (ROSADO et al., 2007). Нейротоксические эффекты зависят от дозы и могут быть связаны с длительным периодом полувыведения препарата. У кошек с нейротоксичностью можно наблюдать потерю аппетита, психические изменения, летаргию, атаксию, тремор морды, гиперестезию, слабость тазовых конечностей и иногда судороги (LEVINE et al. 2011). Данным кошкам может потребоваться интенсивная ветеринарная поддержка для устранения побочных эффектов (ROSADO et al., 2007).
После приема препарата консистенция фекалий инфицированных кошек обычно быстро улучшается в течение нескольких дней и полностью нормализуется после двухнедельного лечения (GOOKIN et al., 2006; BURGENER et al., 2009; HOLLIDAY et al., 2009; BELL et al., 2010). В некоторых случаях у инфицированных кошек диарея может не проходить в течение нескольких недель после начала лечения из-за выраженного колита (TOLBERT & GOOKIN, 2009). Симптомы заболевания могут вернуться после лечения, так как не всегда происходит полное изгнание паразита (BURGENER et al., 2009; GOOKIN et al., 2010). Инфекция обычно проходит после повторного лечения (GOOKIN et al., 2006).
Исследования показали, что лечение другими лекарственными средствами, такими как фенбендазол, паромомицин, тинидазол, метронидазол и фуразолидон, улучшало консистенцию кала в течение всего периода лечения, но, т.к. возбудитель не был ликвидирован, диарея возвращалась после прекращения лечения (KATHER et al., 2007).
Прогноз
Прогноз по T. foetus хороший. У 88% кошек с диареей консистенция кала самостоятельно нормализуется через 2 года после заражения (FOSTER et al., 2004).
Средняя продолжительность диареи составляет 135 дней (XENOULIS et al., 2010). Однако самопроизвольное устранение T. foetus встречается редко. Рецидивирующая диарея, связанная со стрессом или изменениями во флоре кишечника, является распространенным явлением (FOSTER et al., 2004). Кроме того, исследования показывают, что хроническая инфекция может предрасполагать кошек к воспалительным процессам в кишечнике (GOOKIN et al., 2001).
Профилактика
Котята и молодые животные, выращенные в условиях агломерации, более подвержены инфекции из-за стресса или иммунной незрелости. Таким образом, минимизация стресса и избежание скученности являются важными факторами для снижения вероятности развития трихомоноза. Как упоминалось ранее, паразит стабилен и жизнеспособен в окружающей среде в течение нескольких дней, что подчеркивает необходимость хорошей дезинфекции лежаков, транспортных сумок и туалетов (HALE et al., 2009).
Заключение
Кошачий трихомоноз является относительно новой проблемой ветеринарной медицины и вызывается паразитом T. foetus. Болезнь может протекать бессимптомно или в виде хронической диареи. Диагноз может быть сложным, так как требует более специфических исследований. К сожалению, микроскопия в большинстве ветеринарных клиник все еще не является рутиной. Знание этой новой болезни важно для постановки верного диагноза и правильного лечения.
References
Adl SM, Simpson AG, Farmer MA, Andersen RA, Anderson OR, Barta JR, et al. The new higher level classification of eukaryotes with emphasis on the taxonomy of protists. J Eukaryot Microbiol 2005; 52(5): 399-451. http://dx.doi.org/10.1111/j.1550-7408.2005.00053.x. PMid:16248873.
Arranz-Solís D, Pedraza-Díaz S, Miró G, Rojo-Montejo S, Hernández L, Ortega-Mora LM, et al. Tritrichomonas foetus infection in cats with diarrhea from densely housed origins. Vet Parasitol 2016; 221: 118-122. ttp://dx.doi.org/10.1016/j.vetpar.2016.03.019. PMid:27084482.
Barr SC. Enteric protozoal infections. In: Greene CE. Infectious diseases of the dog and cat. 2nd ed. Philadelphia: WB Saunders; 1998. p. 482-91.
Bell ET, Gowan RA, Lingard AE, McCoy RJ, Slapeta J, Malik R. Naturally occurring Tritrichomonas foetus infections in Australian cats: 38 cases. J Feline Med Surg 2010; 12(12): 889-898. http://dx.doi.org/10.1016/j. jfms.2010.06.003. PMid:20817588.
Bissett SA, Gowan RA, O’Brien CR, Stone MR, Gookin JL. Feline diarrhoea associated with Tritrichomonas foetus and Giardia co-infection in an Australian cattery. Aust Vet J 2008; 86(11): 440-443. http://dx.doi. org/10.1111/j.1751-0813.2008.00356.x. PMid:18959533.
Bissett SA, Stone ML, Malik R, Norris JM, O’Brien C, Mansfield CS, et al. Observed occurrence of Tritrichomonas foetus and other enteric parasites in Australian cattery and shelter cats. J Feline Med Surg 2009; 11(10): 803-807. http://dx.doi.org/10.1016/j.jfms.2009.02.001. PMid:19285895.
BonDurant RH, Campero CM, Anderson ML, Van Hoosear KA. Detection of Tritrichomonas foetus by polymerase chain reaction in cultured isolates, cervicovaginal mucus, and formalin-fixed tissues from infected heifers and fetuses. J Vet Diagn Invest 2003; 15(6): 579-584.http://dx.doi.org/10.1177/104063870301500613. PMid:14667024.
Brugerolle G, Lee J. Phylum Parabasalia. In: Lee J, Leedale G, Bradbury P (eds.). The Illustrated Guide to the Protozoa. 2nd ed. Society of Protozoologists, Lawrence; 2000. p. 1196-1210.
Brumpt E. Recherches morphologiques et expérimentales sur le Trichomonas felis Da Cunha et Muniz, 1922, parasite du chat et du chien. Ann Parasitol Hum Comp 1925; 3(3): 239-251. http://dx.doi.org/10.1051/ parasite/1925033239.
Burgener I, Frey CF, Kook P, Gottstein B. Tritrichomonas foetus: a new intestinal parasite in Swiss cats. Schweiz Arch Tierheilkd 2009; 151(8): 383- 389. http://dx.doi.org/10.1024/0036-7281.151.8.383. PMid:19653162.
Burgess DE, McDonald CM. Analysis of adhesion and cytotoxicity of Tritrichomonas foetus to mammalian cells by use of monoclonal antibodies. Infect Immun 1992; 60(10): 4253-4259. PMid:1398936.
Ceplecha V, Svoboda M, Cepicka I, Husnik R, Horackova K, Svobodova V. InPouchTM TF-Feline medium is not specific for Tritrichomonas foetus. Vet Parasitol 2013; 196(3-4): 503-505. http://dx.doi.org/10.1016/j. vetpar.2013.04.015. PMid:23643452.
CeplechaV, SvobodovaV, Lendon C, Husnik R, Horackova K, Svoboda M. A survey of feline trichomonosis suggests a low incidence of Tritrichomonas blagburni among cats in the Czech Republic. Vet Med 2017; 62(5): 269- 273. http://dx.doi.org/10.17221/106/2016-VETMED.
Clothier KA, Villanueva M, Torain A, Hult C, Wallace R. Effects of bacterial contamination of media on the diagnosis of Tritrichomonas foetus by culture and real-time PCR. Vet Parasitol 2015; 208(3-4): 143- 149. http://dx.doi.org/10.1016/j.vetpar.2015.01.006. PMid:25639514.
Dąbrowska J, Karamon J, Kochanowski M, Jędryczko R, Cencek T. Tritrichomonas foetus infection in cat — first detection in Poland. Acta Parasitol 2015; 60(4): 605-608. http://dx.doi.org/10.1515/ap-2015- 0084. PMid:26408578.
DaCunha AM, Muniz J. Sobre um flagellado parasito do gato. Trab Inst Oswaldo Cruz 1922; 36: 285-286.
Dahlgren SS, Gjerde B, Pettersen HY. First record of natural Tritrichomonas foetus infection of the feline uterus. J Small Anim Pract 2007; 48(11): 654-657. http://dx.doi.org/10.1111/j.1748-5827.2007.00405.x. PMid:17725583.
Dimski DS. Helminth and noncoccidial protozoan parasites of the gastrointestinal tract. In: Sherding RG, editors. The Cat: Diseases and Clinical Management, 2nd ed. New York: Churchill Livingstone; 1989. p. 459-477.
Doi J, Hirota J, Morita A, Fukushima K, Kamijyo H, Ohta H, et al. Intestinal Tritrichomonas suis (=T. foetus) infection in Japanese cats. J Vet Med Sci 2012; 74(4): 413-417. http://dx.doi.org/10.1292/jvms.11- 0171. PMid:22104396.
Duarte RP, Rocha PRDA, Nakamura AA, Cipriano RS, Viol MA, Melo GD, et al. Detection of natural occurrence of Tritrichomonas foetus in cats in Araçatuba, São Paulo, Brazil. Pesq Vet Bras 2018; 38(2): 309-314. http://dx.doi.org/10.1590/1678-5150-pvb-5115.
Felleisen RS, Lambelet N, Bachmann P, Nicolet J, Muller N, Gottstein B. Detection of Tritrichomonas foetus by PCR and DNA enzyme immunoassay based on rRNA gene unit sequences. J Clin Microbiol 1998; 36(2): 513- 519. PMid:9466768.
Felleisen RS. Comparative sequence analysis of 5.8S rRNA genes and internal transcribed spacer (ITS) regions of trichomonadid protozoa. Parasitology 1997; 115(Pt 2): 111-119. http://dx.doi.org/10.1017/ S0031182097001212. PMid:10190167.
Felleisen RS. Host-parasite interaction in bovine infection with Tritrichomonas foetus. Microbes Infect 1999; 1(10): 807-816. http://dx.doi.org/10.1016/ S1286-4579(99)80083-5. PMid:10816086.
Foster DM, Gookin JL, Poore MF, Stebbins ME, Levy MG. Outcome of cats with diarrhea and Tritrichomonas foetus infection. J Am Vet Med Assoc 2004; 225(6): 888-892. http://dx.doi.org/10.2460/javma.2004.225.888. PMid:15485048.
Frey CF, Schild M, Hemphill A, Stünzi P, Müller N, Gottstein B, et al. Intestinal Tritrichomonas foetus infection in cats in Switzerland detected by in vitro cultivation and PCR. Parasitol Res 2009; 104(4): 783-788. http://dx.doi.org/10.1007/s00436-008-1255-2. PMid:18998166.
Gookin JL, Birkenheuer AJ, Breitschwerdt EB, Levy MG. Single-tube nested PCR for diagnosis of Tritrichomonas foetus in feline feces. J Vet Clin Microbiol 2002; 40(11): 4126-4130. http://dx.doi.org/10.1128/ JCM.40.11.4126-4130.2002. PMid:12409385.
Gookin JL, Birkenheuer AJ, St John V, Spector M, Levy MG. Molecular characterization of trichomonads from feces of dogs with diarrhea. J Parasitol 2005; 91(4): 939-943. http://dx.doi.org/10.1645/GE-474R.1. PMid:17089769.
Gookin JL, Breitschwerdt EB, Levy MG, Gager RB, Benrud JG. Diarrhea associated with trichomonosis in cats. J Am Vet Med Assoc 1999; 215(10): 1450-1454. PMid:10579040.
Gookin JL, Copple CN, Papich MG, Poore MF, Stauffer SH, Birkenheuer AJ, et al. Efficacy of ronidazole for treatment of feline Tritrichomonas foetus infection. J Vet Intern Med 2006; 20(3): 536-543. http://dx.doi. org/10.1111/j.1939-1676.2006.tb02893.x. PMid:16734086.
Gookin JL, Foster DM, Poore MF, Stebbins ME, Levy MG. Use of a commercially available culture system for diagnosis of Tritrichomonas foetus infection in cats. J Am Vet Med Assoc 2003; 222(10): 1376-1379. http://dx.doi.org/10.2460/javma.2003.222.1376. PMid:12762381.
Gookin JL, Hanrahan K, Levy MG. The conundrum of feline trichomonosis. J Feline Med Surg 2017; 19(3): 261-274. http://dx.doi. org/10.1177/1098612X17693499. PMid:28245739.
Gookin JL, Levy MG, Law JM, Papich MG, Poore MF, Breitschwerdt EB. Experimental infection of cats with Tritrichomonas foetus. Am J Vet Res 2001; 62(11): 1690-1697. http://dx.doi.org/10.2460/ajvr.2001.62.1690. PMid:11703009.
Gookin JL, Stauffer SH, Coccaro MR, Poore MF, Levy MG, Papich MG. Efficacy of tinidazole for treatment of cats experimentally infected with Tritrichomonas foetus. Am J Vet Res 2007; 68(10): 1085-1088. http:// dx.doi.org/10.2460/ajvr.68.10.1085. PMid:17916015.
Gookin JL, Stebbins ME, Hunt E, Burlone K, Fulton M, Hochel R, et al. Prevalence of and risk factors for feline Tritrichomonas foetus and Giardia infection. J Clin Microbiol 2004; 42(6): 2707-2710. http://dx.doi. org/10.1128/JCM.42.6.2707-2710.2004. PMid:15184456.
Gookin JL, Stone MR, Yaeger MJ, Meyerholz DK, Moisan P. Fluorescence in situ hybridization for identification of Tritrichomonas foetus in formalin-fixed and paraffin-embedded histological specimens of intestinal trichomoniasis. Vet Parasitol 2010; 172(1-2): 139-143. http://dx.doi. org/10.1016/j.vetpar.2010.04.014. PMid:20447769.
Grahn RA, BonDurant RH, van Hoosear KA, Walker RL, Lyons LA. An improved molecular assay for Tritrichomonas foetus. Vet Parasitol 2005; 127(1): 33-41. http://dx.doi.org/10.1016/j.vetpar.2004.08.018. PMid:15619373.
Gray SG, Hunter AS, Stone MR, Gookin JL. Assessment of reproductive tract disease in cats at risk for Tritrichomonas foetus infection. Am J Vet Res 2010; 71(1): 76-81. http://dx.doi.org/10.2460/ajvr.71.1.76. PMid:20043785.
Gunn-Moore DA, McCann TM, Reed N, Simpson KE, Tennant B. Prevalence of Tritrichomonas foetus infection in cats with diarrhoea in the UK. J Feline Med Surg 2007; 9(3): 214-218. http://dx.doi.org/10.1016/j. jfms.2007.01.003. PMid:17446107.
Gunn-Moore DA, Tennant B. Tritrichomonas foetus diarrhoea in cats. Vet Rec 2007; 160(24): 850-851. http://dx.doi.org/10.1136/vr.160.24.850-b. PMid:17575251.
Hale S, Norris JM, Slapeta J. Prolonged resilience of Tritrichomonas foetus in cat faeces at ambient temperature. Vet Parasitol 2009; 166(1-2): 60- 65. http://dx.doi.org/10.1016/j.vetpar.2009.07.032. PMid:19683398.
Ho MS, Conrad PA, Conrad PJ, LeFebvre RB, Perez E, BonDurant RH. BonDurant RH. Detection of bovine trichomoniasis with a specific DNA probe and PCR amplification system. J Clin Microbiol 1994; 32(1): 98-104. PMid:8126211.
Holliday M, Deni D, Gunn-Moore DA. Tritrichomonas foetus infection in cats with diarrhoea in a rescue colony in Italy. J Feline Med Surg 2009; 11(2): 131-134. http://dx.doi.org/10.1016/j.jfms.2008.06.004. PMid:18774326.
Hora AS, Miyashiro SI, Cassiano FC, Brandão PE, Reche-Junior A, Pena HFJ. Report of the first clinical case of intestinal trichomoniasis caused by Tritrichomonas foetus in a cat with chronic diarrhoea in Brazil. BMC Vet Res 2017; 13(1): 109. ttp://dx.doi.org/10.1186/s12917-017-1026- 3. Mid:28412947.
Hosein A, Kruth AS, Pearl DL, Richardson D, Maggs JC, Peach HA, et al. Isolation of Tritrichomonas foetus from cats sampled at a cat clinic, cat shows and a humane society in southern Ontario. J Feline Med Surg 2013; 15(8): 706-711. http://dx.doi.org/10.1177/1098612X13475617. PMid:23362340.
Jordan HE. Trichomonas spp. in feline: a case report. Vet Med 1956; 51: 23-24.
Kather EJ, Marks SL, Kass PH. Determination of the in vitro susceptibility of feline Tritrichomonas foetus to 5 Antimicrobial agents. J Vet Intern Med 2007; 21(5): 966-970. http://dx.doi.org/10.1111/j.1939-1676.2007. tb03050.x. PMid:17939550.
Kessel JF. Trichomoniasis in kittens. Trans R Soc Trop Med Hyg 1928; 22(1): 61-80. http://dx.doi.org/10.1016/S0035-9203(28)90155-8.
Kingsbury DD, Marks SL, Cave NJ, Grahn RA. Identification of Tritrichomonas foetus and Giardia spp. infection in pedigree show cats in New Zealand. N Z Vet J 2010; 58(1): 6-10. http://dx.doi.org/10.10 80/00480169.2010.65054. PMid:20200569.
Klein B, Langbein-Detsch I, Muller E, Heusinger A. Prävalenz von Tritrichomonas foetus in Kotproben von Katzen mit Durchfall aus Deutschland. Kleintiermedizin 2010; 7/8: 243-247.
Köster LS, Chow C, Yao C. Trichomonosis in cats with diarrhoea in Hong Kong, China, between 2009 and 2014. JFMS Open Rep 2015; 1(2): 2055116915623561. PMid:28491403.
Kuehner KA, Marks SL, Kass PH, Sauter-Louis C, Grahn RA, Barutzki D, et al. Tritrichomonas foetus infection in purebred cats in Germany: prevalence of clinical signs and the role of co-infection with other enteroparasites. J Feline Med Surg 2011; 13(4): 251-258. http://dx.doi. org/10.1016/j.jfms.2010.12.002. PMid:21288749.
LeVine DN, Papich MG, Gookin JL, Davidson GS, Davis JL, Hayes RB. Ronidazole pharmacokinetics after intravenous and oral immediate-release capsule administration in healthy cats. J Feline Med Surg 2011; 13(4): 244-250. http://dx.doi.org/10.1016/j.jfms.2010.12.001. PMid:21239199.
LeVine DN. Veterinary Protozoology, 1st ed. Ames: ISU Press; 1985.
Levy MG, Gookin JL, Poore M, Birkenheuer AJ, Dykstra MJ, Litaker RW. Tritrichomonas foetus and not Pentatrichomonas hominis is the etiologic agent of feline trichomonal diarrhea. J Parasitol 2003; 89(1): 99-104. http://dx.doi.org/10.1645/0022-3395(2003)089[0099:TFANPH]2.0. CO;2. PMid:12659310.
Lim S, Park SI, Ahn KS, Oh DS, Ryu JS, Shin SS. First report of feline intestinal trichomoniasis caused by Tritrichomonas foetus in Korea. Korean J Parasitol 2010; 48(3): 247-251. http://dx.doi.org/10.3347/ kjp.2010.48.3.247. PMid:20877505.
Lun ZR, Chen XG, Zhu XQ, Li XR, Xie MQ. Are Tritrichomonas foetus and Tritrichomonas suis synonyms? Trends Parasitol 2005; 21(3): 122-125. http://dx.doi.org/10.1016/j.pt.2004.12.001. PMid:15734659.
Mancianti F, Nardoni S, Mugnaini L, Zambernardi L, Guerrini A, Gazzola V, et al. A retrospective molecular study of select intestinal protozoa in healthy pet cats from Italy. J Feline Med Surg 2015; 17(2): 163-167. http:// dx.doi.org/10.1177/1098612X14533549. PMid:24793744.
Mardell EJ, Sparkes AH. Chronic diarrhoea associated with Tritrichomonas foetus infection in a British cat. Vet Rec 2006; 158(22): 765-766. http:// dx.doi.org/10.1136/vr.158.22.765. PMid:16751313.
Miró G, Hernández L, Montoya A, Arranz-Solís D, Dado D, Rojo-Montejo S, et al. First description of naturally acquired Tritrichomonas foetus infection in a Persian cattery in Spain. Parasitol Res 2011; 109(4): 1151- 1154. http://dx.doi.org/10.1007/s00436-011-2359-7. PMid:21509446.
Morin-Adeline V, Lomas R, O’Meally D, Stack C, Conesa A, Šlapeta J. Comparative transcriptomics reveals striking similarities between the bovine and feline isolates of Tritrichomonas foetus: consequences for in silico drug-target identification. BMC Genomics 2014; 15(1): 955. http:// dx.doi.org/10.1186/1471-2164-15-955. PMid:25374366.
Mostegl MM, Wetscher A, Richter B, Nedorost N, Dinhopl N, Weissenbock H. Detection of Tritrichomonas foetus and Pentatrichomonas hominis in intestinal tissue specimens of cats by chromogenic in situ hybridization. Vet Parasitol 2012; 183(3-4): 209-214. http://dx.doi.org/10.1016/j. vetpar.2011.07.050. PMid:21856079.
Mugnaini L, Papini R, Gorini G, Passantino A, Merildi V, Mancianti F. Pattern and predictive factors of endoparasitism in cats in Central Italy. Rev Med Vet 2012; 163(2): 89-94.
Paris JK, Wills S, Balzer HJ, Shaw D, Gunn-Moore D. Enteropathogen co-infection in UK cats with diarrhoea. BMC Vet Res 2014; 10(1): 13. http://dx.doi.org/10.1186/1746-6148-10-13. PMid:24410914.
Pereira-Neves A, Benchimol M. Tritrichomonas foetus: budding from multinucleated pseudocysts. Protist 2009; 160(4): 536-551. http://dx.doi.org/10.1016/j.protis.2009.05.001. PMid:19616999.
Pereira-Neves A, Ribeiro KC, Benchimol M. Pseudocysts in trichomonads — new insights. Protist 2003; 154(3-4): 313-329. http://dx.doi. org/10.1078/143446103322454095. PMid:14658492.
Pham D. Chronic intermittent diarrhea in a 14-month-old Abyssinian cat. Can Vet J 2009; 50(1): 85-87. PMid:19337620.
Polak KC, Levy JK, Crawford PC, LeuteneggerCM, Moriello KA. Infectious diseases in large-scale cat hoarding investigations. Vet J 2014; 201(2): 189-195. http://dx.doi.org/10.1016/j.tvjl.2014.05.020. PMid:24934262.
Profizi C, Cian A, Meloni D, Hugonnard M, Lambert V, Groud K, et al. Prevalence of Tritrichomonas foetus infections in French catteries. Vet Parasitol 2013; 196(1-2): 50-55. http://dx.doi.org/10.1016/j.vetpar.2013.01.021. PMid:23433647.
Queen EV, Marks SL, Farver TB. Prevalence of selected bacterial and parasitic agents in feces from diarrheic and healthy control cats from Northern California. J Vet Intern Med 2012; 26(1): 54-60. http://dx.doi. org/10.1111/j.1939-1676.2011.00843.x. PMid:22182203.
Raab O, Greenwood S, Vanderstichel R, Gelens H. A cross-sectional study of Tritrichomonas foetus infection in feral and shelter cats in Prince Edward Island, Canada. Can Vet J 2016; 57(3): 265-270. PMid:26933262.
Romatowski J. An uncommon protozoan parasite (Pentatrichomonas hominis) associated with colitis in three cats. Feline Pract 1996; 24(5): 10-14.
Romatowski J. Pentatrichomonas hominis infection in four kittens. J Am Vet Med Assoc 2000; 216(8): 1270-1272. http://dx.doi.org/10.2460/ javma.2000.216.1270. PMid:10767968.
Rosa IA, Souza W, Benchimol M. Changes in the structural organization of the cytoskeleton of Tritrichomonas foetus during trophozoite-pseudocyst transformation. Micron 2015; 73: 28-35. http://dx.doi.org/10.1016/j. micron.2015.03.008. PMid:25880467.
Rosado TW, Specht A, Marks SL. Neurotoxicosis in 4 cats receiving ronidazole. J Vet Intern Med 2007; 21(2): 328-331. http://dx.doi. org/10.1111/j.1939-1676.2007.tb02968.x. PMid:17427396.
Santos CS, Jesus VL, McIntosh D, Berto BP, Lopes CWG. Co-infection by Tritrichomonas foetus and Pentatrichomonas hominis in asymptomatic cats. Pesq Vet Bras 2015; 35(12): 980-988. http://dx.doi.org/10.1590/ S0100-736X2015001200007.
Schrey C, Mundhenk L, Gruber A, Henning K, Frey C. Tritrichomonas foetus as a cause of diarrhoea in three cats. Kleintierpraxis 2009; 54(2): 93-96.
Skirrow S, BonDurant R, Farley J, Correa J. Efficacy of ipronidazole against trichomoniasis in beef bulls. J Am Vet Med Assoc 1985; 187(4): 405-407. PMid:4030475.
Slapeta J, Craig S, McDonell D, Emery D. Tritrichomonas foetus from domestic cats and cattle are genetically distinct. Exp Parasitol 2010; 126(2): 209-213. http://dx.doi.org/10.1016/j.exppara.2010.04.024. PMid:20438726.
Stauffer SH, Birkenheuer AJ, Levy MG, Marr H, Gookin JL. Evaluation of four DNA extraction methods for the detection of Tritrichomonas foetus in feline stool specimens by polymerase chain reaction. J Vet Diagn Invest 2008; 20(5): 639-641. http://dx.doi.org/10.1177/104063870802000518. PMid:18776100.
Steiner JM, Xenoulis PG, Read SA, Suchodolski JS, Globokar M, Huisinga E, et al. Identification of Tritrichomonas foetus DNA in feces from cats with diarrhea from Germany and Austria. J Vet Intern Med 2007; 21(3): 649.
Stockdale H, Rodning S, Givens M, Carpenter D, Lenz S, Spencer J, et al. Experimental infection of cattle with a feline isolate of Tritrichomonas foetus. J Parasitol 2007; 93(6): 1429-1434. http://dx.doi.org/10.1645/ GE-1305.1. PMid:18314690.
Stockdale HD, Dillon AR, Newton JC, Bird RC, Bondurant RH, Deinnocentes P, et al. Experimental infection of cats (Felis catus) with Tritrichomonas foetus isolated from cattle. Vet Parasitol 2008; 154(1-2): 156-161. http://dx.doi.org/10.1016/j.vetpar.2008.02.024. PMid:18394809.
Stockdale HD, Givens MD, Dykstra CC, Blagburn BL. Tritrichomonas foetus infections in surveyed pet cats. Vet Parasitol 2009; 160(1-2): 13- 17. http://dx.doi.org/10.1016/j.vetpar.2008.10.091. PMid:19070434.
Stockdale HD, Spencer JA, Dykstra CC, Blagburn BL, West GS, Hankes T, et al. Feline trichomoniasis: an emerging disease? Compend Contin Educ Vet 2006; 28(6): 463-471.
Sun Z, Stack C, Slapeta J. Sequence differences in the diagnostic region of the cysteine protease 8 gene of Tritrichomonas foetus parasites of cats and cattle. Vet Parasitol 2012; 186(3-4): 445-449. http://dx.doi.org/10.1016/j. vetpar.2011.12.001. PMid:22204891.
Tachezy J, Tachezy R, Hampl V, Sedinová M, Vanacová S, Vrlík M, et al. Cattle pathogen Tritrichomonas foetus (Riedmuller, 1928) and pig commensal Tritrichomonas suis (Gruby & Delafond, 1843) belong to the same species. J Eukaryot Microbiol 2002; 49(2): 154-163. http:// dx.doi.org/10.1111/j.1550-7408.2002.tb00360.x. PMid:12046599.
Tanabe M. Morphological studies on trichomonas. J Parasitol 1926; 12(3): 120-130. http://dx.doi.org/10.2307/3271220.
Tolbert MK, Gookin JL. Mechanisms of Tritrichomonas foetus Pathogenicity in Cats with Insights from Venereal Trichomonosis. J Vet Intern Med 2016; 30(2): 516-526. http://dx.doi.org/10.1111/jvim.13920. PMid:26946069.
Tolbert MK, Gookin JL. Tritrichomonas foetus: A new agent of feline diarrhea. Compend Contin Educ Vet 2009; 31(8): 374-381, 390, quiz 381. PMid:19866444.
Tysnes K, Gjerde B, Nodtvedt A, Skancke E. A cross-sectional study of Tritrichomonas foetus infection among healthy cats at shows in Norway. Acta Vet Scand 2011; 53(1): 39. http://dx.doi.org/10.1186/1751-0147- 53-39. PMid:21689400.
Van der Saag M, McDonell D, Slapeta J. Cat genotype Tritrichomonas foetus survives passage through the alimentary tract of two common slug species. Vet Parasitol 2010; 177(3-4): 262-266. http://dx.doi.org/10.1016/j. vetpar.2010.11.054. PMid:21185122.
van Doorn DC, De Bruin MJ, Jorritsma RA, Ploeger HW, Schoormans A. Prevalence of Tritrichomonas foetus among Dutch cats. Tijdschr Diergeneeskd 2009; 134(17): 698-700. PMid:19774881.
Vermeulen BD. Tritrichomonas foetus in young cats with chronic diarrhoea: Comparison of different diagnostic methods [PhD Thesis]. Utrecht: Utrecht University; 2009.
Veronesi F, Gazzonis AL, Napoli E, Brianti E, Santoro A, Zanzani SA, et al. Cross-sectional survey on Tritrichomonas foetus infection in Italian cats. Vet Parasitol Reg Stud Rep 2016; 6: 14-19.
Walden HS, Dykstra C, Dillon A, Rodning S, Givens D, Bird R, et al. A new species of Tritrichomonas (Sarcomastigophora: Trichomonida) from the domestic cat (Felis catus). Parasitol Res 2013; 112(6): 2227- 2235. http://dx.doi.org/10.1007/s00436-013-3381-8. PMid:23525691.
Warton̄a A, Honigberg BM. Structure of trichomonads as revealed by scanning electron microscopy. J Protozool 1979; 26(1): 56-62. http:// dx.doi.org/10.1111/j.1550-7408.1979.tb02732.x. PMid:314517.
Xenoulis PG, Lopinski DJ, Read SA, Suchodolski JS, Steiner JM. Intestinal Tritrichomonas foetus infection in cats: a retrospective study of 104 cases. J Feline Med Surg 2013; 15(12): 1098-1103. http://dx.doi. org/10.1177/1098612X13495024. PMid:23838083.
Xenoulis PG, Saridomichelakis MN, Read SA, Suchodolski JS, Steiner JM. Detection of Tritrichomonas foetus in cats in Greece. J Feline Med Surg 2010; 12(10): 831-833. http://dx.doi.org/10.1016/j.jfms.2010.05.010. PMid:20674428.
Yaeger MJ, Gookin JL. Histologic features associated with Tritrichomonas foetus induced colitis in domestic cats. Vet Pathol 2005; 42(6): 797-804. http://dx.doi.org/10.1354/vp.42-6-797. PMid:16301576.
YaoC, Koster L, Halper B, DundasJ, Nair R. Failure to detect Tritrichomonas foetus in a cross-sectional survey in the populations of feral cats and owned outpatient cats on St Kitts, West Indies. JFMS Open Rep 2018; 4(1); 1-6. PMid:30202541.
Yao C, Koster LS. Tritrichomonas foetus infection, a cause of chronic diarrhea in the domestic cat. Vet Res 2015; 46(1): 35. http://dx.doi. org/10.1186/s13567-015-0169-0. PMid:25880025.
Zanzani SA, Gazzonis AL, Scarpa P, Olivieri E, Balzer HJ, Manfredi MT. Coinfection with Tritrichomonas foetus and Giardia duodenalis in Two Cats with Chronic Diarrhea. Case Rep Vet Med. 2016 Sep 6;2016:5705168. doi: 10.1155/2016/5705168. PMID: 29955418; PMCID: PMC6005279
Источник: What is known about Tritrichomonas foetus infection in cats? Bastos BF, Almeida FM, Brener B. Rev Bras Parasitol Vet. 2019 Jan-Mar;28(1):1-11. doi: 10.1590/S1984-29612019005. Epub 2019 Mar 11. PMID: 30892464
Назад
Введение
Ветеринарным врачам общей практики часто приходится наблюдать молодых кошек по поводу диареи. Врачи обычно включают в дифференциальный диагноз диареи паразитарные заболевания кишечника, и таких пациентов часто эмпирически лечат противопаразитарными препаратами, не проводя дообследования. Во многих случаях такой подход эффективен, поскольку обеспечивает относительно быстрое улучшение состояния и купирование симптомов. Хотя инфекция родом Giardia и различными гельминтами обычно полностью купируется этими препаратами, менее часто диагностируемую Tritrichomonas foetus, простейшее, по внешнему виду аналогичное роду Giardia, при таком эмпирическом лечении полностью устранить невозможно. Этот паразит может стать причиной фрустрации у владельцев кошек и ветеринарных врачей, поскольку симптомы вначале могут отвечать на терапию стандартными противопаразитарными препаратами, но после прекращения лечения быстро рецидивировать. Кроме того, без специальной диагностики этих простейших иногда сложно выявить. Поэтому вполне вероятно, что повышение уровня информированности об этом возбудителе позволит быстрее его выявлять и эффективнее элиминировать у молодых кошек с отсутствием явной реакции на лечение или при рецидиве диареи.
Заболеваемость, распространенность и предрасположенность
Tritrichomonas foetus (T. foetus) распространена по всему миру, с расчетным показателем распространенности 10-59% (1). Данных о географической распространенности сравнительно мало; однако в одном популяционном исследовании кошек в Великобритании рассчитали, что носителями этого простейшего могут быть примерно 20% здоровых кошек, а в отдельном исследовании распространенности T. foetus в образцах кала при диарее, поступивших в лаборатории Великобритании, паразита выявляли в 14,4% образцов (2). С другой стороны, в исследовании группы кошек в США, участвующих в выставках, распространенность инфекции T. foetus оказалась выше и составила 31% (3). Распространенность T. foetus наиболее высока у чистопородных кошек и у кошек, содержащихся в группах. Было показано, что вероятность носительства повышается по мере повышения количества животных на квадратный метр площади в местах их содержания – таким образом, скученность, по-видимому, является одним из важных факторов риска. Аналогичным образом, повышенный риск инфицирования выявлен при использовании общих туалетных лотков и при вылизывании животными друг друга (2,3). Вызываемая T. foetus диарея обычно наблюдается у молодых кошек (в среднем в возрасте до 8 месяцев), причем более 75% случаев поражения происходят в возрасте менее одного года. Однако риск носительства сохраняется для кошек любого возраста, и в части случаев могут развиваться клинические признаки заболевания (1,4).е:
Этиология и патогенез
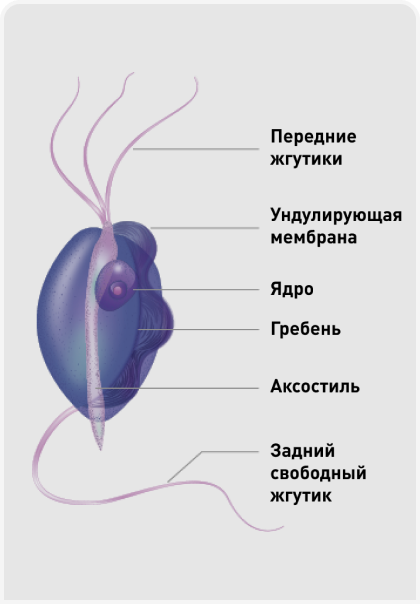
Рисунок 1. T. foetus – микроорганизм длиной 10-26 мкм и шириной 3-5 мкм, форму которого часто описывают как «грушевидную» или «веретенообразную». У каждого микроорганизма имеется три передних жгутика, обеспечивающих ему подвижность..
T. foetus представляет собой жгутиковое простейшее, существующее только в форме трофозоита. Таким образом, оно не формирует цист (в отличие от лямблий) и размножается путем простого деления надвое. Визуально микроорганизмы имеют длину примерно 10-26 мкм и ширину примерно 3-5 мкм, и их форму часто называют «грушевидной» или «веретенообразной». Каждый микроорганизм имеет три передних жгутика (по сравнению с родом Pentatrichomonas, имеющим пять жгутиков), обеспечивающих этому простейшему подвижность (Рисунок 1) (1,5). У кошек T. foetus паразитирует в основном в желудочно-кишечном тракте, локализуясь преимущественно в толстой кишке и, в меньшей степени, в дистальной части подвздошной кишки (6). Инвазия вызывает воспаление слизистой, проявляющееся лимфоплазмоцитарным или нейтрофильным колитом (7). Другие неоднократно описанные клинические признаки – раздражение анальной области и возможное недержание кала. При инвазии в толстой кишке простейшие находятся в непосредственной близости от поверхности слизистой кишечника и часто связываются с эпителиальными клетками и криптами слизистой толстой кишки. При контакте с кишечной стенкой микроорганизмы связываются в ней путем специфичного лиганд-рецепторного взаимодействия, причем это связывание конкурентное и насыщаемое.
Микроорганизм связывается с различными молекулами на поверхности клеток, включая лектины сиаловой кислоты, липофосфогликаны, цистеиновые протеазы, белки адгезии. После связывания микроорганизмы становятся способны разрушать молекулы иммуноглобулинов и лактоферринов, тем самым уклоняясь от действия иммунной системы (8). Паразит передается почти исключительно фекально-оральным путем. Трофозоиты выделяются с фекалиями инфицированных кошек и в этой форме при попадании в организм другой кошки могут вызывать инфицирование. В настоящее время точно неизвестно, имеются ли у этого паразита промежуточные хозяева, однако показано, что трофозоиты T. foetus могут сохранять жизнеспособность при проглатывании и транзите через кишечник наземных брюхоногих моллюсков, таких как слизни, и при последующем проглатывании восприимчивой кошкой сохраняют инфекционность (Рисунок 2) (9). В окружающей среде трофозоиты могут выживать несколько дней, если остаются во влажных каловых массах, однако в сухих и аэробных условиях высыхают и погибают (10).
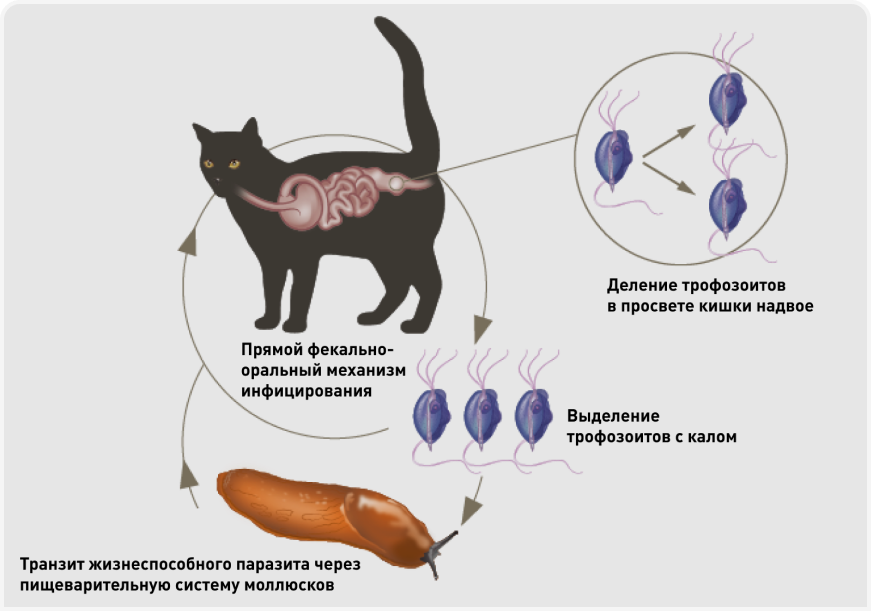
Рисунок 2. Жизненный цикл T. foetus обычно прямой (фекально-оральное инфицирование), хотя описаны случаи заражения при проглатывании трофозоитов после их прохождения через пищеварительный тракт моллюсков..
Клинические проявления
Поражаются кошки любого возраста, породы и пола. Обычно заболевание клинически проявляется хронической толстокишечной диареей с периодическими обострениями и ремиссиями. Диарея часто полуоформленная («коровьей лепешкой»), но иногда водянистая, и в некоторых случаях может содержать свежую кровь и/или слизь. Нередко развивается тенезм, у некоторых животных периодически имеет место частичное недержание кала. Кал во многих случаях также может иметь выраженный неприятный запах. Вследствие диареи и обусловленного ею регулярного вылизывания (Рисунок 3) часто развиваются выраженные эритема и отек промежности и заднего прохода, болезненные для кошки; реже воспаление и тенезм приводят к выпадению прямой кишки (1,5). Других клинических проявлений, помимо диареи и воспаления в области промежности, в большинстве случаев не выявляют. В ряде случаев описана некоторая задержка в росте, и у отдельных пациентов отмечают снижение массы тела относительно нормы. Также описаны общие неспецифические проявления, такие как ухудшение состояния шерстного покрова, но специфичных клинических симптомов не описано (1,5).

Рисунок 3. Диарея у кошки может привести к чрезмерному вылизыванию, и в результате – к развитию выраженных эритемы и отека в области промежности.
Диагностика
Подозрение на инфекцию Tritrichomonas foetus должно возникать при выявлении соответствующих этому заболеванию данных анамнеза и клинических проявлений. Перечень дифференциальных диагнозов представлен в Таблице 1, и для дифференциации T. foetus от указанных патологий требуется провести тщательное клиническое обследование. Данные стандартных исследований крови в случае T. foetus обычно неспецифичны, и часто все параметры остаются в пределах нормы. Однако, поскольку риск инфекции T. foetus повышен в основном для молодых пациентов, при выявлении отклонений в анализе крови у молодых животных важно не допустить гипердиагностики (например, при выявлении повышения уровней щелочной фосфатазы и фосфата). Некоторые изменения могут также быть вторичными на фоне хронических клинических проявлений заболевания. Наиболее часто в таких случаях выявляют изменения уровней электролитов, особенно гипокалиемию, гипонатриемию и гипохлоремию, в результате продолжающейся диареи. Как правило, они легкие и субклинические, однако при более тяжелом течении болезни могут произойти и более глубокие изменения (1,5). Хотя при анализе крови невозможно выявить какие-либо специфичные для инфекции T. foetus изменения, это исследование остается ценной частью диагностического обследования, поскольку позволяет исключить дифференциальные диагнозы, выявить сопутствующие заболевания и оценить электролитные изменения, которые необходимо купировать в рамках плана лечения. Как и при анализе крови, при использовании методов визуальной диагностики у кошек с инфекцией T. foetus выявляют сравнительно немного специфичных данных (5). При тяжелом течении с развитием выраженного колита при УЗИ органов брюшной полости можно выявить признаки утолщения слизистой кишечника (локального или диффузного), хотя отсутствие таких данных не исключает диагноза паразитарной инвазии. При выявлении утолщения кишечной стенки ее слои обычно остаются сохранными; в противном случае следует в большей степени подозревать не инфекцию T. foetus, а поражение инфильтративной опухолью.Как и при анализе крови, в таких случаях имеются веские основания использовать один из методов визуальной диагностики. Отсутствие других клинических данных косвенно свидетельствует в пользу диагноза инфекции T. foetus, и «визуализация» оказывается ценным методом исследования для дифференциальной диагностики.

Таблица 1. Перечень дифференциальных диагнозов при толстокишечной диарее у кошек.
Окончательный диагноз
Окончательный диагноз инфекции T. foetus можно установить либо при прямой визуализации микроорганизма, либо при исследовании кала методом полимеразной цепной реакции (ПЦР). Перед приготовлением мазка или проведением ПЦР для увеличения числа микроорганизмов также можно провести культивирование кала, увеличив таким образом чувствительность этих методов. Прямую визуализацию проводят с помощью световой микроскопии мазка кала. Этот метод исследования относительно простой; требуются только световой микроскоп и мазки, и его считают идеальным методом первого ряда для выявления T. foetus. Поэтому его следует применять во всех случаях первичного выявления у кошек толстокишечной диареи. При анализе мазка кала важно, что при световой микроскопии микроорганизмы родов Giardia и Pentatrichomonas hominis могут быть очень сходны с T. foetus, и поэтому затем следует провести точное определение всех визуализированных видов паразитов (3,11).
Это правило важно главным образом для принятия решений по лечению, поскольку простейшие P. hominis непатогенны и лечения не требуют (1), в то время как лямблиоз, как правило, реагирует на лечение значительно лучше, чем T. foetus, и обычно его можно купировать обычными противопаразитарными препаратами (например, фенбендазолом), в отличие от инфекции T. foetus. Мазки можно получить из образцов нескольких типов. Проще всего получить образцы из самопроизвольно выделенного кала; однако если пациент отказывается испражняться в условиях клиники, образцы кала можно успешно получить альтернативными методами. Важно отметить, что исследование образцов нормального кала (в отсутствие диареи) редко позволяет получить положительные результаты, поэтому проводить исследование таких образцов не рекомендуется (1).
Опытным путем установлено, что адекватными методами получения образцов служат извлечение кала из просвета толстой кишки ректальной петлей и промывание толстой кишки (1). Промывание кишечника проводят аналогично промыванию (лаважу) трахеи, обеспечив седацию кошки и вливая в прямую и ободочную кишки жидкость. После инстилляции жидкости для облегчения ее перемешивания можно осторожно пропальпировать толстую кишку через брюшную стенку, и только затем извлекать жидкость. Это позволяет получать образцы двух типов: первый – взвесь, каплю которой можно поместить на предметное стекло и получить влажный препарат для прямой световой микроскопии; второй – более крупный образец для центрифугирования, позволяющий сформировать гранулу для последующего исследования методом ПЦР.
Мазок кала для микроскопии получают по методике приготовления влажного препарата. Из промывных образцов содержимого толстой кишки берут каплю, которую можно сразу же поместить на предметное стекло и высушить на воздухе. Образцы из выделенных при диарее каловых масс или полученные ректальной петлей сначала следует взвесить в стерильном физиологическом растворе, и только затем продолжать процедуру получения образца. После высыхания образец можно фиксировать и непосредственно в процедурной окрасить по Романовскому, чтобы облегчить визуализацию паразитов. После закрытия покровным стеклом образец затем можно просматривать под световым микроскопом при 20-40-кратном увеличении. Чтобы облегчить выявление паразитов, можно опустить конденсор ниже.
Образцы кала для мазка необходимо исследовать свежими (в течение шести часов после получения) (10), поэтому перевозить их во внешнюю лабораторию неоптимально. После шести часов диагностическая чувствительность выявления T. foetus в мазках кала начинает снижаться, поэтому исследование рекомендуется проводить в процедурной сразу же после приготовления мазка (12). Метод исследования мазка кала очень прост, недорог и обеспечивает очень высокую специфичность диагностики (то есть явное выявление паразита означает, что он с высокой вероятностью присутствует); однако чувствительность этого метода невысока. При количественном исследовании для определения этого показателя обнаружили, что чувствительность однократного исследования мазка кала может составлять лишь 14%, и поэтому настоятельно рекомендуется, чтобы повысить вероятность выявления микроорганизма, оценивать несколько мазков из нескольких образцов (3). Чувствительность может дополнительно снижаться при присутствии в образце загрязнителей, таких как гигиенический наполнитель для лотков, и поэтому в случаях направления образцов во внешние лаборатории важно до отправления отделить такие загрязнители от образца (12). Также чувствительность тестирования уменьшается при антимикробном лечении (например, метронидазолом), и уменьшить влияние такого лечения можно, отменив по крайней мере за несколько дней до исследования все виды антибактериальной терапии (1).
«
Повышение уровня информированности о возбудителе Tritrichomonas foetus позволит быстрее его выявлять и эффективнее элиминировать у молодых кошек с отсутствием явной реакции на лечение или при рецидиве диареи
Дэн Томпсон
Альтернативным методом диагностики инфекции T. foetus в кале считают ПЦР. Это исследование можно провести в качестве исследования первого ряда, но оно дороже и занимает больше времени, чем визуальный анализ мазка кала, и поэтому часто его назначают после получения отрицательного результата микроскопии мазка. Ввиду низкой чувствительности микроскопии мазка кала во всех случаях подозрения на инфекцию T. foetus, не идентифицированным при микроскопии, показано проведение ПЦР кала. Этот метод также можно использовать для подтверждения диагноза по данным микроскопии мазка, если точность идентификации паразита вызывает сомнение.
Метод ПЦР основан на обнаружении какого-либо из целого ряда высококонсервативных регионов генома T. foetus; чаще всего используют праймеры для генов ITS1 и ITS2 (13). Метод ПЦР позволяет обнаруживать живых и мертвых паразитов, и для их обнаружения оказалось достаточно иметь в образце 10 микроорганизмов (14). Чувствительность метода ПЦР не описана, однако предполагается, что она может быть значительно выше, чем у микроскопии мазка кала. Также она может изменяться в зависимости от плотности микроорганизмов в образце, причем увеличение количества отдельных паразитов приводит к повышению чувствительности. Важная особенность метода ПЦР – высокая специфичность для выявления возбудителей рода Tritrichomonas. Это означает, что при носительстве Giardia или Pentatrichomonas у кошки диагноз по данным микроскопии мазка может быть неверно истолкован как инфекция T. foetus, но при ПЦР эти другие паразиты не будут обнаружены, кроме случаев сочетанной инфекции ими и T. Foetus (11). Таким образом, ПЦР служит ценным подтверждающим методом после идентификации паразита при микроскопии мазка, и поэтому во всех случаях настоятельно рекомендуется наряду с микроскопией мазка кала проводить ПЦР (15).
Образцы для ПЦР можно получать аналогично используемым для получения мазка кала. Опять же, рекомендуется объединить несколько образцов за несколько дней, и для увеличения чувствительности исследования анализировать их совместно, поскольку описано непостоянное выделение паразита в кале (7). Образцы материала диареи можно направлять в свежем виде, либо центрифугировать образцы промывания толстой кишки, получать гранулы и направлять для анализа уже их. Хотя чувствительность ПЦР выше, чем микроскопии мазка кала, из-за небольшого числа микроорганизмов в образцах этот метод также может приводить к ложноотрицательным результатам. Чтобы повысить его чувствительность, требуется большее количество организмов, и одним из решений может быть культивирование микроорганизма перед исследованием.
Рисунок 4. Коммерческий набор для культивирования T. foetus в образцах кала доступен во многих странах.
Выпускается коммерческий набор (Рисунок 4) для культивирования T. foetus в образцах кала.1 Этот набор представляет собой закрытый блок, в который требуется внести очень небольшую гранулу кала (размером примерно с рисовое зернышко). Культивировать образцы требуется около 72 часов при температуре 37°C, и до 12 дней при комнатной температуре (16). Недостатком этого метода является заметное увеличение общего времени диагностики, однако ему также свойствен ряд преимуществ. Во-первых, увеличение количества микроорганизмов увеличивает чувствительность микроскопии и ПЦР мазка кала. Во-вторых, набор также содержит ряд ингибиторов роста, подавляющих одновременный рост родов Giardia и Pentatrichomonas. Эти ингибиторы предотвращают рост обоих паразитов, поэтому все обнаруженные в мазке кала простейшие после культивирования с очень высокой вероятностью окажутся T. foetus, а не другими сходными паразитами (16). С учетом вышеупомянутой информации, «золотым стандартом» исследования на Tritrichomonas foetus следует считать культивирование кала с последующей прямой микроскопией мазка и ПЦР образца кала. 1InPouch TF (Biomed Diagnostics, Уайт-сити, штат Орегон, США).
Лечение
Процесс лечения и элиминирования T. foetus может оказаться сложным и разочаровывающим. Начального клинического эффекта часто удается достичь после курса терапии метронидазолом, но этот препарат не позволяет элиминировать инфекцию, поэтому, несмотря на первоначальное клиническое улучшение, после отмены препарата диарея рецидивирует (12). Фактически лечение метронидазолом увеличивает общую продолжительность сохранения клинических проявлений заболевания, поэтому при подтвержденном диагнозе не рекомендуется (1). Аналогично, пробное лечение метронидазолом считают неприемлемым для дифференцирования инфекции Giardia (которая иногда может купироваться терапией метронидазолом) и инфекции T. foetus (которая никогда не элиминируется метронидазолом). К сожалению, T. foetus относительно устойчивы к обычным противомикробным и противопаразитарным препаратам. В настоящее время эффективным для элиминирования инфекции считают только один препарат. Это препарат из семейства нитроимидазолов, ронидазол (ronidazole) (17). На момент написания статьи ронидазол не лицензирован и не одобрен иным образом для использования у кошек ни в одной из стран мира, но доступен в некоторых ветеринарных аптеках с рецептурно-производственным отделом для использования не по утвержденным показаниям в отсутствие эффективных лицензированных методов лечения. Эта форма препарата относительно дорогая, но рекомендуется благодаря надежности обеспечиваемых аптеками с рецептурно-производственным отделом дозы и состава. Если этот вид лечения недоступен, или если расходы признаны чрезмерными, препарат также можно приобрести в форме порошка, в которой его используют для лечения паразитарных заболеваний у голубей.
Эту лекарственную форму не рекомендуют для использования в качестве препарата первого ряда из-за неизвестного качества и потенциально неодинакового состава, но в отдельных наблюдениях она оказалась эффективна для элиминации инфекции у кошек. В литературе описана схема дозирования ронидазола по 30 мг/кг каждые 24 часа внутрь в течение 14 дней (18). Препарат хорошо переносится многими кошками, однако описан ряд побочных эффектов. Как правило, по характеру они аналогичны наблюдаемым для высоких доз метронидазола, и большинство из них связаны с проявлением нейротоксичности. Чаще всего наблюдают такие побочные эффекты, как вялость, снижение аппетита, атаксия и, если препарат не отменить, судороги (19). Большинство побочных эффектов быстро разрешаются после отмены препарата, но, если лечение после выявления побочных эффектов не прекращено, может потребоваться активная поддерживающая терапия (1). Побочные эффекты наблюдаются значительно чаще, чем при лечении метронидазолом, и считаются связанными со сравнительно более длительным периодом полувыведения ронидазола по сравнению с метронидазолом.Если после лечения диарея рецидивирует, в принципе, целесообразно повторить курс лечения, особенно при заметном улучшении состояния на фоне приема препарата и последующем резком ухудшении после завершения курса терапии. Однако если после начального курса лечения отмечен период хорошего самочувствия, а ухудшение произошло через несколько недель или месяцев, целесообразно подтвердить инфекцию T. foetus, поскольку клинические проявления могут быть вызваны другим заболеванием. Наряду с лечением ронидазолом, имеются ограниченные данные и об эффективности других стратегий лечения. Автору неизвестны какие-либо публикации относительно диетологических рекомендаций при этом заболевании, но можно руководствоваться общими правилами ведения энтеропатий: любые изменения в диету следует вносить только на основании взвешенного решения, поскольку иногда они могут приводить к толстокишечной диарее, особенно при использовании низкокачественных или несбалансированных кормов. Дополнительная противомикробная терапия не показана. Доказательных данных в пользу или против применения БАД и пробиотиков нет, поэтому рекомендации в их отношении дать невозможно.
Прогноз
Лечение ронидазолом обычно приводит к относительно быстрому улучшению консистенции и качества стула уже в первые 14 дней лечения. Однако в более тяжелых случаях для улучшения может потребоваться несколько больше времени; считают, что этот срок коррелирует с активностью воспаления в кишечнике и обусловлен более высокой паразитарной нагрузкой (1). У кошек, не получавших лечения инфекции T. foetus, диарея в конечном итоге разрешается самостоятельно примерно в 88% случаев, но для разрешения может потребоваться до двух лет (20). У 55% кошек после самостоятельного разрешения диареи инфицирование сохраняется, и потому они могут продолжать выделять трофозоиты и представлять опасность заражения для других кошек. Поэтому применять эту стратегию ведения пациентов не рекомендуется.
Заключение
Толстокишечная диарея у молодых кошек, наблюдаемых в общеклинической ветеринарной практике, встречается относительно часто. При таких клинических проявлениях в круг дифференциальной диагностики важно включать Tritrichomonas foetus, причем оценить вероятность этого диагноза уже на начальных этапах диагностического поиска. Золотым стандартом обследования считают культивирование кала с последующими микроскопией и ПЦР мазка кала. Лечение следует начинать после установления диагноза, и в настоящее время единственным эффективным препаратом считают ронидазол.
Литература
- Gookin JL. Trichomoniasis. In: Greene CE, ed. Infectious diseases of the dog and cat. 4th Ed. St Louis: Saunders 2012;797-801.
- Gunn-Moore DA, McCann TM, Reed N, et al. Prevalence of Tritrichomonas foetus infection in cats with diarrhea in the UK. J Feline Med Surg 2007;9:214-218.
- Gookin JL, Stebbins ME, Hunt E, et al. Prevalence of and risk factors for feline Tritrichomonas foetus and Giardia infection. J Clin Microbiol 2004;42:2707-2710.
- Gookin JL, Breitschwerdt EB, Levy MG, et al. Diarrhea associated with trichomonosis in cats. J Am Vet Med Assoc 2009;215:1450-1455.
- Lappin MR. Trichomoniasis. In: Sykes JE, ed. Canine and Feline Infectious Diseases. St Louis: Saunders 2014;779-783.
- Gookin JL, Levy MG, Law JM, et al. Experimental infection of cats with Tritrichomonas foetus. Am J Vet Res 2001;62:1690-1697.
- Yaeger M, Gookin JL. Histologic features of Tritrichomonas foetus colitis in domestic cats. Vet Pathol 2005;42:797-804.
- Tolbert MK, Gookin JL. Mechanisms of Tritrichomonas foetus pathogenicity in cats with insights from venereal trichomonosis. J Vet Intern Med 2016;30:516-552.
- Van der Saag M, McDonell D, Slapeta J. Cat genotype Tritrichomonas foetus survives passage through the alimentary tract of two common slug species. Vet Parasitol 2011;177:262-266.
- Hale S, Norris JM, Slapeta J. Prolonged resilience of Tritrichomonas foetus in cat feces at ambient temperature. Vet Parasitol 2009;166:60-65.
- Gookin JL, Stauffer SH, Levy MG. Identification of Pentatrichomonas hominis in feline fecal samples by polymerase chain reaction assay. Vet Parasitol 2007;145:11-15.
- Foster DM, Gookin JL, Poore MF, et al. Outcome of cats with diarrhea and Tritrichomonas foetus. J Vet Intern Med 2003;17:380.
- Gookin JL, Birkenheuer AJ, Breitschwerdt EB, et al. Single-tube nested PCR for diagnosis of Tritrichomonas foetus in feline feces. J Clin Microbiol 2002;40:4126-4130.
- Stauffer SH, Birkenheuer AJ, Levy MG, et al. Evaluation of four DNA extraction methods for the detection of Tritrichomonas foetus in feline stool specimens by polymerase chain reaction. J Vet Diagn Invest 2008;20:639-641.
- Gookin JL, Birkenheuer AJ, St. John V, et al. Molecular characterization of trichomonads from feces of dogs with diarrhea. J Parasitol 2005; 91:939-943.
- Gookin JL, Foster DM, Poore MF, et al. Use of a commercially available culture system for diagnosis of Tritrichomonas foetus infection in cats. J Am Vet Med Assoc 2003;222:1376-1379.
- Gookin JL, Copple CN, Papich MG, et al. Efficacy of ronidazole for treatment of feline Tritrichomonas foetus infection. J Vet Intern Med 2006;20:536-543.
- LeVine DN, Papich MG, Gookin JL, et al. Ronidazole pharmacokinetics after intravenous and oral immediate-release capsule administration in healthy cats. J Feline Med Surg 2011;13:244-250.
- Rosado TW, Specht A, Marks SL. Neurotoxicosis in 4 cats receiving ronidazole. J Vet Intern Med 2007;21:328-331.
- Foster DM, Gookin JL, Poore MF, et al. Outcome of cats with diarrhea and Tritrichomonas foetus. J Am Vet Med Assoc 2004;225:888-892.
Трихомоноз – болезнь, вызываемая простейшими микроорганизмами, которые обычно живую в кишечнике и вызывают его воспаление. Данное заболевание может быть причиной диареи, потери веса и даже выпадения прямой кишки.
Заражение отмечается у котят и кошек, проживающих в приюте. Чаще всего болеют животные до двух лет.
Возбудитель

Трихомонада (Tritrichomonas fetus) – это одноклеточный простейший организм.
Данный высокоподвижный жгутиковый паразит обитает в дистальных отделах тонкой подвздошной и толстой – слепой и толстой кишки, где вызывает воспаление и толстокишечную диарею.
Этот паразит специфичен для кошек. У больных из них наблюдается частая зловонная диарея, иногда со слизью, свежей кровью, с тенезмами, но в целом они остаются бодрыми и не теряют в весе.
Инфекция чаще встречается у кошек, живущих в среде с несколькими животными, особенно из племенных колоний. В некоторых исследованиях чистокровные животные подвергаются повышенному риску заражения, хотя в разных исследованиях сообщается о разных породных связях. Могут быть затронуты группы, а также отдельные кошки в домашнем хозяйстве.
Инфекция T. fetus чаще регистрируется у кошек в возрасте 1 года и младше. Половой предрасположенности не существует.
По статистике у 39% кошек с диареей будет выделен в кале T. fetus.
Механизм, с помощью которого T. fetus вызывает диарею, не ясен. Паразит находится в слизи на поверхности слизистой оболочки дистальных отделов тонкой и толстой кишки и факторы адгезии могут иметь важное значение. Организм может вырабатывать токсины и вызывать воспалительную реакцию в толстой кишке.
Мало что известно об иммунитете к тритрихомонадам. Чаще лечение имеет положительную динамику, что говорит о том, что у инфицированных кошек развивается эффективный иммунный ответ.
Симптомы и признаки
Не все инфекции связаны с клиническими признаками. Паразит поражает толстую кишку, а признаки диареи обычно наводят на мысль о колите с частым выделением небольшого количества жидкости с полуоформленными фекалиями часто с кровью, слизью, метеоризмом и тенезмами в лотке.
Клинические признаки трихомоноза у кошки могут быть не постоянными, а диарея иметь неприятный зловонный запах.
В одном исследовании средняя продолжительность диареи составила 135 дней.
У некоторых пораженных кошек развивается недержание кала и перианальный отек. Иногда сообщается об анорексии и депрессии. Но в целом кошки имеют удовлетворительное физическое состояние без системных признаков.
Основные признаки:
- жидкий стул на протяжении длительного времени;
- примеси слизи и крови в кале;
- потеря веса;
- вялость, слабость, снижение аппетита;
- выпадение прямой кишки при тяжелом течении заболевания.
Паразита иногда обнаруживают в половых путях, но, по-видимому, это не связано с репродуктивными заболеваниями. В одном случае сообщалось о заражении матки T. fetus. Также задокументировано присутствие T. fetus в носовой полости кошки с хроническими гнойными выделениями в сочетании с Mycoplasma felis, хотя для выяснения патогенности возбудителя в этом случае требуется дополнительные исследования.
Доступные методы диагностики

Нативный мазок
Микроорганизм можно идентифицировать в свежих фекалиях в течение нескольких часов после сбора, путем прямого исследования, которое выявляет подвижные трофозоиты.
Единственный жгутик вызывает резкие движения вперед, что может помочь в дифференциации от трофозоитов видов Giardia. Фекалии суспендируют в физиологическом растворе и исследуют под световой микроскопией с покровным стеклом. Если с ними выделяется слизь, то исследуют и ее. Чувствительность метода всего 14,7%
Культура
Диагноз трихомоноз у кошки может быть поставлен путем культивирования организма.
Бак посев может занять до семи дней. Этот метод часто дает ложноотрицательные результаты при задержке анализа на трихомоноз у кошек. В одном исследовании сообщалось о чувствительности системы культивирования InPouch на уровне 58,8%. В России данный метод не используется.
ПЦР
Трихомоноз у кошки также можно диагностировать с помощью метода ПЦР, который в настоящее время широко доступна почти во всех лабораториях.
ПЦР может быть очень чувствительной и позволяет обнаружить ДНК даже нежизнеспособных трофозоитов. Недостатком ПЦР является возможность выявления инфекций, которые могут не иметь клинического значения. Однако положительный результат ПЦР при наличии подозрительных признаков обычно достаточен для постановки диагноза.
Гистопатология
Трофозоиты могут присутствовать в биопсийном материале, но их трудно идентифицировать, поэтому предпочтительны менее инвазивные методы диагностики образцов фекалий – ПЦР, нативный мазок.
Отбор проб для диагностики
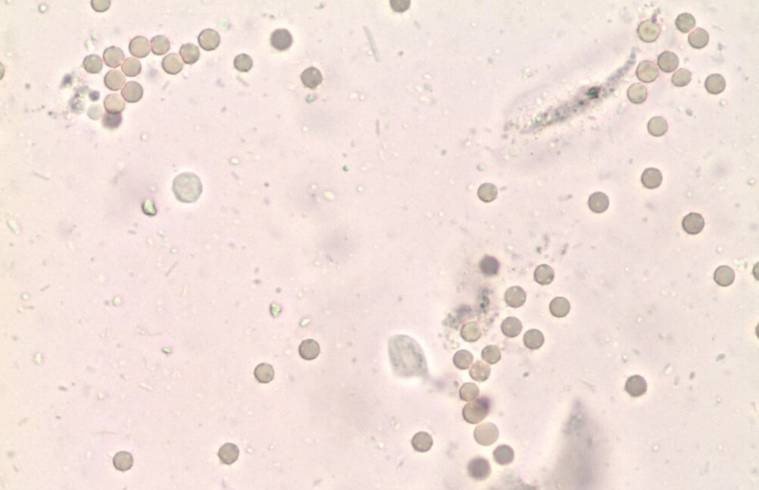
Считается, что образцы кала со слизью являются предпочтительными образцами для повышения чувствительности тестирования T. fetus для всех прямых диагностических методов.
Также рекомендовано взятие глубокого смыва из ободочной кишки. Данный метод сбора материала умеренно болезненный и неприятный, в некоторых случаях требует успокоительных препаратов.
Лечение трихомоноза у кошек
Препаратом для лечения является Ронидазол, родственный Метронидазолу. Это единственный препарат с доказанной эффективностью против T. Fetus.
Ронидазол не лицензирован для применения у кошек. Перед использованием необходимо получить информированное подписанное согласие. Данный препарат должен назначается ветеринарным врачом, так как имеет побочные эффекты.
Среди них:
- нейротоксические признаки;
- вялость;
- отсутствие аппетита;
- атаксия;
- судороги;
- тремор.
Также Ронидазол является тератогенным, поэтому его нельзя давать беременным или кормящим кошкам. Терапия длительная – от нескольких недель.
Рецидивы после удачного лечения или неэффективного лечения, могут возникать у 25% пролеченных кошек. Однако неэффективность лечения не более вероятна в семьях с несколькими кошками. Диарея обычно проходит спонтанно даже у нелеченых кошек, хотя это может занять несколько месяцев или дольше.
Чтобы снизить риск повторного заражения кошки трихомонозом и передачи, должна проводится гигиена туалетного лотка, и, если возможно, инфицированных кошек следует изолировать.
Сведение к минимуму стресса и недопущение скученного содержания в семьях с несколькими кошками также могут быть важны для сведения к минимуму инфекции.
Говорят, что тритрихомонады легко погибают в среде с большинством дезинфицирующих средств, поэтому важна регулярная уборка зараженных домовладений.
Ключевой вопрос без ответа: когда инфекция выявлена в группе кошек, каких особей следует лечить — всех животных в группе или только кошек с диареей.
Разумный подход состоит в том, чтобы лечить только кошек, у которых есть признаки и положительные результаты мазков кала.
Кроме того, следует помнить, что коинфекция другими кишечными патогенами может возникать особенно в семьях с несколькими животными, что может усложнить диагностику и реакцию на медикаменты.
Прогноз
Прогноз при инфекции T. fetus обычно благоприятный и у 88% кошек с диареей консистенция фекалий возвращается к норме спонтанно. Это происходит через 2 года после заражения
Зоонозный риск
На вопрос трихомоноз у кошек передается ли человеку мы можем ответить так: T. fetus не считается зоонозным заболеванием, но при обращении с инфицированными кошками и их фекалиями следует соблюдать правила гигиены, особенно лицами с ослабленным иммунитетом.
20 февраля 2023г.
