Поливитамины с макро- и микроэлементами и растительными компонентами
Фармако-терапевтическая группа
Поливитаминное средство+мультиминерал
Состав
Активное вещество — норгестрел.
Таблетки 0.075 мг в упаковках на 100 циклов (на 1 цикл
требуется 28 таблеток).
Показания к применению
Предупреждение беременности.
Противопоказания к применению
Тромбофлебит, опухоль молочной железы или половых органов, перенесенный инсульт, ИБС, ангина, эпилепсия, диабет, гипертензия, холецистит, психические
расстройства, маточные кровотечения, подозрение на беременность.
Возможные побочные эффекты
ВНИМАНИЕ! Если вы подозреваете, что при приеме препарата ваше самочувствие ухудшилось, появились какие-то побочные эффекты, нужно сразу же обратиться очно к врачу, назначившему препарат!
Повышенная свертываемость крови»
тромбоэмболические состояния, повышение риска возникновения нарушений мозгового кровообращения; болезненность
а молочной железе, тошнота, рвота, изменения в весе, пигмен-тирование
кожи лица и отечность голеностопного сустава.
Редко — маточное кровотечение, нарушение менструального
цикла, желтуха, депрессивное состояние.
Дозировка, как принимать Оврет
Начинать прием препарата следует с 1
дня менструального цикла по 1 таблетке в одно и то же время,
либо после завтрака, либо перед сном. После использования
таблеток в первой упаковке следует начинать прием из следующей упаковки независимо от того, есть ли в данный момент
менструальные кровотечения или нет. Возможны задержки
менструаций при приеме препарата, но не более 45 дней. В
таких случаях необходима консультация гинеколога для выяснения возможности беременности. В случае пропуска очередной таблетки необходимо быстро ее принять. Если
пропущено более 2-х приемов препарата подряд, цикл прерывают и до начала следующего менструального периода следует
пользоваться другими методами контрацепции. С началом
регулярных менструаций (следующий период) прием препарата возобновляют.
Дополнительные указания при приеме Оврет
Одновременное назначение антибиотиков
снижает контрацептивный эффект препарата.
Недостаточная доза или прерывание лечения, особенно при инсулинзависимом сахарном диабете (1 типа) может привести к гипергликемии и диабетическому кетоацидозу.
Опыта клинического применения у детей младше 6 лет нет. НовоРапид следует использовать у детей вместо обычного инсулина короткого действия только в тех случаях, если быстрое начало действия может оказать лучший эффект — например, если ребенку трудно соблюдать необходимый интервал между инъекциями и приемом пищи.
Сопутствующие заболевания, в частности, инфекции, обычно увеличивают, а поражения почек или печени — уменьшают потребность в инсулине. Перевод больного на новый тип или торговую марку инсулина нужно осуществлять под строгим медицинским контролем.
При использовании препарата НовоРапид Пенфилл может потребоваться большее число инъекций в сутки или изменение дозы, по сравнению с таковыми при использовании обычных препаратов инсулина. Если возникнет потребность в коррекции дозы, это может произойти уже при первом введении или в первые несколько недель или месяцев после перевода.
После компенсации углеводного обмена у больных могут измениться типичные для них симптомы-предвестники гипогликемии, о чем их следует проинформировать. Пропуск приема пищи или незапланированная физическая нагрузка могут привести к гипогликемии. С особой осторожностью применять во время работы водителям транспортных средств и людям, профессия которых связана с повышенной концентрацией внимания, т.к. может развиться гипогликемия, особенно у пациентов со слабо выраженными или отсутствующими симптомами предвестниками гипогликемии или ее частыми эпизодами. В таких случаях следует серьезно подумать о том, желательно ли пациенту водить автомобиль. Картридж Пенфилл предназначен исключительно для индивидуального пользования. После инъекции в течение минимум 6 с игла должна оставаться под кожей для полного введения дозы.
Передозировка
Симптомы: боль в животе, тошнота, рвота, заторможенность, сонливость, депрессия, головная боль, шум в ушах, метаболический ацидоз, кома, острая почечная недостаточность, снижение АД, брадикардия, тахикардия, фибрилляция предсердий, остановка дыхания.
Лечение: промывание желудка (только в течение часа после приема), активированный уголь, щелочное питье, форсированный диурез; при необходимости проводят симптоматическую терапию.
Как хранить препарат
Препарат следует хранить в сухом, недоступном для детей месте при температуре не выше 25°C. Срок годности – 2 года.
Условия отпуска
Препарат разрешен к применению в качестве средства безрецептурного отпуска.
Информация для врачей о препарате Оврет
Фармакодинамика
Стероидный гестагенный препарат, действующий на репродуктивную функцию женщин.
Подавляет овуляцию, препятствует прикреплению к стенке
матки уже оплодотворенной яйцеклетки, предупреждая наступление беременности. Контрацептивный эффект приблизительно равен 97 %.
Фармакокинетика
При приеме внутрь ибупрофен практически полностью абсорбируется из ЖКТ. Одновременный прием пищи замедляет скорость всасывания. Метаболизируется в печени (90%). T1/2 составляет 2-3 ч.
80% дозы выводится с мочой преимущественно в виде метаболитов (70%), 10% — в неизмененном виде; 20% выводится через кишечник в виде метаболитов.
Взаимодействие с другими веществами
с другими лекарственными препаратами.
Следует избегать одновременного применения двух и более НПВС в связи с повышением риска развития побочных эффектов. При одновременном применении ибупрофен снижает противовоспалительное и антиагрегационное действие ацетилсалициловой кислоты(возможно повышение частоты развития острой коронарной недостаточности у больных,получающих в качестве антиагрегантного средства малые дозы ацетилсалициловойкислоты, после начала приема ибупрофена). При применении с тромболитическими ЛС(алтеплазой, стрептокиназой, урокиназой) одновременно повышается риск развития кровотечений. Ибупрофен усиливает действие непрямых антикоагулянтов,антиагрегантов, фибринолитиков. Индукторы микросомального окисления (фенитоин, этанол, барбитураты, рифампицин,фенилбутазон, трициклические антидепрессанты) увеличивают продукцию гидроксилированных активных метаболитов, повышая риск развития тяжелых гепатотоксических реакций.
Ингибиторы микросомального окисления снижают риск гепатотоксического действия.Антациды и колестирамин снижают абсорбцию ибупрофена. Кофеин усиливает анальгезирующий эффект ибупрофена. Цефамандол, цефоперазон, цефотетан,вальпроевая кислота увеличивают частоту развития гипопротромбинемии.Миелотоксичные ЛС усиливают проявления гематотоксичности ибупрофена. Циклоспорин и препараты золота усиливают влияние ибупрофена на синтез ПГ в почках,что проявляется повышением нефротоксичности. Ибупрофен повышает плазменную концентрацию циклоспорина и вероятность развития его гепатотоксических эффектов.ЛС, блокирующие канальцевую секрецию, снижают выведение и повышают плазменную концентрацию ибупрофена.Ибупрофен снижает действие гипотензивных ЛС (в т.ч. БКК и ингибиторов АПФ),натрийуретическую и диуретическую активность фуросемида и гидрохлоротиазида,эффективность урикозурических ЛС. Усиливает побочные эффектыминералокортикоидов, глюкокортикоидов, эстрогенов, этанола.
Усиливает эффект пероральных гипогликемических ЛС и инсулина. Повышает концентрацию в кровидигоксина, препаратов лития и метотрексата. Ибупрофен может снижать клиренс аминогликозидов (при одновременном назначении может повышаться риск нефротоксичности и ототоксичности). Ибупрофен для в/в введения не следует смешивать с другими ЛС.
Смотрите также:
- Октреотид Сан — раствор, инструкция лекарства
- Онгецин — лиофилизат, инструкция лекарства
- ОРВИС® Рино — таблетки, инструкция лекарства
- Офлоксацин Сандоз® — таблетки, инструкция лекарства
К сведению

Наши партнеры
PubMed — национальная библиотека медицины на английском
Инструкция по применению Мавирет 100 мг + 40 мг 84 шт. таблетки
Форма выпуска, упаковка и состав
Таблетки, покрытые пленочной оболочкой розового цвета, продолговатые, двояковыпуклые, с гравировкой «NXT» на одной стороне.
| 1 таб. | |
| глекапревир | 100 мг |
| пибрентасвир | 40 мг |
Вспомогательные вещества: коповидон К28, D-альфа-токоферола макрогола сукцинат, кремния диоксид коллоидный, кроскармеллоза натрия, натрия стеарилфумарат, пропиленгликоля монокаприлат тип II; пленочное покрытие Опадрай II розовый (Opadry® II 32F240023): гипромеллоза 2910, лактозы моногидрат, титана диоксид, макрогол 3350, железа оксид красный.
3 шт. — блистеры (7) — пачки картонные (4) — пачки картонные.
Фармакологическое действие
Механизм действия
Мавирет – комбинация двух пангенотипных противовирусных средств прямого действия в фиксированных дозах – глекапревира (ингибитора протеазы NS3/4A) и пибрентасвира (ингибитора NS5A), воздействующих на различные этапы жизненного цикла вируса гепатита С.
Глекапревир
Глекапревир представляет собой ингибитор протеазы вируса гепатита С (ВГС) NS3/4A, которая необходима для протеолитического расщепления кодирующего вирус гепатита С полипротеина (для дальнейшего превращения в зрелые формы белков NS3, NS4A, NS4B, NS5A и NS5B) и имеет важное значение для репликации вируса. В биохимических исследованиях глекапревир ингибировал протеолитическую активность рекомбинантных протеаз вируса гепатита С NS3/4A из клинических изолятов вируса генотипов 1a, 1b, 2a, 2b, 3а, 4а, 5а и 6а со значениями IC50 от 3.5 до 11.3 нМ.
Пибрентасвир
Пибрентасвир является пангенотипным ингибитором белка NS5A вируса гепатита С, который необходим для репликации вирусной РНК и сборки вириона. Механизм действия пибрентасвира был изучен в ходе исследований противовирусной активности на клеточных культурах и исследований по определению характера лекарственной резистентности.
Противовирусная активность
Значения ЕС50 глекапревира и пибрентасвира против полноразмерных или гибридных репликонов, кодирующих NS3 или NS5A из лабораторных штаммов, представлены в таблице 1.
Таблица 1. Активность глекапревира и пибрентасвира против клеточных линий репликона генотипов ВГС 1-6
| Подтип ВГС | EC50 глекапревира, нМ | EC50 пибрентасвира, нМ |
| 1а | 0.85 | 0.0018 |
| 1b | 0.94 | 0.0043 |
| 2a | 2.2 | 0.0023 |
| 2b | 4.6 | 0.0019 |
| 3a | 1.9 | 0.0021 |
| 4a | 2.8 | 0.0019 |
| 5a | Н/П | 0.0014 |
| 6a | 0.86 | 0.0028 |
Н/П – неприменимо.
Значения ЕС50 глекапревира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов, представлены в таблице 2.
Таблица 2. Активность глекапревира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов вируса ВГС генотипов 1–6
| Подтип ВГС | Глекапревир | Пибрентасвир | ||
| Количество клинических изолятов | Медиана EC50, нМ (диапазон) | Количество клинических изолятов | Медиана EC50, нМ (диапазон) | |
| 1а | 11 | 0.08 (0.05–0.12) | 11 | 0.0009 (0.0006–0.0017) |
| 1b | 9 | 0.29 (0.20–0.68) | 8 | 0.0027 (0.0014–0.0035) |
| 2a | 4 | 1.6 (0.66–1.9) | 6 | 0.0009 (0.0005–0.0019) |
| 2b | 4 | 2.2 (1.4–3.2) | 11 | 0.0013 (0.0011–0.0019) |
| 3a | 2 | 2.3 (0.71–3.8) | 14 | 0.0007 (0.0005–0.0017) |
| 4a | 6 | 0.41 (0.31–0.55) | 8 | 0.0005 (0.0003–0.0013) |
| 4b | Н/П | Н/П | 3 | 0.0012 (0.0005–0.0018) |
| 4d | 3 | 0.17 (0.13–0.25) | 7 | 0.0014 (0.0010–0.0018) |
| 5a | 1 | 0.12 | 1 | 0.0011 |
| 6a | Н/П | Н/П | 3 | 0.0007 (0.0006–0.0010) |
| 6e | Н/П | Н/П | 1 | 0.0008 |
| 6p | Н/П | Н/П | 1 | 0.0005 |
Н/П – неприменимо.
Активность in vitro
Оценка комбинации глекапревира и пибрентасвира на репликонных клеточных культурах генотипа ВГС 1 не выявила каких-либо признаков антагонизма противовирусной активности.
Резистентность
В культуре клеток
Для репликонов был проведен фенотипический анализ аминокислотных замен в белках NS3 или NS5A, выделенных в культуре клеток или значимых для класса ингибиторов.
Замены, значимые для класса ингибиторов протеазы ВГС, в положениях 36, 43, 54, 55, 56, 155, 166 или 170 в белке NS3 не оказывают влияния на активность глекапревира. Для генотипа 2 аминокислотные замены в NS3 в положении 168 не оказывают влияния, в то время как некоторые замены в положении 168 вызывают снижение чувствительности к глекапревиру до 55 раз (генотипы 1, 3, 4) или снижение чувствительности более чем в 100 раз (генотип 6). Некоторые замены в положении 156 вызывают снижение чувствительности к глекапревиру более чем в 100 раз (генотипы 1–4). Аминокислотные замены в положении 80 не снижают чувствительность к глекапревиру, кроме замены Q80R в генотипе 3a, которая снижает чувствительность к глекапревиру в 21 раз.
Единичные замены, важные для класса ингибиторов протеазы NS5A в положениях 24, 28, 30, 31, 58, 92 или 93 в NS5A в генотипах 1–6 не оказывают никакого влияния на активность пибрентасвира. Например, в генотипе 3a аминокислотные замены A30K или Y93H не влияют на активность пибрентасвира. Некоторые комбинации замен в генотипах 1а и 3а (включая A30K+Y93H в генотипе 3а) демонстрируют снижение чувствительности к пибрентасвиру. В репликоне генотипа 3b присутствие встречающихся в природе полиморфизмов K30 и M31 в белке NS5A снижало чувствительность к пибрентасвиру в 24 раза по сравнению с активностью пибрентасвира в репликоне генотипа 3a.
Фармакокинетика
Фармакокинетические свойства компонентов препарата Мавирет представлены в таблице 3.
Таблица 3. Фармакокинетические свойства компонентов препарата Мавирет у здоровых добровольцев
| Глекапревир | Пибрентасвир | |
| Всасывание | ||
| Tmax (ч)a | 5.0 | 5.0 |
| Влияние пищи (по сравнению с приемом натощак)b | ↑ 83–163% | ↑ 40–53% |
| Распределение | ||
| % связывания с белками плазмы | 97.5 | >99.9 |
| Коэффициент распределения кровь/плазма | 0.57 | 0.62 |
| Биотрансформация | ||
| Метаболизм | вторичный | отсутствует |
| Выведение | ||
| Основной путь выведения | с желчью | с желчью |
| T1/2 (ч) в равновесном состоянии | 6–9 | 23–29 |
| % выведения с мочойc | 0.7 | 0 |
| % выведения с каломc | 92.1d | 96.6 |
| Клеточный транспорт | ||
| Субстрат для транспортера | P-гликопротеин, BCRP и OATP1B1/3 | P-гликопротеин и не исключая BCRP |
a Медиана Tmax у здоровых добровольцев после приема однократной дозы глекапревира и пибрентасвира.
b Среднее системное воздействие при приеме с пищей со средним и высоким содержанием жиров.
c Прием однократной дозы [14C] глекапревира или [14C] пибрентасвира в исследованиях массового баланса.
d Окислительные метаболиты или их продукты обмена составляли 26% радиоактивной дозы. Метаболиты глекапревира в плазме не наблюдались.
У пациентов с хроническим гепатитом С без цирроза после 3 дней монотерапии либо только глекапревиром 300 мг/сут (N=6) или только пибрентасвиром 120 мг/сут (N=8) геометрическое среднее значение AUC24 составило 13600 нг×ч/мл для глекапревира и 459 нг×ч/мл для пибрентасвира. Оценка фармакокинетических параметров с использованием популяционных фармакокинетических моделей имеет присущую им неопределенность из-за нелинейности дозы и перекрестного взаимодействия между глекапревиром и пибрентасвиром. Основываясь на популяционной фармакокинетической модели для препарата Мавирет при хроническом гепатите С, установившиеся значения AUC24 для глекапревира и пибрентасвира были 4800 и 1430 нг×ч/мл у пациентов без цирроза (N=1804) и 10500 и 1530 нг×ч/мл у пациентов с циррозом печени (N=280) соответственно. По сравнению со здоровыми пациентами (N=230) популяционные оценки AUC24,ss были аналогичны (разница в 10%) для глекапревира и на 34% ниже для пибрентасвира у пациентов, инфицированных вирусом гепатита С без цирроза.
Линейность/нелинейность
AUC глекапревира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы (при приеме 1200 мг 1 раз/сут наблюдалась в 516 раз больше экспозиция, чем при приеме 200 мг 1 раз/сут). Данное явление может быть вызвано насыщением механизмов транспорта или эффлюксных переносчиков.
AUC пибрентасвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы до 120 мг (при приеме 120 мг 1 раз/сут наблюдалось увеличение экспозиции более чем в 10 раз по сравнению с приемом 30 мг 1 раз/сут), но установленная линейная фармакокинетика в дозах ≥120 мг. Нелинейное увеличение экспозиции <120 мг может быть связано с насыщением эффлюксных переносчиков.
Биодоступность пибрентасвира при взаимодействии с глекапревиром в 3 раза выше по сравнению с применением только пибрентасвира. У глекапревира наблюдалось меньшее влияние пибрентасвира.
Фармакокинетика у особых групп пациентов
Раса/этническая принадлежность. Не требуется коррекция дозы препарата Мавирет в зависимости от расы или этнической принадлежности.
Пол/масса тела. Не требуется коррекция дозы препарата Мавирет в зависимости от пола или массы тела.
Пациенты пожилого возраста. У пациентов пожилого возраста коррекция дозы препарата Мавирет не требуется. Популяционный фармакокинетический анализ ВГС-инфицированных пациентов в возрасте от 12 до 88 лет показал, что возраст не оказывает клинически значимого влияния на действие глекапревира и пибрентасвира.
Дети. У детей в возрасте 12 лет и старше коррекция дозы препарата Мавирет не требуется. Содержание глекапревира и пибрентасвира в плазме крови у детей было сопоставимо с таковым у взрослых в исследованиях фазы 2/3. Фармакокинетика глекапревира и пибрентасвира не изучалась у детей в возрасте до 12 лет.
Пациенты с нарушением функции почек. Значение AUC глекапревира и пибрентасвира повышалось не более чем на 56% у пациентов без ВГС с легкой, умеренной и тяжелой степенью нарушения функции почек, не получавших диализ, по сравнению с пациентами с нормальной функцией почек. Значение AUC глекапревира и пибрентасвира было одинаковым у пациентов без ВГС на диализе и пациентов, не получающих его (разница ≤18%). В популяционном фармакокинетическом анализе у пациентов с ВГС и терминальной стадией почечной недостаточности, на диализе или без него, наблюдались значения AUC глекапревира на 86% выше, а пибрентасвира на 54% выше, чем у пациентов с нормальной функцией почек. При оценке концентраций глекапревира и пибрентасвира, не связанных с белками плазмы, может наблюдаться более выраженный рост AUC. В целом, изменения воздействия препарата Мавирет у ВГС-инфицированных пациентов с нарушением функции почек на диализе или без него не были клинически значимыми.
Пациенты с печеночной недостаточностью. При приеме в рекомендуемой дозе значение AUC глекапревира у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью было на 33% выше, класса B – на 100% выше, а класса С – в 11 раз выше, чем у пациентов без ВГС с нормальной функцией печени. Значение AUC пибрентасвира не менялось у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью и было на 26% выше у пациентов с печеночной недостаточностью класса B и на 114% – класса С. При оценке концентраций несвязанных глекапревира и пибрентасвира может иметь место более выраженный рост AUC.
Популяционный фармакокинетический анализ показал, что после приема препарата Мавирет пациентами с ВГС и компенсированным циррозом печени воздействие глекапревира было примерно в 2 раза выше, а пибрентасвира – аналогичным таковому у пациентов с ВГС без цирроза. Механизм различий между экспозицией глекапревира у пациентов с хроническим гепатитом С с циррозом или без цирроза неизвестен.
Взаимодействие с другими лекарственными препаратами
Были проведены исследования взаимодействия глекапревира/пибрентасвира с другими лекарственными препаратами, которые могут вступать во взаимодействия с глекапревиром/пибрентасвиром и препаратами, которые часто применяются в исследованиях фармакокинетического взаимодействия. В таблицах 4 и 5 ниже представлены фармакокинетические эффекты при взаимодействии глекапревира/пибрентасвира с другими лекарственными препаратами, которые показали потенциальные клинически значимые изменения.
Таблица 4. Лекарственное взаимодействие: изменения фармакокинетических параметров глекапревира (ГЛЕ) или пибрентасвира (ПИБ) в присутствии одновременно назначаемого лекарственного препарата
| Совместно применяемый препарат | Доза совместно применяемого препарата | Доза ГЛЕ/ПИБ | N | Препарат прямого противовирусного действия | Соотношение центральных значений (90% ДИ) | ||
| Cmax | AUC | Cmin | |||||
| Карбамазепин | 200 мг 2 раза/сут | 300/120 мг однократно |
10 | ГЛЕ | 0.33 (0.27; 0.41) | 0.34 (0.28; 0.40) | — |
| ПИБ | 0.50 (0.42; 0.59) | 0.49 (0.43; 0.55) | — | ||||
| Рифампицин | 600 мг (первая доза) | 300/120 мг однократно |
12 | ГЛЕ | 6.52 (5.06; 8.41) | 8.55 (7.01; 10.4) | — |
| ПИБ | ↔ | ↔ | — | ||||
| 600 мг 1 раз/сут | 300/120 мг однократноa |
12 | ГЛЕ | 0.14 (0.11; 0.19) | 0.12 (0.09; 0.15) | — | |
| ПИБ | 0.17 (0.14; 0.20) | 0.13 (0.11; 0.15) | — | ||||
| Циклоспорин | 100 мг однократно | 300/120 мг 1 раз/сут |
12 | ГЛЕb | 1.30 (0.95; 1.78) | 1.37 (1.13; 1.66) | 1.34 (1.12; 1.60) |
| ПИБ | ↔ | ↔ | 1.26 (1.15; 1.37) | ||||
| 400 мг однократно | 300/120 мг однократно |
11 | ГЛЕ | 4.51 (3.63; 6.05) | 5.08 (4.11; 6.29) | — | |
| ПИБ | ↔ | 1.93 (1.78; 2.09) | — | ||||
| Атазанавир (ATZ) + ритонавир (RTV) | ATZ 300 мг + RTV 100 мг 1 раз/сут | 300/120 мг 1 раз/сутс |
12 | ГЛЕ | ≥4.06 (3.15; 5.23) | ≥6.53 (5.24; 8.14) | ≥14.3 (9.85; 20.7) |
| ПИБ | ≥1.29 (1.15; 1.45) | ≥1.64 (1.48; 1.82) | ≥2.29 (1.95; 2.68) | ||||
| Дарунавир (DRV) + RTV | DRV 800 мг + RTV 100 мг 1 раз/сут | 300/120 мг 1 раз/сут |
8 | ГЛЕ | 3.09 (2.26; 4.20) | 4.97 (3.62; 6.84) | 8.24 (4.40; 15.4) |
| ПИБ | ↔ | ↔ | 1.66 (1.25; 2.21) | ||||
| Лопинавир/ Ритонавир |
400/100 мг 2 раза/сут |
300/120 мг 1 раз/сут |
9 | ГЛЕ | 2.55 (1.84; 3.52) | 4.38 (3.02; 6.36) | 18.6 (10.4; 33.5) |
| ПИБ | 1.40 (1.17; 1.67) |
2.46 (2.07; 2.92) |
5.24 (4.18; 6.58) |
↔ = без изменений (соотношение центральных значений от 0.80 до 1.25).
a Влияние рифампицина на глекапревир и пибрентасвир через 24 ч после приема последней дозы рифампицина.
b У пациентов после трансплантации печени, инфицированных ВГС, которые получали лечение циклоспорином в дозе 100 мг/сут или менее, экспозиция глекапревира была в 2.4 раза выше по сравнению с пациентами, которые не принимали циклоспорин.
c Было отмечено влияние атазанавира и ритонавира на концентрацию глекапревира и пибрентасвира после приема первой дозы глекапревира и пибрентасвира.
Таблица 5. Лекарственное взаимодействие: фармакокинетические параметры для совместно применяемого препарата при одновременном применении с глекапревиром/пибрентасвиром
| Совместно применяемый препарат | Доза совместно применяемого препарата | доза ГЛЕ/ПИБ | N | Соотношение центральных значений (90% ДИ) | ||
| Cmax | AUC | Cmin | ||||
| Дигоксин | 0.5 мг однократно | 400/120 мг 1 раз/сут | 12 | 1.72 (1.45; 2.04) | 1.48 (1.40; 1.57) | — |
| Дабигатран | дабигатрана этексилат 150 мг однократно | 300/120 мг 1 раз/сут | 11 | 2.05 (1.72; 2.44) | 2.38 (2.11; 2.70) | — |
| Правастатин | 10 мг 1 раз/сут | 400/120 мг 1 раз/сут | 12 | 2.23 (1.87; 2.65) | 2.30 (1.91; 2.76) | — |
| Розувастатин | 5 мг 1 раз/сут | 400/120 мг 1 раз/сут | 11 | 5.62 (4.80; 6.59) | 2.15 (1.88; 2.46) | — |
| Аторвастатин | 10 мг 1 раз/сут | 400/120 мг 1 раз/сут | 11 | 22.0 (16.4; 29.6) | 8.28 (6.06; 11.3) | — |
| Ловастатин | ловастатин 10 мг 1 раз/сут |
300/120 мг 1 раз/сут | 12 | ↔ | 1.70 (1.40; 2.06) | — |
| Метаболит ловастатина, ловастатиновая кислота |
5.73 (4.65; 7.07) | 4.10 (3.45; 4.87) | — | |||
| Симвастатин | симвастатин 5 мг 1 раз/сут |
300/120 мг 1 раз/сут | 12 | 1.99 (1.60; 2.48) | 2.32 (1.93; 2.79) | — |
| Метаболит симвастатина, симвастатиновая кислота |
10.7 (7.88; 14.6) | 4.48 (3.11; 6.46) | — | |||
| Этинилэстрадиол (ЭЭ) | ЭЭ/норгестимат 35 мкг/250 мкг 1 раз/сут | 300/120 мг 1 раз/сут | 11 | 1.31 (1.24; 1.38) | 1.28 (1.23; 1.32) | 1.38 (1.25; 1.52) |
| Норгестрел | 1.54 (1.34; 1.76) | 1.63 (1.50; 1.76) | 1.75 (1.62; 1.89) | |||
| Норгестромин | ↔ | 1.44 (1.34; 1.54) | 1.45 (1.33; 1.58) | |||
| Этинилэстрадиол | ЭЭ/левоноргестрел 20 мкг/100 мкг 1 раз/сут | 300/120 мг 1 раз/сут |
12 | 1.30 (1.18; 1.44) | 1.40 (1.33; 1.48) | 1.56 (1.41; 1.72) |
| Норгестрел | 1.37 (1.23; 1.52) | 1.68 (1.57; 1.80) | 1.77 (1.58; 1.98) |
↔ = без изменений (соотношение центральных значений от 0.80 до 1.25).
Показания
лечение хронического гепатита С у взрослых и детей с 12 лет.
Режим дозирования
Для приема внутрь.
Таблетки следует глотать целиком во время еды, не разжевывать, не раздавливать и не ломать.
Лечение препаратом Мавирет должно назначаться специалистом и проводиться под наблюдением врача, обладающего опытом лечения пациентов с хроническим гепатитом С.
Взрослые и дети в возрасте от 12 лет
Рекомендуемая доза препарата Мавирет составляет 300 мг/120 мг в один прием (3 таб. по 100 мг/40 мг) 1 раз/сут.
В таблицах 6 и 7 представлена рекомендуемая продолжительность лечения препаратом Мавирет на основе данных, полученных на популяции пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6, с компенсированным циррозом печени или без него.
Таблица 6. Рекомендуемая продолжительность лечения для пациентов, ранее не получавших лечение
| Популяция пациентов | Рекомендуемая продолжительность лечения | |
| Без цирроза печени | С циррозом печени | |
| ГТ 1–6 | 8 недель | 8 недель |
Таблица 7. Рекомендуемая продолжительность лечения для пациентов, не ответивших на предыдущую терапию
| Популяция пациентов | Предшествующий режим терапии | Рекомендуемая продолжительность лечения | |
| Без цирроза печени | С циррозом печени | ||
| ГТ 1 | Ингибиторы NS5A1 без предшествующей терапии ингибиторами протеазы NS3/4А | 16 недель | 16 недель |
| Ингибиторы протеазы NS3/4А2 без предшествующей терапии ингибиторами NS5A | 12 недель | 12 недель | |
| ГТ 1, 2, 4, 5 или 6 | Предшествующая терапия, следующими режимами: интерферон (или пегилированный интерферон) + рибавирин; интерферон (или пегилированный интерферон) + рибавирин + софосбувир; софосбувир + рибавирин. |
8 недель | 12 недель |
| ГТ 3 | Предшествующая терапия, следующими режимами: интерферон (или пегилированный интерферон) + рибавирин; интерферон (или пегилированный интерферон) + рибавирин + софосбувир; софосбувир + рибавирин. |
16 недель | 16 недель |
1 В клинических исследованиях пациенты получали предшествующую терапию, содержащую ледипасвир и софосбувир или даклатасвир с пегилированным интерфероном и рибавирином.
2 В клинических исследованиях пациенты получали предшествующую терапию, содержащую симепревир и софосбувир, или симепревир, боцепревир, или телапревир с пегилированным интерфероном или рибавирином.
Пропуск приема препарата
В случае пропуска приема препарата Мавирет его можно осуществить в течение 18 ч после планового времени приема. Если с момента планового времени приема препарата Мавирет прошло более 18 ч, не следует принимать пропущенную дозу, а следующую дозу следует принять в обычное время по расписанию. Не следует принимать двойную дозу препарата.
Если в течение 3 ч после приема препарата Мавирет произошла рвота, необходимо принять дополнительную дозу препарата. Если рвота произошла позднее 3 ч после применения препарата Мавирет, прием дополнительной дозы не требуется.
Особые группы пациентов
У пациентов пожилого возраста коррекция дозы препарата Мавирет не требуется.
У пациентов с почечной недостаточностью, включая пациентов на диализе, коррекция дозы препарата Мавирет не требуется.
У пациентов с печеночной недостаточностью легкой степени тяжести (класс А по шкале Чайлд-Пью) коррекция дозы препарата Мавирет не требуется. Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс B по шкале Чайлд-Пью) и противопоказан пациентам с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью).
У детей в возрасте 12 лет и старше коррекция дозы не требуется. Отсутствуют данные о безопасности и эффективности применения препарата Мавирет у детей в возрасте до 12 лет.
Пациенты после трансплантации печени или почки
Пациенты после трансплантации печени или почки могут применять препарат Мавирет в течение 12 недель (см. раздел «Особые указания»). В случае если пациенту назначена более длительная терапия (в течение 16 недель), и во время терапии была проведена трансплантация печени, то 16-недельный курс лечения должен быть доведен до конца.
Пациенты с ко-инфекцией ВГС/ВИЧ-1
Следует выполнять рекомендации, указанные в Таблицах 6 и 7. Рекомендации по дозированию препарата Мавирет при совместном применении с препаратами для терапии ВИЧ-1 представлены в разделе «Лекарственное взаимодействие».
Побочное действие
Резюме профиля безопасности
Оценка безопасности препарата Мавирет у пациентов с компенсированной функцией печени (с циррозом печени или без него) была проведена по результатам регистрационных исследований фазы 2 и 3, в которых участвовали около 2300 взрослых пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6, получавших Мавирет в течение 8, 12 или 16 недель.
Наиболее частыми нежелательными реакциями (частота ≥10%) были головные боли и утомляемость. Менее чем у 0.1% пациентов, получавших лечение препаратом Мавирет, развились серьезные нежелательные реакции (транзиторная ишемическая атака). Доля пациентов, которые окончательно прекратили получать лечение препаратом Мавирет по причине развития нежелательных реакций, составила 0.1%. Тип и тяжесть нежелательных реакций у пациентов с циррозом печени были сопоставимы с таковыми у пациентов без цирроза печени.
Таблица нежелательных реакций
У пациентов, получавших лечение препаратом Мавирет, сообщалось о развитии нежелательных реакций, представленных ниже. Список нежелательных реакций сгруппирован согласно классу систем органов и по частоте встречаемости. Частота встречаемости определяется следующим образом: очень часто (>1/10), часто (от >1/100 до <1/10), нечасто (от >1/1000 до <1/100), редко (от >1/10000 до <1/1000) и очень редко (<1/10000).
Таблица 8. Нежелательные реакции, наблюдавшиеся при приеме препарата Мавирет
| Частота развития | Нежелательные реакции |
| Со стороны нервной системы | |
| Очень часто | Головная боль |
| Со стороны ЖКТ | |
| Часто | Тошнота, диарея |
| Общие нарушения | |
| Очень часто | Утомляемость |
| Часто | Астения |
Описание отдельных нежелательных реакций
Нежелательные реакции у взрослых пациентов с тяжелым нарушением функции почек, включая пациентов на диализе
Безопасность препарата Мавирет у пациентов с хронической болезнью почек (стадия 4 или стадия 5, включая пациентов на диализе) и хронической инфекцией, вызванной вирусом гепатита С генотипов 1, 2, 3, 4, 5 или 6 с компенсированной печеночной недостаточностью (с циррозом печени или без него) оценивалась у 104 пациентов. Наиболее частыми нежелательными реакциями у пациентов с тяжелым нарушением функции почек были кожный зуд (17.3%) и утомляемость (11.5%).
Нежелательные реакции у взрослых пациентов после трансплантации почек или печени
Безопасность препарата Мавирет оценивалась у 100 пациентов после трансплантации печени или почек, инфицированных вирусом гепатита С генотипами 1, 2, 3, 4 или 6 без цирроза печени. Общий профиль безопасности у пациентов после трансплантации печени или почек был сопоставим с профилем безопасности у пациентов в исследованиях 2 и 3 фазы. Наблюдались следующие нежелательные реакции с частотой равной или более 5% у пациентов, принимавших Мавирет в течение 12 недель: головная боль (17%), усталость (16%), тошнота (8%) и зуд (7%). У 81% пациентов, принимавших препарат Мавирет, отмечались нежелательные реакции легкой степени тяжести. У 2% пациентов наблюдались серьезные нежелательные реакции. Не было ни одного случая полной отмены препарата из-за нежелательных реакций.
Оценка безопасности у взрослых пациентов с ко-инфекцией ВГС/ВИЧ-1
Общий профиль безопасности у пациентов с ко-инфекцией ВГС/ВИЧ-1 был сравним с таковым у пациентов с моноинфекцией ВГС.
Повышение уровня билирубина в сыворотке крови
У 1% пациентов наблюдалось повышение уровня общего билирубина как минимум в 2 раза выше ВГН, что было связано с глекапревир-опосредованным ингибированием белков-переносчиков билирубина и метаболизма билирубина. Повышение уровня билирубина было бессимптомным, временным и обычно возникало на ранней стадии лечения. Повышение уровня билирубина возникало преимущественно за счет непрямой фракции и не было ассоциировано с повышением уровня АЛТ.
Нежелательные реакции у детей
Безопасность препарата Мавирет у детей, инфицированных ВГС генотипов 1-6, оценивалась в открытом исследовании 2/3 фазы с участием 47 пациентов в возрасте от 12 до 18 лет, получавших терапию в течение 8-16 недель. Нежелательные реакции, зафиксированные в ходе данного исследования, были сопоставимы с реакциями, наблюдаемыми у взрослых пациентов (см. таблицу 8).
Пострегистрационные данные
В результате пострегистрационного наблюдения при применении препарата Мавирет были выявлены нежелательные реакции. Т.к. данные реакции были получены добровольно от неопределенной группы пациентов, установить частоту этих реакций или их связь с приемом препарата Мавирет не представляется возможным.
Нарушения со стороны иммунной системы: ангионевротический отек.
Нарушения со стороны кожи и подкожно-жировой клетчатки: зуд.
Противопоказания к применению
повышенная чувствительность к любому действующему веществу препарата или к любому из вспомогательных веществ;
пациенты с тяжелой печеночной недостаточностью (класс C по шкале Чайлд-Пью);
совместное применение со следующими препаратами: атазанавир, аторвастатин, симвастатин, дабигатрана этексилат, препаратами, содержащими эстрадиол, сильными индукторами Р-гликопротеина и CYP3A, например, рифампицин, карбамазепин, препараты зверобоя продырявленного (Hypericum perforatum), фенобарбитал, фенитоин, примидон;
детский возраст до 12 лет;
дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция.
С осторожностью
Препарат Мавирет не рекомендуется применять совместно с омепразолом (40 мг), дарунавиром/ритонавиром, эфавирензом, лопинавиром/ритонавиром, ловастатином, циклоспорином (>100 мг/сут).
Препарат Мавирет следует применять с осторожностью со следующими препаратами: дигоксин, правастатин, розувастатин, флувастатин, питавастатин, такролимус.
Применение при беременности и кормлении грудью
Беременность
Данные о применении глекапревира или пибрентасвира у беременных женщин ограничены или отсутствуют. За время исследований имело место менее 300 случаев беременности.
Исследования глекапревира и пибрентасвира на крысах и мышах не продемонстрировали наличие прямого токсического действия на репродуктивную функцию. Наличие токсического воздействия на беременную самку с последующим выкидышем наблюдалось у кроликов при применении глекапревира, что исключило возможность дальнейших исследований. В качестве меры предосторожности, препарат Мавирет не рекомендуется применять во время беременности.
Период грудного вскармливания
Неизвестно, выделяются ли глекапревир или пибрентасвир с грудным молоком. Доступные данные исследований фармакокинетики у животных показали экскрецию глекапревира и пибрентасвира с молоком, поэтому нельзя исключить риск для новорожденных и детей первого года жизни. Должно быть принято решение либо прекратить грудное вскармливание, либо прекратить терапию препаратом Мавирет или воздержаться от нее, принимая во внимание соотношение пользы грудного вскармливания для ребенка и пользы терапии для женщины.
Фертильность
Исследования влияния глекапревира и/или пибрентасвира на фертильность у человека не проводились. Исследования у животных не показали негативного воздействия глекапревира или пибрентасвира на фертильность при экспозиции, превышающей значения, достигаемые у пациентов в результате приема рекомендованных доз препаратов.
Применение при нарушениях функции печени
У пациентов с печеночной недостаточностью легкой степени тяжести (класс А по шкале Чайлд-Пью) коррекция дозы препарата не требуется.
Препарат не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс B по шкале Чайлд-Пью) и противопоказан пациентам с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью).
Применение при нарушениях функции почек
У пациентов с почечной недостаточностью, включая пациентов на диализе, коррекция дозы препарата Мавирет не требуется.
Применение у детей
Противопоказано применение препарата в детском возрасте до 12 лет.
Применение у пожилых пациентов
У пациентов пожилого возраста коррекция дозы препарата не требуется.
Особые указания
Реактивация вирусного гепатита В
Во время лечения противовирусными препаратами прямого действия сообщалось о реактивации вируса гепатита B, в некоторых случаях со смертельным исходом. Перед началом терапии все пациенты должны проходить обследование на наличие ВГВ. Пациенты с ко-инфекцией ВГВ/ВГС подвержены риску реактивации ВГВ, поэтому следует проводить их мониторинг и ведение с соблюдением современных рекомендаций.
Потенциальные эффекты полной элиминации ВГС из организма препаратами прямого противовирусного действия
У пациентов может наблюдаться улучшение функционирования печени в результате лечения ХВГС, выражающееся в улучшении метаболизма глюкозы в печени. Для пациентов с сахарным диабетом это означает улучшение показателей концентрации глюкозы в крови. Редкие случаи симптоматической гипогликемии были зарегистрированы в рамках терапии препаратами прямого противовирусного действия, поэтому у пациентов с сахарным диабетом рекомендуется проводить тщательный мониторинг концентрации глюкозы в крови для определения целесообразности коррекции доз гипогликемических препаратов.
Нарушение функции печени
Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс B по шкале Чайлд-Пью) и противопоказан пациентам с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью) (см. разделы «Режим дозирования», «Противопоказания»).
Взаимодействие с другими лекарственными препаратами
Подробную информацию см. в разделе «Лекарственное взаимодействие».
Влияние на способность к управлению транспортными средствами и механизмами
Препарат Мавирет не оказывает влияния или оказывает незначительное влияние на способность к вождению транспортными средствами и управлению механизмами.
Передозировка
Наибольшая задокументированная доза, принятая здоровыми добровольцами, составила 1200 мг 1 раз/сут в течение 7 дней для глекапревира и 600 мг 1 раз/сут в течение 10 дней для пибрентасвира. Бессимптомное повышение АЛТ в сыворотке (>5 раз ВГН) наблюдалось у 1 из 70 здоровых добровольцев после приема нескольких доз глекапревира (700 мг или 800 мг) 1 раз/сут в течение ≥7 дней.
Лечение: в случае передозировки необходимо контролировать состояние пациента на наличие признаков токсического поражения (см. раздел «Побочное действие»). Соответствующее симптоматическое лечение должно быть начато немедленно. Гемодиализ в незначительной степени способствует выделению из организма глекапревира и пибрентасвира.
Лекарственное взаимодействие
Возможное влияние препарата Мавирет на другие лекарственные препараты
Глекапревир и пибрентасвир – ингибиторы Р-гликопротеина (P-GP), белка резистентности рака молочной железы (BCRP) и полипептида, транспортирующего органические анионы (OATP) 1B1/3.
Одновременное применение с препаратом Мавирет может привести к повышению концентрации в плазме препаратов, являющихся субстратами Р-гликопротеина (дабигатрана этексилат, дигоксин), BCRP (розувастатин) или OATP1B1/3 (аторвастатин, ловастатин, правастатин, розувастатин, симвастатин). См. рекомендации по лекарственному взаимодействию с чувствительными субстратами P-гликопротеина, BCRP и OATP1B1/3 в таблице 9. Для других субстратов P-гликопротеина, BCRP и OATP1B1/3 может потребоваться коррекция дозы.
Глекапревир и пибрентасвир – слабые ингибиторы изоферментов системы цитохрома P450 CYP3A и уридинглюкуронозилтрансферазы (UGT) 1A1 in vivo. Не отмечалось клинически значимого увеличения системного воздействия для чувствительных субстратов CYP3A (мидазолам, фелодипин) и UGT1A1 (ралтегравир) при одновременном приеме с препаратом Мавирет.
Применение глекапревира и пибрентасвира ингибирует помпу, экспортирующую желчные кислоты (BSEP) in vitro.
Не ожидается клинически значимого ингибирования субстратов CYP1A2, CYP2C9, CYP2C19, CYP2D6, UGT1A6, UGT1A9, UGT1A4, UGT2B7, OCT1, OCT2, OAT1, OAT3, MATE1 и MATE2K.
Пациенты, получающие антагонисты витамина К
На фоне лечения препаратом Мавирет может наступить изменение функции печени, поэтому рекомендуется тщательный мониторинг МНО.
Потенциальное влияние других лекарственных препаратов на препарат Мавирет
Совместный прием с сильными индукторами P-гликопротеина/CYP3A
Лекарственные препараты, являющиеся сильными индукторами P-гликопротеина и CYP3A (рифампицин, карбамазепин, зверобой продырявленный (Hypericum perforatum), фенобарбитал, фенитоин и примидон), могут вызвать существенное снижение концентрации глекапревира и пибрентасвира в плазме крови, привести к снижению терапевтического эффекта препарата Мавирет и потере вирусологического ответа. Применение таких препаратов одновременно с препаратом Мавирет противопоказано.
Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются умеренными индукторами P-гликопротеина и CYP3A, может вызвать снижение концентрации глекапревира и пибрентасвира в плазме крови (окскарбазепин, эсликарбазепин, лумакафтор, кризотиниб). Одновременное применение с умеренными индукторами не рекомендуется (см. раздел «Особые указания»).
Глекапревир и пибрентасвир являются субстратами эффлюксных переносчиков P-гликопротеина и/или BCRP. Глекапревир также является субстратом транспортеров печеночного захвата OATP1B1/3. Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются ингибиторами P-гликопротеина и BCRP (циклоспорин, кобицистат, дронедарон, итраконазол, кетоконазол, ритонавир), может замедлить выведение глекапревира и пибрентасвира и может вызвать повышение экспозиции противовирусных препаратов в плазме крови. Лекарственные препараты, являющиеся ингибиторами OATP1B1/3 (элвитегравир, циклоспорин, дарунавир, лопинавир), могут вызвать повышение системной концентрации глекапревира.
Установленное и другое потенциально возможное лекарственное взаимодействие
В таблице 9 приведено влияние отношения средних значений, вычисленных методом наименьших квадратов (90-процентный доверительный интервал) на концентрацию препарата Мавирет и сопутствующих лекарственных препаратов. Направление стрелки указывает направление изменения воздействия (Cmax и AUC) глекапревира, пибрентасвира и сопутствующего лекарственного препарата (↑ – увеличение более чем на 25%, ↓ – снижение более чем на 20%, ↔ – нет изменения (снижение на ≤20% или увеличение на ≤25%).
Таблица 9. Взаимодействие между препаратом Мавирет и другими лекарственными средствами
| Лекарственные препараты по терапевтическим областям/возможным механизмам взаимодействия | Влияние на концентрацию лекарственного препарата | Cmax | AUC | Cmin | Клинически значимые комментарии |
| Блокаторы рецепторов ангиотензина II | |||||
| Лозартан 50 мг однократно | ↑ лозартан | 2.51 (2.00, 3.15) |
1.56 (1.28, 1.89) |
– | Коррекция дозы не требуется. |
| ↑ лозартан карбоновая кислота | 2.18 (1.88, 2.53) |
↔ | – | ||
| Валсартан 80 мг однократно (ингибирование OATP1B1/3) |
↑ валсартан | 1.36 (1.17, 1.58) |
1.31 (1.16, 1.49) |
– | Коррекция дозы не требуется. |
| Антиаритмические препараты | |||||
| Дигоксин 0.5 мг однократно (ингибирование P-гликопротеина) |
↑ дигоксин | 1.72 (1.45, 2.04) |
1.48 (1.40, 1.57) |
– | Рекомендуется соблюдать осторожность и контролировать терапевтическую концентрацию дигоксина. |
| Антикоагулянты | |||||
| Дабигатрана этексилат 150 мг однократно (ингибирование P-гликопротеина) | ↑ дабигатран | 2.05 (1.72, 2.44) |
2.38 (2.11, 2.70) |
– | Одновременное применение противопоказано (см. раздел «Противопоказания»). |
| Противосудорожные препараты | |||||
| Карбамазепин 200 мг 2 раза/сут (индукция P- гликопротеина/CYP3A) | ↓ глекапревир | 0.33 (0.27, 0.41) |
0.34 (0.28, 0.40) |
– | Одновременное применение может привести к снижению терапевтического эффекта препарата Мавирет, и поэтому оно противопоказано (см. раздел «Противопоказания»). |
| ↓ пибрентасвир | 0.50 (0.42, 0.59) |
0.49 (0.43, 0.55) |
– | ||
| Фенитоин, фенобарбитал, примидон | Не изучено. Ожидается: ↓ глекапревир и ↓ пибрентасвир |
||||
| Антимикобактериальные препараты | |||||
| Рифампицин 600 мг однократно (ингибирование OATP1B1/3) | ↑ глекапревир | 6.52 (5.06, 8.41) |
8.55 (7.01, 10.4) |
– | Одновременное применение противопоказано (см. раздел «Противопоказания»). |
| ↔ пибрентасвир | ↔ | ↔ | – | ||
| Рифампицин 600 мг 1 раз/сутa (индукция P-гликопротеина/CYP3A) | ↓ глекапревир | 0.14 (0.11, 0.19) |
0.12 (0.09, 0.15) |
– | |
| ↓ пибрентасвир | 0.17 (0.14, 0.20) |
0.13 (0.11, 0.15) |
– | ||
| Препараты, содержащие этинилэстрадиол | |||||
| Этинилэстрадиол (ЭЭ)/норгестимат 35 мкг/250 мкг 1 раз/сут | ↑ ЭЭ | 1.31 (1.24, 1.38) |
1.28 (1.23, 1.32) |
1.38 (1.25, 1.52) |
Одновременное применение препарата Мавирет с препаратами с содержанием этинилэстрадиола противопоказано из-за риска увеличения уровня АЛТ (см. раздел «Противопоказания»). При применении левоноргестрела, норэтиндрона или норгестимата в качестве контрацептивного средства на основе прогестагена коррекция дозы не требуется. |
| ↑ норэлгестромин | ↔ | 1.44 (1.34, 1.54) |
1.45 (1.33, 1.58) |
||
| ↑ норгестрел | 1.54 (1.34, 1.76) |
1.63 (1.50, 1.76) |
1.75 (1.62, 1.89) |
||
| ЭЭ/левоноргестрел 20 мкг/100 мкг 1 раз/сут | ↑ ЭЭ | 1.30 (1.18, 1.44) |
1.40 (1.33, 1.48) |
1.56 (1.41, 1.72) |
|
| ↑ норгестрел | 1.37 (1.23, 1.52) |
1.68 (1.57, 1.80) |
1.77 (1.58, 1.98) |
||
| Препараты растительного происхождения | |||||
| Зверобой продырявленный (Hypericum perforatum) (индукция P-гликопротеина/CYP3A) | Не изучено. Ожидается: ↓ глекапревир и ↓ пибрентасвир |
Одновременное применение может привести к снижению терапевтического эффекта препарата Мавирет, поэтому данная комбинация противопоказана (см. раздел «Противопоказания»). | |||
| Противовирусные препараты для лечения ВИЧ-инфекции | |||||
| Атазанавир + ритонавир 300/100 мг 1 раз/сутb | ↑ глекапревир | ≥4.06 (3.15, 5.23) |
≥6.53 (5.24, 8.14) |
≥14.3 (9.85, 20.7) |
Одновременное применение препарата Мавирет с атазанавиром противопоказано из-за риска увеличения уровня АЛТ (см. раздел «Противопоказания»). |
| ↑ пибрентасвир | ≥1.29 (1.15, 1.45) |
≥1.64 (1.48, 1.82) |
≥2.29 (1.95, 2.68) |
||
| Дарунавир + ритонавир 800/100 мг 1 раз/сут | ↑ глекапревир | 3.09 (2.26, 4.20) |
4.97 (3.62, 6.84) |
8.24 (4.40, 15.4) |
Одновременное применение с дарунавиром не рекомендуется. |
| ↔ пибрентасвир | ↔ | ↔ | 1.66 (1.25, 2.21) |
||
| Эфавиренз/эмтрицитабин/тенофовир дизопроксил фумарат (ТДФ) 600/300/200 мг 1 раз/сут | ↑ тенофовир | ↔ | 1.29 (1.23, 1.35) |
1.38 (1.31, 1.46) |
Одновременное применение с эфавирензом может привести к снижению терапевтического эффекта препарата Мавирет и не рекомендуется. Не ожидается клинически значимого взаимодействия препарата Мавирет с ТДФ. |
| Влияние эфавиренза/эмтрицитабина/ТДФ на глекапревир и пибрентасвир не оценивалось в данном исследовании, но воздействие глекапревира и пибрентасвира было значительно ниже, чем в других исследованиях подобных доз. | |||||
| Элвитегравир/кобицистат/эмтрицитабин/тенофовира алафенамид (ингибирование P-гликопротеина, BCRP и OATP кобицистатом, ингибирование OATP элвитегравиром) | ↔ тенофовир | ↔ | ↔ | ↔ | Коррекция дозы не требуется. |
| ↑ глекапревир | 2.50 (2.08, 3.00) |
3.05 (2.55, 3.64) |
4.58 (3.15, 6.65) |
||
| ↑ пибрентасвир | ↔ | 1.57 (1.39, 1.76) |
1.89 (1.63, 2.19) |
||
| Лопинавир/ритонавир 400/100 мг 2 раза/сут | ↑ глекапревир | 2.55 (1.84, 3.52) |
4.38 (3.02, 6.36) |
18.6 (10.4, 33.5) |
Одновременное применение не рекомендуется. |
| ↑ пибрентасвир | 1.40 (1.17, 1.67) |
2.46 (2.07, 2.92) |
5.24 (4.18, 6.58) |
||
| Ралтегравир 400 мг 2 раза/сут (ингибирование UGT1A1) | ↑ ралтегравир | 1.34 (0.89, 1.98) |
1.47 (1.15, 1.87) |
2.64 (1.42, 4.91) |
Коррекция дозы не требуется. |
| Противовирусные препараты, применяемые для лечения вирусного гепатита С | |||||
| Софосбувир 400 мг однократно (ингибирование P-гликопротеина/BCRP) |
↑ софосбувир | 1.66 (1.23, 2.22) |
2.25 (1.86, 2.72) |
– | Коррекция дозы не требуется. |
| ↑ GS-331007 | ↔ | ↔ | 1.85 (1.67, 2.04) |
||
| ↔ глекапревир | ↔ | ↔ | ↔ | ||
| ↔ пибрентасвир | ↔ | ↔ | ↔ | ||
| Ингибиторы ГМГ-КоА редуктазы | |||||
| Аторвастатин 10 мг 1 раз/сут (ингибирование OATP1B1/3, P-гликопротеина, BCRP, CYP3A) | ↑ аторвастатин | 22.0 (16.4, 29.5) |
8.28 (6.06, 11.3) |
– | Одновременное применение препарата Мавирет и симвастатина противопоказано (см. раздел «Противопоказания»). |
| Симвастатин 5 мг 1 раз/сут (ингибирование OATP1B1/3, P-гликопротеина, BCRP) | ↑ симвастатин | 1.99 (1.60, 2.48) |
2.32 (1.93, 2.79) |
– | |
| ↑ симвастатиновая кислота | 10.7 (7.88, 14.6) |
4.48 (3.11, 6.46) |
– | ||
| Ловастатин 10 мг 1 раз/сут (ингибирование OATP1B1/3, P-гликопротеина, BCRP) | ↑ ловастатин | ↔ | 1.70 (1.40, 2.06) |
– | Одновременное применение не рекомендуется. При применении ловастатина доза не должна превышать 20 мг/сут, а пациенты должны находиться под наблюдением. |
| ↑ ловастатиновая кислота | 5.73 (4.65, 7.07) |
4.10 (3.45, 4.87) |
– | ||
| Правастатин 10 мг 1 раз/сут (ингибирование OATP1B1/3) | ↑ правастатин | 2.23 (1.87, 2.65) |
2.30 (1.91, 2.76) |
– | Рекомендуется соблюдать осторожность. Доза правастатина не должна превышать 20 мг/сут, а доза розувастатина не должна превышать 5 мг/сут. |
| Розувастатин 5 мг 1 раз/сут (ингибирование OATP1B1/3, BCRP) | ↑ розувастатин | 5.62 (4.80, 6.59) |
2.15 (1.88, 2.46) |
– | |
| Флувастатин, питавастатин | Не изучено. Ожидается: ↑ флувастатин и ↑ питавастатин |
Возможно взаимодействие с флувастатином и питавастатином, рекомендуется соблюдать осторожность при одновременном применении. Рекомендуется применение статина в низкой дозе при начале лечения ПППД. | |||
| Иммунодепрессанты | |||||
| Циклоспорин 100 мг однократно | ↑ глекапревирc | 1.30 (0.95, 1.78) |
1.37 (1.13, 1.66) |
1.34 (1.12, 1.60) |
Препарат Мавирет не рекомендуется для лечения пациентов, которым требуется прием стабильной дозы циклоспорина >100 мг/сут. |
| ↑ пибрентасвир | ↔ | ↔ | 1.26 (1.15, 1.37) |
||
| Циклоспорин 400 мг однократно | ↑ глекапревир | 4.51 (3.63, 6.05) |
5.08 (4.11, 6.29) |
– | |
| ↑ пибрентасвир | ↔ | 1.93 (1.78, 2.09) |
– | ||
| Такролимус 1 мг однократно (ингибирование CYP3A4/P-гликопротеина) | ↑ такролимус | 1.50 (1.24, 1.82) |
1.45 (1.24, 1.70) |
– | Препарат Мавирет в сочетании с такролимусом следует принимать с осторожностью. Возможно увеличение концентрации такролимуса. Следовательно, рекомендуется мониторинг концентрации такролимуса и соответствующая коррекция дозы. |
| ↔ глекапревир | ↔ | ↔ | ↔ | ||
| ↔пибрентасвир | ↔ | ↔ | ↔ | ||
| Ингибиторы протонового насоса | |||||
| Омепразол 20 мг 1 раз/сут (повышает значение pH в желудке) | ↓ глекапревир | 0.78 (0.60, 1.00) |
0.71 (0.58, 0.86) |
– | Одновременное применение с омепразолом в дозе 40 мг 1 раз/сут может привести к снижению терапевтического эффекта препарата Мавирет и не рекомендовано. |
| ↔ пибрентасвир | ↔ | ↔ | – | ||
| Омепразол 40 мг 1 раз/сут (за час до приема пищи) | ↓ глекапревир | 0.36 (0.21, 0.59) |
0.49 (0.35, 0.68) |
– | |
| ↔ пибрентасвир | ↔ | ↔ | – | ||
| Омепразол 40 мг 1 раз/сут ежедневно (вечером, отдельно от приема пищи) | ↓ глекапревир | 0.54 (0.44, 0.65) |
0.51 (0.45, 0.59) |
– | |
| ↔ пибрентасвир | ↔ | ↔ | – | ||
| Антагонисты витамина К | |||||
| Антагонисты витамина К | Не изучено. | При одновременном применении со всеми антагонистами витамина К рекомендуется тщательный мониторинг МНО. Это связано с изменениями функции печени во время терапии препаратом Мавирет. |
ПППД — препарат прямого противовирусного действия.
a Влияние рифампицина на глекапревир и пибрентасвир через 24 ч после приема последней дозы рифампицина.
b Указано влияние атазанавира и ритонавира на первую дозу глекапревира и пибрентасвира.
c Экспозиция глекапревира у инфицированных ВГС пациентов после трансплантации, получавших циклоспорин в дозе 100 мг/сут или меньше, была в 4 раза выше, чем у тех, кто не получал циклоспорин.
Дополнительные исследования межлекарственного взаимодействия проводились со следующими лекарственными препаратами: абакавир, амлодипин, бупренорфин, кофеин, декстрометорфан, долутегравир, эмтрицитабин, фелодипин, ламивудин, ламотриджин, метадон, мидазолам, налоксон, норэтиндрон или другие контрацептивные средства, содержащие прогестин, рилпивирин, тенофовира алафенамид и толбутамид. Клинически значимого взаимодействия не выявлено.
Условия хранения препарата
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата
Срок годности — 3 года. Не применять после истечения срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Эсциталопрам (таблетки, покрытые пленочной оболочкой, 5 мг), инструкция по медицинскому применению РУ № ЛП-005230
Дата последнего изменения: 02.05.2023
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Нозологическая классификация (МКБ-10)
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакокинетика
- Фармакодинамика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Производитель
- Аналоги (синонимы) препарата Эсциталопрам
- Заказ в аптеках Москвы
Действующее вещество
ATX
Фармакологическая группа
Лекарственная форма
Таблетки,
покрытые пленочной оболочкой.
Состав
1 таблетка
содержит:
|
Наименование компонента |
Количество, мг |
||
|
Действующее вещество: |
|||
|
Эсциталопрама |
6,39 мг |
12,78 мг |
25,56 мг |
|
в |
5 мг |
10 мг |
20 мг |
|
Вспомогательные вещества: |
до получения таблетки (без оболочки) массой: |
||
|
90 мг |
180 мг |
300 мг |
|
|
Лактозы |
54,185 мг |
108,37 мг |
176,39 мг |
|
Целлюлоза микрокристаллическая |
20,85 мг |
41,7 мг |
69,5 мг |
|
Кроскармеллоза |
3,75 мг |
7,5 мг |
12,5 мг |
|
Повидон K‑25 |
2,025 мг |
4,05 мг |
6,75 мг |
|
Крахмал |
1,875 мг |
3,75 мг |
6,25 мг |
|
Магния |
0,925 мг |
1,85 мг |
3,05 мг |
|
Вспомогательные вещества: |
до получения таблетки (с оболочкой) массой: |
||
|
95 мг |
185 мг |
305 мг |
|
|
Состав оболочки: |
|||
|
Гипромеллоза |
3,43 мг |
3,43 мг |
3,43 мг |
|
Титана |
0,728 мг |
0,728 мг |
0,728 мг |
|
Макрогол‑400 |
0,612 мг |
0,612 мг |
0,612 мг |
|
Диметикон 100 |
0,23 мг |
0,23 мг |
0,23 мг |
Описание лекарственной формы
Таблетки 5 мг:
круглые, двояковыпуклые, без риски, покрытые пленочной оболочкой белого цвета.
На поперечном разрезе таблетка белого или почти белого цвета.
Таблетки 10 мг:
круглые, двояковыпуклые, без риски, покрытые пленочной оболочкой белого цвета.
На поперечном разрезе таблетка белого или почти белого цвета.
Таблетки 20 мг:
круглые, двояковыпуклые, с риской, покрытые пленочной оболочкой белого цвета.
На поперечном разрезе таблетка белого или почти белого цвета.
Фармакокинетика
Всасывание
Всасывание
почти полное и не зависит от приема пищи. Среднее время достижения максимальной
концентрации в плазме крови (Tmax) составляет 4 часа после
многократного применения. Абсолютная биодоступность эсциталопрама составляет около
80%.
Распределение
Кажущийся
объем распределения после перорального применения составляет от 12 до
26 л/кг. Связывание эсциталопрама и его основных метаболитов с белками
плазмы крови ниже 80%.
Метаболизм
Эсциталопрам
метаболизируется в печени до деметилированного и дидеметилированного
метаболитов. Оба вещества являются фармакологически активными. Азот может
окисляться до метаболита N‑оксида. Основное вещество и его метаболиты
частично выделяются в форме глюкуронидов. После многократного применения средняя
концентрация деметил‑ и дидеметил‑метаболитов обычно составляет
28–31% и менее 5% соответственно от концентрации эсциталопрама.
Биотрансформация
эсциталопрама в деметилированный метаболит происходит главным образом с помощью
изофермента CYP2C19. Возможно некоторое участие изоферментов CYP3A4 и CYP2D6. У
лиц со слабой активностью изофермента CYP2C19 концентрация эсциталопрама в
2 раза выше, чем в случаях с высокой активностью этого изофермента.
Значительных изменений концентрации препарата в случаях со слабой активностью
изофермента CYP2D6 обнаружено не было.
Выведение
Период
полувыведения (T1/2) после многократного применения составляет около
30 часов. Клиренс при пероральном применении (Cloral)
составляет около 0,6 л/мин. У основных метаболитов эсциталопрама T1/2
более продолжителен.
Эсциталопрам
и его основные метаболиты выводятся печенью (метаболический путь) и почками;
большая часть выводится в виде метаболитов с мочой.
Кинетика
эсциталопрама линейна. Равновесная концентрация достигается примерно через
1 неделю. Средняя равновесная концентрация в 50 нмоль/л (от 20 до
125 нмоль/л) достигается при суточной дозе 10 мг.
Пациенты пожилого возраста (старше 65 лет)
У
пожилых пациентов эсциталопрам выводится медленнее, чем у более молодых
пациентов. Количество вещества, находящегося в системном кровотоке,
рассчитанное с помощью фармакокинетического показателя «площадь под кривой»
(AUC) у пожилых пациентов на 50% больше, чем у молодых здоровых добровольцев.
Фармакодинамика
Эсциталопрам
является антидепрессантом, селективным ингибитором обратного захвата серотонина
(СИОЗС) с высокой аффинностью к первичному месту связывания. Эсциталопрам также
связывается с аллостерическим местом связывания белка-транспортера, с аффинностью
меньшей в 1000 раз. Аллостерическая модуляция белка-транспортера усиливает
связывание эсциталопрама в первичном месте связывания, что приводит к более
полному ингибированию обратного захвата серотонина. Эсциталопрам не имеет
совсем или имеет очень слабую способность связываться с рядом рецепторов,
включая: серотониновые 5‑HT1A‑, 5‑HT2‑рецепторы,
дофаминовые D1‑ и D2‑рецепторы, α1‑,
α2‑, β‑адренергические рецепторы, гистаминовые
H1, мускариновые холинергические, бензодиазепиновые и опиатные
рецепторы.
Показания
Депрессивные
эпизоды любой степени тяжести, панические расстройства с/без агорафобии,
социальное тревожное расстройство (социальная фобия), генерализованное
тревожное расстройство, обсессивно-компульсивное расстройство.
Противопоказания
Повышенная
чувствительность к эсциталопраму и другим компонентам препарата; одновременный
прием неселективных необратимых ингибиторов моноаминооксидазы (МАО);
одновременный прием пимозида; детский и подростковый возраст (до 18 лет)
(эффективность и безопасность применения не подтверждены).
С осторожностью
Выраженная
почечная недостаточность (клиренс креатинина (КК) ниже 30 мл/мин), мания и
гипомания, фармакологически неконтролируемая эпилепсия, выраженное суицидальное
поведение, сахарный диабет, цирроз печени, склонность к кровотечениям;
закрытоугольная глаукома или глаукома в анамнезе; одновременный прием с
ингибитором МАО A (моклобемидом) и ингибитором МАО B (селегилином);
серотонинергическими лекарственными препаратами, снижающими порог судорожной
готовности; литием, триптофанами; лекарственными препаратами, содержащими
зверобой продырявленный; пероральными антикоагулянтами и лекарственными
препаратами, влияющими на свертываемость крови; препаратами, способными вызвать
гипонатриемию; препаратами, метаболизирующимися с участием изофермента CYP2C19;
этанолом; электросудорожная терапия; пожилой возраст; беременность; период
грудного вскармливания.
Применение при беременности и кормлении грудью
Применение при беременности
Имеются
ограниченные данные о приеме эсциталопрама во время беременности.
Исследования
эсциталопрама на животных продемонстрировали репродуктивную токсичность.
Эсциталопрам
во время беременности следует принимать только в случаях крайней необходимости
и после тщательной оценки соотношения польза/риск.
Если
прием эсциталопрама продолжается на поздних сроках беременности, особенно в
третьем триместре, то за новорожденными следует установить наблюдение. В случае
если прием эсциталопрама продолжался вплоть до родов или был прекращен
незадолго до родов, у новорожденного возможно развитие симптомов «отмены».
В
случае применения матерью СИОЗС или селективных ингибиторов обратного захвата
серотонина и норадреналина (СИОЗСН) на поздних сроках беременности, у
новорожденного могут развиться следующие побочные эффекты: угнетение дыхания,
цианоз, апноэ, судорожные расстройства, скачки температуры, трудности с
кормлением, рвота, гипогликемия, гипертония, мышечная гипотония,
гиперрефлексия, тремор, повышенная нервно-рефлекторная возбудимость,
раздражительность, летаргический сон, постоянный плач, сонливость, плохой сон.
Данные симптомы могут возникнуть вследствие развитая синдромам «отмены» или
серотонинергического действия. В большинстве случаев подобные осложнения
возникают в течение 24 часов после рождения.
Данные
эпидемиологических исследований позволяют предположить, что применение СИОЗС во
время беременности, особенно на поздних сроках, может увеличить риск развития
устойчивой легочной гипертензии у новорожденных (PPHN). Наблюдаемый риск
составил около 5 случаев на 1000 беременностей.
Данные
наблюдений указывают на повышенный (менее чем в 2 раза) риск послеродового
кровотечения после применения препаратов групп СИОЗС/СИОЗСН в течение одного
месяца до родов.
Применение в период грудного вскармливания
Ожидается,
что эсциталопрам будет выделяться с грудным молоком, поэтому во время лечения
эсциталопрамом кормление грудью не рекомендуется.
Фертильность
Данные
исследований на животных показали, что некоторые СИОЗС могут влиять на качество
спермы. Данных исследований этого аспекта на животных для эсциталопрама нет.
Сообщения о применении некоторых СИОЗС у человека показали, что влияние этих
лекарственных препаратов на качество спермы является обратимым. До сих пор
влияния эсциталопрама на фертильность у человека не наблюдалось.
Способ применения и дозы
ЭСЦИТАЛОПРАМ
назначают перорально один раз в сутки вне зависимости от приема пищи.
Депрессивные эпизоды
Обычно
назначают по 10 мг 1 раз в сутки. В зависимости от индивидуальной
реакции пациента доза может быть увеличена до максимальной — 20 мг в
сутки.
Антидепрессивный
эффект обычно развивается через 2–4 недели после начала лечения. После
исчезновения симптомов депрессии, как минимум, еще в течение 6 месяцев
необходимо продолжать терапию для закрепления полученного эффекта.
Паническое расстройство с/без агорафобии
Рекомендуемая
начальная доза в течение первой недели терапии составляет 5 мг в сутки,
которая затем увеличивается до 10 мг в сутки. В зависимости от
индивидуальной реакции пациента доза может быть увеличена до максимальной —
20 мг в сутки. Максимальный терапевтический эффект достигается примерно
через три месяца после начала терапии. Терапия длится несколько месяцев.
Социальное тревожное расстройство (социальная фобия)
Обычно
назначают 10 мг один раз в сутки. В зависимости от индивидуальной реакции
пациента доза может быть увеличена до максимальной — 20 мг в сутки.
Ослабление симптомов обычно развивается через 2–4 недели после начала
лечения.
Поскольку
социальное тревожное расстройство является заболеванием с хроническим течением,
минимальная рекомендуемая длительность терапевтического курса составляет
3 месяца. Для предотвращения рецидивов заболевания препарат может
назначаться в течение 6 месяцев или дольше в зависимости от индивидуальной
реакции пациента. Рекомендуется регулярно проводить оценку проводимого лечения.
Генерализованное тревожное расстройство
Обычно
назначают 10 мг один раз в сутки. В зависимости от индивидуальной реакции
пациента доза может быть увеличена до максимальной — 20 мг в сутки.
Минимальная
рекомендуемая длительность терапевтического курса составляет 3 месяца. Для
предотвращения рецидивов заболевания допускается длительное применение
препарата (6 месяцев и дольше). Рекомендуется регулярно проводить оценку
проводимого лечения.
Обсессивно-компульсивное расстройство
Обычно
назначают 10 мг один раз в сутки. В зависимости от индивидуальной реакции
пациента доза впоследствии может быть увеличена до максимальной — 20 мг в
сутки.
Поскольку
обсессивно-компульсивное расстройство является заболеванием с хроническим
течением, курс лечения должен быть достаточно длительным для обеспечения
полного избавления от симптомов и длиться, по меньшей мере, 6 месяцев. Для
предотвращения рецидивов рекомендуется лечение не менее 1 года.
Пациенты пожилого возраста (старше 65 лет)
Рекомендуется
применять половину обычной рекомендуемой дозы (5 мг в сутки) и более
низкую максимальную дозу (10 мг в сутки).
Дети и подростки (до 18 лет)
ЭСЦИТАЛОПРАМ
не следует применять у детей и подростков младше 18 лет (см. раздел
«Особые указания»). Кроме того, нет достаточного объема данных долгосрочных
исследований по безопасности применения препарата у детей и подростков,
касающихся роста, созревания, когнитивного и поведенческого развития.
Сниженная функция почек
При
легкой и умеренной почечной недостаточности коррекции доз не требуется.
Пациентам с выраженной почечной недостаточностью (КК ниже 30 мл/мин)
следует назначать препарат с осторожностью.
Сниженная функция печени
Рекомендуемая
начальная доза в течение первых двух недель лечения составляет 5 мг в сутки.
В зависимости от индивидуальной реакции пациента доза может быть увеличена до
10 мг в сутки.
Сниженная активность изофермента CYP2C19
Для
пациентов со слабой активностью изофермента CYP2C19 рекомендуемая начальная
доза в течение первых двух недель лечения составляет 5 мг в сутки. В
зависимости от индивидуальной реакции пациента доза может быть увеличена до
10 мг в сутки.
Прекращение лечения
При
прекращении лечения препаратом ЭСЦИТАЛОПРАМ дозу следует уменьшать постепенно в
течение 1–2 недель во избежание возникновения синдрома «отмены».
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Побочные
эффекты наиболее часто развиваются на первой или второй неделе лечения и затем
обычно становятся менее интенсивными и возникают реже при продолжении терапии.
Ниже
перечислены побочные эффекты, возникающие при приеме препаратов, принадлежащих
к классу СИОЗС и отмеченные при приеме эсциталопрама. Информация представлена
на основании данных плацебо-контролируемых клинических исследований и
спонтанных сообщений.
По
данным Всемирной организации здравоохранения (ВОЗ) нежелательные реакции
классифицированы в соответствии с их частотой развития следующим образом: очень
часто (>1/10); часто (>1/100, <1/10); нечасто (>1/1000, <1/100);
редко (>1/10000, <1/1000); очень редко (<1/10000); частота неизвестна
— по имеющимся данным установить частоту возникновения не представлялось
возможным.
Нарушения со стороны крови и лимфатической системы
Частота неизвестна:
тромбоцитопения.
Нарушения со стороны иммунной системы
Редко:
анафилактические реакции.
Нарушения со стороны эндокринной системы
Частота неизвестна:
недостаточная секреция антидиуретического гормона (АДГ).
Нарушения со стороны обмена веществ и питания
Часто: снижение
аппетита, повышение аппетита, увеличение веса.
Нечасто: снижение веса.
Частота неизвестна:
гипонатриемия, анорексия2.
Нарушения со стороны психики
Часто: тревога,
беспокойство, необычные сновидения, снижение либидо, аноргазмия (у женщин).
Нечасто: бруксизм,
ажитация, нервозность, панические атаки, спутанность сознания.
Редко: агрессия,
деперсонализация, галлюцинации.
Частота неизвестна:
мания, суицидальные мысли, суицидальное поведение.
Случаи
появления суицидальных мыслей и поведения были отмечены при приеме
эсциталопрама и сразу после отмены терапии1.
Нарушения со стороны нервной системы
Часто: бессонница,
сонливость, головокружение, парестезии, тремор.
Нечасто: нарушение
вкусовых ощущений, нарушение сна, синкопальные состояния.
Редко: серотониновый
синдром.
Частота неизвестна:
дискинезия, двигательные нарушения, судорожные расстройства, психомоторное
возбуждение/акатизия2.
Нарушения со стороны органа зрения
Нечасто: мидриаз
(расширение зрачка), нарушение зрения.
Нарушения со стороны органа слуха и лабиринтные нарушения
Нечасто: тиннитус (шум в
ушах).
Нарушения со стороны сердечно-сосудистой системы
Нечасто: тахикардия.
Редко: брадикардия.
Частота неизвестна:
удлинение интервала QT на электрокардиограмме, ортостатическая гипотензия.
Со стороны дыхательной системы, органов грудной клетки и
средостения
Часто: синуситы,
зевота.
Нечасто: носовое
кровотечение.
Нарушения со стороны желудочно-кишечного тракта
Очень часто:
тошнота.
Часто: диарея, запор,
рвота, сухость во рту.
Нечасто:
желудочно-кишечное кровотечение (в том числе ректальное кровотечение).
Нарушения со стороны печени и желчевыводящих путей
Частота неизвестна:
гепатит, нарушения функциональные показателей печени.
Нарушения со стороны кожи и подкожных тканей
Часто: повышенная
потливость.
Нечасто: крапивница,
алопеция, сыпь, зуд.
Частота неизвестна:
экхимоз, ангионевротический отек.
Нарушения со стороны скелетно-мышечной и соединительной
ткани
Часто: миалгия,
артралгия.
Нарушения со стороны почек и мочевыводящих путей
Частота неизвестна:
задержка мочи.
Нарушения со стороны репродуктивной системы и молочных желез
Часто: импотенция, нарушение
эякуляции (у мужчин).
Нечасто: метроррагия
(маточное кровотечение), меноррагия (у женщин).
Частота неизвестна:
галакторея, послеродовое кровотечение3, приапизм (у мужчин).
Общие нарушения и реакции в месте введения
Часто: слабость,
гипертермия.
Нечасто: отеки.
1 Имеются
сообщения о случаях суицидальных настроений и суицидального поведения во время
приема эсциталопрама или сразу же после прекращения лечения.
2 Сообщения
о данных явлениях поступили в отношении лечебного класса СИОЗС.
3 Данное
нежелательное явление зарегистрировано как класс-эффект для препаратов групп
СИОЗС/СИОЗСН (см. раздел «Применение при беременности и в период грудного
вскармливания»).
В
пострегистрационный период были отмечены случай удлинения интервала QT, в
основном у пациентов с ранее существующими заболеваниями сердца.
В
двойных слепых плацебо-контролируемых исследованиях ЭКГ у здоровых добровольцев
изменение от базового значения QTc (коррекция по формуле Фридеричиа)
составило 4,3 мсек при дозе 10 мг/сут и 10,7 мсек — при
30 мг/сут.
Эпидемиологические
исследования с участием пациентов в возрасте 50 лет и старше показали
существование повышенного риска костных переломов у пациентов, принимающих
СИОЗС и трициклические антидепрессанты. Механизм возникновения этого риска не
установлен.
Отмена
препаратов группы СИОЗС/СИОЗСН (особенно резкая) часто приводит к возникновению
симптомов «отмены». Наиболее часто возникают головокружение, расстройства
чувствительности (в том числе парестезии и ощущения прохождения тока),
расстройства сна (в том числе бессонница и интенсивные сновидения), ажитация
или тревога, тошнота и/или рвота, тремор, спутанность сознания, повышенное
потоотделение, головная боль, диарея, сердцебиение, эмоциональная
нестабильность, раздражительность, расстройства зрения. Как правило, эти
эффекты выражены слабо или умеренно и быстро проходят, однако, у некоторых
пациентов они могут проявляться в более острой форме и/или более длительно.
Рекомендуется проводить постепенную отмену препарата путем снижения его дозы.
Взаимодействие
Фармакодинамическое взаимодействие
Неселективные необратимые ингибиторы МАО
Сообщалось
о возникновении серьезных нежелательных реакций при одновременном приеме СИОЗС
и неселективных необратимых ингибиторов МАО, а также при начале приема ингибиторов
МАО больными, незадолго до этого прекратившими прием СИОЗС. В некоторых
случаях у пациентов развивался серотониновый синдром.
Применять
эсциталопрам одновременно с неселективными необратимыми ингибиторами МАО
запрещено. Прием эсциталопрама может быть начат через 14 дней после отмены
приема необратимых ингибиторов МАО. Перед началом приема неселективных
необратимых ингибиторов МАО должно пройти не менее 7 дней после окончания
приема эсциталопрама.
Обратимый селективный ингибитор МАО A (моклобемид)
Из-за
риска развития серотонинового синдрома не рекомендуется применять эсциталопрам
одновременно с ингибитором МАО A моклобемидом. В случае если прием такой
комбинации препаратов признан клинически необходимым, рекомендуется начать с
минимально возможных доз, а также проводить постоянный клинический мониторинг
состояния пациента. Прием эсциталопрама можно начать, как минимум, через один
день после отмены обратимого ингибитора МАО A моклобемида.
Необратимый ингибитор МАО B (селегилин)
Из-за
риска развития серотонинового синдрома необходимо соблюдать осторожность при
приеме эсциталопрама одновременно с необратимым ингибитором МАО B
селегилином.
Серотонинергические лекарственные препараты
Совместное
применение с серотонинергическими лекарственными препаратами (например,
трамадолом, суматриптаном и другими триптанами) может привести к развитию
серотонинового синдрома.
Лекарственные препараты, снижающие порог судорожной
готовности
СИОЗС
могут снижать порог судорожной готовности. Требуется проявлять осторожность при
одновременном с эсциталопрамом применении других лекарственных препаратов,
снижающих порог судорожной готовности (трициклических антидепрессантов, СИОЗС,
антипсихотических препаратов (нейролептиков) — производных фенотиазина,
тиоксантена и бутирофенона, мефлохина, бупропиона и трамадола).
Литий, триптофан
Поскольку
зарегистрированы случаи усиления действия при одновременном применении СИОЗС и
лития или триптофана, рекомендуется проявлять осторожность при одновременном
применении эсциталопрама с этими препаратами.
Зверобой продырявленный
Одновременное
применение СИОЗС и препаратов, содержащих зверобой продырявленный (Hypericum
perforatum), может привести к увеличению числа побочных эффектов.
Антикоагулянты и средства, влияющие на свертываемость крови
Нарушения
свертываемости крови может возникнуть при одновременном применении
эсциталопрама с пероральными антикоагулянтами и лекарственными препаратами,
влияющими на свертываемость крови (например, атипичными нейролептиками и
производными фенотиазина, большинством трициклических антидепрессантов,
ацетилсалициловой кислотой и нестероидными противовоспалительными препаратами,
тиклопидином, дипиридамолом). В подобных случаях при начале или окончании
терапии эсциталопрамом необходим тщательный мониторинг свертываемости крови.
Одновременный прием с нестероидными противовоспалительными препаратами может
привести к увеличению числа кровотечений.
Фармакокинетическое взаимодействие
Влияние других лекарственных препаратов на фармакокинетику
эсциталопрама
Метаболизм
эсциталопрама в основном осуществляется при участии изофермента CYP2C19.
В меньшей степени в метаболизме могут принимать участие изоферменты CYP3A4
и CYP2D6. Метаболизм основного метаболита — деметилированного эсциталопрама —
видимо, частично катализируется изоферментом CYP2D6.
Одновременное
применение эсциталопрама и омепразола (ингибитор изофермента CYP2C19) приводит
к умеренному (приблизительно 50%) повышению концентрации эсциталопрама в плазме
крови.
Одновременный
прием эсциталопрама и циметидина (ингибитора изоферментов CYP2D6, CYP3A4 и
CYP1A2) приводит к повышению (примерно 70%) концентрации эсциталопрама в плазме
крови.
Таким
образом, применять максимально возможные дозы эсциталопрама одновременно с
ингибиторами изофермента CYP2C19 (например, омепразолом, флуоксетином,
флувоксамином, лансопразолом, тиклопидином) и циметидином следует с
осторожностью. При одновременном приеме эсциталопрама и вышеуказанных
препаратов на основе клинической оценки может потребоваться уменьшение дозы
эсциталопрама.
Влияние эсциталопрама на фармакокинетику других
лекарственных средств
Эсциталопрам
является ингибитором изофермента CYP2D6. Необходимо проявлять осторожность при
одновременном применении эсциталопрама и лекарственных препаратов,
метаболизирующихся с помощью этого изофермента и имеющих малый терапевтический
индекс, например, флекаинида, пропафенона и метопролола (в случаях применения
при сердечной недостаточности), или лекарственных препаратов, в основном
метаболизирующихся посредством CYP2D6 и действующих на ЦНС, например,
антидепрессантов: дезипрамина, кломипрамина, нортриптилина или
антипсихотических препаратов: рисперидона, тиоридазина, галоперидола. В этих
случаях может потребоваться коррекция дозы.
Одновременное
применение эсциталопрама и дезипрамина или метопролола приводит к двукратному
увеличению концентрации двух последних препаратов.
Эсциталопрам
может незначительно ингибировать изофермент CYP2C19. Поэтому рекомендуется
проявлять осторожность при одновременном применении эсциталопрама и
лекарственных препаратов, метаболизирующихся изоферментом CYP2C19.
Передозировка
Данные
о передозировке эсциталопрамом ограничены, во многих таких случаях имелась и
передозировка другими препаратами. В большинстве случаев симптомы передозировки
не проявляются или проявляются слабо. Случаи передозировки эсциталопрамом (без
приема других препаратов) с летальным исходом единичны, в большинстве случаев
имеет место также передозировка и другими препаратами.
Симптомы
При
передозировке эсциталопрамом в основном возникают симптомы со стороны
центральной нервной системы (ЦНС) (от головокружения, тремора и ажитации до
редких случаев развития серотонинового синдрома, судорожных расстройств и
комы), со стороны желудочно-кишечного тракта (тошнота/рвота),
сердечно-сосудистой системы (гипотензия, тахикардия, удлинение
интервала QT и аритмия) и нарушения электролитного баланса (гипокалиемия,
гипонатриемия).
Лечение
Специфического
антидота не существует. Следует обеспечить нормальную проходимость дыхательных
путей, оксигенацию и вентиляцию легких. Следует провести промывание желудка и
назначить активированный уголь. Промывание желудка следует провести как можно
быстрее после приема препарата. Рекомендуется контролировать показатели работы
сердца и других жизненно важных органов и проводить симптоматическую и
поддерживающую терапию.
Особые указания
Применение у детей и подростков в возрасте до 18 лет
Антидепрессанты
не следует назначать детям и подросткам в возрасте до 18 лет из‑за
повышенного риска возникновения суицидального поведения (попыток суицида и
суицидальных мыслей), враждебности (с преобладанием агрессивного поведения,
склонности к конфронтации и раздражению). В случае принятия на основании
клинической оценки решения о начале терапии антидепрессантами пациент должен
находиться под тщательным наблюдением.
При
применении препаратов, принадлежащих к терапевтической группе СИОЗС, включая
эсциталопрам, следует учитывать следующее.
Парадоксальная тревога
У
некоторых пациентов с паническим расстройством в начале лечения
антидепрессантами может наблюдаться усиление тревоги. Подобная парадоксальная
реакция обычно исчезает в течение первых двух недель лечения. Чтобы снизить
вероятность возникновения анксиогенного эффекта рекомендуется использовать
низкие начальные дозы.
Судорожные припадки
Следует
отменить эсциталопрам в случае первичного развития судорожных припадков или в
случае усиления их частоты (у пациентов с ранее диагностированной эпилепсией).
СИОЗС не следует применять у больных с нестабильной эпилепсией; при
контролируемых припадках необходимо тщательное наблюдение.
Мания/гипомания
Эсциталопрам
должен с осторожностью применяться у больных с манией/гипоманией в анамнезе.
При развитии маниакального состояния эсциталопрам должен быть отменен.
Сахарный диабет
У
пациентов с сахарным диабетом лечение эсциталопрамом может изменить
концентрацию глюкозы в крови. Поэтому может потребоваться коррекция доз
инсулина и/или пероральных гипогликемических препаратов.
Суицид/суицидальные мысли или клиническое ухудшение
Депрессия
связана с повышенным риском возникновения суицидальных мыслей, нанесения себе
телесных повреждений и суицида (суицидальные явления). Этот риск сохраняется до
наступления выраженной ремиссии. Поскольку улучшения может не наблюдаться в
течение первых нескольких недель терапии или даже большего промежутка времени,
пациенты должны находиться под постоянным наблюдением до наступления улучшения
их состояния.
Общая
клиническая практика показывает, что на ранних стадиях выздоровления возможно
увеличение риска самоубийства.
Другие
психические состояния, для лечения которых назначают эсциталопрам, также могут
быть связаны с повышенным риском возникновения суицидальных событий и явлений.
Кроме того, эти состояния могут являться сопутствующей патологией по отношению
к депрессивному эпизоду.
При
лечении пациентов с другими психическими расстройствами следует соблюдать те же
самые предосторожности, что при лечении пациентов с депрессивным эпизодом.
Пациенты,
имеющие в анамнезе суицидальное поведение, или пациенты со значительным уровнем
размышления на суицидальные темы до начала лечения в большей степени подвержены
риску суицидальных мыслей или попыток суицида, поэтому во время лечения за ними
должно вестись тщательное наблюдение. Мета‑анализ плацебо-контролируемых
клинических исследований антидепрессантов с участием взрослых пациентов с
психическими нарушениями показал, что при приеме антидепрессантов у пациентов
моложе 25 лет существует повышенный риск суицидального поведения по
сравнению с приемом плацебо. Медикаментозное лечение этих пациентов и, в
частности, пациентов с высокой степенью риска суицида, должно сопровождаться
тщательным наблюдением, особенно на ранней стадии лечения и при изменениях
дозы.
Пациенты
(и лица, ухаживающие за пациентами) должны быть предупреждены о необходимости
контролировать любые проявления клинического ухудшения, суицидального поведения
или мыслей, а также необычных изменений в поведении, и немедленно обращаться за
медицинской консультацией при появлении этих симптомов.
Акатизия/психомоторное возбуждение
Применение
СИОЗС/СИОЗСН ассоциируется с развитием акатизии, характеризующейся развитием
субъективно неприятного или угнетающего беспокойства и потребности в постоянном
движении, часто в сочетании с неспособностью сидеть или стоять. Это чаще всего
проявляется в течение первых нескольких недель лечения. У пациентов с такими
симптомами повышение дозы может привести к ухудшению.
Гипонатриемия
Гипонатриемия,
возможно связанная с нарушением секреции АДГ, на фоне приема СИОЗС возникает
редко и обычно исчезает при отмене терапии. Осторожность должна проявляться при
назначении эсциталопрама и других СИОЗС лицам, входящим в группу риска развития
гипонатриемии: пожилым, больным с циррозом печени и принимающим препараты,
способные вызывать гипонатриемию.
Кровотечение
При
приеме СИОЗС были отмечены случаи развития кожных кровоизлияний (экхимоз и
пурпура). Прием лекарственных препаратов групп СИОЗС/СИОЗСН может повышать риск
развития послеродового кровотечения (см. разделы «Применение при
беременности и в период грудного вскармливания», «Побочное действие»).
Необходимо
с осторожностью применять эсциталопрам у пациентов, принимающих пероральные
антикоагулянты и лекарства, влияющие на свертываемость крови, а также у больных
со склонностью к кровотечениям.
Электросудорожная терапия (ЭСТ)
Поскольку
клинический опыт одновременного применения СИОЗС и ЭСТ ограничен, то при
одновременном применении эсциталопрама и ЭСТ следует соблюдать осторожность.
Обратимые селективные ингибиторы МАО A
Сочетать
эсциталопрам и ингибиторы МАО A не рекомендуется из-за риска развития
серотонинового синдрома.
Серотониновый синдром
Необходимо
с осторожностью применять эсциталопрам одновременно с лекарственными
препаратами, обладающими серотонинергическим действием, например, суматриптаном
или другими триптанами, трамадолом и триптофаном.
У
больных, принимающих эсциталопрам и другие СИОЗС одновременно с
серотонинергическими препаратами, в редких случаях развивался серотониновый
синдром. На его развитие может указывать комбинация таких симптомов, как
ажитация, тремор, миоклонус и гипертермия. Если это произошло, следует
немедленно прекратить одновременное лечение СИОЗС и серотонинергическими
препаратами и начать симптоматическое лечение.
Закрытоугольная глаукома
СИОЗС,
в том числе эсциталопрам, могут влиять на размер зрачков, вызывая мидриаз. За
счет данного эффекта может уменьшаться угол обзора, а в дальнейшем может
повышаться внутриглазное давление и развиваться закрытоугольная глаукома;
особенно это характерно для пациентов с предрасположенностью к такому состоянию.
В связи с этим следует с особой осторожностью применять эсциталопрам у
пациентов с закрытоугольной глаукомой или с наличием глаукомы в анамнезе.
Алкоголь
Эсциталопрам
не вступает с алкоголем в фармакодинамическое или фармакокинетическое
взаимодействие. Однако, как и в случае с другими психотропными лекарственными
препаратами, одновременное применение эсциталопрама и алкоголя не
рекомендуется.
Влияние на способность управлять
транспортными средствами, механизмами
Несмотря
на то, что эсциталопрам не влияет на интеллектуальные функции и психомоторную
активность, в период лечения больным не рекомендуется управлять автомобилем или
механизмами.
Форма выпуска
Таблетки,
покрытые пленочной оболочкой, 5 мг, 10 мг, 20 мг.
По
7 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и
фольги алюминиевой печатной лакированной.
1,
2, 3, 4, 5 контурных ячейковых упаковок вместе с инструкцией по применению
помещают в пачку из картона.
По
10 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и
фольги алюминиевой печатной лакированной.
1,
2, 3, 4, 5, 6, 7, 8, 9, 10 контурных ячейковых упаковок вместе с
инструкцией по применению помещают в пачку из картона.
Условия отпуска из аптек
Условия хранения
Хранить
при температуре не выше 25 °C.
Хранить
в недоступном для детей месте.
Срок годности
3 года.
Не
применять по истечении срока годности, указанного на упаковке.
Производитель
Производитель/Организация, принимающая претензии
ООО
«ПРАНАФАРМ»
РФ,
443068, г. Самара, ул. Ново-Садовая, дом 106, корпус 81
E‑mail: info@pranapharm.ru
www.pranapharm.ru
Тел.:
(846) 334-52-32, 207-12-61
Факс:
(846) 335-15-61, 207-41-62
Описание проверено
-
Комкова Людмила Александровна
(Провизор)
Опыт работы: более 12 лет
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Эсциталопрам (Escitalopram)
💊 Состав препарата Эсциталопрам
✅ Применение препарата Эсциталопрам
Препарат отпускается по рецепту
Температура хранения: от 2 до 25 °С

Описание активных компонентов препарата
Эсциталопрам
(Escitalopram)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.07.03
Владелец регистрационного удостоверения:
Код ATX:
N06AB10
(Эсциталопрам)
Лекарственная форма
|
Препарат отпускается по рецепту |
Эсциталопрам |
Таблетки, покрытые пленочной оболочкой, 10 мг: 10, 14, 28, 30 или 56 шт. рег. №: ЛП-(008467)-(РГ-RU) Предыдущий рег. №: ЛП-003256 |
Форма выпуска, упаковка и состав
препарата Эсциталопрам
Таблетки, покрытые пленочной оболочкой белого или почти белого цвета, круглые, двояковыпуклые, с риской на одной стороне; на поперечном разрезе ядра таблеток имеют белый или почти белый цвет.
Вспомогательные вещества: целлюлоза микрокристаллическая силицированная (просолв SMCC) — 124.33 мг, в т.ч.: [целлюлоза микрокристаллическая — 121.843 мг, кремния диоксид коллоидный — 2.487 мг], кроскармеллоза натрия — 6.9 мг, тальк — 4.5 мг, магния стеарат — 1.5 мг.
Состав пленочной оболочки: гипромеллоза — 4.5 мг, макрогол (полиэтиленгликоль) — 0.9 мг, тальк — 1.25 мг, титана диоксид (E171) – 0.85 мг).
7 шт. — упаковки ячейковые контурные (2) — пачки картонные.
7 шт. — упаковки ячейковые контурные (4) — пачки картонные.
7 шт. — упаковки ячейковые контурные (8) — пачки картонные.
10 шт. — упаковки ячейковые контурные (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (3) — пачки картонные.
28 шт. — банки полимерные (1) — пачки картонные.
Фармакологическое действие
Антидепрессант. Селективно ингибирует обратный захват серотонина; повышает концентрацию нейромедиатора в синаптической щели, усиливает и пролонгирует действие серотонина на постсинаптические рецепторы. Эсциталопрам практически не связывается с серотониновыми (5-HT), допаминовыми (D1 и D2) рецепторами, α-адрено-, м-холинорецепторами, а также с бензодиазепиновыми и опиоидными рецепторами.
Антидепрессивный эффект обычно развивается через 2-4 нед. после начала лечения. Максимальный терапевтический эффект лечения панических расстройств достигается примерно через 3 мес после начала лечения.
Фармакокинетика
Всасывание не зависит от приема пищи. Биодоступность — 80%. Время достижения Cmax в плазме — 4 ч. Кинетика эсциталопрама линейна. Css достигается через 1 нед. Средняя Css составляет 50 нмоль/л (от 20 до 125 нмоль/л) и достигается при дозе 10 мг/сут. Кажущийся Vd — от 12 до 26 л/кг. Связывание с белками плазмы — 80%. Метаболизируется в печени до активных деметилированного и дидеметилированного метаболитов. После многократного применения средняя концентрация деметил- и дидеметилметаболитов составляет 28-31% и менее 5% соответственно от концентрации эсциталопрама. Метаболизм эсциталопрама с образованием деметилированного метаболита происходит главным образом при участии изоферментов CYP2C19, CYP3A4 и CYP2D6. У лиц со слабой активностью изофермента CYP2C19 концентрация эсциталопрама может быть в 2 раза выше, чем у лиц с высокой активностью этого изофермента. Значительных изменений концентрации препарата при слабой активности изофермента CYP2D6 не отмечается. T1/2 после многократного применения — 30 ч. У основных метаболитов эсциталопрама T1/2 более продолжителен. Клиренс — 0.6 л/мин. Эсциталопрам и его основные метаболиты выводятся печенью и большая часть — почками, частично выводится в форме глюкуронидов. T1/2 и AUC увеличивается у пациентов пожилого возраста.
Показания активных веществ препарата
Эсциталопрам
Депрессия, панические расстройства (в т.ч. с агорафобией).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Принимают внутрь, независимо от приема пищи. В зависимости от показаний разовая доза — 10-20 мг/сут. Максимальная суточная доза — 20 мг. Длительность лечения — несколько месяцев. При прекращении лечения доза должна постепенно снижаться в течение 1-2 нед. для того, чтобы избежать возникновения синдрома «отмены».
Для пациентов пожилого возраста (старше 65 лет) рекомендуемая доза — 5 мг/сут, максимальная суточная доза — 10 мг.
При нарушении функции печени рекомендуемая начальная в течение первых 2 нед. лечения составляет 5 мг/сут. В зависимости от индивидуальной реакции доза может быть увеличена до 10 мг/сут.
Для пациентов со слабой активностью изофермента CYP2C19 рекомендуемая начальная доза в течение первых 2 нед. лечения — 5 мг/сут. В зависимости от индивидуальной реакции доза может быть увеличена до 10 мг/сут.
Побочное действие
Со стороны нервной системы: головокружение, слабость, бессонница или сонливость, судороги, тремор, двигательные нарушения, серотониновый синдром (ажитация, тремор, миоклонус, гипертермия), галлюцинации, мания, спутанность сознания, ажитация, тревога, деперсонализация, панические атаки, повышенная раздражительность, расстройства зрения.
Со стороны пищеварительной системы: тошнота, рвота, сухость слизистой оболочки полости рта, нарушения вкусовых ощущений, снижение аппетита, диарея, запор, изменение показателей функции печени.
Со стороны сердечно-сосудистой системы: ортостатическая гипотензия.
Со стороны эндокринной системы: снижение секреции АДГ, галакторея.
Со стороны половой системы: снижение либидо, импотенция, нарушение эякуляции, аноргазмия (у женщин).
Со стороны мочевыделительной системы: задержка мочи.
Дерматологические реакции: кожная сыпь, зуд, экхимозы, пурпура, повышенное потоотделение.
Аллергические реакции: ангионевротический отек, анафилактические реакции.
Со стороны обмена веществ: гипонатриемия, гипертермия.
Со стороны костно-мышечной системы: артралгия, миалгия.
Прочие: синуситы, синдром «отмены» (головокружение, головные боли и тошнота).
Противопоказания к применению
Одновременный прием ингибиторов МАО, детский и подростковый возраст до 15 лет, беременность, период лактации, повышенная чувствительность к эсциталопраму.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период лактации (грудного вскармливания).
Применение при нарушениях функции печени
C осторожностью следует применять при циррозе печени.
Применение при нарушениях функции почек
C осторожностью следует применять у пациентов с почечной недостаточностью (КК менее 30 мл/мин).
Применение у детей
Противопоказан в детском и подростковом возрасте до 15 лет.
Применение у пожилых пациентов
C осторожностью следует применять у пациентов пожилого возраста.
Особые указания
C осторожностью следует применять у пациентов с почечной недостаточностью (КК менее 30 мл/мин), гипоманией, манией, при фармакологически неконтролируемой эпилепсии, при депрессии с суицидальными попытками, сахарном диабете, у пациентов пожилого возраста, при циррозе печени, при склонности к кровотечениям, одновременно с приемом лекарственных средств, снижающих порог судорожной готовности, вызывающих гипонатриемию, с этанолом, с препаратами, метаболизирующимися с участием изоферментов системы CYP2C19.
Эсциталопрам следует назначать только через 2 нед. после отмены необратимых ингибиторов МАО и через 24 ч после прекращения терапии обратимым ингибитором МАО. Неселективные ингибиторы МАО можно назначать не ранее чем через 7 дней после отмены эсциталопрама.
У некоторых пациентов с паническим расстройством в начале лечения эсциталопрамом может наблюдаться усиление тревоги, которая исчезает обычно в течение последующих 2 нед. лечения. Чтобы уменьшить вероятность возникновения тревоги, рекомендуется использовать низкие начальные дозы.
Следует отменить эсциталопрам в случае развития эпилептических припадков или их учащении при фармакологически неконтролируемой эпилепсии.
При развитии маниакального состояния эсциталопрам следует отменить.
Эсциталопрам способен повышать концентрацию глюкозы в крови при сахарном диабете, что может потребовать коррекции доз гипогликемических препаратов.
Клинический опыт применения эсциталопрама свидетельствует о возможном увеличении риска реализации суицидальных попыток в первые недели терапии, в связи с чем очень важно осуществлять тщательное наблюдение за пациентами в этот период.
Гипонатриемия, связанная со снижением секреции АДГ, на фоне приема эсциталопрама возникает редко и обычно исчезает при его отмене.
При развитии серотонинового синдрома эсциталопрам следует немедленно отменить и назначить симптоматическое лечение.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения пациентам следует избегать вождения автотранспорта и другой деятельности, требующей высокой концентрации внимания и скорости психомоторных реакций.
Лекарственное взаимодействие
При одновременном применении с ингибиторами МАО повышается риск развития серотонинового синдрома и серьезных побочных реакций.
Совместное применение с серотонинергическими средствами (в т.ч. с трамадолом, триптанами) может привести к развитию серотонинового синдрома.
При одновременном применении с препаратами, снижающими порог судорожной готовности, повышает риск развития судорог.
Эсциталопрам усиливает эффекты триптофана и препаратов лития, повышает токсичность препаратов зверобоя, эффекты лекарственных средств, влияющих на свертывание крови (необходим контроль показателей свертывания крови).
Препараты, метаболизирующиеся с участием изофермента CYP2C19 (в т.ч. омепразол), а также являющиеся сильными ингибиторами CYP3A4 и CYP2D6 (в т.ч. флекаинид, пропафенон, метопролол, дезипрамин, кломипрамин, нортриптилин, рисперидон, тиоридазин, галоперидол), повышают концентрацию эсциталопрама в плазме крови.
Эсциталопрам повышает концентрацию в плазме дезипрамина и метопролола в 2 раза.
Адрес производителя
|
Березовский фармацевтический завод , ЗАО |
Россия |
623704, Свердловская область, г. Берёзовский, улица Кольцевая, д. 13а |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
-
Ленуксин®
(GEDEON RICHTER, Венгрия) -
Мирацитол
(НАНОЛЕК, Россия) -
Селектра
(ABBOTT PRODUCTS OPERATIONS, Швейцария) -
Цивельт
(ГРОТЕКС, Россия) -
Ципралекс
(H.LUNDBECK, Дания) -
Элицея®
(KRKA d.d., Novo mesto, Словения) -
Элицея® КУ-Таб®
(KRKA d.d., Novo mesto, Словения) -
Эсциталопрам
(ПРАНАФАРМ, Россия) -
Эсциталопрам Канон
(КАНОНФАРМА ПРОДАКШН, Россия) -
Эсциталопрам-АЛСИ
(АЛСИ Фарма, Россия)
Все аналоги
(15)
Овитрель раствор — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛС-002622
Торговое наименование препарата
Овитрель®
Международное непатентованное наименование
Хориогонадотропин альфа
Лекарственная форма
раствор для подкожного введения
Состав
Один заполненный шприц с 0,5 мл раствора содержит: активное вещество — хориогонадотропин альфа 250 мкг (6500 ME) и вспомогательные вещества: маннитол 27,3 мг, метионин 0,1 мг, полоксамер 188 0,05 мг, фосфорная кислота 0,49 мг, натрия гидроксид q.s. для корректировки рН, вода для инъекций до 0,5 г.
Описание
Прозрачный или слегка опалесцирующий бесцветный или светло-желтый раствор.
Фармакотерапевтическая группа
Лютеинизирующее средство
Код АТХ
G03GA08
Фармакодинамика:
Овитрель® содержит хориогонадотропин альфа, который производится при помощи рекомбинантной ДНК технологии. Он имеет ту же аминокислотную последовательность, что и естественный человеческий хорионический гонадотропин. Хорионический гонадотропин связывает трансмембранные рецепторы лютеинизирующего гормона (ЛГ) на поверхности клеток теки и гранулезы яичника. Вызывает инициирование ооцитарного мейоза, разрыв фолликулов(овуляцию), формирование желтого тела, продукцию прогестерона и эстрадиола желтым телом.
Фармакокинетика:
Всасывание и распределение
После внутривенного введения хориогонадотропин альфа распределяется во внеклеточную жидкость с периодом полураспределения около 4,5 часов. Стационарный объем распределения и общий клиренс составляют 6 л и 0,2 л/час соответственно.
При подкожном введении хориогонадотропина альфа абсолютная биодоступность составляет приблизительно 40%, конечный период полувыведения — около 30 часов.
Выведение и метаболизм
Метаболизм и выведение хориогонадотропина альфа аналогичны эндогенному хорионическому гонадотропину.
Показания:
В протоколе индукции множественного созревания фолликулов для вспомогательных репродуктивных технологий (ВРТ), в том числе для экстракорпорального оплодотворения (ЭКО), с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизации в конце стимуляции роста фолликулов.
Противопоказания:
— Гиперчувствительность к активному компоненту и к любому из вспомогательных компонентов, входящих в состав препарата;
— Опухоли гипотоламуса и гипофиза;
— Объемные новообразования яичника или кисты, несвязанные с поликистозом яичников.
— Вагинальные кровотечения неясной этиологии.
— Рак яичника, матки или молочной железы.
— Внематочная беременность в течение 3 предыдущих месяцев.
— Тромбоэмболия.
— Первичная овариальная недостаточность.
— Врожденные пороки развития половых органов, несовместимые с беременностью.
— Фибромиома матки, несовместимая с беременностью.
— Постменопауза.
С осторожностью:
С осторожностью следует назначать Овитрель® пациенткам, страдающим тяжелыми системными заболеваниями, в тех случаях, когда беременность может привести к их обострению.
Беременность и лактация:
В период беременности и грудного вскармливания препарат Овитрель® не назначается.
Данные об экскреции хориогонадотропина альфа в грудное молоко отсутствуют.
Способ применения и дозы:
Овитрель® вводится подкожно. Каждый шприц или шприц-ручка предназначены только для однократного использования.
Лечение следует проводить только под руководством врача, имеющего опыт в лечении бесплодия.
В протоколе индукции множественного созревания фолликулов для ВРТ, в том числе для ЭКО, с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов:
Овитрель® в дозе 250 мкг (содержимое 1 шприца или 1 шприц-ручки) вводится однократно через 24-48 часов после последнего введения препарата фолликулостимулирующего гормона или ЛГ и достижения оптимального уровня развития фолликула.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизаиии в конце стимуляции роста фолликулов:
Овитрель® в дозе 250 мкг (содержимое 1 шприца или 1 шприц-ручки) вводится однократно через 24-48 часов после достижения оптимального уровня развития фолликула. Рекомендуется половой контакт в день введения препарата Овитрель® и на следующий день.
Рекомендации по самостоятельному введению препарата Овитрель®.
Самостоятельное введение возможно только пациентами, прошедшими соответствующее обучение и имеющими возможность обратиться за советом к врачу- специалисту.
При самостоятельном введении пациентке следует внимательно прочитать и строго следовать нижеприведенной инструкции по введению препарата:
Перед введением:
1. Вымойте руки. Важно чтобы Ваши руки и предметы, которые Вы используете, были чистыми.
2. Подготовьте чистую поверхность и разложите на ней все, что нужно для инъекции:
1. два тампона, смоченных спиртом (к упаковке не прилагаются);
2. один шприц с препаратом или одна шприц-ручка и игла для инъекции.
Для шприца:
1. Введение инъекции:Сразу же проведите инъекцию:
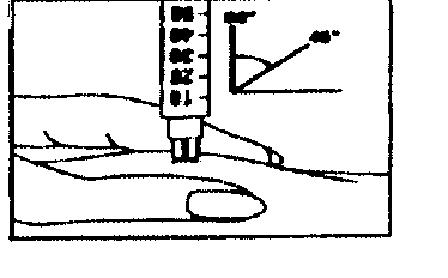
Выберите место для инъекции в соответствии с рекомендациями Вашего лечащего врача или медсестры (живот, передняя часть бедра). Протрите выбранный участок тампоном со спиртом. Сильно стяните кожу пальцами и коротким энергичным движением направьте иглу под углом 45° — 90° в кожную складку. Проводите подкожную инъекцию, как Вас учили. Избегайте попадания препарата непосредственно в вену. Вводите раствор, осторожно нажимая на поршень. Используйте столько времени, сколько Вам нужно для того, чтобы ввести весь объем раствора. Сразу же после инъекции выньте иглу и протрите круговыми движениями кожу в месте инъекции тампоном со спиртом.
2. Утилизация использованных принадлежностей: Сразу после инъекции поместите использованный шприц в контейнер для хранения острых предметов. Весь неиспользованный раствор должен быть уничтожен.
Для шприц-ручки:
Используйте шприц-ручку только для себя, не позволяйте пользоваться ей никому другому.
Вводите препарат Овитрель® так, как показывал врач или медсестра.
На иллюстрации ниже показан внешний вид шприц-ручки с указанием ее отдельных элементов:
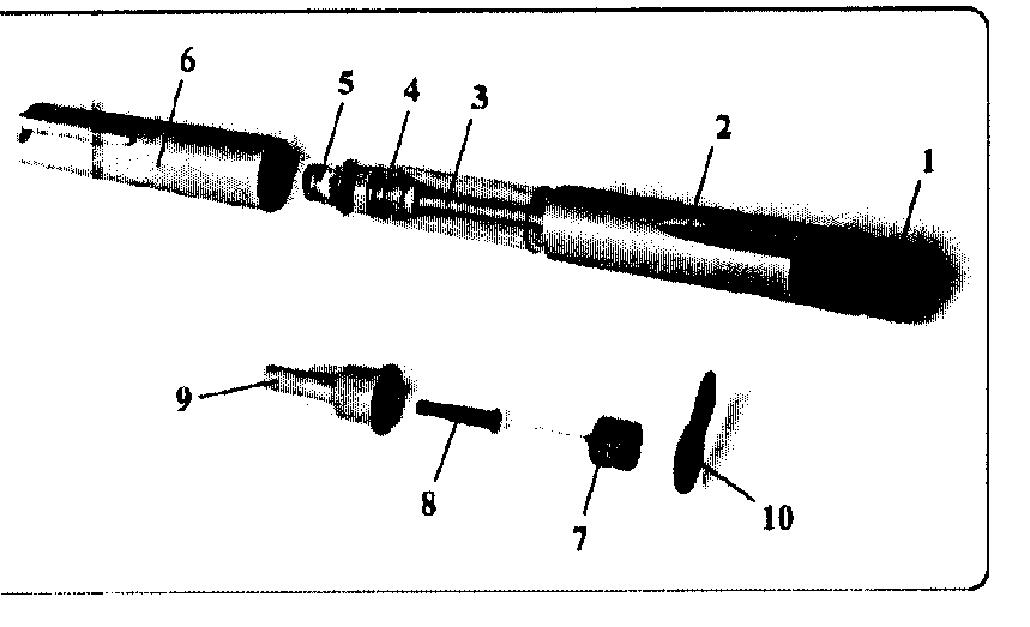
1. кнопка для установки дозы
2. табло указателя дозы
3. поршень
4. отсек с резервуаром
5. наконечник с резьбой
6. колпачок шприц-ручки
7. съемная игла
8. внутренний колпачок иглы
9. наружний колпачок иглы
10. защитная наклейка
1. Подготовка шприц-ручки к проведению инъекции
1.1 Снимите колпачок со шприц-ручки
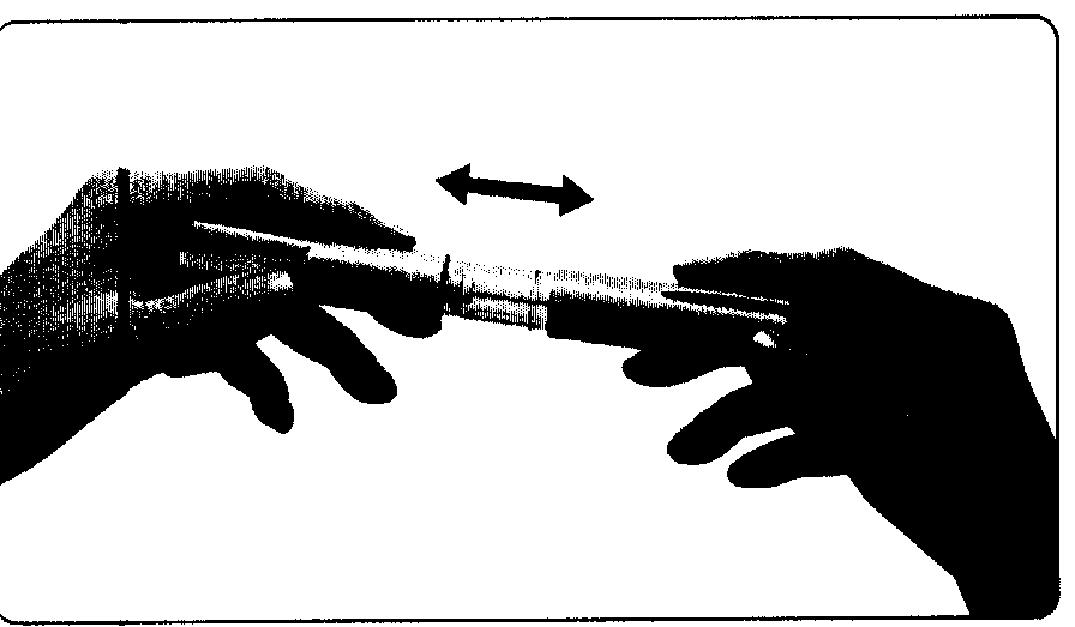
1.2 Наденьте иглу
— Возьмите иглу — используйте только одноразовые иглы, поставляемые вместе с предварительно заполненной шприц-ручкой Овитрель®.
— Убедитесь в том, что защитная наклейка на наружном колпачке иглы не повреждена и не ослаблена.
ВНИМАНИЕ:
Если защитная наклейка повреждена или ослаблена, не используйте эту иглу. Возьмите другую. Неиспользованную иглу выбросьте вместе с надетым на нее наружным колпачком. Инструкции по утилизации ненужных игл получите у своего врача или медсестры.
— Снимите защитную наклейку.
— Прочно удерживайте наружный колпачок иглы.
— Вставьте наконечник шприц-ручки с резьбой в наружный колпачок иглы и навинчивайте наружный колпачок до тех пор, пока он прочно не зафиксируется.

1.3 Удалите крупные воздушные пузырьки:
— Внимательно осмотрите отсек с резервуаром.
— Если Вы не обнаружили крупного воздушного пузырька, значит, шприц-ручка готова к использованию. В таком случае перейдите к пункту 2 «Установка дозы на 250».
Воздушный пузырек считается крупным, если полностью заполняет наконечник отсека с картриджем при удерживании шприц-ручки иглой вверх (см. рисунок). Если Вы видите внутри отсека с резервуаром большой воздушный пузырек, его необходимо удалить. В шприц-ручке может оставаться несколько мелких воздушных пузырьков, прилипших к внутренней стенке отсека с резервуаром. Не обращайте внимания на мелкие пузырьки, их удалять не обязательно.
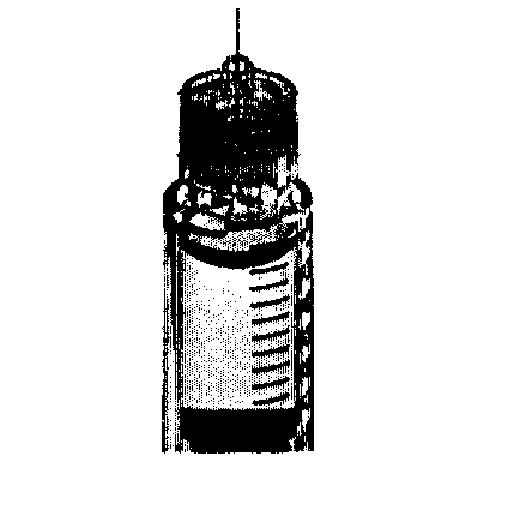
Чтобы удалить крупный воздушный пузырек
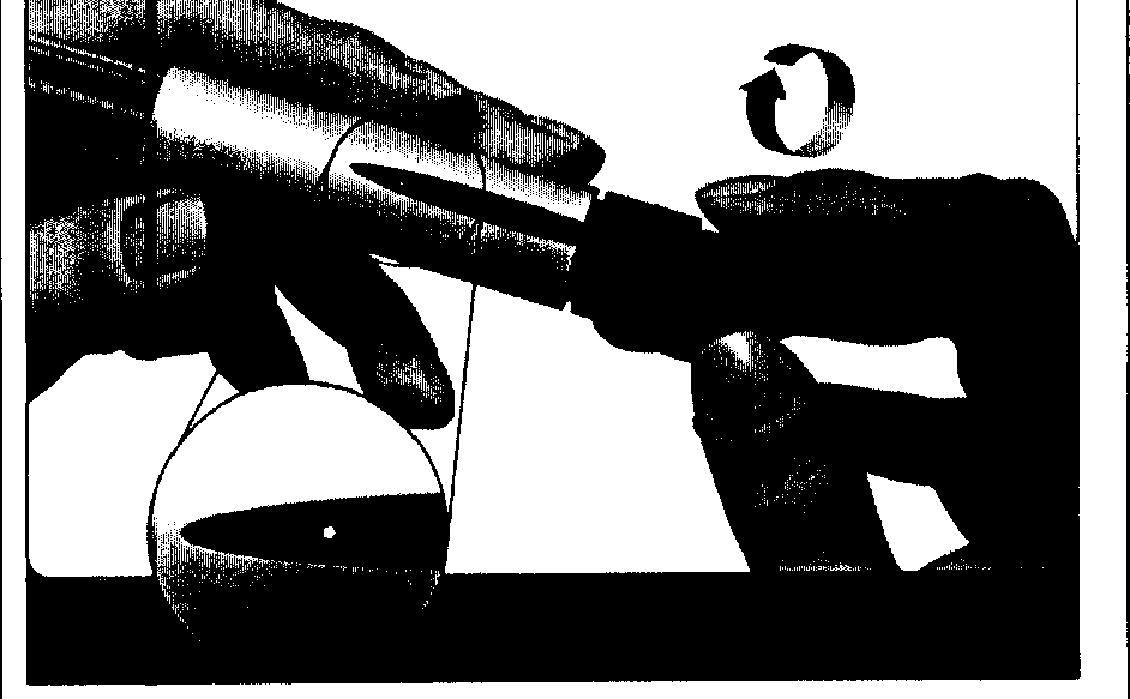
1. Осторожно поворачивайте кнопку для установки дозы по часовой стрелке до тех пор, пока на табло указателя дозы не появится точка (-). Если Вы проскочили это положение, просто поверните кнопку обратно на точку (-).
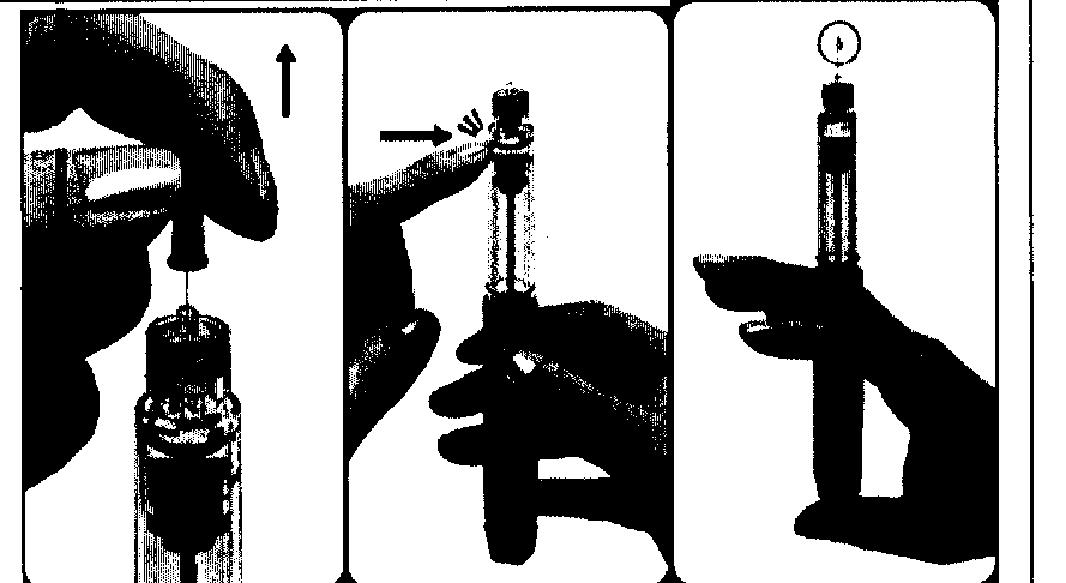
2. Затем снимите внутренний колпачок иглы и удерживайте шприц-ручку иглой вверх.
3. Слегка постучите по отсеку с резервуаром пальцем так, чтобы все воздушные пузырьки всплыли наверх к игле. Продолжая удерживать шприц-ручку иглой вверх и плавно нажимая на кнопку для установки дозы продвиньте поршень настолько, чтобы выпустить воздушный пузырек.
4. На кончике иглы должна появиться капля раствора; это означает, что Ваша шприц-ручка готова к проведению инъекции.
5. Если раствор не проступил на кончике иглы, повторите манипуляции, описанные выше, еще раз (максимальное количество попыток — 2), начиная с шага 1 (пункт «Чтобы удалить большой воздушный пузырек»).
2. Установка дозы на 250
— Аккуратно поворачивайте кнопку для установки дозы по часовой стрелке до тех пор, пока на табло указателя дозы вместо прямой линии не появится число «250».
— Проворачивая кнопку для установки дозы не следует на нее давить или, наоборот, оттягивать.

— На табло указателя дозы должно появиться число «250», как показано на рисунке ниже.
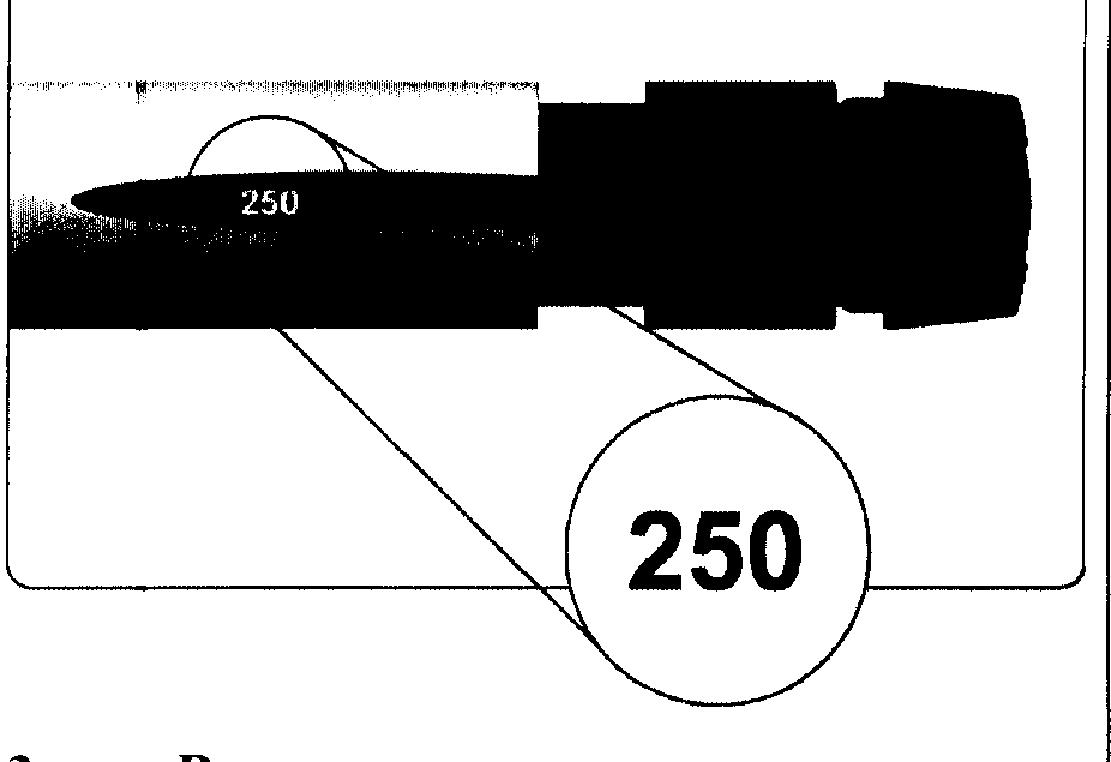
3. Введение дозы
1. Выберите место для инъекции, указанное врачом или медсестрой.
2. Продезинфицируйте место инъекции, протерев его тампоном, смоченным в спирте.
3. Убедитесь еще раз, чтона табло выставлено число «250». Если на табло числа нет, необходимо установить правильную дозу (см. раздел 2 «Установка дозы на 250»).
4. Аккуратно снимите внутренний колпачок и выбросьте его (если это еще не было сделано при выполнении инструкций из пункта 1.3 «Удалите крупные воздушные пузырьки»).
Введите дозу в соответствии с указаниями Вашего врача или медсестры
— Сначала медленно введите иглу под кожу, после чего надавите на кнопку для установки дозы до упора, как показано на рисунке ниже.
— Число с дозировкой, указанное на табло указателя дозы, вернется обратно в положение «О». Это означает, что была введена вся доза.
— Оставьте иглу под кожей при нажатой кнопке для установки дозы минимум на 10 секунд.
— По прошествии 10 секунд выньте иглу, удерживая кнопку для установки дозы в нажатом положении.
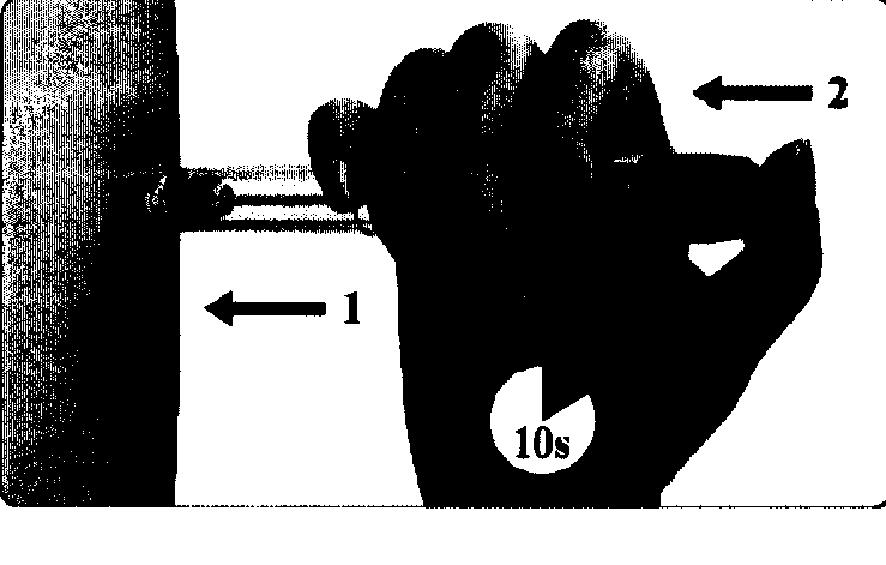
4. После инъекции
4.1 Убедитесь, что на табло указателя дозы появилось число «0»
— Это означает, что доза была введена полностью. Не предпринимайте попыток провести инъекцию второй раз.
— Если на табло число «0» не появилось, свяжитесь с Вашим врачом или медсестрой.
4.2 Снятие иглы
— Крепко удерживайте шприц-ручку за отсек с резервуаром.
— Осторожно наденьте наружный колпачок на иглу.
— Затем сожмите наружный колпачок и отвинтите иглу.

— Будь осторожны, не уколитесь об иглу.
— Теперь наденьте колпачок шприц-ручки обратно на ручку.
4.3 Утилизация
— Никогда не используйте иглу или шприц-ручку повторно.
— Выполнив инъекцию утилизируйте использованную иглу и шприц-ручку, соблюдая меры предосторожности.
— Лучше всего поместить ее обратно в упаковку от производителя. Лекарственные препараты не следует выбрасывать в канализацию или утилизировать вместе с бытовыми отходами. Когда шприц-ручка закончится, получите у своего врача или медсестры инструкции по ее утилизации.
Если Вы ввели слишком большую дозу препарата,могут появиться симптомы синдрома гиперстимуляции яичников (СГЯ), которые описаны в разделе «Особые указания» или «Побочные эффекты». Если эти симптомы появились, проконсультируйтесь с врачом.
Если Вы забыли ввести препарат, проконсультируйтесь с врачом как можно скорее.
Побочные эффекты:
При применении лекарственного препарата Овитрель® возможно развитие побочных эффектов.В процессе сравнительных клинических исследованиях различных доз препарата Овитрель® была показана дозозависимость появления таких побочных эффектов как СГЯ, тошнота и рвота. СГЯ наблюдался приблизительно у 4% пациентов, получавших Овитрель® Тяжелая форма СГЯ отмечалась менее, чем у 0,5% пациентов.
В зависимости от частоты появления побочные эффекты расцениваются как очень частые (≥1/10), частые (≥1/100 и <1/10), нечастые (≥1/1000 и <1/100), редкие (≥1/10000 и <1/1000), очень редкие (<1/10000, включая единичные сообщения). Частота побочных эффектов в каждой группе указана в порядке убывания.Взависимости от частоты встречаемости побочные явления могут быть разделены на группы:
Иммунная система: очень редко — от легкой до тяжелой реакции гиперчувствительности, включая анафилактические реакции и шок.
ЦНС: нечасто — депрессия, раздражительность, возбуждение.
Нервная система: часто — головная боль.
Сосудистая система: очень редко — тромбоэмболия, обычно связанная с тяжелой формой СГЯ.
Пищеварительная система: часто тошнота, рвота, боль в животе, нечасто -диарея.
Кожа и подкожная клетчатка: очень редко -легкие обратимые кожные реакции в виде сыпи.
Репродуктивная система и молочные железы: часто — СГЯ легкой или средней степени тяжести, нечасто — тяжелая форма СГЯ, болезненность молочных желез.
Общие и местные реакции: часто — утомляемость, реакции в месте инъекции.
Передозировка:
Данные о передозировке препаратом отсутствуют. Тем не менее, при передозировке процессе стимуляции яичников возможно развитие СГЯ (см. «Особые указания»).
Клинически он характеризуется образованием крупных кист яичника с риском их разрыва (перфорации), симптомами асцита и циркуляторными расстройствами.
Взаимодействие:
Данные о взаимодействии с другими лекарственными средствами отсутствуют. Тем не менее, пациентке необходимо информировать врача о всех лекарственных средствах (в том числе безрецептурных), которые она принимает в настоящее время или недавно принимала.
Особые указания:
Перед началом лечения необходимо установить причины бесплодия у пациентки и ее партнера и оценить предполагаемые факторы риска при наступлении беременности. Особенно следует учитывать симптомы гипотиреоза, адренокортикальной недостаточности, гиперпролактинемии, наличие опухолей
гипофиза или гипоталамуса, и применяемые специфические методы терапии.
Синдром гиперстимуляции яичников (СГЯ)
В процессе стимуляции яичников повышается риск возникновения СГЯ из-за одновременного созревания большого числа фолликулов.
СГЯ может стать серьезным осложнением, характеризующимся образованием крупных кист яичника с риском их разрыва, увеличением веса, одышкой, олигурией или наличием асцита в клинической картине циркуляторных нарушений. СГЯ тяжелой степени в редких случаях может сопровождаться гемоперитонеумом, острым легочным дистресс-синдромом, перекрутом яичника и тромбоэмболией.
С целью снижения риска СГЯ в протоколе стимуляции роста фолликулов рекомендуется тщательное наблюдение за ответной реакцией яичников при помощи ультразвукового исследования и определение уровня эстрадиола в крови перед началом курса лечения и во время него.
При ановуляции риск развития СГЯ повышается при концентрации эстрадиола в плазме крови > 1500 пг/мл (5400 пмоль/л) и наличие более 3 фолликулов диаметром 14 мм или более. При ВРТ риск развития СГЯ повышается при концентрации эстрадиола > 3000 пг/мл (11000 пмоль/л) или наличии 18 или более фолликулов диаметром 11 мм и более.
СГЯ, вызванный чрезмерным ответом яичника, можно избежать, если отменить введение чХГ. Поэтому, если уровень эстрадиола в сыворотке крови > 5500 пг/мл (20 ООО пмоль/л) и/или когда в наличии 30 или более фолликулов, следует воздержаться от применения чХГ. Пациенткам рекомендуют воздержаться от коитуса или использовать барьерные методы контрацепции не менее 4-х дней.
Многоплодная беременность
По сравнению с естественным оплодотворением при проведении стимуляции возрастает риск многоплодной беременности. В большинстве случаев рождаются двойни. При применении методов вспомогательной репродукции количество родившихся младенцев соответствует числу эмбрионов, перенесенных в полость матки.
Использование рекомендованных доз препарата Овитрель®, схемы лечения и тщательный мониториг в процессе терапии минимизируют риск возникновения СГЯ и многоплодной беременности.
Невынашивание беременности
Статистика выкидышей после лечения ановуляторного бесплодия, в том числе с помощью ВРТ, превышает показатели в среднем по популяции, но сравнима с другими видами бесплодия.
Внематочная беременность
У пациенток с заболеваниями маточных труб в анамнезе повышен риск внематочной беременности независимо от того, получена ли беременность обычным путем или в процессе лечения бесплодия. Вероятность внематочной беременности после применения вспомогательных репродуктивных технологий выше, чем в общей популяции.
Врожденные аномалии развития
Частота врожденных аномалий после применения программ ВРТ может быть несколько выше, чем при естественной беременности и родах. Тем не менее, неизвестно, связано ли это с особенностью родителей (например, возраст матери, качество спермы) и многоплодной беременностью или же непосредственно с процедурами ВРТ.
Тромбоэмболические осложнения
У пациенток с недавно перенесенными или текущими тромбоэмболическими заболеваниями, а также при вероятном риске их возникновения при наличии заболевания в анамнезе или у родственников, применение гонадотропинов может увеличить этот риск или осложнить течение данных заболеваний. Для пациенток данной группы польза от терапии должна быть соотнесена с возможным риском. Следует отметить, что беременность сама по себе, как и СГЯ, несет повышенный риск тромбоэмболических нарушений, таких как эмболия легких, ишемический инсульт или инфаркт миокарда.
Влияние на лабораторные показатели
Ведение препарата Овитрель® может влиять на иммунологическую картину уровня чХГ в сыворотке крови и в моче в течение 10 дней и привести к появлению ложноположительной реакции при проведении теста на беременность.
Прочая информация
Во время проведения терапии препаратом Овитрель® возможна незначительная стимуляция функции щитовидной железы.
Если проявления побочных реакций усиливаются или Вы отмечаете побочные эффекты, не упомянутые в инструкции, пожалуйста, сообщите об этом Вашему лечащему врачу.
В течение срока годности препарат (только для шприцев) может храниться вне холодильника при температуре не выше 25 °С 30 дней. Если по истечении 30 дней такого хранения препарат не был использован, он должен быть уничтожен.
Влияние на способность управлять транспортными средствами и механизмами:
Практически не влияет на управление транспортным средством или каким-либо другим механизмом.
Форма выпуска/дозировка:
Раствор для подкожного введения, 250 мкг/0,5 мл.
Упаковка:
0,5 мл раствора, содержащего 250 мкг (6500 ME) хориогонадотропина альфа в бесцветном стеклянном шприце с иглой для инъекций, закрытой защитным колпачком с резиновой прокладкой.
0,5 мл раствора, содержащего 250 мкг (6500 ME) хориогонадотропина альфа в шприц-ручке.
1 шприц упакован в пластиковый контейнер, помещенный в картонную пачку с Инструкцией по применению.
1 шприц-ручка и 1 игла для инъекции упакованы в пластиковый контейнер, помещенный в картонную пачку с инструкцией по применению.
Условия хранения:
При температуре 2 — 8 °С в оригинальной упаковке. Не замораживать. Хранить в недоступном для детей месте.
Срок годности:
2 года. Не использовать препарат после истечения срока годности.
Условия отпуска
По рецепту
Производитель
Мерк Сероно С.п.А., Via delle Magnolie 15 (loc. frazione Zona Industriale), 70026 Modugno (BA), Italy, Италия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
Мерк Сероно С.п.А.
Купить Овитрель раствор в ГорЗдрав
Купить Овитрель раствор в megapteka.ru
Купить Овитрель раствор в Планета Здоровья
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
