Содержание
-
Русское название
-
Английское название
-
Латинское название
-
Брутто формула
-
Фармакологическая группа вещества Ланаделумаб
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Ланаделумаб
-
Противопоказания
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Ланаделумаб
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Ланаделумаб
Русское название
Ланаделумаб
Английское название
Lanadelumab
Латинское название
Lanadelumabum (род. Lanadelumabi)
Брутто формула
C6468H10016N1728O2012S47
Фармакологическая группа вещества Ланаделумаб
Нозологическая классификация
Код CAS
1426055-14-2
Фармакологическое действие
—
ингибирующее протеолитическую активность калликреина.
Характеристика
Ланаделумаб — неплазматическое производное, полностью человеческое моноклональное антитело (IgG1/κ — легкая цепь), полученное методом рекомбинантной ДНК-технологии с использование клеток яичника китайского хомячка (СНО). Исходя из аминокислотной последовательности, молекулярная масса негликозилированного ланаделумаба составляет 146 кДа. Расчетная молекулярная масса полностью восстановленной легкой цепи составляет 23 кДа. Расчетная молекулярная масса полностью восстановленной и негликозилированной тяжелой цепи составляет 49 кДа.
Фармакология
Механизм действия
Ланаделумаб — полностью человеческое моноклональное антитело (IgG1/κ — легкая цепь), которое связывает калликреин плазмы и ингибирует его протеолитическую активность. Плазменный калликреин — это протеаза, которая расщепляет кининоген с высокой молекулярной массой (high-molecular-weight-kininogen, HMWK) с образованием расщепленного HMWK (cleaved HMWK, cHMWK) и высвобождением брадикинина, сильного вазодилататора, что повышает проницаемость сосудов и приводит к отечности и боли, ассоциированной с наследственным ангионевротическим отеком (НАО). У пациентов с НАО из-за дефицита или дисфункции ингибитора C1 (C1-INH) нормальная регуляция активности калликреина в плазме отсутствует, что приводит к неконтролируемому увеличению активности калликреина в плазме и приступам ангионевротического отека. Ланаделумаб снижает активность калликреина в плазме и обеспечивает контроль избыточного образования брадикинина у пациентов с НАО.
Фармакодинамика
Зависимое от концентрации ингибирование активности калликреина в плазме, измеренное как снижение уровней cHMWK, было продемонстрировано после п/к введения ланаделумаба в дозе 150 мг каждые 4 нед, 300 мг каждые 4 нед или 300 мг каждые 2 нед у пациентов с НАО.
Ланаделумаб не увеличивал интервал QT/QTc.
Фармакокинетика
После п/к введения фармакокинетика ланаделумаба была приблизительно пропорциональна дозе в диапазоне терапевтических доз у пациентов с НАО (таблица 1). Фармакокинетические свойства и экспозиция (в равновесном состоянии) ланаделумаба у пациентов с НАО после п/к введения 150 мг каждые 4 нед, 300 мг каждые 4 нед и 300 мг каждые 2 нед представлены в таблице 1. После п/к введения ланаделумаба Cmax в плазме достиглась в течение 5 дней, а конечный T1/2 составлял ~ 2 нед. Предполагаемое время для достижения Css — примерно 70 дней. В равновесном состоянии средний коэффициент кумуляции составлял приблизительно 1,44; 1,42 и 2,43 для режимов дозирования 150 мг каждые 4 нед, 300 мг каждые 4 нед и 300 мг каждые 2 нед соответственно.
Таблица 1
Средние (SD) фармакокинетические параметры ланаделумаба после п/к введения (испытание 1)
| Фармакокинетические параметры | Ланаделумаб | ||
| 150 мг каждые 4 нед (n=28) | 300 мг каждые 4 нед (n=29) | 150 мг каждые 2 нед (n=27) | |
| Cl/F, л/сут | 0,667 (0,162) | 0,742 (0,239) | 0,809 (0,37) |
| Vss/F, л | 14,1 (2,93) | 14,9 (4,45) | 16,6 (4,79) |
| AUCτ,ss, мкг·сут/мл | 233 (56,6) | 441 (137) | 408 (138) |
| Cmax,ss, мкг/мл | 12 (3,01) | 23,3 (7,94) | 34,4 (11,2) |
| Cmin,ss, мкг/мл | 4,81 (1,4) | 8,77 (2,8) | 25,4 (9,18) |
| Tmax, сут | 5,17 (1,09) | 5,17 (1,12) | 4,11 (0,377) |
| T1/2, сут | 14,9 (2) | 14,2 (1,89) | 15 (2,48) |
Cl/F — кажущийся Vd; AUCτ,ss — AUC в течение интервала дозирования в равновесном состоянии; Cmax,ss и Cmin,ss — концентрации в равновесном состоянии; T1/2 — конечный T1/2.
Особые группы пациентов
Популяционный фармакокинетический анализ показал, что возраст, пол и расовая принадлежность не оказывают значимого влияния на фармакокинетику ланаделумаба после поправки на массу тела. Масса тела была определена как важная ковариата, описывающая вариабельность клиренса и Vd, что приводит к более высокой экспозиции (AUC и Cmax) у пациентов с меньшей массой тела. Однако это различие не считается клинически значимым, и какая-либо корректировка дозы не рекомендуется ни для одной из этих демографических групп.
Педиатрическая популяция
На основе популяционного фармакокинетического анализа, средняя AUCss (±SD) ланаделумаба составила 629 (204) мкг·сут/мл после п/к введения ланаделумаба в дозе 300 мг каждые 2 нед у педиатрических пациентов от 12 до 18 лет. Это примерно на 37% выше, чем средняя AUCss у взрослых пациентов (460 мкг·сут/мл) при том же режиме дозирования из-за более низкой массы тела у педиатрических пациентов.
Нарушение функции почек
Специальных исследований для оценки фармакокинетики ланаделумаба у пациентов с нарушением функции почек не проводили. На основании популяционного фармакокинетического анализа, почечная недостаточность (расчетная СКФ от 60 до 89 мл/мин/1,73 м2, легкая степень, N=98) и от 30 до 59 мл/мин/1,73 м2, средняя степень, N=9) не влияла на клиренс или Vd ланаделумаба.
Сопутствующие ЛС
Применение анальгетиков, антибактериальных, антигистаминных, противовоспалительных и противоревматических ЛС не влияло на клиренс и Vd ланаделумаба.
При острых приступах НАО использование ЛС для экстренной помощи, таких как плазменный и рекомбинантный ингибитор C1-эстеразы человека, икатибант или экаллантид, не оказывало влияния на клиренс и Vd ланаделумаба.
Доклиническая токсикология
Канцерогенность, мутагенность, влияние на фертильность
Исследования оценки канцерогенного потенциала ланаделумаба на животных не проводили. В опубликованной литературе говорится о брадикинине, содержание которого повышено при НАО, как о протуморогенной молекуле. Однако риск развития злокачественного новообразования у человека из-за антитела, ингибирующего активность калликреина плазмы, такого как ланаделумаб, снижающего уровни брадикинина, в настоящее время неизвестен.
На фертильность самцов и самок ланаделумаб не влияет, что основывается на отсутствии наблюдаемых неблагоприятных гистопатологических изменений в репродуктивных органах у половозрелых обезьян Cynomolgus, у которых ланаделумаб применяли в течение 13 нед п/к в дозах до 50 мг/кг/нед (что приводило к экспозиции, примерно к 22 раза превышающей таковую при МРДЧ на основе AUC).
Клинические исследования
Испытание 1 (NCT02586805)
Эффективность ланаделумаба для предотвращения приступов ангионевротического отека у пациентов в возрасте 12 лет и старше с НАО I или II типа была продемонстрирована в многоцентровом рандомизированном двойном слепом плацебо-контролируемом исследовании в параллельных группах (испытание 1).
В исследование были включены 125 взрослых и подростков с НАО I или II типа, у которых наблюдалось как минимум одно подтвержденное исследователем обострение за 4 нед в течение вводного периода. Пациенты были рандомизированы в 1 из 4 параллельных групп лечения, стратифицированных с учетом исходной частоты приступов, в соотношении 3:2:2:2 (плацебо, ланаделумаб 150 мг каждые 4 нед, ланаделумаб 300 мг каждые 4 нед или ланаделумаб 300 мг каждые 2 нед путем п/к инъекции) в течение 26-недельного периода лечения. Пациенты в возрасте ≥18 лет должны были прекратить прием других профилактических ЛС против НАО до включения в исследование; тем не менее всем пациентам было разрешено использовать заведомо эффективные ЛС для лечения острых приступов НАО.
В целом 90% пациентов имели НАО I типа. Приступы ангионевротического отека гортани в анамнезе были зарегистрированы у 65% пациентов, и 56% ранее получали длительное профилактическое лечение. Во время вводного периода исследования частота ≥3 приступов в месяц наблюдалась у 52% пациентов в целом.
Во всех группах лечения ланаделумабом наблюдалось клинически выраженное и статистически значимое снижение средней частоты приступов НАО по сравнению с плацебо по всем первичным и вторичным конечным точкам в популяции рандомизированных пациентов согласно назначенному лечению (Intent-to-Treat population, ITT), как показано в таблице 2.
Таблица 2
Результаты первичных и вторичных измерений эффективности — ITT-популяция
| Статистика конечной точки | Плацебо (n=41) | Ланаделумаб | ||
| 150 мг каждые 4 нед (n=28) | 300 мг каждые 4 нед (n=29) | 300 мг каждые 2 нед (n=27) | ||
| Количество приступов НАО с 0 по 182-й день1 | ||||
| LS Средняя (95% ДИ) ежемесячная частота приступов2 | 1,97 (1,64; 2,36) | 0,48 (0,31; 0,73) | 0,53 (0,36; 0,77) | 0,26 (0,14; 0,46) |
| Снижение по сравнению с плацебо, % (95% ДИ)3 | 76 (61; 85) | 73 (59; 82) | 87 (76; 93) | |
| Скорректированные p-значения4 | <0,001 | <0,001 | <0,001 | |
| Количество приступов НАО, требующих неотложной терапии, с 0 по 182-й день | ||||
| LS Средняя (95% ДИ) ежемесячная частота приступов2 | 1,64 (1,34; 2) | 0,31 (0,18; 0,53) | 0,42 (0,28; 0,65) | 0,21 (0,11; 0,4) |
| Снижение по сравнению с плацебо, % (95% ДИ)3 | 81 (66; 89) | 74 (59; 84) | 87 (75; 93) | |
| Скорректированные p-значения4 | <0,001 | <0,001 | <0,001 | |
| Количество умеренных или тяжелых приступов НАО с 0 по 182-й день | ||||
| LS Средняя (95% ДИ) ежемесячная частота приступов2 | 1,22 (0,97; 1,52) | 0,36 (0,22; 0,58) | 0,32 (0,2; 0,53) | 0,2 (0,11; 0,39) |
| Снижение по сравнению с плацебо, % (95% ДИ)3 | 70 (50; 83) | 73 (54; 84) | 83 (67; 92) | |
| Скорректированные p-значения4 | <0,001 | <0,001 | <0,001 |
SD = стандартное отклонение; LS = метод наименьших квадратов
Примечание: результаты получены на основе модели регрессии Пуассона, учитывающей избыточную дисперсию с фиксированными эффектами для группы лечения (категориальная) и нормализованной исходной частотой приступов (непрерывная), а также логарифм времени в днях для каждого пациента, наблюдаемого во время периода лечения, в качестве переменной смещения в модели.
1 Первичная конечная точка эффективности.
2 Основанная на модели частота обострений в период лечения НАО (приступы/4 нед).
3 Рассчитано как отношение, на основе модели, частоты обострений НАО в период лечения (ланаделумаб/плацебо) минус 1, умноженное на 100.
4 Скорректированные значения p для множественных тестов.
Среднее снижение частоты приступов НАО было стабильно выше в группах лечения ланаделумабом по сравнению с плацебо, независимо от указания в анамнезе на предшествующую длительную профилактическую терапию, наличие ларингеальных атак или их частоты во время вводного периода.
Дополнительные предварительно определенные исследовательские конечные точки включали процент пациентов, у которых не было приступов в течение всего 26-недельного периода лечения, и процент пациентов, достигших порогового (≥50%, ≥70%, ≥90%) снижения частоты приступов НАО по сравнению с вводным периодом в течение 26-недельного периода лечения. Снижение частоты приступов НАО на ≥50% наблюдалось у 100% пациентов, получавших 300 мг каждые 2 нед или каждые 4 нед, и у 89% пациентов, получавших 150 мг каждые 4 нед, по сравнению с 32% пациентов, получавшими плацебо. Снижение частоты приступов НАО на ≥70% наблюдалось у 89, 76 и 79% пациентов, получавших 300 мг каждые 2 нед, 300 мг каждые 4 нед и 150 мг каждые 4 нед соответственно, по сравнению с 10% пациентов, получавших плацебо. Снижение частоты приступов НАО на ≥90% наблюдалось у 67, 55 и 64% пациентов, получавших 300 мг каждые 2 нед, 300 мг каждые 4 нед и 150 мг каждые 4 нед соответственно, по сравнению с 5% пациентов, получавших плацебо.
Процент пациентов без приступов в течение всего 26-недельного периода лечения составил 44, 31 и 39% в группах лечения ланаделумабом в дозах 300 мг каждые 2 нед, 300 мг каждые 4 нед и 150 мг каждые 4 нед соответственно по сравнению с 2% пациентов, получавших плацебо.
Испытание 2 (NCT02741596)
Пациенты, завершившие испытание 1, могли быть включены в открытое продленное исследование. Пациенты, возобновившие терапию, независимо от группы рандомизации в испытании 1, получали однократную дозу ланаделумаба 300 мг при входе в исследование и наблюдались до возникновения первого приступа НАО. Все конечные точки эффективности были исследовательскими в этом неконтролируемом неслепом исследовании. На 4-й нед после введения дозы примерно у 80% пациентов, которые принимали 300 мг каждые 2 нед (n=25) в испытании 1, приступов не было. После первого приступа НАО все пациенты получали лечение в открытом исследовании ланаделумаба 300 мг каждые 2 нед.
Применение вещества Ланаделумаб
Профилактика приступов наследственного ангионевротического отека у пациентов от 12 лет и старше.
Противопоказания
Нет.
Применение при беременности и кормлении грудью
Беременность
Резюме рисков
Нет доступных данных о применении ланаделумаба у беременных женщин, чтобы информировать о каких-либо рисках, связанных с его применением. Моноклональные антитела, такие как ланаделумаб, проходят через плаценту в III триместре беременности, поэтому возможное воздействие на плод, вероятно, будет больше в III триместре беременности. Расширенное исследование пре- и постнатального развития (рППНР), проведенное у беременных обезьян при дозах, приводящих к экспозиции, в 33 раза превышающей достигаемую при МРДЧ (на основе AUC), не выявило каких-либо доказательств вреда для развивающегося плода.
Фоновый риск серьезных врожденных дефектов и выкидыша для указанной популяции неизвестен. В общей популяции США оценочный фоновый риск серьезных врожденных дефектов и выкидыша при клинически признанной беременности составляет от 2 до 4% и от 15 до 20% соответственно.
Данные
Данные у животных. В исследовании рППНР беременным обезьянам Cynomolgus вводили ланаделумаб 1 раз в неделю п/к, что приводило к экспозиции, превышающей МРДЧ в 33 раза (на основе AUC с п/к дозами для самки до 50 мг/кг/нед) с 20-го дня беременности, в период начала органогенеза, до родов. Эффектов, связанных с ланаделумабом, на протекание беременности или роды не наблюдалось. Введение ланаделумаба самке не оказывало влияния на эмбриофетальное развитие, выживаемость, рост или постнатальное развитие потомства в возрасте до 3 мес. Ланаделумаб проникал через плаценту у обезьян. Потомство подвергалось экспозиции ланаделумаба в концентрации, составляющей примерно 50% от таковой в плазме самки, до 21 дня постнатального развития (ПНР 21). Концентрации ланаделумаба были приблизительно одинаковыми в плазме крови самки и потомства к ПНР 90.
Грудное вскармливание
Резюме рисков
Нет данных о присутствии ланаделумаба в грудном молоке, его воздействии на грудного ребенка или его влиянии на выработку молока. Ланаделумаб был обнаружен в молоке лактирующих обезьян Cynomolgus в концентрации примерно 0,2% от концентрации в плазме крови самки. Следует учитывать преимущества грудного вскармливания для развития и здоровья наряду с клинической потребностью матери в ланаделумабе и любыми возможными неблагоприятными последствиями для грудного ребенка от воздействия ланаделумаба или основного состояния матери.
Данные
Данные у животных. Имеющиеся фармакокинетические данные у обезьян Cynomolgus показали экскрецию ланаделумаба с молоком примерно 0,2% от уровня в плазме самки.
Побочные действия вещества Ланаделумаб
Опыт клинических испытаний
Поскольку клинические испытания проводятся с различным набором условий, частота встречаемости побочных реакций, наблюдаемых в этих испытаниях, не может непосредственно сравниваться с частотой в других клинических испытаниях и может не отражать наблюдаемую в клинической практике.
Безопасность ланаделумаба главным образом основана на 26-недельном рандомизированном двойном слепом плацебо-контролируемом исследовании с параллельными группами (испытание 1) с участием 125 пациентов с НАО I или II типа. Отобранные пациенты также могли участвовать в открытом расширенном исследовании (испытание 2) до 130 нед. В испытании 1 по крайней мере одну дозу ланаделумаба получили 84 пациента с НАО в возрасте от 12 лет и старше. В целом 70% пациентов были женского пола и 90% принадлежали к европеоидной расе, средний возраст составлял 41 год. Доля пациентов, которые преждевременно прекратили прием из-за побочных эффектов, составила 1,2% для пациентов, получавших ланаделумаб, и 4,9% для пациентов, получавших плацебо. Смертельных случаев в исследовании не было.
Профиль безопасности ланаделумаба в целом был схожим для всех подгрупп пациентов, включая анализ по возрасту, полу и географическому региону.
В таблице 3 представлены побочные реакции, возникшие у ≥10% пациентов в любой группе лечения ланаделумабом, которые также возникали с большей частотой, чем в группе плацебо в испытании 1.
Таблица 3
Побочные реакции, наблюдавшиеся у ≥10% пациентов, получавших ланаделумаб в испытании 1
| Побочная реакция | Плацебо (N=41) | Ланаделумаб | |||
| 150 мг каждые 4 нед (N=28) | 300 мг каждые 4 нед (N=29) | 300 мг каждые 2 нед (N=27) | Общее (N=84) | ||
| n (%) | n (%) | n (%) | n (%) | n (%) | |
| Реакции в месте инъекции1 | 14 (34) | 16 (57) | 13 (45) | 15 (56) | 44 (52) |
| Инфекция верхних дыхательных путей2 | 13 (32) | 3 (11) | 9 (31) | 12 (44) | 24 (29) |
| Головная боль3 | 9 (22) | 3 (11) | 6 (21) | 9 (33) | 18 (21) |
| Сыпь4 | 2 (5) | 2 (7) | 3 (10) | 1 (4) | 6 (7) |
| Миалгия | 0 | 1 (4) | 0 | 3 (11) | 4 (5) |
| Головокружение | 0 | 1 (4) | 3 (10) | 1 (4) | 5 (6) |
| Диарея | 2 (5) | 3 (11) | 0 | 1 (4) | 4 (5) |
N = количество пациентов; n = количество пациентов, у которых отмечалась реакция.
1 Реакции в месте инъекции включают боль, эритему, кровоподтек, гематому, кровотечение, зуд, припухлость, уплотнение, парестезию, реакцию, ощущение тепла, отек и сыпь.
2 Включает инфекцию верхних дыхательных путей, вирусную инфекцию верхних дыхательных путей.
3 Включает головную боль, головную боль напряжения, синусовую головную боль.
4 Включает сыпь, макулопапулезную сыпь, эритематозную сыпь.
Реакции в месте инъекции в основном заключались в боли, покраснении и кровоподтеках в месте инъекции. Не было значимой разницы в реакциях в месте инъекции при самостоятельном введении.
Менее частые побочные реакции
Другие побочные реакции, которые чаще возникали у пациентов, получавших ланаделумаб, по сравнению с плацебо, включают гиперчувствительность (1% vs 0%), повышение уровня АСТ (2% vs 0%) и повышение уровня АЛТ (2% vs 0%).
Данные по безопасности продолжающегося открытого расширенного исследования, в котором приняли участие 109 пациентов с перенесенным НАО из исследования 1 и 103 пациента с неизлечимым НАО, согласуются с контролируемыми данными по безопасности из исследования 1.
Лабораторные отклонения
Повышение уровня трансаминаз
В течение периода плацебо-контролируемого лечения в испытании 1 количество пациентов, получавших ланаделумаб, с максимальным уровнем трансаминаз (АЛТ или АСТ) >8, >5 или >3 раз выше ВГН составляло 1 (1,2%), 0 (0%) или 3 (3,6%) соответственно по сравнению с 0 у пациентов, получавших плацебо. Повышение уровня трансаминаз было бессимптомным и транзиторным. Ни у одного пациента не было повышения уровня общего билирубина >2 ВГН. Один пациент, получавший ланаделумаб, окончательно прекратил лечение из-за повышения уровня трансаминаз (4,1 ВГН АСТ). Не было сообщений о серьезных побочных реакциях в связи с повышением уровня трансаминаз ни у одного из пациентов.
Иммуногенность
Как и в случае всех терапевтических белков, существует возможность развития иммуногенности. Обнаружение образования антител во многом зависит от чувствительности и специфичности анализа. Кроме того, наблюдаемая частота положительного результата на антитела (включая нейтрализующие антитела) в анализе может зависеть от нескольких факторов, включая методологию анализа, обработку образцов, время сбора образцов, сопутствующие ЛС и основное заболевание. По этим причинам сравнение частоты обнаружения антител к ланаделумабу в исследовании, описанном ниже, с частотой обнаружения антител в других исследованиях или к другим веществам может оказаться неинформативным.
В испытании 1 у 10 (12%) пациентов, получавших ланаделумаб, и у 2 (5%) пациентов, получавших плацебо, в течение периода лечения имелся по крайней мере 1 образец с положительным результатом на антитела (ADA); титры антител были низкими (от 20 до 1280). Наблюдаемый ADA-ответ был транзиторным у 2/10 пациентов, получавших ланаделумабо, и у 1/2 пациентов, получавших плацебо. Ранее существовавший низкий титр антител наблюдался у 3 пациентов, получавших ланаделумаб, и у 1 пациента, получавшего плацебо. У двух пациентов, получавших 150 мг каждые 4 нед, были антитела с низким титром, классифицируемые как нейтрализующие.
Развитие ADA, включая нейтрализующие антитела против ланаделумаба, не оказывало неблагоприятного действия на фармакокинетику, фармакодинамику, безопасность или клинический ответ.
Взаимодействие
Исследований, посвященных взаимодействию с другими ЛС, не проводили.
Влияние на лабораторные тесты
Коагуляционные тесты. Ланаделумаб может увеличивать значение АЧТВ в результате взаимодействия ланаделумаба с реагентами определения АЧТВ. Реагенты, используемые в лабораторном тесте определения АЧТВ, инициируют внутренний путь коагуляции за счет активации калликреина плазмы в контактной системе. Ингибирование калликреина плазмы ланаделумабом может увеличить АЧТВ, определяемое с помощью этого анализа. В испытании 1 пролонгирование АЧТВ (>1 ВГН) наблюдалось в одной или нескольких точках времени у 3, 9 и 11 пациентов, получавших ланаделумаб 150 мг каждые 4 нед, 300 мг каждые 4 нед и 300 мг каждые 2 нед соответственно, по сравнению 5 пациентами, получавшими плацебо. Только у одного пациента в группе лечения в дозе 300 мг каждые 2 нед наблюдалось кратковременное удлинение АЧТВ ≥1,5 ВГН, при этом у пациента продолжалась терапия гепарином. Ни одно из повышений АЧТВ у пациентов, получавших ланаделумаб, не ассоциировалось с побочными эффектами, связанными с патологическим кровотечением. Не наблюдалось различий в значениях МНО между группами лечения.
Передозировка
Клинического опыта передозировки ланаделумаба нет.
Способ применения и дозы
П/к. Рекомендуемая начальная доза — 300 мг каждые 2 нед. Интервал дозирования 300 мг каждые 4 нед также эффективен и может быть рассмотрен, если пациент находится в стадии компенсации (например, без приступов) более 6 мес.
Меры предосторожности
Реакции гиперчувствительности
Были отмечены реакции гиперчувствительности. В случае развития тяжелой реакции гиперчувствительности следует прекратить введение ланаделумаба и начать соответствующее лечение.
Применение в педиатрии
Безопасность и эффективность ланаделумаба оценивали в подгруппе пациентов (N=10) от 12 до <18 лет в испытании 1. Результаты анализа в подгруппе по возрасту соответствовали общим результатам исследования (см. «Побочные действия», Фармакокинетика и Клинические исследования). Еще 13 подростков от 12 до <18 лет были включены в открытое расширенное исследование.
Безопасность и эффективность ланаделумаба у детей младше 12 лет не установлены.
Применение в гериатрии
Безопасность и эффективность ланаделумаба оценивали в подгруппе пациентов (N=5) в возрасте ≥65 лет в испытании 1. Результаты анализа подгрупп по возрасту соответствовали общим результатам исследования (см. «Побочные действия», Фармакокинетика и Клинические исследования).
Источники информации
rxlist.com, 2021.
Описание проверено
-
Лобанова Елена Георгиевна
(фармаколог, доктор медицинских наук, профессор)
Опыт работы: более 30 лет
Торговые названия с действующим веществом Ланаделумаб
Rec.INN
зарегистрированное ВОЗ
Фармакологическое действие
Полностью человеческое моноклональное антитело (иммуноглобулин G1 (IgG1)/κ-легкая цепь), при производстве которого используется технология рекомбинантной ДНК в клетках яичников китайских хомячков (СНО).
Ланаделумаб ингибирует протеолитическую активность активированного калликреина в плазме. Повышение активности калликреина в плазме вызывает приступ ангионевротического отека у пациентов с наследственным ангионевротическим отеком вследствие протеолиза кининогена с высокой молекулярной массой с последующим образованием расщепленного кининогена с высокой молекулярной массой. Ланаделумаб обеспечивает длительный контроль активности калликреина в плазме, и, тем самым, ограничивает образование брадикинина у пациентов с наследственным ангионевротическим отеком.
Фармакокинетика
Фармакокинетика ланаделумаба показала линейный дозозависимый характер в диапазоне доз до 400 мг и воспроизводимую экспозицию после п/к введения препарата в течение до 12 месяцев. У пациентов, получавших препарат, содержащий ланаделумаб, в дозе 300 мг 1 раз/2 нед., среднее значение AUC в равновесном состоянии, Cssmax и Cssmin составили 408 мкг×сут/мл, 34.4 мкг/мл, и 25.4 мкг/мл соответственно. Предполагаемое время для достижения Css составило около 70 сут. После п/к введения ланаделумаба время до достижения Cmax составляет около 5 сут. Среднее значение Vd ланаделумаба у пациентов с наследственным ангионевротическим отеком составляет 14.5 л. Ланаделумаб является терапевтическим моноклональным антителом, и, как предполагается, не связывается с белками плазмы. Среднее значение общего клиренса ланаделумаба составляет 0.0297 л/ч, терминальный T1/2 составляет 14 сут.
Показания активного вещества
ЛАНАДЕЛУМАБ
Для профилактики рецидивирующих приступов наследственного ангионевротического отека у пациентов в возрасте 12 лет и старше.
Режим дозирования
Для п/к введения.
Рекомендуемая начальная доза составляет 300 мг 1 раз/2 нед. Пациентам, у которых на фоне терапии стабильно отсутствуют приступы, доза ланаделумаба может быть снижена до 300 мг 1 раз/4 нед., особенно пациентам с низкой массой тела.
Побочное действие
Со стороны иммунной системы: часто — реакции гиперчувствительности, которые включают зуд, дискомфорт и ощущение покалывания языка.
Со стороны нервной системы: часто — головокружение.
Со стороны кожи и подкожных тканей: часто — макуло-папулезная сыпь.
Со стороны печени: часто — повышение активности АЛС и АСТ.
Местные реакции: очень часто — боль, эритема, кровоподтек, дискомфорт, гематома, кровотечение, зуд, припухлость, уплотнение, парестезия, ощущение тепла, отек и сыпь.
Противопоказания к применению
Повышенная чувствительность к ланаделумабу; детский возраст до 12 лет; беременность, период грудного вскармливания.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
Не проводились исследования ланаделумаба у пациентов с печеночной недостаточностью. Предполагается, что печеночная недостаточность не влияет на экспозицию ланаделумаба. Не требуется корректировать дозу у пациентов с печеночной недостаточностью.
Применение при нарушениях функции почек
Не проводились исследования ланаделумаба у пациентов с почечной недостаточностью тяжелой степени. Предполагается, что почечная недостаточность не влияет на экспозицию ланаделумаба. Не требуется корректировать дозу у пациентов с почечной недостаточностью.
Применение у детей
Противопоказано применение у детей в возрасте до 12 лет.
Применение у пожилых пациентов
Ожидается, что возраст пациента не будет влиять на экспозицию ланаделумаба. Не требуется корректировать дозу препарата у пациентов старше 65 лет.
Особые указания
Не предназначен для лечения острых приступов наследственного ангионевротического отека.
В случае развития тяжелой реакции гиперчувствительности, необходимо немедленно прекратить введение ланаделумаба и начать соответствующую терапию.
Ланаделумаб может повышать значения АЧТВ в результате взаимодействия ланаделумаба с реагентами, применяемыми для определения АЧТВ. Указанные реагенты инициируют внутренний путь коагуляции посредством активации плазменного калликреина в контактной системе. Ингибирование плазменного калликреина ланаделумабом может увеличить АЧТВ, определяемое с помощью этого метода. Ни одно из повышений АЧТВ у пациентов, получавших ланаделумаб, не ассоциировалось с патологическим кровотечением.
Лекарственное взаимодействие
Как и предполагалось, сопутствующее применение ингибитора С1 эстеразы в качестве неотложной терапии оказывает аддитивное действие на индуцированный ланаделумабом cHNWK-ответ, исходя из механизма действия ланаделумаба и ингибитора С1 эстеразы.
Такзайро — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-006876
Торговое наименование:
Такзайро
Международное непатентованное или группировочное наименование:
ланаделумаб
Лекарственная форма:
раствор для подкожного введения
Состав
В 1 мл раствора содержится:
действующее вещество: ланаделумаб – 150 мг,
вспомогательные вещества: натрия гидрофосфата дигидрат – 5,3 мг, лимонной кислоты моногидрат – 4,1 мг, L-гистидин – 7,8 мг, натрия хлорид – 5,3 мг, полисорбат 80-0,1 мг, вода для инъекций до 1,0 мл.
Описание
Прозрачный либо опалесцирующий раствор, от бесцветного до желтоватого цвета.
Фармакотерапевтическая группа
Наследственного ангионевротического отека (НАО) средство лечения.
Код ATX:
В06АС05
Фармакологические свойства
Характеристика препарата
Ланаделумаб представляет собой полностью человеческое моноклональное антитело (иммуноглобулин G1 (IgG1)/ κ-легкая цепь), при производстве которого используется технология рекомбинантной ДНК в клетках яичников китайских хомячков (СНО).
Механизм действия
Ланаделумаб ингибирует протеолитическую активность активированного калликреина в плазме. Повышение активности калликреина в плазме вызывает приступ ангионевротического отека у пациентов с НАО посредством протеолиза кининогена с высокой молекулярной массой (High Molecular Weight Kininogen, HMWK) с последующим образованием расщепленного кининогена с высокой молекулярной массой (cleaved High Molecular Weight Kininogen,, cHMWK) и высвобождением брадикинина. Ланаделумаб обеспечивает длительный контроль активности калликреина в плазме, и, тем самым, ограничивает образование брадикинина у пациентов с НАО.
Фармакодинамика
Зависимая от концентрации препарата Такзайро степень ингибирования калликреина в плазме, измеренная как снижение концентрации cHMWK, была продемонстрирована после подкожного введения препарата в дозе 150 мг 1 раз в 4 недели [1 раз/4 нед], 300 мг 1 раз в 4 недели [1 раз/4 нед] или 300 мг 1 раз в 2 недели [1 раз/2 нед] пациентам с НАО.
Фармакокинетическая-фармакодинамическая взаимосвязь между ланаделумабом и cHMWK описывается с помощью непрямой фармакологической модели экспозиция-ответ. Наибольшее снижение скорости образования cHMWK – на 53,7%, – было достигнуто при воздействии ланаделумаба в концентрации полумаксимального ингибирования (IC50), равной 5705 нг/мл.
Клиническая эффективность и безопасность
Эффективность и безопасность ланаделумаба подтверждена, главным образом, результатами исследования HELP, которое представляло собой многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование в параллельных группах с участием 125 пациентов (115 взрослых и 10 подростков) с НАО I или II типа. Пациентов рандомизировали в одну из четырех параллельных групп лечения и стратифицировали с учетом исходной частоты приступов, в соотношении 3:2:2:2 (плацебо, ланаделумаб 150 мг 1 раз/4 нед, ланаделумаб 300 мг 1 раз/4 нед, или ланаделумаб 300 мг 1 раз/2 нед в виде подкожной инъекции в течение 26 недель терапии).
Медиана (диапазон) возраста исследуемой популяции составила 42 (12-73) года. Женщины из общего числа составили 70% (88 пациенток). Приступы ангионевротического отека гортани в анамнезе отмечены у 65% (81/125) пациентов, при этом 56% (70/125) пациентов ранее получали длительную профилактическую терапию (ДПТ). Во время вводного периода исследования средняя частота приступов составила 3,7 атак/месяц, а у 52% (65/125) пациентов наблюдалось ≥3 атак/месяц. Во всех группах терапии препаратом Такзайро отмечено статистически значимое снижение средней частоты приступов НАО по сравнению с группой плацебо по всем первичным и вторичным конечным точкам в популяции пациентов, принявших хотя бы одну дозу препарата (ITT).
Среднее снижение частоты атак НАО было стабильно выше в группах терапии препаратом Такзайро по сравнению с группой плацебо, независимо от указания в анамнезе на длительную профилактическую терапию, наличия ларингеальных атак или их частоты во время вводного периода.
Доля пациентов, у которых отсутствовали приступы в течение последних 16 недель исследования (со дня 70 до дня 182), составила 77% в группе лечения препаратом в дозе 300 мг 1 раз/2 нед по сравнению с 3% пациентов в группе плацебо. 100% пациентов, получавших препарат в дозе 300 мг 1 раз/2 нед или 1 раз/4 нед и 89% пациентов, получавших препарат в дозе 150 мг 1 раз/4 нед, достигли, как минимум, 50% снижения частоты приступов НАО по сравнению с вводным периодом.
Во всех группах терапии препаратом Такзайро наблюдалось улучшение как общей оценки с помощью вопросника «Качество жизни у пациентов с ангионевротическим отеком (AE-QoL)», так и отдельных его категорий (работоспособность, утомляемость/настроение, страх/обида и питание) по сравнению с группой плацебо; наиболее выраженное улучшение было отмечено в категории «работоспособность». Более низкое количество баллов указывало на менее выраженное нарушение (или лучшее, зависимое от состояния здоровья, качество жизни). Снижение на 6 баллов считалось клинически значимым улучшением. Доля пациентов, которые достигли клинически значимого улучшения по данным AE-QoL, составила 65% (отношение шансов по сравнению с плацебо, [95% ДИ]= 3,2 [1,1; 9,2]), 63% (2,9 [1,1; 8,1]), и 81% (7,2 [2,2; 23,4]), в группах терапии препаратом Такзайро в дозе 150 мг 1 раз/4 нед, 300 мг 1 раз/4 нед, и 300 мг 1 раз/2 нед, соответственно, по сравнению с 37% пациентов в группе плацебо.
Длительную безопасность и эффективность профилактической терапии препаратом Такзайро для предотвращения приступов НАО оценивали в открытом продленном исследовании HELP. Всего 212 взрослых пациентов и подростков с симптоматическим НАО I или II типа получили, как минимум, одну дозу ланаделумаба в этом исследовании, включая 109 пациентов, включенных из двойного слепого исследования HELP, и 103 новых (ранее не рандомизированных в двойное слепое исследование) пациентов, включая 19 пациентов из исследования lb фазы, у которых историческая исходная частота приступов была ≥1 приступа в течение 12 недель. Пациентам разрешалось начать самостоятельно вводить препарат после первых двух доз, которые были введены медицинскими работниками, и завершения обучения правильной технике подкожных инъекций. Промежуточный анализ показал, что эффект сохранялся до 1 года терапии.
Фармакокинетика
Фармакокинетику однократного и многократного введения ланаделумаба изучали у пациентов с НАО. Фармакокинетика ланаделумаба показала линейный дозозависимый характер в диапазоне доз до 400 мг и воспроизводимую экспозицию после подкожного введения препарата в течение до 12 месяцев. Абсолютная биодоступность ланаделумаба после подкожного введения не была определена. В исследовании HELP у пациентов, получавших препарат в дозе 300 мг 1 раз/2 нед, среднее (SD) значение площади под кривой «концентрация-время» в равновесном состоянии (AUCtau,ss), максимальная концентрация в равновесном состоянии (Cmax,ss) и минимальная концентрация в равновесном состоянии (Cmin,ss) составили 408 мкг*сут/мл (138), 34,4 мкг/мл (11,2), и 25,4 мкг/мл (9,18), соответственно. Предполагаемое время для достижения равновесной концентрации составило около 70 суток.
Всасывание
После подкожного введения ланаделумаба время до достижения максимальной концентрации составляет около 5 суток. Место подкожной инъекции (бедро, плечо или живот) и факт самостоятельного выполнения инъекции не влияли на абсорбцию ланаделумаба.
Распределение
Среднее значение (SD) объема распределения ланаделумаба у пациентов с НАО составляет 14,5 л (4,53). Ланаделумаб является терапевтическим моноклональным антителом, и. как предполагается, не связывается с белками плазмы.
Выведение
Среднее (SD) значение общего клиренса ланаделумаба составляет 0,0297 л/час (0,0124), а терминальный период полувыведения равен 14 суткам.
Особые группы пациентов
Никаких специальных исследований параметров фармакокинетики ланаделумаба у особых групп пациентов, включая критерии пола, возраста, наличие беременности, почечной или печеночной недостаточности, не проводилось.
Результаты анализа популяционной фармакокинетики, скорректированной по массе тела, не выявили очевидного влияния пола или возраста (от 12 до 75 лет) на клиренс или объем распределения ланаделумаба.
Хотя масса тела была идентифицирована как важный фактор, определяющий вариабельность клиренса, режим дозирования 300 мг 1 раз/2 нед позволял получить достаточную экспозицию для целевого показания (см. раздел «Фармакодинамика»).
Почечная и печеночная недостаточность
В связи с тем, что моноклональные антитела к IgG, в основном, элиминируются путем внутриклеточного катаболизма, влияние почечной или печеночной недостаточности на клиренс ланаделумаба маловероятно. В соответствии с этим, результаты анализа популяционной фармакокинетики не показали влияния почечной недостаточности на клиренс или объем распределения ланаделумаба (рассчитанная скорость клубочковой фильтрации: от 60 до 89 мл/мин/1,73 м² [легкая степень, N = 98] и от 30 до 59 мл/мин/1,73 м² [среднетяжелая степень, N = 9]).
Показания к применению
Препарат Такзайро показан для профилактики рецидивирующих приступов наследственного ангионевротического отека у пациентов в возрасте 12 лет и старше.
Противопоказания
- Повышенная чувствительность к ланаделумабу или любому из вспомогательных веществ
- Детский возраст до 12 лет (недостаточно клинических данных)
- Беременность и период грудного вскармливания
Применение при беременности и в период грудного вскармливания
Беременность
Данные о применении ланаделумаба у беременных женщин либо отсутствуют, либо крайне ограниченны. Исследования, проведенные на животных, не выявили прямого или косвенного токсичного влияния препарата на репродуктивную функцию и развитие плода. В исследованиях пре- и постнатального развития у беременных яванских макак, которым вводили ланаделумаб 1 раз в неделю в дозах 10 или 50 мг/кг (наибольшая из исследуемых доз), не выявлено влияния ланаделумаба на беременность и роды, эмбриофетальное развитие, выживаемость, рост и/или постнатальное развитие детенышей. В этих исследованиях экспозиция была примерно в 32 раза выше, чем после введения препарата пациентам в дозе 300 мг 1 раз/2 нед в пересчете на AUC. В качестве меры предосторожности рекомендуется избегать применения ланаделумаба во время беременности.
Период грудного вскармливания
Отсутствуют данные о выделении ланаделумаба в грудное молоко. Известно, что иммуноглобулины человека выделяются в грудное молоко в первые дни после родов, но вскоре их концентрация снижается. Следовательно, в этот короткий период невозможно исключить риск для ребенка, получающего грудное вскармливание.
Фертильность
Оценка влияния ланаделумаба на фертильность человека не проводилась. Влияние ланаделумаба на фертильность оценивали на половозрелых яванских макаках. В ходе 13-недельного исследования было установлено, что ланаделумаб при подкожном введении в дозах 10-50 мг/кг (наибольшая из исследуемых доз) 1 раз в неделю не влиял на фертильность самцов или самок. В ходе исследования фертильности экспозиция у половозрелых яванских макак была примерно в 20 и 22 раза выше, чем после введения препарата в дозе 300 мг 1 раз/2 нед в пересчете на Сmax и AUC, соответственно. Установлено, что ланаделумаб не оказывал влияния на фертильность самцов и самок яванских макак.
Способ применения и дозы
Применение препарата Такзайро необходимо начинать под наблюдением врача, имеющего опыт лечения пациентов с НАО.
Препарат Такзайро может вводить сам пациент или лицо, осуществляющее уход за ним, после обучения правильной технике подкожных инъекций медицинским работником (см. подраздел «Инструкция по применению препарата»).
Режим дозирования
Рекомендуемая начальная доза составляет 300 мг ланаделумаба (препарата Такзайро) 1 раз/2 нед. Пациентам, у которых на фоне терапии стабильно отсутствуют приступы, доза ланаделумаба может быть снижена до 300 мг 1 раз/4 нед, особенно пациентам с низкой массой тела.
Препарат Такзайро не предназначен для лечения острых приступов НАО (см. раздел «Особые указания»).
Введение пропущенной дозы препарата
Следует особо обратить внимание, что, если введение очередной дозы препарата Такзайро пропущено, ее следует ввести как можно скорее, однако, так, чтобы интервал между дозами был не менее 10 суток.
Особые группы пациентов
Пожилые
Ожидается, что возраст пациента не будет влиять на экспозицию ланаделумаба. Не требуется корректировать дозу препарата у пациентов старше 65 лет (см. раздел «Фармакокинетика»).
Применение у пациентов с печеночной недостаточностью
Не проводились исследования препарата у пациентов с печеночной недостаточностью. Предполагается, что печеночная недостаточность не влияет на экспозицию ланаделумаба. Не требуется корректировать дозу препарата у пациентов с печеночной недостаточностью (см. раздел «Фармакокинетика»).
Пациенты с почечной недостаточностью
Не проводились исследования препарата у пациентов с почечной недостаточностью тяжелой степени. Предполагается. что почечная недостаточность не влияет на экспозицию ланаделумаба или его профиль безопасности. Не требуется корректировать дозу препарата у пациентов с почечной недостаточностью (см. раздел «Фармакокинетика»).
Дети
В связи с отсутствием данных, безопасность и эффективность препарата Такзайро у детей младше 12 лет не установлены.
Способ применения
Только для подкожного введения.
Каждый флакон препарата Такзайро предназначен только для однократного применения.
Препарат необходимо вводить только в рекомендованные области: живот, бедро и верхнюю наружную часть плеча (см. раздел «Фармакокинетика»). Рекомендуется чередовать области проведения инъекции.
Перед введением препарата необходимо проверить внешний вид каждого флакона. Раствор должен быть прозрачным или слегка желтоватым. Если раствор изменил окраску или содержит посторонние включения, его нельзя использовать.
Следует избегать энергичного перемешивания.
Этапы введения
В асептических условиях наберите необходимую дозу препарата Такзайро из флакона в шприц с помощью иглы размера 18G. Поменяйте иглу на шприце на иглу размера 27 G или другую иглу, подходящую для выполнения подкожной инъекции. Введите препарат Такзайро подкожно в область живота, бедра или плеча.
Флакон с любым количеством оставшегося раствора следует утилизировать.
Неиспользованный лекарственный препарат или использованные при его применении расходные материалы должны быть утилизированы в соответствии с местными требованиями. Все использованные иглы и шприцы рекомендуется сложить в контейнер для отходов острых предметов.
Инструкция по применению препарата
Удостоверьтесь, что Вы прочитали, поняли и будете следовать всем поэтапным инструкциям по введению препарата Такзайро. Если у вас остались вопросы, обратитесь к своему врачу или медсестре.
Помимо стеклянного флакона, каждая упаковка препарата Такзайро содержит:
Можно использовать только те шприцы, тупоконечные и остроконечные иглы (см. описание выше), которые вложены в эту упаковку, или те, которые рекомендовал врач.
Шприцы, тупоконечные и остроконечные иглы можно использовать только однократно. После использования шприцы и иглы помещают в контейнер для отходов острых предметов. Нельзя использовать поврежденные шприцы, а также тупоконечные и остроконечные иглы, которые выглядят поврежденными.
Вам также потребуются:
- Салфетки, смоченные спиртом.
- Контейнер для отходов острых предметов: использованных флаконов, игл и шприцев. Вы можете получить расходные материалы у своего врача, фармацевта или медсестры.
Выполнение инъекции препарата Такзайро можно разделить на 5 этапов:
- Подготовка флакона с препаратом Такзайро
- Прикрепление тупоконечной иглы к одноразовому шприцу
- Наполнение одноразового шпица препаратом Такзайро и замена тупоконечной иглы на остроконечную для подкожного введения препарата
- Выбор и подготовка области для введения инъекции
- Введение препарата Такзайро
Этап 1. Подготовка флакона с препаратом Такзайро
✓ Достаньте флакон с препаратом из холодильника и перед использованием выдержите его 15 минут при комнатной температуре (15-25°С).
✓ Очистите Ваше рабочее место и вымойте руки перед подготовкой препарата к введению.
После мытья рук и до проведения инъекции не дотрагивайтесь до любых поверхностей или частей Вашего тела.
✓ Возьмите препарат Такзайро и расходные материалы и поместите их на хорошо освещенное рабочее место.
✓ Выньте флакон из упаковки.
Не используйте флакон, если пластиковый колпачок, закрывающий пробку, отсутствует.
✓ Осторожно переверните флакон 3-5 раз для перемешивания раствора. Не трясите флакон, так как это может привести к образованию пены.
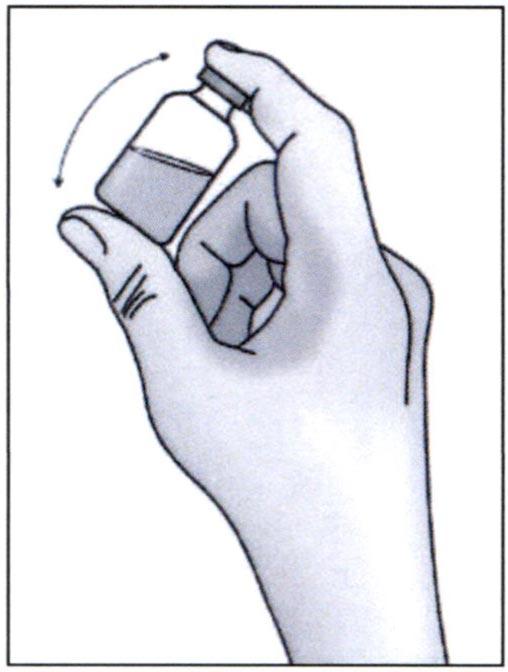
✓ Проверьте раствор во флаконе на наличие посторонних включений или изменение цвета (в нормальном состоянии раствор бесцветный или слегка желтоватый). Не используйте раствор, если обнаружили посторонние включения или изменение цвета раствора.
Важно: Не трясите флакон.
✓ Удалите пластиковый колпачок с флакона.
НО не удаляйте резиновую пробку.
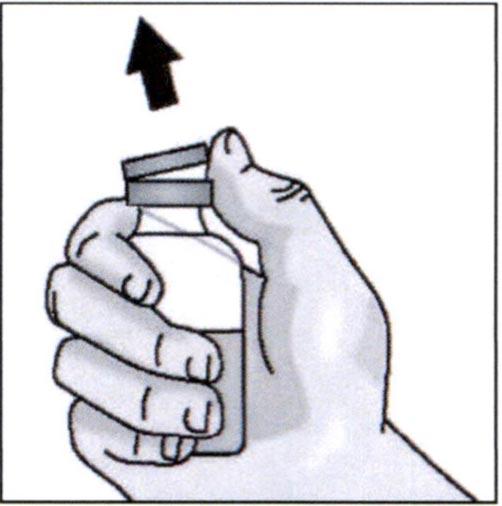
✓ Поставьте флакон на ровную поверхность. Протрите резиновую пробку салфеткой, смоченной в спирте, и оставьте высохнуть.
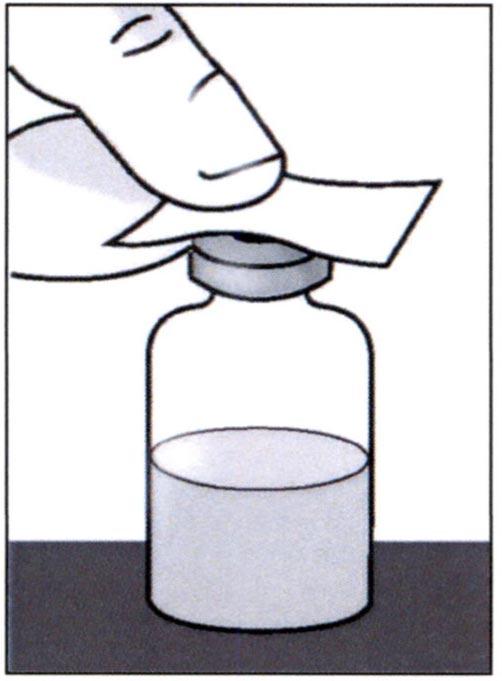
Этап 2. Прикрепление тупоконечной иглы к одноразовому шприцу
✓ Наверните на 3 мл шприц тупоконечную иглу размера 18G для прокалывания пробки флакона.
Важно:
Не удаляйте колпачок с иглы во время прикрепления иглы к шприцу.
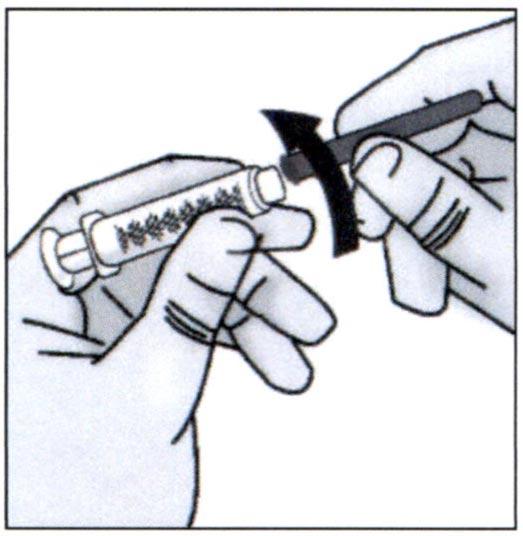
✓ Оттяните назад поршень шприца для заполнения его воздухом в количестве, равном количеству раствора во флаконе.
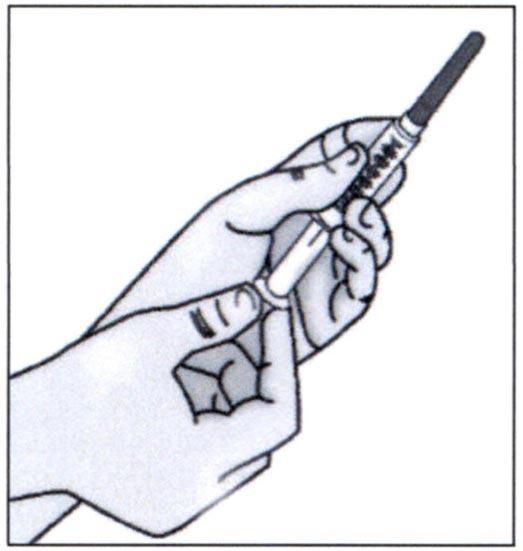
✓ Снимите колпачок с иглы, прикрепленной к шприцу, не касаясь иглы. Не тяните за поршень.
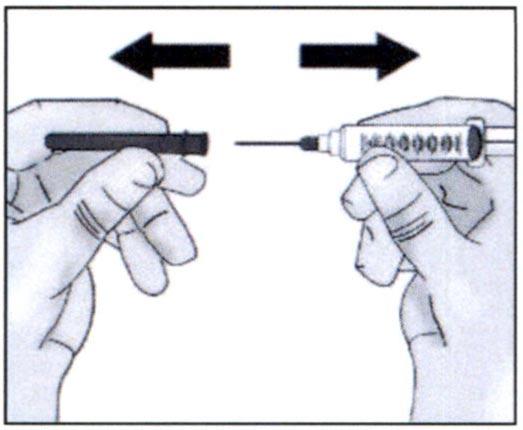
Этап 3. Наполнение одноразового шпица препаратом Такзайро и замена тупоконечной иглы на иглу для подкожных инъекций
✓ Проколите тупоконечной иглой резиновую пробку флакона в центре.
✓ Надавите на поршень вниз, чтобы ввести воздух во флакон, и удерживайте поршень в таком положении.
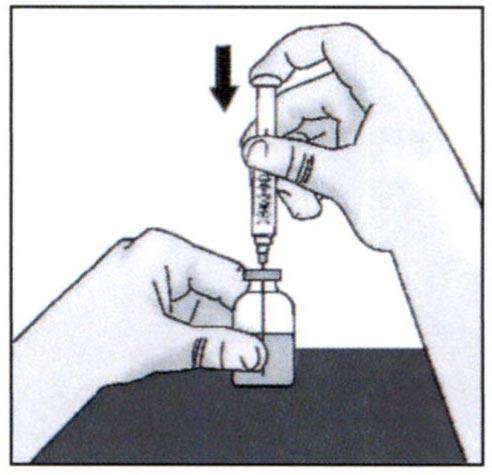
✓ Медленно переверните флакон вверх дном с прикрепленными иглой и шприцем.
Оттяните поршень назад, чтобы набрать в шприц полную дозу препарата из флакона.
Важно:
Обязательно держите кончик иглы в жидкости, чтобы избежать попадания воздуха в шприц при вытягивании поршня
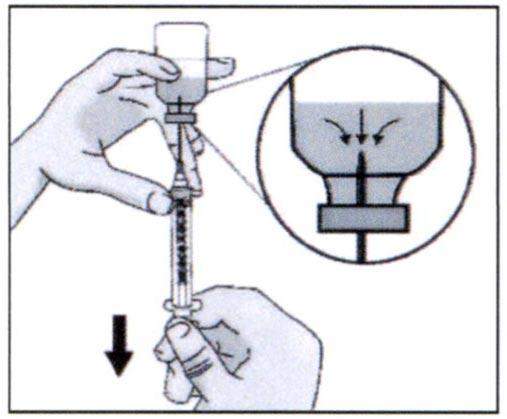
✓ Удалите большие пузырьки воздуха, аккуратно постукивая пальцами по шприцу до тех пор, пока пузырьки не поднимутся к верхней части шприца. Медленно надавите на поршень, чтобы воздух вышел обратно во флакон до тех пор, пока раствор не достигнет верхней части шприца.
Повторяйте эти этапы до тех пор, пока не удалите большие пузырьки воздуха.
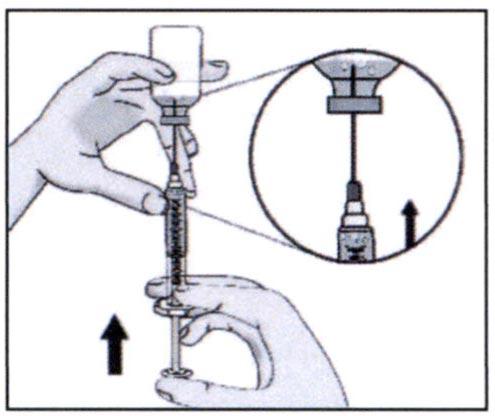
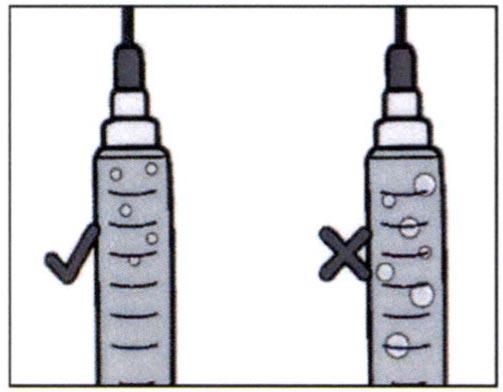
✓ He вынимая иглу из флакона, открутите шприц, удерживая верх иглы и поворачивая шприц против часовой стрелки.
Верните шприц в вертикальное положение.
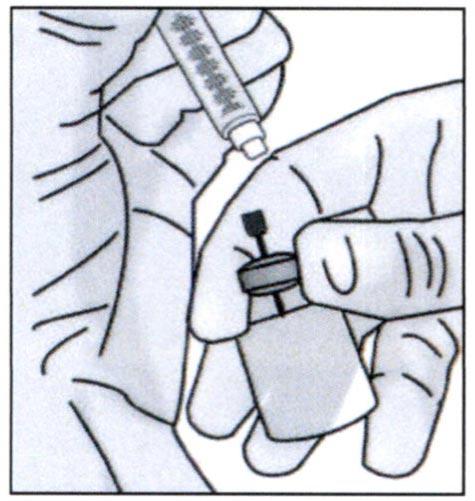
✓ Выкиньте использованную тупоконечную иглу размера 18G и сам флакон в контейнер для отходов острых предметов.
✓ Прикрутите остроконечную иглу размера 27G×1/2 дюйма (0,4×13 мм) для проведения подкожной инъекции
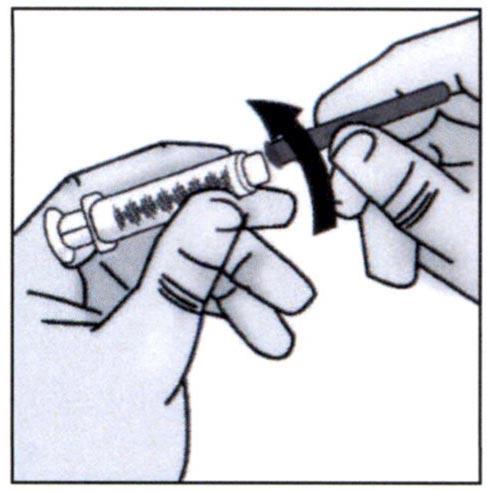
Важно:
Не удаляйте колпачок с иглы во время прикрепления иглы к шприцу.
Не используйте иглу с тупым концом размера 18G для введения препарата Такзайро, так как это может вызвать болевые ощущения и кровотечение месте инъекции.
Этап 4. Выбор и подготовка области для инъекции
✓ Выберите место для инъекций на животе, бедре или плече.
Инъекцию необходимо выполнять подкожно.
✓ Протрите место инъекции спиртовой салфеткой и подождите, пока кожа в этом месте полностью высохнет.
Важно:
- Для поддержания здоровья кожи важно чередовать места инъекций.
- Область, которая выбрана для инъекции, должна находиться на расстоянии не менее 5 см от шрамов или пупка.
Не выбирайте участки кожи с кровоподтёком, припухлостью или болезненными ощущениями. - Если Вы выполняете инъекцию самостоятельно, не рекомендуется выбирать для введения препарата наружную часть плеча.
Этап 5. Введение препарата Такзайро
✓ Снимите колпачок с иглы, прикрученной к шприцу, не касаясь иглы.
Не тяните за поршень.
Не прикасайтесь к кончику иглы и не касайтесь им любой другой поверхности.
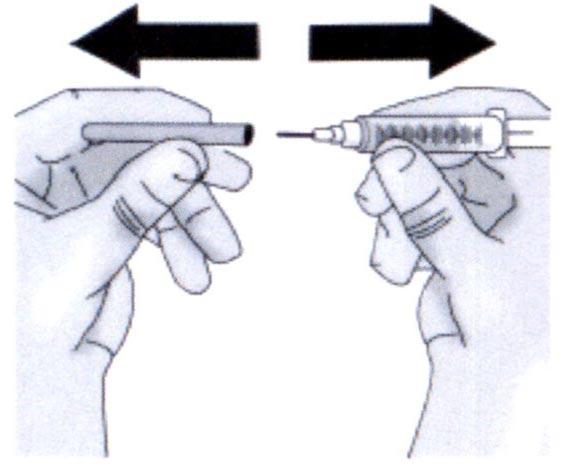
Важно:
Инъекцию препарата Такзайро следует сделать в течение 2 часов с момента заполнения шприца препаратом, если готовый шприц находится при комнатной температуре.
Разрешается поместить шприц с препаратом в холодильник при температуре 2-8 °С и использовать его для проведения инъекции в течение 8 часов.
✓ Осторожно сожмите примерно 3 см кожи в протертом спиртовой салфеткой месте и введите иглу.
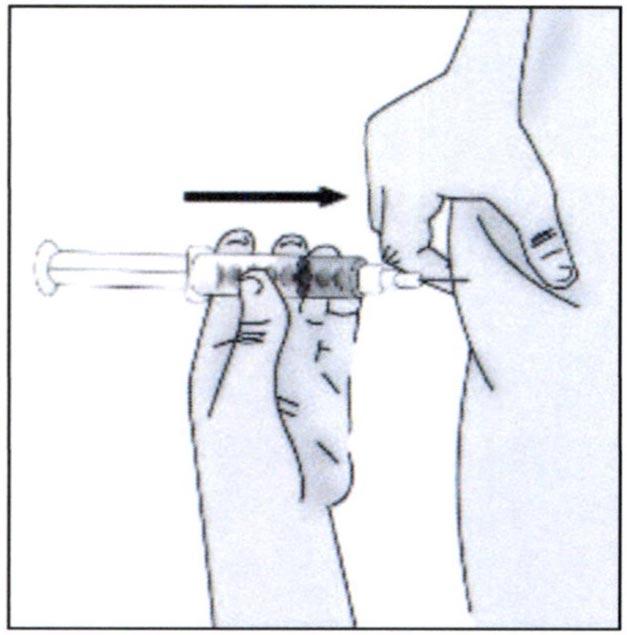
Важно:
Обязательно вводите иглу в подкожную область, которая располагается не слишком близко к поверхности кожи (слой кожи) и не слишком глубоко (мышцы)
✓ Медленно давите на поршень, пока не введете весь препарат.
Отпустите кожу и осторожно выньте иглу.
Не закрывайте иглу колпачком.
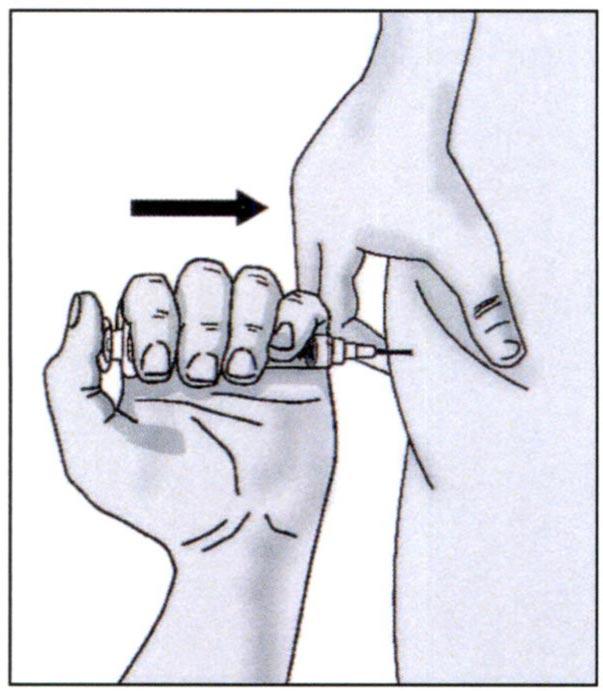
✓ Поместите использованные иглу для подкожных инъекций 27G×1/2 дюйма (0,4×13 мм) и шприц в контейнер для отходов острых предметов.
Химическая и физическая стабильность препарата после вскрытия упаковки была продемонстрирована в течение 2 часов при температуре не выше 25 °С и в течение 8 часов при температуре от 2 до 8 °С. С точки зрения микробиологической безопасности, если условия подготовки к проведению инъекции не исключают риск микробного загрязнения, препарат должен быть использован немедленно. Препарат Такзайро может быть введен пациенту в течение 2 часов после заполнения дозирующего шприца при его хранении при комнатной температуре. Альтернативно, дозирующий шприц может быть помещен в холодильник при температуре от 2 до 8 °С и должен быть использован в течение 8 часов. Ответственность за продолжительность и условия хранения раствора препарата в шприце несет либо медицинский работник, либо пациент (при самостоятельном применении).
Побочное действие
Краткая характеристика профиля безопасности
Наиболее частыми (52,4%) нежелательными лекарственными реакциями (НЛР), ассоциируемыми с введением препарата Такзайро, были реакции в месте введения, в том числе, боль, эритема и кровоподтек в месте введения. Из этих локальных НЛР, 97% были слабой степени тяжести, а 90% разрешились в течение 1 суток (средняя продолжительность локальной НЛР составила 6 минут).
Реакции гиперчувствительности (зуд легкой и средней степени тяжести, дискомфорт и ощущение покалывания языка) отмечались у 1,2% пациентов (см. раздел «Особые указания»).
В Таблице 1 представлены НЛР, зарегистрированные в клиническом исследовании HELP, в которое было включено 84 пациента с НАО, получивших, по крайней мере, одну дозу препарата Такзайро.
Частоту НЛР, оценивали следующим образом: очень часто (≥1/10); часто (≥1/100, но <1/10); нечасто (≥1/1,000, но <1/100); редко (≥1/10,000, но <1/1,000); очень редко (<1/10,000).
Таблица 1: Нежелательные лекарственные реакции, зарегистрированные на фоне применения ланаделумаба
| Класс системы органов | Нежелательная лекарственная реакция | Частота |
| Нарушения со стороны иммунной системы | Реакции гиперчувствительности* | Часто |
| Нарушения со стороны нервной системы | Головокружение | Часто |
| Нарушения со стороны кожи и подкожных тканей | Макуло-папулезная сыпь | Часто |
| Нарушения со стороны скелетно-мышечной и соединительной ткани | Миалгия | Часто |
| Общие расстройства и реакции в месте введения | Реакции в месте инъекции** | Очень часто |
| Лабораторные и инструментальные данные | Повышение активности аланинаминотрансферазы | Часто |
| Повышение активности аспартатаминотрансферазы | Часто |
* Реакции гиперчувствительности включают: зуд, дискомфорт и ощущение покалывания языка.
** Реакции в месте инъекции включают: боль, эритему, кровоподтек, дискомфорт, гематому, кровотечение, зуд, припухлость, уплотнение, парестезию, реакцию, ощущение тепла, отек и сыпь.
Дети
Безопасность применения препарата Такзайро оценивали в подгруппе из 23 пациентов в возрасте от 12 до 18 лет. Результаты анализа в подгруппе соответствовали результатам анализа данных всех пациентов.
Иммуногенность
Терапия ланаделумабом ассоциировалась с выработкой антител к препарату у 11,9% (10/84) пациентов. У всех пациентов титры антител были низкими. У 20% (2/10) пациентов присутствие антител в крови было кратковременным. Нейтрализующие антитела к ланаделумабу были обнаружены у 2,4% (2/84) пациентов, получавших лечение препаратом Такзайро.
Выработка антител к ланаделумабу, в том числе, нейтрализующих антител, не оказывала неблагоприятного влияния на профили фармакокинетики и фармакодинамики препарата или на его клинический ответ.
Передозировка
Случаев передозировки не зарегистрировано. Доступная информация для идентификации признаков и симптомов передозировки отсутствует. В случае появления симптомов рекомендуется проводить симптоматическую терапию. Доступный антидот отсутствует.
Взаимодействие с другими лекарственными средствами
Не проводилось исследований лекарственного взаимодействия. Учитывая характеристики ланаделумаба, фармакокинетических взаимодействий с одновременно применяемыми лекарственными препаратами не предполагается.
Как и предполагалось, сопутствующее применение ингибитора С1 эстеразы в качестве неотложной терапии оказывает аддитивное действие на индуцированный ланаделумабом cHMWK-ответ, исходя из механизма действия ланаделумаба и ингибитора С1 эстеразы (см. раздел «Фармакодинамика»).
Особые указания
Прослеживаемость
С целью улучшения прослеживаемости применения биологических лекарственных средств, необходимо точно регистрировать название и номер серии применяемого лекарственного препарата.
Реакции гиперчувствительности
Были отмечены реакции гиперчувствительности. В случае развития тяжелой реакции гиперчувствительности, необходимо немедленно прекратить введение препарата Такзайро и начать соответствующую терапию.
Общие указания
Препарат Такзайро не предназначен для лечения острых приступов НАО. В случае развития острого приступа НАО необходимо начать индивидуально подобранную неотложную терапию другими зарегистрированными препаратами.
Клинические данные о применении ланаделумаба у пациентов с НАО и нормальной активностью С1-ингибитора отсутствуют.
Влияние на показатели свертывающей системы крови
Ланаделумаб может повышать значения активированного частичного тромбопластинового времени (АЧТВ) в результате взаимодействия ланаделумаба с методом определения АЧТВ. Реагенты, применяемые для определения АЧТВ, инициируют внутренний путь коагуляции посредством активации плазменного калликреина в контактной системе. Ингибирование плазменного калликреина ланаделумабом может увеличить АЧТВ, определяемое с помощью этого метода. Ни одно из повышений АЧТВ у пациентов, получавших препарат Такзайро, не ассоциировалось с патологическим кровотечением. Не наблюдалось различий в значениях международного нормализованного отношения (МНО) между группами терапии.
Содержание натрия
Лекарственный препарат Такзайро содержит менее 1 ммоль натрия (23 мг) на один флакон, то есть фактически является препаратом, не содержащим натрий.
Влияние на способность управлять транспортными средствами и механизмами
Препарат Такзайро не обладает каким-либо значимым влиянием на способность к управлению транспортными средствами и механизмами.
Форма выпуска
Раствор для подкожного введения, 150 мг/мл
2,0 мл препарата помещают во флакон из прозрачного бесцветного стекла (тип I, Евр. Фарм.) вместимостью 5 мл, укупоренный хлорбутилкаучуковой пробкой с алюминиевой обкаткой и отрывной полипропиленовой крышечкой типа «flip-off».
По одному флакону на пластиковом фиксаторе для флакона вместе с одноразовым шприцем, тупоконечной иглой 18G для наполнения шприца, иглой для подкожных инъекций 27G×1/2 дюйма и инструкцией по применению помещают в картонную пачку.
Для контроля первого вскрытия пачки предусмотрено наличие специального стикера.
Условия хранения
Хранить при температуре от 2 до 8 °С в картонной пачке для защиты от воздействия света.
Не замораживать.
Хранить в недоступном для детей месте.
В пределах срока годности флаконы с препаратом могут храниться пациентом при температуре не выше 25 °С в течение 14 дней, после чего препарат использованию не подлежит и должен быть утилизирован.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения:
Шайер Фармасьютикалс Айерленд Лимитед, Ирландия
Shire Pharmaceuticals Ireland Limited
Block 2 & 3, Miesian Plaza 50-58 Baggot Street Lower, Dublin 2, D02 Y754, Ireland
Производитель готовой лекарственной формы и первичный упаковщик:
Каталент Индиана, ЛЛС, США
Catalent Indiana, LLC
1300 South Patterson Drive Bloomington, IN 47403, USA
Выпускающий контроль качества:
Шайер Фармасьютикалс Айерленд Лимитед, Ирландия
Shire Pharmaceuticals Ireland Limited,
Block 2 & 3, Miesian Plaza 50-58 Baggot Street Lower, Dublin 2, D02 Y754, Ireland
Претензии потребителей направлять по адресу:
ООО «Такеда Фармасьютикалс»
119048 Москва, ул. Усачева, д.2, стр. 1
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Инструкция по применению Такзайро 15 мг/мл 2 мл 1 шт. раствор для подкожного введения
Состав
В 1 мл раствора содержится:
действующее вещество: ланаделумаб – 150 мг,
вспомогательные вещества: натрия гидрофосфата дигидрат – 5,3 мг, лимонной кислоты моногидрат – 4,1 мг, L-гистидин – 7,8 мг, натрия хлорид – 5,3 мг, полисорбат 80-0,1 мг, вода для инъекций до 1,0 мл.
Фармакологическое действие
Ланаделумаб ингибирует протеолитическую активность активированного калликреина в плазме. Повышение активности калликреина в плазме вызывает приступ ангионевротического отека у пациентов с НАО посредством протеолиза кининогена с высокой молекулярной массой (High Molecular Weight Kininogen, HMWK) с последующим образованием расщепленного кининогена с высокой молекулярной массой (cleaved High Molecular Weight Kininogen,, cHMWK) и высвобождением брадикинина. Ланаделумаб обеспечивает длительный контроль активности калликреина в плазме, и, тем самым, ограничивает образование брадикинина у пациентов с НАО.
Фармакодинамика
Зависимая от концентрации препарата Такзайро степень ингибирования калликреина в плазме, измеренная как снижение концентрации cHMWK, была продемонстрирована после подкожного введения препарата в дозе 150 мг 1 раз в 4 недели [1 раз/4 нед], 300 мг 1 раз в 4 недели [1 раз/4 нед] или 300 мг 1 раз в 2 недели [1 раз/2 нед] пациентам с НАО.
Фармакокинетическая-фармакодинамическая взаимосвязь между ланаделумабом и cHMWK описывается с помощью непрямой фармакологической модели экспозиция-ответ. Наибольшее снижение скорости образования cHMWK – на 53,7%, – было достигнуто при воздействии ланаделумаба в концентрации полумаксимального ингибирования (IC50), равной 5705 нг/мл.
Фармакокинетика
Наследственного ангионевротического отека (НАО) средство лечения.
Показания
Препарат Такзайро показан для профилактики рецидивирующих приступов наследственного ангионевротического отека у пациентов в возрасте 12 лет и старше.
Режим дозирования
Применение препарата Такзайро необходимо начинать под наблюдением врача, имеющего опыт лечения пациентов с НАО.
Препарат Такзайро может вводить сам пациент или лицо, осуществляющее уход за ним, после обучения правильной технике подкожных инъекций медицинским работником (см. подраздел «Инструкция по применению препарата»).
Рекомендуемая начальная доза составляет 300 мг ланаделумаба (препарата Такзайро) 1 раз/2 нед. Пациентам, у которых на фоне терапии стабильно отсутствуют приступы, доза ланаделумаба может быть снижена до 300 мг 1 раз/4 нед, особенно пациентам с низкой массой тела.
Препарат Такзайро не предназначен для лечения острых приступов НАО (см. раздел «Особые указания»).
Введение пропущенной дозы препарата
Следует особо обратить внимание, что, если введение очередной дозы препарата Такзайро пропущено, ее следует ввести как можно скорее, однако, так, чтобы интервал между дозами был не менее 10 суток.
Особые группы пациентов
Пожилые
Ожидается, что возраст пациента не будет влиять на экспозицию ланаделумаба. Не требуется корректировать дозу препарата у пациентов старше 65 лет (см. раздел «Фармакокинетика»).
Применение у пациентов с печеночной недостаточностью
Не проводились исследования препарата у пациентов с печеночной недостаточностью. Предполагается, что печеночная недостаточность не влияет на экспозицию ланаделумаба. Не требуется корректировать дозу препарата у пациентов с печеночной недостаточностью (см. раздел «Фармакокинетика»).
Пациенты с почечной недостаточностью
Не проводились исследования препарата у пациентов с почечной недостаточностью тяжелой степени. Предполагается. что почечная недостаточность не влияет на экспозицию ланаделумаба или его профиль безопасности. Не требуется корректировать дозу препарата у пациентов с почечной недостаточностью (см. раздел «Фармакокинетика»).
Дети
В связи с отсутствием данных, безопасность и эффективность препарата Такзайро у детей младше 12 лет не установлены.
Способ применения
Только для подкожного введения.
Каждый флакон препарата Такзайро предназначен только для однократного применения.
Препарат необходимо вводить только в рекомендованные области: живот, бедро и верхнюю наружную часть плеча (см. раздел «Фармакокинетика»). Рекомендуется чередовать области проведения инъекции.
Перед введением препарата необходимо проверить внешний вид каждого флакона. Раствор должен быть прозрачным или слегка желтоватым. Если раствор изменил окраску или содержит посторонние включения, его нельзя использовать.
Следует избегать энергичного перемешивания.
Этапы введения
В асептических условиях наберите необходимую дозу препарата Такзайро из флакона в шприц с помощью иглы размера 18G. Поменяйте иглу на шприце на иглу размера 27 G или другую иглу, подходящую для выполнения подкожной инъекции. Введите препарат Такзайро подкожно в область живота, бедра или плеча.
Противопоказания
Повышенная чувствительность к ланаделумабу или любому из вспомогательных веществ
Детский возраст до 12 лет (недостаточно клинических данных)
Беременность и период грудного вскармливания
Применение при беременности и в период грудного вскармливания
Беременность
Данные о применении ланаделумаба у беременных женщин либо отсутствуют, либо крайне ограниченны. Исследования, проведенные на животных, не выявили прямого или косвенного токсичного влияния препарата на репродуктивную функцию и развитие плода. В исследованиях пре- и постнатального развития у беременных яванских макак, которым вводили ланаделумаб 1 раз в неделю в дозах 10 или 50 мг/кг (наибольшая из исследуемых доз), не выявлено влияния ланаделумаба на беременность и роды, эмбриофетальное развитие, выживаемость, рост и/или постнатальное развитие детенышей. В этих исследованиях экспозиция была примерно в 32 раза выше, чем после введения препарата пациентам в дозе 300 мг 1 раз/2 нед в пересчете на AUC. В качестве меры предосторожности рекомендуется избегать применения ланаделумаба во время беременности.
Период грудного вскармливания
Отсутствуют данные о выделении ланаделумаба в грудное молоко. Известно, что иммуноглобулины человека выделяются в грудное молоко в первые дни после родов, но вскоре их концентрация снижается. Следовательно, в этот короткий период невозможно исключить риск для ребенка, получающего грудное вскармливание.
Фертильность
Оценка влияния ланаделумаба на фертильность человека не проводилась. Влияние ланаделумаба на фертильность оценивали на половозрелых яванских макаках. В ходе 13-недельного исследования было установлено, что ланаделумаб при подкожном введении в дозах 10-50 мг/кг (наибольшая из исследуемых доз) 1 раз в неделю не влиял на фертильность самцов или самок. В ходе исследования фертильности экспозиция у половозрелых яванских макак была примерно в 20 и 22 раза выше, чем после введения препарата в дозе 300 мг 1 раз/2 нед в пересчете на Сmax и AUC, соответственно. Установлено, что ланаделумаб не оказывал влияния на фертильность самцов и самок яванских макак.
Условия хранения
Хранить при температуре от 2 до 8 °С в картонной пачке для защиты от воздействия света.
Не замораживать.
Хранить в недоступном для детей месте.
В пределах срока годности флаконы с препаратом могут храниться пациентом при температуре не выше 25 °С в течение 14 дней, после чего препарат использованию не подлежит и должен быть утилизирован.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Инструкция по применению препарата
Удостоверьтесь, что Вы прочитали, поняли и будете следовать всем поэтапным инструкциям по введению препарата Такзайро®. Если у вас остались вопросы, обратитесь к своему врачу или медсестре.
Помимо стеклянного флакона, каждая упаковка препарата Такзайро® содержит:
— Один пустой одноразовый шприц на 3 мл.
— Одну тупоконечную иглу размера 18G (для наполнения шприца). Используется для переноса лекарственного раствора из флакона в одноразовый шприц.
— Одну иглу для подкожных инъекций размера 27G х 1/2 дюйма (0,4 х 13 мм) с острым концом. Используется для подкожного введения препарата.
Можно использовать только те шприцы, тупоконечные и остроконечные иглы (см. описание выше), которые вложены в эту упаковку, или те, которые рекомендовал врач.
Шприцы, тупоконечные и остроконечные иглы можно использовать только однократно. После использования шприцы и иглы помещают в контейнер для отходов острых предметов. Нельзя использовать поврежденные шприцы, а также тупоконечные и остроконечные иглы, которые выглядят поврежденными.
Вам также потребуются:
— Салфетки, смоченные спиртом.
— Контейнер для отходов острых предметов: использованных флаконов, игл и шприцев. Вы можете получить расходные материалы у своего врача, фармацевта или медсестры.
Выполнение инъекции препарата Такзайро® можно разделить на 5 этапов:
1. Подготовка флакона с препаратом Такзайро®
2. Прикрепление тупоконечной иглы к одноразовому шприцу
3. Наполнение одноразового шприца препаратом Такзайро® и замена тупоконечной на остроконечную для подкожного введения препарата
4. Выбор и подготовка области для введения инъекции
5. Введение препарата Такзайро®
Этап 1. Подготовка флакона с препаратом Такзайро®
— Достаньте флакон с препаратом из холодильника и перед использованием выдержите его 15 минут при комнатной температуре (15-25 °С).
— Очистите Ваше рабочее место и вымойте руки перед подготовкой препарата к введению.
После мытья рук и до проведения инъекции не дотрагивайтесь до любых поверхностей или частей Вашего тела.
— Возьмите препарат Такзайро® и расходные материалы и поместите их на хорошо освещенное рабочее место.
— Выньте флакон из упаковки.
Не используйте флакон, если пластиковый колпачок, закрывающий пробку, отсутствует.
— Осторожно переверните флакон 3-5 раз для перемешивания раствора. Не трясите флакон, так как это может привести к образованию пены.
— Проверьте раствор во флаконе на наличие посторонних включений или изменение цвета (в нормальном состоянии раствор бесцветный или слегка желтоватый). Не используйте раствор, если обнаружили посторонние включения или изменение цвета раствора.
Важно:
Не трясите флакон.
— Удалите пластиковый колпачок с флакона. НО не удаляйте резиновую пробку.
— Поставьте флакон на ровную поверхность. Протрите резиновую пробку салфеткой, смоченной в спирте, и оставьте высохнуть.
Этап 2. Прикрепление тупоконечной иглы к одноразовому шприцу
— Наверните на 3 мл шприц тупоконечную иглу размера 18G для прокалывания пробки флакона.
Важно:
Не удаляйте колпачок с иглы во время прикрепления иглы к шприцу.
— Оттяните назад поршень шприца для заполнения его воздухом в количестве, равном количеству раствора во флаконе.
— Снимите колпачок с иглы, прикрепленной к шприцу, не касаясь иглы. Не тяните за поршень.
Этап 3. Наполнение одноразового шприца препаратом Такзайро® и замена тупоконечной иглы на иглу для подкожных инъекций
— Проколите тупоконечной иглой резиновую пробку флакона в центре.
— Надавите на поршень вниз, чтобы ввести воздух во флакон, и удерживайте поршень в таком положении.
— Медленно переверните флакон вверх дном с прикрепленными иглой и шприцем.
Оттяните поршень назад, чтобы набрать в шприц полную дозу препарата из флакона.
Важно:
Обязательно держите кончик иглы в жидкости, чтобы избежать попадания воздуха в шприц при вытягивании поршня
— Удалите большие пузырьки воздуха, аккуратно постукивая пальцами по шприцу до тех пор, пока пузырьки не поднимутся к верхней части шприца. Медленно надавите на поршень, чтобы воздух вышел обратно во флакон до тех пор, пока раствор не достигнет верхней части шприца.
Повторяйте эти этапы до тех пор, пока не удалите большие пузырьки воздуха.
— He вынимая иглу из флакона, открутите шприц, удерживая верх иглы и поворачивая шприц против часовой стрелки.
Верните шприц в вертикальное положение.
— Выкиньте использованную тупоконечную иглу размера 18G и сам флакон в контейнер для отходов острых предметов.
— Прикрутите остроконечную иглу размера 27G х 1/2 дюйма (0,4 х 13 мм) для проведения подкожной инъекции
Важно:
Не удаляйте колпачок с иглы во время прикрепления иглы к шприцу.
Не используйте иглу с тупым концом размера 18G для введения препарата Такзайро® так как это может вызвать болевые ощущения и кровотечение в месте инъекции.
Этап 4. Выбор и подготовка области для инъекции
— Выберите место для инъекций на животе, бедре или плече. Инъекцию необходимо выполнять подкожно.
— Протрите место инъекции спиртовой салфеткой и подождите, пока кожа в этом месте полностью высохнет.
Важно:
— Для поддержания здоровья кожи важно чередовать места инъекций.
— Область, которая выбрана для инъекции, должна находиться на расстоянии не менее 5 см от шрамов или пупка.
Не выбирайте участки кожи с кровоподтёком, припухлостью или болезненными ощущениями.
— Если Вы выполняете инъекцию самостоятельно, не рекомендуется выбирать для введения препарата наружную часть плеча.
Этап 5. Введение препарата Такзайро®
— Снимите колпачок с иглы, прикрученной к шприцу, не касаясь иглы.
Не тяните за поршень.
Не прикасайтесь к кончику иглы и не касайтесь им любой другой поверхности.
Важно:
Инъекцию препарата Такзайро® следует сделать в течение 2 часов с момента заполнения шприца препаратом, если готовый шприц находится при комнатной температуре.
Разрешается поместить шприц с препаратом в холодильник при температуре 2-8°С и использовать его для проведения инъекции в течение 8 часов.
— Осторожно сожмите примерно 3 см кожи в протертом спиртовой салфеткой месте и введите иглу.
Важно:
Обязательно вводите иглу в подкожную область, которая располагается не слишком близко к поверхности кожи (слой кожи) и не слишком глубоко (мышцы)
— Медленно давите на поршень, пока не введете весь препарат.
Отпустите кожу и осторожно выньте иглу. Не закрывайте иглу колпачком.
— Поместите использованные иглу для подкожных инъекций 27G х 1/2 дюйма (0,4 х 13 мм) и шприц в контейнер для отходов острых предметов.
Химическая и физическая стабильность препарата после вскрытия упаковки была продемонстрирована в течение 2 часов при температуре не выше 25 °С и в течение 8 часов при температуре от 2 до 8 °С. С точки зрения микробиологической безопасности, если условия подготовки к проведению инъекции не исключают риск микробного загрязнения, препарат должен быть использован немедленно. Препарат Такзайро® может быть введен пациенту в течение 2 часов после заполнения дозирующего шприца при его хранении при комнатной температуре. Альтернативно, дозирующий шприц может быть помещен в холодильник при температуре от 2 до 8 °С и должен быть использован в течение 8 часов. Ответственность за продолжительность и условия хранения раствора препарата в шприце несет либо медицинский работник, либо пациент (при самостоятельном применении).
Способ применения препарата в предварительно заполненном шприце
Только для подкожного введения.
Каждый предварительно заполненный шприц с препаратом Такзайро® предназначен только для однократного использования. Препарат готов к использованию.
Препарат необходимо вводить только в рекомендованные области: живот, бедро и верхнюю наружную часть плеча (см. раздел «Фармакокинетика»). Рекомендуется чередовать области проведения инъекции.
Перед использованием необходимо визуально оценить внешний вид каждого предварительно заполненного шприца. Раствор должен быть прозрачным или слегка желтоватым. Не следует использовать раствор, который поменял цвет или содержит частицы.
Следует избегать встряхивания.
Любой неиспользованный лекарственный препарат или отходы следует утилизировать в соответствии с местными требованиями.
Все иглы и шприцы следует утилизировать в контейнере для острых предметов.
Инструкция по применению препарата
Удостоверьтесь, что Вы прочитали, поняли и будете следовать всем поэтапным инструкциям по введению препарата Такзайро®. Если у вас остались вопросы, обратитесь к своему врачу или медсестре.
Предварительно заполненный шприц Такзайро® — лекарственный препарат для одноразового применения с фиксированной дозой (300 мг/2 мл), предназначен для подкожного введения медицинскими работниками, лицами, осуществляющими уход, или самостоятельного введения.
Устройство предварительно заполненного шприца Такзайро®
ШАГ 1: Подготовка к введению
а. Приготовьте спиртовые салфетки, ватный шарик/марлевую салфетку, лейкопластырь и контейнер для утилизации острых предметов (рис. А) и разместите их на чистой ровной поверхности в хорошо освещенном месте. Данные расходные материалы не входят в упаковку лекарственного препарата Такзайро®.
Рисунок А
b. Достаньте препарат Такзайро® из холодильника, откройте картонную пачку и извлеките предварительно заполненный шприц из пластикового фиксатора (лотка).
— Не используйте предварительно заполненный шприц Такзайро®, если пломба для контроля вскрытия открыта или разрушена.
— Перед инъекцией дайте предварительно заполненному шприцу нагреться до комнатной температуры в течение как минимум 15-30 минут.
— Лекарственный препарат чувствителен к высоким температурам. Запрещено применять внешние источники тепла, такие как горячая вода, для нагрева предварительно заполненного шприца Такзайро®.
— Не снимайте защитный колпачок иглы до полной готовности к введению.
с. Вымойте руки водой с мылом, тщательно вытрите.
d. Проверьте срок годности на этикетке
— Не используйте препарат Такзайро® после истечения срока годности.
е. Осмотрите предварительно заполненный шприц Такзайро® на предмет повреждений и убедитесь, что лекарственный препарат представляет собой бесцветный или слегка желтоватого цвета раствор.
— Не используйте препарат, если шприц поврежден — например, треснувший шприц.
— Если раствор поменял цвет, помутнел или содержит хлопья или частицы, не применяйте лекарственный препарат, сообщите об этом своему специалисту области здравоохранения.
— В предварительно заполненном шприце Такзайро® могут присутствовать пузырьки воздуха. Это нормально и не повлияет на дозу.
ШАГ 2: Выбор и подготовка места для инъекции
а. Выберите область для введения препарата Такзайро®: живот, бёдра или плечо (внешняя часть плеча не рекомендуется, если инъекция делается самостоятельно).
— Важно менять места инъекций, чтобы кожа оставалась здоровой. Каждую новую инъекцию следует делать на расстоянии не менее 3 см от последнего места инъекции.
— Не вводите инъекцию в участки тела, где кожа раздражена, покраснела, покрыта синяками или инфицирована.
— Область для инъекции должна находиться на расстоянии не менее 5 см от шрамов или пупка.
b. Протрите место инъекции спиртовой салфеткой и подождите, пока кожа в этом месте полностью высохнет.
— Не обмахивайте чистое место веером и не дуйте на него.
— Не прикасайтесь к этой области снова, прежде чем сделать инъекцию.
с. Снимите защитный колпачок иглы с предварительно заполненного шприца Такзайро®. Осторожно потяните защитный колпачок иглы одной рукой и крепко удерживайте середину предварительно заполненного шприца Такзайро® другой рукой. Утилизируйте защитный колпачок иглы.
— Не надевайте защитный колпачок обратно на иглу предварительно заполненного шприца.
— Не применяйте предварительно заполненный шприц Такзайро®, если он упал без защитного колпачка иглы или если игла повреждена или погнулась.
— Не прикасайтесь к игле и не давайте игле касаться чего-либо.
ШАГ 3: Введение препарата Такзайро®
а. Возьмите предварительно заполненный шприц Такзайро® одной рукой, как карандаш.
Не прикасайтесь к игле и не нажимайте на поршень.
b. Другой рукой осторожно соберите в складку примерно 3 см кожи в очищенном месте инъекции.
c. Одним быстрым и коротким движением введите иглу в кожу. Обязательно держите иглу на месте.
d. Медленно надавливайте на поршень, пока не будет введена вся жидкость, и шприц не опустеет, затем осторожно отпустите кожу.
e. Медленно извлеките иглу, удерживая шприц под тем же углом.
f. При необходимости прижимайте ватный шарик или марлевую салфетку к месту инъекции и удерживайте 10 секунд.
— Не растирайте место инъекции. Может наблюдаться небольшое кровотечение. Это нормально.
— При необходимости закройте место инъекции лейкопластырем.
g. Утилизируйте использованный предварительно заполненный шприц Такзайро®.
— Не касайтесь иглы.
— Чтобы избежать травм от укола иглой — не следует повторно надевать защитный колпачок на иглу.
— Утилизируйте использованные предварительно заполненные шприцы Такзайро® в контейнер для утилизации острых предметов сразу после использования.
— Запрещено применять повторно предварительно заполненный шприц Такзайро® и любые принадлежности для инъекции.
Важно: всегда хранить контейнер для утилизации острых предметов в недоступном для детей месте.
