Инструкции
для практических работ
9 класс.
К учебнику Габриеляна О.С.
Составитель учитель химии
МБОУ СОШ №2 г. Кировск
Румянцева Е.М.
2013
Практическая работа №1.
Осуществление цепочки химических превращений.
I ВАРИАНТ
Повторить правила техники безопасности:
Цель: Осуществить реакции, соответствующие указанным цепочкам превращений.
Проведите реакции, в которых осуществляются предложенные ниже химические превращения:
1)MgCO3 → MgCl2 → Mg(OH)2 → MgSO4
2)ZnCl2 → Zn(OH)2 → ZnCl2
↓
Na2 [ZnOH4]
Опыт 1. Инструкция к выполнению первой цепочки переходов.
1)Выданы пробирки №1, №2, №3. В пр.№1насыпана соль MgCO3. Для осуществления превращений приливайте по 1-2 мл необходимых реактивов;
-после проведения 1-ого опыта отделите раствор от непрореагировавшего вещества, слейте его в пр. №2;
— в пр.№2 к полученному после добавления выбранного вами реактива осадку добавьте 1-2 мл воды, перемешайте смесь и отфильтруйте в стаканчик, промойте осадок 2-3мл воды;
— осадок перенесите стеклянной палочкой в пр. №3 и осуществите третье превращение.
Опыт 2. Инструкция к выполнению второй цепочки переходов.
2)Для осуществления второй цепочки переходов выданы пробирки №4, №5;
а) в обе пробирки прилейте по 1-2 мл раствора хлорида цинка и получите в обеих пробирках студенистый осадок гидроксида цинка (реактива приливайте по 1-2 мл в каждую пробирку).
б) в пр.№4 получите ZnCl2, в пр.№5 получите Na2Zn(OH)4.Составьте молекулярные и ионные уравнения реакций. Для отчёта оформите таблицу:
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
1цепочка ……… 2цепочка |
…………………. |
1) 2) 3)……………………….. 1) 2) 3) |
………… |
Практическая работа №1.
Осуществление цепочки химических превращений.
II ВАРИАНТ
Повторить правила техники безопасности:
Цель: Изучить способы получения и свойства гидроксидов металла.
Проведите реакции, в которых осуществляются предложенные ниже химические превращения:
1)CuSO4 → Cu(OH)2 → CuO → Cu
2)AlCl3 → Al(OH)3 → AlCl3
↓
NaAl(OH)4
Инструкция к выполнению первой цепочки переходов.
1)Для выполнения первой цепочки превращений выданы пробирки №1, №2. В пр.№1насыпана соль CuSO4 . Для осуществления 1-ого опыта приливайте 1-2 мл необходимого реактива.
2)Второй и третий переход проводите в этой же пробирке (№1). В пробирку №2 положен кусочек алюминия.
Инструкция к выполнению второй цепочки переходов.
2)Для осуществления второй цепочки переходов выданы пробирки №3, №4. В обе пробирки прилейте по 1-2 мл раствора хлорида алюминия и получите в обеих пробирках студенистый осадок гидроксида алюминия (используйте 1-2 мл раствора реактива). В пр.№3 получите AlCl3, в пр.№4 получите NaAl(OH)4
Составьте молекулярные и ионные уравнения реакций.
Для отчёта оформите таблицу
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт 1 ……………. Опыт 2 |
…………………….. |
……………………………… |
…………… |
Практическая работа №6.
Получение, собирание и распознавание газов.
Цель: изучить лабораторные способы получения, собирания и распознавания газов.
Вариант №I
Опыт1: получение, собирание и распознавание водорода.
Повторите правила техники безопасности:
Проверка на герметичность
1)Наденьте на пробирку №1пробку с газоотводной трубкой, проверьте прибор на герметичность.
2)В пробирку положите 1-2 гранулы цинка, прилейте 1-2 мл соляной кислоты, пробирку закрепите в штативе вертикально и наденьте на газоотводную трубку пробирку №2.
3)Через некоторое время собранный в пробирке №2 газ (держите пробирку вертикально) поднесите к пламени спиртовки. Вы должны услышать либо глухой хлопок п-пах, либо «лающий» звук (в чём причина различий?).
Заполните таблицу, напишите уравнения 2-ух проведённых реакций, составьте электронный баланс, сделайте выводы о лабораторном способе получения, собирания и распознавания водород
Оформите отчёт в таблице.
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт 1 …………… Опыт 2 |
…………………… |
1) 2) ……………………………………………….. 1) 2) 3) |
…………. |
Опыт2: получение, собирание и распознавание аммиака
Повторите правила техники безопасности:
1)Соберите прибор для получения газа: пробирку № 4 закройте пробкой с газоотводной трубкой согнутой под прямым углом и проверьте прибор на герметичность: наденьте на стеклянную трубку длинную резиновую трубку так, чтобы стеклянная трубка оставалась сухой (почему?), после проверки снимите резиновую трубку.
2)Смешайте в фарфоровой чашечке по 1-ой чайной ложечке (ложечки возьмите разные) сульфата аммония (или хлорида аммония) и гидроксида кальция, поместите смесь в сухую пробирку, закройте пробкой с газоотводной трубкой согнутой под прямым углом и повёрнутой вверх ( можно проконсультироваться с рис.113 стр.190 учебника); дно пробирки со смесью немного приподнимите, на стеклянную трубку наденьте сухую пробирку №5.
3)Прогрейте сначала всю пробирку №4, а затем то место, где находится смесь. Не прекращая нагревания, определите наличие аммиака по изменению цвета влажной фенолфталеиновой бумажки, поднесённой к отверстию пробирки-приёмника (№5).
4)Прекратите нагревание, снимите пробирку №5 с аммиаком с трубочки, сразу же отверстие трубочки закройте кусочком влажной ваты, а пробирку с аммиаком закройте большим пальцем. Опустите пробирку с аммиаком в кристаллизатор с водой, впустите капельку воды, закройте снова пробирку под водой, палец будет втягиваться в пробирку, так как в ней образовался вакуум . Снова под водой отнимите палец. Что наблюдаете?
5)Закройте пробирку пальцем под водой и выньте её из сосуда. Разделите содержимое пробирки на две части; В одну добавьте 2-3 капли фенолфталеина, в другую – 2-3 капли хлорида алюминия. Что наблюдаете?
Составьте отчёт, заполнив таблицу, составьте 3 уравнения проведённых реакций, сделайте вывод о лабораторном способе получения, собирания и распознавания аммиака.
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт 1 …………… Опыт 2 |
…………………… |
1) 2) ……………………………………………….. 1) 2) 3) |
…………. |
Практическая работа №6.
Получение, собирание и распознавание газов.
Цель: применить лабораторные способы получения, собирания и распознавания газов.
Вариант №I I
Опыт1: получение, собирание и распознавание оксида углерода (IV). Повторите правила техники безопасности:
1)Соберите прибор Кирюшкина для получения газа, проверьте его на герметичность.
2)В пробирку на резиновое кольцо поместите несколько кусочков мрамора.
3)Откройте зажим и прилейте в воронку соляной кислоты так, чтобы она покрыла поверхность мрамора.
4)Опускайте газоотводную трубку поочерёдно в пробирки №1, №2:
-в пр.№1 – известковая вода;
-в пр.№2 – дистиллированная вода, подкрашенная лакмусом.
Что наблюдаете? По окончании опыта закройте зажим. Заполните таблицу (см. ниже).
Опыт2: получение, собирание и распознавание кислорода.
1)Соберите прибор для получения газа: наденьте на пробирку №3 пробку с газоотводной трубкой (трубка должна быть достаточной длины, чтобы её можно было опустить вниз), проверьте прибор на герметичность.
2) Закрепите пробирку вертикально в штативе, поместите в неё 2-3 мл раствора пероксида водорода и добавьте на кончике шпателя оксида марганца(IV). Что наблюдаете? Закройте сразу пробирку пробкой с газоотводной трубкой.
3)Поместите газоотводную трубку в пустой химический стакан; через некоторое время проверьте наличие в нём кислорода тлеющей лучинкой.Составьте отчёт, заполнив таблицу:
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт1 …………… Опыт2 |
………………………. |
……………………………… |
…………… |
Практическая работа №4
Экспериментальные задачи по теме «Подгруппа кослорода»
Цель: провести реакции, подтверждающие наличие в растворе данных ионов; решить задачи, на распознавание веществ, используя минимальное число реактивов.
Вариант №I). Повторите правила техники безопасности:
Выполняем задания из учебника № 1, 4, 6.
1)В пробирки №1 и №2 прилить по 2-3 мл раствора серной кислоты. В пр. № 1 добавить реактив на катион водорода (1-2 мл); в пр.№2 добавить реактив на сульфат-ион (1-2 мл).
4) В пробирках №3, №4 и№5 находятся растворы веществ. Необходимо определить в какой из трёх пробирок находится раствор соляной кислота, в какой – серной кислоты, в какой — гидроксида натрия. Для этого разделите содержимое каждой пробирки на две части (пустые пробирки стоят в параллельном ряду).
В первый ряд во все три пробирки добавьте по 2-3 капли индикатора: определите щёлочь.
В две пробирки с пока неопознанными веществами (в те, в которые вы не приливали индикатор, в параллельном ряду) добавьте несколько капель реактива, который вы выбрали для определения кислот.
6)В пробирку № 6 насыпана соль (крист.). Прилейте 3-4 мл дистиллированной воды, растворите соль, разделите раствор соли на две пробирки (часть отлейте в пр. №7);
В пр.№6 добавьте несколько капель раствора реактива на хлорид и иодид-ион, в пр. №7 — несколько капель раствора реактива на сульфат-ион.
Составьте молекулярные и ионные уравнения реакций.
Для отчёта оформите таблицу
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
№1 ……… №4 ………………….. №6 |
…………………. ……………………… |
1) 2) ……………………………….. 1) 2) ……………………………….. 1) |
………… ………….. |
Практическая работа №4
Экспериментальные задачи по теме «Подгруппа кослорода»
Цель: провести реакции, подтверждающие наличие в растворе данных ионов; решить задачи, на распознавание веществ, используя минимальное число реактивов.
Вариант №II). Повторите правила техники безопасности:
Выполняем задания из учебника № 2,4,5.
2)В пробирку № 1 положите 2-3 гранулы цинка. Прилейте в неё 2-3 мл серной кислоты. Что наблюдаете? Составьте уравнение методом электронного баланса, укажите окислитель и восстановитель.
4) В пробирках №2, №3 и№4 находятся растворы электролитов. Необходимо определить в какой из трёх пробирок находится раствор соляной кислоты, в какой — серной кислоты, в какой – гидроксида натрия. Для этого разделите содержимое каждой пробирки на две части (пустые пробирки стоят в параллельном ряду).
В первый ряд во все три пробирки добавьте по 2-3 капли индикатора: определите щёлочь.
В две пробирки с неопределёнными пока растворами веществ (в те, в которые вы не приливали индикатор, в параллельном ряду) добавьте несколько капель реактива, который вы выбрали для определения кислот. Составьте молекулярные и ионные уравнения реакций.
5) В пробирку №5 прилейте 2-3 мл дистиллированной воды, растворите кристаллическое вещество, добавьте несколько капель реактива, выбранного вами для обнаружения сульфат-ионов.
Для отчёта оформите таблицу
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
№2 ……… №4 ………………….. №5 |
…………………. ……………………… |
1) 2) ……………………………….. 1) 2) ……………………………….. 1) |
………… ………….. |
Практическая работа №3
Решение экспериментальные задач на распознавание и получение веществ.
Цель: провести реакции, подтверждающие наличие в растворе данных ионов; решить задачи, на распознавание веществ, используя минимальное число реактивов. Повторите правила техники безопасности:
Вариант №I
Выполняем вариант №1 стр.86 и задание №3 стр.87 учебника.
- В пробирках №1, №2 и №3 находятся твёрдые вещества: гидроксид натрия, карбонат калия и хлорид бария. Определите в какой пробирке находится каждое из веществ с помощью одного реактива.
а) растворите каждое из исследуемых веществ в 3-4 мл воды;
б) прилейте в пробирки 1,2 и 3по 1-2 мл выбранного вами реактива.
Что наблюдаете? Составьте отчёт, заполнив таблицу; запишите уравнения проделанных реакций в молекулярном и ионном видах.
- В пробирку №4 налейте 1-2мл раствора хлорида алюминия. Добавьте 2-3 капли выбранного вами реактива для проведения реакции обмена; к полученному осадку (опишите его внешний вид, характер) добавляйте реактив до получения алюмината натрия.
Заполните таблицу; запишите уравнения проделанных реакций в молекулярном и ионном видах.
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт 1 …………… Опыт 2 |
1) 2) …………………………… 1) 2) |
Практическая работа №3
Решение экспериментальные задач на распознавание и получение веществ.
Цель: провести реакции, подтверждающие наличие в растворе данных ионов; решить задачи, на распознавание веществ, используя минимальное число реактивов. ). Повторите правила техники безопасности:
Вариант №II
Выполняем вариант№4стр. 86 и задание №1 стр.86 учебника.
- В пробирках №1, №2 и №3 находятся твёрдые вещества: хлорид натрия, хлорид алюминия и хлорид железа (III) . Определите, в какой пробирке находится каждое из веществ с помощью одного реактива:
а) растворите каждое из исследуемых веществ в 3-4 мл воды;
б) прилейте в пробирки №1, №2 и №3по 1-2 мл выбранного вами реактива. Что наблюдаете?
в) Опишите внешний вид выпавших осадков; докажите их характер, прилив необходимое количество выбранного вами для этой цели реактива.
Что наблюдаете? Составьте отчёт, заполнив таблицу; запишите уравнения проделанных реакций в молекулярном и ионном видах.
- В пробирке №4 выдан исследуемый образец железного купороса. Для того, чтобы определить, содержит ли он примесь сульфата железа (III):
а) растворите образец в 3-4 мл дистиллированной воды;
б) добавьте 1-2мл раствора выбранного вами реактива.
Заполните таблицу; запишите уравнения проделанной реакции в молекулярном и ионном видах.
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт 1 …………… Опыт 2 |
……………………. |
1) 2) 3) ……………………………………… 1) |
Практическая работа №2
Получение и свойства соединений металлов.
Цель: провести реакции, подтверждающие наличие в растворе данных ионов; получить заданные вещества несколькими способами. ). Повторите правила техники безопасности:
Вариант №I
- Задание №1стр. 84 учебника.
Получите гидроксид алюминия по реакции обмена согласно уравнению:
AlCl3 + 3NaОН = Al(OH)3 + 3NaCl.
Проверим, справедливо ли для химии математическое выражение «от перемены мест слагаемых сумма не изменяется».Для этого проведём данную реакцию двумя способами:
а) в пробирку №1 прилейте 1-2мл раствора хлорида алюминия; к раствору хлорида алюминия добавляйте по каплям раствор гидроксида натрия. Что наблюдаете?
б) в пробирку №2 прилейте 1-2мл раствора гидроксида натрия; к раствору гидроксида натрия прилейте 1-2мл раствора хлорида алюминия. Выпал ли осадок? Почему? Составьте ионные уравнения проведённой реакции, объясните результаты опыта. Оформите отчёт в таблицу.
2) Задание №4 стр. 85 учебника. Получите сульфат железа (II) тремя способами, исходя из предложенных реактивов: а) в пробирке №3 проведите реакцию замещения; б) в пробирках №4 и №5 получите сульфат железа (II) по реакциям обмена.
Составьте уравнения, выразите сущность (для реакций замещения составьте электронный баланс, для реакций обмена – ионные уравнения). Оформите отчёт в таблицу.
- По заданию №5 стр. 85 учебника (изменённое).
Проведите реакции, подтверждающие качественный состав хлорида железа (III): а) в пробирку №6 и №7 прилейте по 1-2 мл раствора хлорида железа (III); б) в пробирку №6 добавьте несколько капель раствора реактива на катион железа (III); в) в пробирку №7 добавьте несколько капель раствора реактива на хлорид-ион.
Составьте отчёт, заполнив таблицу; запишите уравнения проделанных реакций в молекулярном и ионном видах.
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт 1 …………… Опыт 2 …………….. Опыт 3 |
…………………….. ……………………………… |
1) …………………………… 1) 2) 3) ……………………………….. 1) 2) |
………….. …………… |
Практическая работа №5
Экспериментальные задачи по теме «Подгруппа азота и углерода».
Цель: провести реакции, подтверждающие наличие в растворе данных ионов; решить задачи, на распознавание веществ, используя минимальное число реактивов. ). Повторите правила техники безопасности:
Вариант №I
- Проведите реакции, подтверждающие, что данное вещество является сульфатом аммония.
Прилейте в пробирки №1 и №2 по 1-2 мл раствора сульфата аммония;
а) в пробирку №1 добавьте несколько капель раствора реактива на катион аммония;
б) в пробирку №2 прилейте несколько капель раствора реактива, выбранного вами для определения сульфат-ионов. Составьте молекулярные и ионные уравнения проделанных реакций; сделайте вывод о качественных реакциях на ионы; отчёт занесите в таблицу.
2) В пробирках №1, №2 и №3 находятся растворы веществ: силиката натрия, карбоната натрия и хлорида бария. Определите, в какой пробирке находится каждое из веществ с помощью одного реактива:
а) определите теоретически реактив;
б) прилейте по несколько капель раствора выбранного вами реактива в каждую пробирку. Что наблюдаете? Составьте молекулярные и ионные уравнения проделанных реакций. Отчёт оформите в таблицу.
3)Проведите реакции, которые соответствуют следующим сокращённым ионным уравнениям: Н + +ОН— = Н2О; 2 Н + + СО32- = СО2 + Н2О.
а) Составьте молекулярные уравнения соответствующих реакций (учитывайте наличие реактивов).
б) Проведите реакции, соответствующие составленным вами уравнениям (растворов веществ берите по1-2мл). Составьте отчёт, заполнив таблицу.
|
Ход работы |
Наблюдение, Рисунок |
Уравнения реакций |
Выводы |
|
Опыт 1 …………… Опыт 2 …………….. Опыт 3 |
…………………….. ……………………………… |
1) 2) …………………………… 1) 2) 3) ……………………………….. 1) 2) |
……….. …………… |
Инструкция 1 по выполнению опытов, подтверждающих общие свойства
карбоновых и минеральных кислот (на примере уксусной кислоты).
1.Карбоновые
кислоты, как и неорганические, изменяют цвет индикаторов.
(доказать!)
2.Взаимодействие
уксусной и соляной кислот с металлическим магнием.
В пробирку №1 с
металлическим магнием, прибавьте уксусную кислоту, а в пробирку №2 с
металлическим магнием прибавьте соляную кислоту (по вариантам) Что наблюдаете?
Напишите
уравнение реакции взаимодействия уксусной и соляной кислот с металлическим
магнием. Дайте характеристику данной реакции.
3.Взаимодействие
уксусной и соляной кислот с основным оксидом.
В пробирку №3 с
оксидом меди (II)
прибавьте уксусную кислоту, а в пробирку №4 с оксидом меди (II) прибавьте
соляную кислоту (по вариантам). Содержимое пробирок (осторожно!) нагрейте. Что
наблюдаете?
Напишите
уравнение реакции взаимодействия уксусной и соляной кислот с оксидом меди (II) в молекулярном
и ионном виде.
4.Взаимодействие
уксусной кислоты с солью более слабой кислоты.
I вариант.
В пробирку №5 с гидрокарбонатом
натрия прибавьте соляную кислоту. Что наблюдаете?
Напишите
уравнение реакции взаимодействия соляной кислоты с гидрокарбонатом натрия в
молекулярном и ионном виде.
II вариант.
В пробирку №6 с мрамором
прибавьте уксусную кислоту. Что наблюдаете?
Напишите
уравнение реакции взаимодействия уксусной кислоты с мрамором в молекулярном и
ионном виде.
5.Взаимодействие
соляной и уксусной кислот со щёлочью.
Налейте в
пробирки №7 и №8 (по вариантам) по 1 мл раствора гидроксида натрия,
прибавьте несколько капель фенолфталеина (до появления розового окрашивания), а
затем налейте немного соляной (пробирка №1) и уксусной (пробирка №2) кислот.
Напишите
уравнение реакции взаимодействия уксусной кислоты с гидроксидом натрия в
ионном и ионном сокращённом виде.
6.Взаимодействие
уксусной кислоты с нерастворимым гидроксидом.
Налейте в
пробирки №9 и №10 (по вариантам) по 1 мл раствора сульфата железа(II) и
прибавьте 1–2 мл раствора гидроксида натрия (отметьте, что наблюдаете), затем
налейте немного соляной (пробирка №9) и уксусной (пробирка №10) кислот.
Напишите
уравнение реакции взаимодействия уксусной кислоты гидроксидом железа(III) в
молекулярном виде.
Инструкция 2 по выполнению опытов, характерных для карбоновых
кислот (на примере уксусной кислоты).
1.Взаимодействие
уксусной кислоты с изоамиловым спиртом.
Налейте в пробирку
1 мл раствора изоамилового спирта, прибавьте столько же уксусной кислоты и 1
мл концентрированной серной кислоты (осторожно!). Содержимое пробирки перемешать и опустить пробирку в
стакан с горячей водой.
*Что ощущаете?
*Напишите
уравнение реакции взаимодействия уксусной кислоты с изоамиловым спиртом.
*Какую роль в этой
реакции выполняет концентрированная серная кислота?
2.Качественная
реакция на уксусную кислоту и её соли (ацетат-ион).
В пробирку
налейте 1 мл раствора ацетата натрия и прибавьте несколько капель раствора
хлорида железа (III).
*Что наблюдаете?
*Напишите
уравнение реакции взаимодействия ацетата натрия и уксусной кислоты с хлоридом
железа (III) в ионном
виде.
3CH3COONa + FeCl3→
(CH3 COO)3Fe + 3NaCl
ацетат железа
(III)
*
Демонстрирует учитель!
3.Горение уксусной
кислоты.
Наряду с аналогий между уксусной кислотой и минеральными кислотами, уксусная
кислота, как кислота органическая, обладает некоторыми особенностями, например
горючестью.
Наливают в
пробирку немного уксусной кислоты и нагревают. При 118°С кислота кипит. Продолжая
нагревание, поджигают пары лучинкой. Они горят слабо светящим пламенем.
Составьте
уравнение реакции горения и дайте объяснение слабой светимости пламени.
4. Яйцо в уксусной
кислоте.
5. Кристаллы
уксусной кислоты.
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ГОРОДСКОГО ОКРУГА БАЛАШИХА «СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА№32»
УТВЕРЖДАЮ
Директор МБОУ «Школа №32»
_____________ Т.Н. Умерникова
«____» ________________201__г.
СОГЛАСОВАНО
Председатель профсоюзного комитета
МБОУ Школа №32
_______________ ____________
«_____» ____________ 201__ г.
ИНСТРУКЦИЯ №24
При проведении демонстрационных опытов по химии
1. ОБЩИЕ ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
1.1. К проведению демонстрационных опытов по химии допускаются педагогические работники, прошедшие медицинский осмотр и инструктаж по охране труда. Учащиеся к подготовке и проведению демонстрационных опытов по химии не допускаются.
1.2. Опасные и вредные производственные факторы:
-
химические ожоги при работе с хим. реактивами без средств индивидуальной защиты;
-
термические ожоги при неаккуратном обращении со спиртовками при нагревании жидкостей;
-
порезы рук при небрежном обращении с лабораторной посудой;
-
отравления токсичными газами при проведении опытов и неисправном вытяжном шкафу.
1.3. При проведении демонстрационных опытов по химии используется специальная одежда: халат хлопчатобумажный, а также средства индивидуальной защиты: фартук прорезиненный, защитные очки, перчатки резиновые.
1.4. Перед проведением демонстрационных опытов по химии убедиться в наличии и исправности первичных средств пожаротушения: огнетушителей, ящика с песком, двух накидок из огнезащитной ткани.
1.5. При получении травмы оказать первую помощь пострадавшему, сообщить об этом администрации учреждения, при необходимости отправить пострадавшего в ближайшее лечебное учреждение.
1.6. После проведения демонстрационных опытов по химии тщательно вымыть руки с мылом.
2. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ ПЕРЕД НАЧАЛОМ РАБОТЫ
2.1. Надеть спецодежду, при работе со щелочными металлами, кальцием, кислотами и щелочами использовать средства индивидуальной защиты.
2.2. Подготовить к работе и проверить исправность оборудования, приборов, лабораторной посуды.
2.3. Перед проведением демонстрационных опытов, при которых возможно загрязнение атмосферы учебных помещений токсичными веществами, проверить исправную работу вентиляции вытяжного шкафа.
3. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ ВО ВРЕМЯ РАБОТЫ
3.1. Для оказания помощи в подготовке и проведении демонстрационных опытов по химии разрешается привлекать лаборанта, учащихся привлекать для этих целей запрещается.
3.2. Химические опыты, при которых возможно загрязнение атмосферы учебных помещений токсичными веществами, необходимо проводить в исправном вытяжном шкафу с включенной вентиляцией.
3.3. Приготавливать растворы из твердых щелочей и концентрированных кислот разрешается только учителю, используя фарфоровую лабораторную посуду, заполнив наполовину ее холодной водой, а затем добавлять небольшими дозами вещество.
3.4. При пользовании пипеткой запрещается засасывать жидкость ртом.
3.5. Взятие навески твердой щелочи разрешается пластмассовой или фарфоровой ложечкой. Запрещается использовать металлические ложечки и насыпать щелочи из склянок через край.
3.6. Тонкостенную лабораторную посуду следует укреплять в зажимах штативов осторожно, слегка поворачивая вокруг вертикальной оси или перемещая вверх-вниз.
3.7. Для нагревания жидкостей разрешается использовать только тонкостенные сосуды. Пробирки перед нагреванием запрещается наполнять жидкостью более чем на треть. Горлышко сосудов при их нагревании следует направлять в сторону от учащихся.
3.8. При нагревании жидкостей запрещается наклоняться над сосудами и заглядывать в них. При нагревании стеклянных пластинок необходимо сначала равномерно прогреть всю пластинку, а затем вести местный нагрев.
3.9. Демонстрировать взаимодействие щелочных металлов и кальция с водой необходимо в химических стаканах типа ВН-600, наполненных не более чем на 0,05 литра.
3.10. Растворы необходимо наливать из сосудов так, чтобы при наклоне этикетка оказывалась сверху. Каплю, оставшуюся на горлышке, снимать краем той посуды, куда наливается жидкость.
4. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ В АВАРИЙНЫХ СИТУАЦИЯХ
4.1. Разлитый водный раствор кислоты или щелочи засыпать сухим песком, совком переместить адсорбент от краев разлива к середине, собрать в полиэтиленовый мешочек и плотно завязать. Место разлива обработать нейтрализующим раствором, а затем промыть водой.
4.2. При разливе легковоспламеняющихся жидкостей или органических веществ объемом до 0,05 л. погасить открытый огонь спиртовки и проветрить помещение. Если разлито более 0,1 л. удалить учащихся из учебного помещения, погасить открытый огонь спиртовки и отключить систему электроснабжения помещения устройством извне комнаты. Разлитую жидкость засыпать сухим песком или опилками, влажный адсорбент собрать деревянным совком в закрывающуюся тару и проветрить помещение до полного исчезновения запаха.
4.3. При разливе легковоспламеняющихся жидкостей и их загорании, немедленно эвакуировать учащихся из помещения, сообщить о пожаре в ближайшую пожарную часть и приступить к тушению очага возгорания первичными средствами пожаротушения.
4.4. В случае, если разбилась лабораторная посуда, не собирать осколки незащищенными руками, а использовать для этой цели щетку и совок.
4.5. При получении травмы оказать первую помощь пострадавшему, сообщить об этом администрации учреждения, при: необходимости отправить пострадавшего в ближайшее лечебное учреждение.
5. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ ПО ОКОНЧАНИИ РАБОТЫ
5.1. Установки, приборы, в которых использовались или образовались вещества 1, 2 и 3 класса опасности, оставить в вытяжном шкафу с работающей вентиляцией до конца занятия, после окончания которого учитель лично производит демонтаж установки, прибора.
5.2. Отработанные водные растворы слить в закрывающийся стеклянный сосуд вместимостью не менее 3 л. для последующего их уничтожения.
5.3. Привести в порядок рабочее место, убрать все хим.реактивы в лаборантскую в закрывающиеся шкафы и сейфы.
5.4. Снять спецодежду, средства индивидуальной защиты и тщательно вымыть руки с мылом.
Заместитель директора по безопасности __________________В.И. Кирков
-
Азбука веры
-
Азбука воспитания
-
Душевное развитие ребенка
Статьи о православном воспитании детей
Пожертвовать
«Если с детьми не говорить о Боге, то всю оставшуюся жизнь придётся говорить с Богом о детях…»
Мария Плетнева
Домашние химические опыты для детей
- Опыт № 1 «Потому что — без воды и ни туды и ни сюды»
- Опыт № 2 «Что растворено в водопроводной воде»
- Опыт № 3 «Что растворено в минеральной воде или вода — универсальный растворитель»
- Опыт № 4 «Фильтрование воды, смешанной с песком»
- Опыт № 5 «Выращиваем кристаллы сахара»
- Опыт № 6 «Получение кристаллов йода»
- Опыт № 7 «Йод-индикатор содержания крахмала»
- Опыт № 8 «Окрашивание пламени или реакция соединения»
Мой личный опыт преподавания химии показал, что такую науку, как химию, очень тяжело изучать без каких-либо первоначальных сведений и практики. Школьники очень часто запускают этот предмет. Лично наблюдала, как ученик 8 класса при слове «химия» начинал морщиться, словно съел лимон.
Позже выяснилось, что из-за нелюбви и непонимания предмета, школу он прогуливал втайне от родителей. Конечно, школьная программа составлена таким образом, что учитель должен дать на первых уроках химии много теории. Практика как бы отходит на второй план именно в тот момент, когда школьник еще не может самостоятельно осознать, нужен ли это предмет ему в дальнейшем. В первую очередь это связано с лабораторным оснащением школ. В больших городах в настоящее время с реактивами и приборами дело обстоит лучше. Что касается провинции, то, как и 10 лет назад, так и в настоящее время, во многих школах нет возможности проводить лабораторные занятия. А ведь процесс изучения и увлечения химией, также как и другими естественными науками, обычно начинается с опытов. И это неслучайно. Многие знаменитые химики, такие как Ломоносов, Менделеев, Парацельс, Роберт Бойль, Пьер Кюри и Мария Склодовская-Кюри (всех этих исследователей школьники изучают также и на уроках физики) уже с детства начинали экспериментировать. Великие открытия этих великих людей были сделаны именно в домашних химических лабораториях, поскольку занятия химией в институтах было доступно только людям с достатком.
И, конечно, самое главное — это заинтересовать ребенка и донести ему, что химия окружает нас повсюду, поэтому процесс ее изучения может быть очень увлекательным. Здесь на помощь придут домашние химические опыты. Наблюдая такие эксперименты, можно в дальнейшем искать объяснение, почему происходит так, а не иначе. А, когда на школьных уроках юный исследователь столкнется с подобными понятиями, объяснения учителя ему будут более понятны, так как у него уже будет свой собственный опыт проведения домашних химических экспериментов и полученные знания.
Очень важно начинать изучение естественных наук с обычных наблюдений и примеров из жизни, которые, как вы считаете, будут наиболее удачными для вашего ребенка. Вот некоторые из них. Вода-это химическое вещество, состоящее из двух элементов, а также газов растворенных в ней. Человек тоже содержит воду. Известно, что там, где нет воды, нет и жизни. Без пищи человек может прожить около месяца, а без воды — всего лишь несколько суток.
Речной песок – это не что иное, как оксид кремния, а также основное сырье для производства стекла.
Человек сам того не подозревает и осуществляет химические реакции каждую секунду. Воздух, который мы вдыхаем, это смесь газов — химических веществ. В процессе выдыхания выделяется еще одно сложное вещество — диоксид углерода. Можно сказать, что мы сами это химическая лаборатория. Можно объяснить ребенку, что мытье рук мылом это тоже химический процесс воды с мылом.
Ребёнку постарше, который, например, уже начал изучать химию в школе можно объяснить, что в организме человека можно обнаружить практически все элементы периодической системы Д. И. Менделеева. В живом организме не только присутствуют все химические элементы, но каждый из них выполняет какую-то биологическую функцию.
Химия-это и лекарства, без которых в настоящее время многие люди не могут прожить и дня.
Растения тоже содержат химическое вещество хлорофилл, которое придает листочку зеленый цвет.
Приготовление пищи — это сложные химические процессы. Здесь можно привести пример того, как поднимается тесто при добавлении дрожжей.
Один из вариантов, как заинтересовать ребенка химией — это взять отдельного выдающегося исследователя и прочитать историю его жизни или посмотреть обучающий фильм про него (сейчас доступны такие фильмы про Д. И. Менделеева, Парацельса, М.В. Ломоносова, Бутлерова).
Многие полагают, что настоящая химия это вредные вещества, экспериментировать с ними опасно, тем более в домашних условиях. Есть много очень увлекательных опытов, которые вы сможете провести со своим ребёнком, не навредив здоровью. И эти домашние химические опыты будут не менее увлекательные и поучительные, чем те, которые идут с взрывами, едкими запахами и клубами дыма.
Некоторые родители опасаются также проводить дома химические опыты из-за их сложности или отсутствия необходимого оборудования и реактивов. Оказывается, что можно обойтись подручными средствами и теми веществами, которые есть у каждой хозяйки на кухне. Их можно купить в ближайшем бытовом магазине или аптеке. Пробирки для проведения домашних химических опытов можно заменить флакончиками от таблеток. Для хранения реактивов можно пользоваться стеклянными банками, например, от детского питания или майонеза.
Стоит помнить, что посуда с реактивами должна иметь этикетку с надписью и быть плотно закрыта. Иногда пробирки нужно нагреть. Чтобы не держать ее в руках при нагревании и не обжечься, можно соорудить такое устройство с помощью бельевой прищепки или куска проволоки.
Также необходимо выделить несколько стальных и деревянных ложечек для перемешивания.
Штатив для держания пробирок можно сделать самим, просверлив в бруске сквозные отверстия.
Для фильтрования полученных веществ вам понадобиться бумажный фильтр. Сделать его очень легко согласно приведенной здесь схеме.
Для детишек, которые еще не ходят в школу или обучаются в младших классах, постановка домашних химических опытов с родителями будет своеобразной игрой. Скорее всего, объяснить какие-то отдельные законы и реакции еще не удастся такому юному исследователю. Однако, возможно, именно такой эмпирический способ открытия окружающего мира, природы, человека, растения через опыты заложит фундамент для изучения естественных наук в дальнейшем. Можно даже устраивать своеобразные конкурсы в семье — у кого опыт получится более удачным и затем демонстрировать их на семейных праздниках.
Независимо от возраста ребенка и его способности читать и писать, советую завести лабораторный журнал, в который можно записывать эксперименты или зарисовывать. Настоящий химик обязательно записывает план работы, список реактивов, зарисовывает приборы и описывает ход работы.
Когда вы вместе с ребенком только начнете изучать эту науку о веществах и проводить домашние химические опыты, первое, что нужно помнить это безопасность.
Для этого нужно следовать следующим правилам безопасности:
1. Настоятельно рекомендую, чтобы все домашние химические опыты проводились только под присмотром взрослых.
2. Лучше выделить отдельный стол для проведения химических опытов в домашних условиях. Если у вас дома не найдется отдельного стола, то опыты лучше проводить на стальном или железном подносе или поддоне.
3. Необходимо обзавестись тонкими и толстыми перчатками (их продают в аптеке или в хозяйственно магазине).
4. Для проведения химических экспериментов лучше всего купить лабораторный халат, но также можно вместо халата использовать плотный фартук.
5. Лабораторная посуда не должна в дальнейшем использоваться для еды.
6. В домашних химических опытах не должно быть жестокого отношения с животными и нарушения экологической системы. Кислотные химические отходы нужно нейтрализовать содой, а щелочные — уксусной кислотой.
7. Если хочешь проверить запах газа, жидкости или реактива, никогда не подноси сосуд прямо к лицу, а, удерживая его на некотором расстоянии, направь, помахивая рукой, воздух над сосудом по направлению к себе и одновременно нюхай воздух.
8. Всегда используй в домашних опытах реактивы в небольшом количестве. Избегай оставлять реактивы в посуде без соответствующей надписи (этикетки) на склянке, из которой должно быть ясно, что находится в склянке.
Начинать изучение химии следует с простых химических экспериментов в домашних условиях, позволяющих ребенку освоить основные понятия. Серия опытов 1-3 позволяют ознакомиться с основными агрегатными состояниями веществ и свойствами воды. Для начала ребенку-дошкольнику вы можете показать, как растворяется в воде сахар и соль, сопроводив это объяснением, что вода универсальный растворитель и является жидкостью. Сахар или соль — твердые вещества, растворяющиеся в жидкости.
Опыт № 1 «Потому что — без воды и ни туды и ни сюды»
Вода-это жидкое химическое вещество, состоящее из двух элементов, а также газов, растворенных в ней. Человек тоже содержит воду. Известно, что там, где нет воды, нет и жизни. Без пищи человек может прожить около месяца, а без воды — всего лишь несколько суток.
Реактивы и оборудование: 2 пробирки, сода, лимонная кислота, вода
Эксперимент: Взять две пробирки. Насыпать в них в равных количествах соду и лимонную кислоту. Затем в одну из пробирок налить воды, а в другую нет. В пробирке, в которой вода была налита вода стал выделяться углекислый газ. В пробирке без воды — ничего не изменилось
Обсуждение: Данный эксперимент объясняет тот факт, что без воды невозможны многие реакции и процессы в живых организмах, а также вода ускоряет многие химические реакции. Школьникам можно объяснить, что произошла обменная реакция, в результате которой выделился углекислый газ.
Опыт № 2 «Что растворено в водопроводной воде»
Реактивы и оборудование: прозрачный стакан, водопроводная вода
Эксперимент: Налить в прозрачный стакан водопроводную воду и поставить ее в теплое место на час. Через час вы увидите на стенках стакана осевшие пузырьки.
Обсуждение: Пузырьки – это не что иное как газы, растворенные в воде. В холодной воде газы растворяются лучше. Как только вода становится теплой, газы перестают растворяться и оседают на стенки. Подобный домашний химический опыт позволяет также познакомить ребенка с газообразным состояние вещества.
Опыт № 3 «Что растворено в минеральной воде или вода — универсальный растворитель»
Реактивы и оборудование: пробирка, минеральная вода, свеча, лупа
Эксперимент: Налить в пробирку минеральную воду и медленно выпаривать ее над пламенем свечи (опыт можно делать на плите в кастрюле, но кристаллы будут хуже видны). По мере испарения воды на стенках пробирка останутся мелкие кристаллы, все они разной формы.
Обсуждение: Кристаллы – это соли, растворенные в минеральной воде. У них разная форма и размер, так как каждый кристаллик носит свою химическую формулу. С ребенком, который уже начал изучать химию в школе, можно почитать этикетку на минеральной воде, где указан ее состав и написать формулы соединений, содержащихся в минеральной воде.
Опыт № 4 «Фильтрование воды, смешанной с песком»
Реактивы и оборудование: 2 пробирки, воронка, бумажный фильтр, вода, речной песок
Эксперимент: Налить в пробирку воду и опустить туда немного речного песка, перемешать. Затем по схеме описанной выше сделать фильтр из бумаги. Вставить сухую чистую пробирку в штатив. Медленно выливать смесь песка с водой через воронку с бумажным фильтром. Речной песок останется на фильтре, а в штативной пробирке вы получите чистую воду.
Обсуждение: Химический опыт позволяет показать, что существуют вещества, не растворяющееся в воде, например, речной песок. Также опыт знакомит с одним из метод очистки смесей веществ от примесей. Здесь можно внести понятия чистые вещества и смеси, которые даются в учебнике химия 8 класса. В данном случае смесью является песок с водой, чистым веществом — фильтрат, речной песок – это осадок.
Процесс фильтрования (описывается в 8 классе) применяют здесь для разделения смеси воды с песком. Чтобы разнообразить изучение данного процесса, можно немного углубиться в историю очистки питьевой воды.
Процессы фильтрования применялись еще в 8-7 веках до н.э. в государстве Урарту (ныне это территории Армении) для очистки питьевой воды. Её жители осуществили постройку водопроводной системы с применением фильтров. В качестве фильтров использовали плотную ткань и древесный уголь. Подобные системы из переплетённых водосточных труб, глиняных каналов, снабженные фильтрами были и на территории древнего Нила у древних египтян, греков и римлян. Воду пропускали через такой фильтр нескскали через такой фильтр несколько раз, в конечном итоге доболько раз, в конечном итоге добиваясь наилучшего качества воды.
Одним из самых интересных опытов является выращивание кристаллов. Опыт очень нагляден и дает представление о многих химических и физических понятиях.
Опыт № 5 «Выращиваем кристаллы сахара»
Реактивы и оборудование: два стакана воды; сахар — пять стаканов; деревянные шпажки; тонкая бумага; кастрюля; прозрачные стаканчики; пищевой краситель (пропорции сахара и воды можно уменьшить).
Эксперимент: Опыт следует начинать с приготовления сахарного сиропа. Берем кастрюлю, выливаем в нее 2 стакана воды и 2,5 стакана сахара. Ставим на средний огонь и, помешивая, растворяем весь сахар. В получившийся сироп высыпаем оставшиеся 2,5 стакана сахара и варим до полного растворения.
Теперь приготовим зародыши кристаллов – палочки. Небольшое количество сахара рассыпаем на бумажке, затем обмакнем палочку в получившейся сироп, и обваляем ее в сахаре.
Берем бумажки и протыкаем шпажкой дырочку посередине таким образом, чтобы бумажка плотно прилегала к шпажке.
Затем разливаем горячий сироп по прозрачным стаканам (важно, чтобы стаканы были прозрачными — так процесс созревания кристаллов будет более увлекателен и нагляден). Сироп должен быть горячим, иначе кристаллы не будут расти.


Можно сделать цветные сахарные кристаллы. Для этого в получившейся горячий сироп добавляют немного пищевого красителя и размешивают его.
Кристаллы будут расти по-разному, некоторые быстро, а некоторым может понадобиться больше времени. По окончании опыта получившиеся леденцы ребенок может съесть, если у него нет аллергии на сладкое.
Если у вас нет деревянных шпажек, то опыт можно повести с обычными нитками.
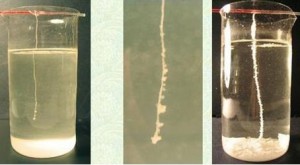
Обсуждение: Кристалл — это твердое состояние вещества. Он имеет определенную форму и определенное количество граней вследствие расположения своих атомов. Кристаллическими считаются вещества, атомы которых расположены регулярно, так что образуют правильную трёхмерную решётку, называемую кристаллической. Кристаллам ряда химических элементов и их соединений присущи замечательные механические, электрические, магнитные и оптические свойства. Например, алмаз – природный кристалл и самый твердый и редкий минерал. Благодаря своей исключительной твердости алмаз играет громадную роль в технике. Алмазными пилами распиливают камни. Существует три способа образования кристаллов: кристаллизация из расплава, из раствора и из газовой фазы. Примером кристаллизации из расплава может служить образование льда из воды (ведь вода – это расплавленный лёд). Пример кристаллизации из раствора в природе – выпадение сотен миллионов тонн соли из морской воды. В данном случае, при выращивании кристаллов в домашних условиях мы имеем дело с наиболее распространённым способам искусственного выращивания — кристаллизация из раствора. Кристаллы сахара растут из насыщенного раствора при медленном испарении растворителя – воды или при медленном понижении температуры.
Следующий опыт позволяет получить в домашних условиях один из самых полезных для человека кристаллических продуктов — кристаллический йод. Перед проведением опыта советую посмотреть вместе с ребенком небольшой фильм «Жизнь замечательных идей. Умный йод». Фильм дает представление о пользе йода и необычной истории его открытия, которая надолго запомниться юному исследователю. А интересна она тем, что первооткрывателем йода была обыкновенная кошка.
Французский ученый Бернар Куртуа в годы наполеоновских войн заметил, что в продуктах, получаемых из золы морских водорослей, которые выбрасывались на берег Франции, находится какое-то вещество, которое разъедает железные и медные сосуды. Но ни сам Куртуа, ни его помощники не знали, как выделить это вещество из золы водорослей. Ускорению открытия помог случай.
На своем небольшом заводе по производству селитры в г. Дижоне Куртуа собирался провести несколько опытов. На столе стояли сосуды, в одном из которых была настойка морских водорослей на спирту, а в другом — смесь серной кислоты с железом. На плечах у ученого сидела его любимая кошка.
В дверь постучали, и напуганная кошка спрыгнула и убежала, хвостом смахнув колбы на столе. Сосуды разбились, содержимое смешалось, и внезапно началась бурная химическая реакция. Когда небольшое облачко из паров и газов осело, удивленный ученый увидел на предметах и обломках какой-то кристаллический налет. Куртуа начал его исследовать. Кристаллы никому до этого неизвестного вещества получили название «йод».
Так был открыт новый элемент, а домашняя кошка Бернара Куртуа вошла в историю.
Опыт № 6 «Получение кристаллов йода»
Реактивы и оборудование: настойкой аптечного йода, вода, стакан или цилиндр, салфетка.
Эксперимент: Смешиваем воду с настойкой йода в пропорции:10мл йода и 10мл воды. И ставим всё в холодильник на 3 часа. В процессе охлаждения йод выпадет в осадок на дне стакана. Сливаем жидкость, вынимаем осадок йода и кладем на салфетку. Выжимаем салфетками до тех пор, пока йод не станет рассыпаться.
Обсуждение: Данный химический эксперимент называется экстрагированием или извлечением одного компонента из другого. В данном случае вода экстрагирует йод из раствора спиртовки. Таким образом, юный исследователь повторит опыт кота Куртуа без дыма и биения посуды.
О пользе йода для дезинфекции ран ваш ребенок уже узнает из фильма. Таким образом, вы покажите, что между химией и медициной есть неразрывная связь. Однако, оказывается, что йод можно применять в качестве индикатора или анализатора содержания другого полезного вещества – крахмала. Следующий опыт познакомит юного экспериментатора с отдельной очень полезной химией – аналитической.
Опыт № 7 «Йод-индикатор содержания крахмала»
Реактивы и оборудование: свежая картошка, кусочки банана, яблока, хлеба, стакан с разведенным крахмалом, стакан с разведённым йодом, пипетка.
Эксперимент: Разрезаем картофель на две части и капаем на него разведенный йод – картошка синеет. Затем капаем несколько капель йода в стакан с разведенным крахмалом. Жидкость тоже синеет.
Капаем с помощью пипетки растворенный в воде йод на яблоко, банан, хлеб, по очереди.
Наблюдаем:
Яблоко — не посинело вообще. Банан – слегка посинел. Хлеб – посинел очень сильно. Эта часть опыта показывает наличие крахмала в различных продуктах.
Обсуждение: Крахмал, вступая в реакцию с йодом, дает синюю окраску. Это свойство дает нам возможность выявить наличие крахмала в различных продуктах. Таким образом, йод является как бы индикатором или анализатором содержания крахмала.
Как известно, крахмал может преобразовываться в сахар, если взять неспелое яблоко и капнуть йода, то оно посинеет, так как яблоко еще не созрело. Как только яблоко созреет весь содержащийся крахмал перейдет в сахар и яблоко при обработке йодом не синеет вообще.
Следующий опыт будет полезен ребятам, которые уже начали изучение химии в школе. Оно знакомит с такими понятиями, как химическая реакция, реакция соединения и качественная реакция.
Опыт № 8 «Окрашивание пламени или реакция соединения»
Реактивы и оборудование: пинцет, поваренная пищевая соль, спиртовка
Эксперимент: Возьмем пинцетом несколько кристалликов крупной поваренной соли поваренной соли. Подержим их над пламенем горелки. Пламя окрасится в желтый цвет.
Обсуждение: Данный эксперимент позволяет провести химическую реакцию горения, которая является примером реакции соединения. Благодаря наличию натрия в составе поваренной соли, при горении происходит его реакция с кислородом. В результате образуется новое вещество – оксид натрия. Появление желтого пламени свидетельствует о том, что реакция прошла. Подобные реакции является качественными реакциями на соединения, содержащие натрий, то есть по ней можно определить содержится натрий в веществе или нет.
4Na+O2=2Na2O
Автор: Плетнева Мария, кандидат химических наук
Ещё статьи о воспитании
- «Вверх»: меняться никогда не поздно Валентина Киденко
- 12 способов воспитать ребенка счастливым
- Без перевода: десять русских слов, которые не объяснить иностранцам
- Вопросы под подушкой. 80 вопросов ребенку перед сном
- Дети-тюфяки и дети-катастрофы – пятнадцать лет спустя Мурашова Е.В.
Входим…
Куки не обнаружены, не ЛК
|
Согласовано Председатель профкома МКОУ СОШ с.Сикачи-Алян П.Т.Донкан _______ ______ «__»_______2014г. |
Утверждено Решением педсовета Протокол №__ от «__»________2014 Директор МКОУ СОШ с.Сикачи-Алян Л.П.Оненко__________ |
Инструкция
по технике безопасности для обучающихся при проведении химических опытов
МКОУ СОШ с.Сикачи-Алян
Хабаровского муниципального района
1. Общие требования безопасности
1. Данная инструкция обязательна для выполнения всеми учащимися, допущенными к химическим опытам.
2. Опасность возникновения травм:
· при работе со спиртовками;
· при работе с горючими жидкостями;
· при работе со стеклянной посудой;
· при использовании электроплитки;
· при работе с растворами кислот и щёлочами.
3. Химические опыты с токсичными веществами (хлор, сероводород, фосфид, оксид углерода, бром, бензол, дихлорэтан, диэтиловый эфир, формалин, уксусная кислота,аммиак ) проводить только в исправном вытяжном шкафу.
4. В кабинете химии должна быть аптечка, укомплектованная необходимыми медикаментами и перевязочными средствами для оказания первой помощи пострадавшим.
2. Требования безопасности перед началом занятий
1. Не трогать приготовленные к работе материалы и оборудование.
2. Внимательно выслушать инструктаж по ТБ при проведении опытов.
3. Получить учебное задание у учителя.
4. Одеть рабочую одежду по указанию учителя.
3. Требования безопасности во время занятий
1. Выполнять все действия только по указанию учителя.
2. Не зажигайте спиртовку одну от другой. Гасить её только колпачком.
3. Выполнять только опыты, определённые учебным заданием.
4. Не делать резких движений, не трогать посторонних предметов.
5. Соблюдать порядок и дисциплину
6. Пользуйтесь электроплиткой только с закрытой нагревательной спиралью.
7. Перед выполнением каждого опыта, выслушайте инструктаж учителя.
8. При нагревании жидкостей не направляйте отверстие пробирки на себя или соседа.
9. Пробирки закрепляйте надёжно в штативных держателях.
10. Кипячение горючих жидкостей выполняйте только на водной бане.
11. Пробирки нужно брать легко, не сжимая их пальцами.
12. Порошковые химикалии брать только пластмассовой ложечкой.
13. Кислотные растворы и щёлочи наливать только в стеклянную посуду.
14. Растворы кислот вливать в воду, но не наоборот.
15. Не пробовать на вкус никакие жидкости и твердые химвещества.
4. Требования безопасности в аварийных ситуациях
1. При плохом самочувствии сообщить об этом учителю .
2. Разбитое стекло убирать только щёткой и совком.
3. При получении травмы немедленно сообщить о случившемся учителю.
4. Разлитые и рассыпанные химикалии не убирать самостоятельно.
5. Требования безопасности по окончании занятий
1. Приведите в порядок своё рабочее место, проверьте его безопасность.
2. Снимите рабочую одежду.
3. Не выносите из кабинета ничего без указания учителя.
4. Вымойте лицо и руки с мылом.
5. О всех недостатках, обнаруженных во время опытов, сообщите учителю.
Учитель химии _____________/______________/
С инструкцией ознакомлен(а):
