- 📜Описание препарата Цинесет
- 💊Состав препарата Цинесет
- ✅Показания препарата Цинесет
- 📅Условия хранения препарата Цинесет
- ⏳Срок годности препарата Цинесет
Код ATX:
Гормоны для системного применения (исключая половые гормоны и инсулины) (H) > Препараты, регулирующие обмен кальция (H05) > Антипаратиреоидные гормоны (H05B) > Прочие антипаратиреоидные препараты (H05BX) > Cinacalcet (H05BX01)
Форма выпуска, состав и упаковка
таб., покр. плен. обол., 30 мг: 14 шт.
Рег. №: 10801/20 от 03.04.2020 — Действующее
Таблетки, покрытые пленочной оболочкой зеленые овальные, с гравировкой «30» на одной стороне.
| 1 таб. | |
| цинакальцет | 30 мг |
| (в виде цинакальцета гидрохлорида ) |
Вспомогательные вещества: крахмал прежелатинизированный, целлюлоза микрокристаллическая рН 102, гидроксипропилцеллюлоза -LH-11, кросповидон, кремния диоксид коллоидный, магния стеарат.
Состав материала пленочной оболочки №65 (Opadry II зеленый 32F210000): гидроксипропилметилцеллюлоза 2910, лактозы моногидрат, титана диоксид, макрогол, Индигокармин алюминиевый лак, Тартразин (Е102) алюминиевый лак, закатный желтый (Е110) FCF алюминиевый лак;
Состав материала пленочной оболочки №66 (Opadry прозрачный 03F190003): гидроксипропилметилцеллюлоза 2910, макрогол.
14 шт. — блистеры из ПВХ/ПЭ/ПВДХ/алюминия (2) — пачки картонные.
таб., покр. плен. обол., 60 мг: 14 шт.
Рег. №: 10801/20 от 03.04.2020 — Действующее
Таблетки, покрытые пленочной оболочкой зеленые овальные, с гравировкой «60» на одной стороне.
| 1 таб. | |
| цинакальцет | 60 мг |
| (в виде цинакальцета гидрохлорида ) |
Вспомогательные вещества: крахмал прежелатинизированный, целлюлоза микрокристаллическая рН 102, гидроксипропилцеллюлоза -LH-11, кросповидон, кремния диоксид коллоидный, магния стеарат.
Состав материала пленочной оболочки №65 (Opadry II зеленый 32F210000): гидроксипропилметилцеллюлоза 2910, лактозы моногидрат, титана диоксид, макрогол, Индигокармин алюминиевый лак, Тартразин (Е102) алюминиевый лак, закатный желтый (Е110) FCF алюминиевый лак;
Состав материала пленочной оболочки №66 (Opadry прозрачный 03F190003): гидроксипропилметилцеллюлоза 2910, макрогол.
14 шт. — блистеры из ПВХ/ПЭ/ПВДХ/алюминия (2) — пачки картонные.
Описание активных компонентов препарата ЦИНЕСЕТ . Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата. Дата обновления: 15.05.2013 г.
Фармакологическое действие
Антипаратиреоидное средство. Кальцийчувствительные рецепторы, находящиеся на поверхности главных клеток паращитовидных желез, являются основными регуляторами секреции паратиреоидного гормона (ПТГ). Цинакальцет обладает кальциймиметическим действием, непосредственно снижающим уровень ПТГ, повышая чувствительность данного рецептора к внеклеточному кальцию. Снижение ПТГ сопровождается снижением содержания кальция в сыворотке крови.
Снижение уровня ПТГ коррелирует с концентрацией цинакальцета. Вскоре после приема цинакальцета уровень ПТГ начинает понижаться: при этом максимальное снижение происходит примерно через 2-6 ч после приема разовой дозы, что соответствует Cmax цинакальцета. После этого концентрация цинакальцета начинает снижаться, а концентрация ПТГ увеличивается в течение 12 ч после приема дозы, и затем супрессия ПТГ остается примерно на одном и том же уровне до конца суточного интервала при режиме дозирования 1 раз/сут.
После достижения равновесного состояния концентрация кальция в сыворотке остается на постоянном уровне в течение всего интервала между приемами цинакальцета.
У больных с вторичным гиперпаратиреозом, принимающих цинакальцет, отмечалось значительное снижение уровня интактного ПТГ (иПТГ), Ca × P (кальций-фосфорное произведение), содержания кальция и фосфора в сыворотке. Снижение концентрации иПТГ и Ca × P поддерживалось на протяжении 12 месяцев терапии. Цинакальцет снижал уровни иПТГ, Ca × P, кальция и фосфора независимо от начальных уровней иПТГ или Ca × P, режима диализа (перитонеальный диализ по сравнению с гемодиализом), продолжительности диализа, и от того, применялся или нет витамин D.
Снижение уровней ПТГ ассоциировалось с незначимым снижением уровней маркеров костного метаболизма (специфической костной ЩФ, N-телопептидов, обновления костной ткани и костного фиброза).
В клинических исследованиях у пациентов с карциномой паращитовидных желез и первичным гиперпаратиреозим цинакальцет в дозах от 30 мг 2 раза/сут до 90 мг 4 раза/сут вызывал снижение концентрации кальция в сыворотке крови на ≥1 мг/дл (≥ 0.25 ммоль/л).
Фармакокинетика
После приема внутрь Cmax цинакальцета в плазме крови достигается примерно через 2-6 ч. Абсолютная биодоступность при приеме натощак, установленная на основании сравнения результатов различных исследований, составляла примерно 20-25%.
Увеличение AUC и Cmax цинакальцета происходит практически линейно в диапазоне доз 30-180 мг 1 раз/сут. При дозах более 200 мг наблюдается насыщение абсорбции, вероятно вследствие плохой растворимости. Фармакокинетические параметры цинакальцета не изменяются со временем.
Css цинакальцета достигается в течение 7 дней с минимальной кумуляцией. Отмечается большой Vd приблизительно 1000 л, что указывает на широкое распределение. Связывание с белками плазмы составляет около 97%, распределяется на минимальном уровне в эритроцитах.
Цинакальцет метаболизируется преимущественно при участии изоферментов CYP3A4 и CYP1A2 (роль CYP1A2 не была подтверждена клиническими методами). Основные метаболиты, обнаруженные в крови, неактивны. Согласно данным исследований in vitro, цинакальцет является мощным ингибитором CYP2D6. Однако при концентрациях, достигавшихся в клинических условиях, цинакальцет не подавляет активности других изоферментов (в т.ч. CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP3A4) и также не является индуктором CYP1A2, CYP2C19 и CYP3A4. После введения здоровым добровольцам 75 мг меченой радиоизотопным методом дозы, цинакальцет подвергался быстрому и значительному окислительному метаболизму с последующей конъюгацией.
Снижение концентрации цинакальцета происходит в 2 этапа: начальный T1/2 составляет примерно 6 ч, конечный T1/2 — 30-40 ч.
Метаболиты в основном выводятся почками: примерно 80% дозы обнаруживалось в моче и 15% в кале.
По сравнению с группой с нормальной функцией печени средние показатели AUC цинакальцета были примерно в 2 раза выше в группе с умеренными нарушениями функции печени, и примерно в 4 раза выше при тяжелой печеночной недостаточности. Средний T1/2 цинакальцета у пациентов с умеренной и тяжелой печеночной недостаточностью увеличивается соответственно на 33% и 70%.
Клиренс цинакальцета может быть ниже у женщин, чем у мужчин.
Клиренс цинакальцета выше у курящих, чем у некурящих. По-видимому, это обусловлено индукцией метаболизма, опосредованного CYP1A2. Если пациент прекращает или начинает курить во время терапии, концентрация цинакальцета в плазме может измениться и потребуется коррекция дозы.
Показания к применению
Вторичный гиперпаратиреоз у пациентов с терминальной стадией почечной недостаточности, находящихся на диализе; гиперкальциемия у пациентов (с целью снижения выраженности), вызванная следующими заболеваниями: карцинома паращитовидных желез и первичный гиперпаратиреоз, если, несмотря на сывороточные концентрации кальция, паратиреоидэктомия клинически неприемлема или противопоказана.
Реклама
Режим дозирования
Для приема внутрь. Рекомендуемая начальная доза составляет 30 мг 1 раз/сут. Затем доза повышается титрованием под контролем содержания ПТГ и кальция в крови. Максимальная доза, в зависимости от показаний и эффективности лечения и может составлять 180-360 мг/сут.
Побочные действия
Со стороны пищеварительной системы: очень часто — тошнота, рвота; часто — анорексия; иногда — диспепсия, диарея.
Со стороны нервной системы: часто — головокружение, парестезии; иногда — судороги.
Со стороны костно-мышечной системы: часто — миалгия.
Со стороны эндокринной системы: часто — снижение уровня тестостерона.
Дерматологические реакции: часто — сыпь.
Аллергические реакции: иногда — реакции гиперчувствительности.
Со стороны сердечно-сосудистой системы: у пациентов с сердечной недостаточностью регистрировались отдельные идиосинкразические случаи снижения АД и/или ухудшения течения сердечной недостаточности.
Прочие: часто — астения, гипокальциемия.
Применение при беременности и кормлении грудью
Клинические данные о применении цинакальцета при беременности отсутствуют. Применение при беременности возможно только в том случае, когда предполагаемая польза для матери превосходит потенциальный риск для плода.
До настоящего времени не изучена возможность выделения цинакальцета с грудным молоком у человека. При необходимости применения препарата в период лактации следует решить вопрос о прекращении грудного вскармливания.
В экспериментальных исследованиях при доклиническом изучении цинакальцета у кроликов показано, что цинакальцет проникает через плацентарный барьер. Не было выявлено прямого отрицательного воздействия на ход беременности, родов или постнатальное развитие. Не было также выявлено ни эмбриотоксического, ни тератогенного действия в ходе экспериментов на беременных самках крыс и кроликов, за исключением снижения массы тела зародышей у крыс при использовании доз, вызывавших токсичность у беременных самок. Цинакальцет выделяется с грудным молоком у лактирующих крыс, при этом отмечается высокое соотношение концентраций в молоке/плазме.
Особые указания
Цинакальцет не следует применять при концентрации кальция в сыворотке крови (с поправкой на альбумин) ниже минимального предела нормального диапазона. Поскольку цинакальцет понижает концентрацию кальция в сыворотке крови, необходимо проводить тщательный мониторинг пациентов в отношении развития гипокальциемии.
В случае гипокальциемии, для повышения уровня кальция в сыворотке крови, можно использовать кальцийсодержащие фосфатсвязывающие препараты, витамин D и/или провести коррекцию концентрации кальция в растворе при диализе. При устойчивой гипокальциемии следует снизить дозу или прекратить применение цинакальцета. Потенциальными признаками развития гипокальциемии могут быть парестезии, миалгии, судороги, тетания.
Цинакальцет не показан пациентам с хронической болезнью почек, не находящимся на диализе, в связи с возрастанием риска развития гипокальциемии (концентрация сывороточного кальция <8.4 мг/дл или <2.1 ммоль/л) по сравнению с пациентами, находящимися на диализе, что может быть обусловлено более низким начальным уровнем кальция и/или наличием остаточной функции почек.
С осторожностью и под тщательным контролем функции печени следует применять цинакальцет у пациентов с печеночной недостаточностью средней и тяжелой степени (по шкале Чайлд-Пью), т.к. в таких случаях концентрация цинакальцета в плазме крови может быть в 2-4 раза выше.
При хроническом подавлении концентрации ПТГ ниже концентрации, составляющей приблизительно 1.5% от ВГН по результатам анализа иПТГ, может развиться адинамическая болезнь кости. Если концентрация ПТГ снижается ниже рекомендуемого диапазона, следует уменьшить дозу цинакальцета и/или витамина D, или прекратить терапию.
Влияние на способность к вождению автотранспорта и управлению механизмами
Некоторые побочные реакции цинакальцета могут влиять на способность к управлению автотранспортом или работе с механизмами.
Лекарственное взаимодействие
Цинакальцет частично метаболизируется изоферментом CYP3A4. Одновременный прием кетоконазола (сильный ингибитор CYP3A4) в дозе 200 мг 2 раза/сут приводил к повышению концентрации цинакальцета в плазме примерно в 2 раза. При необходимости одновременного приема мощных ингибиторов (например, кетоконазол, итраконазол, телитромицин, вориконазол, ритонавир) или индукторов CYP3A4 (например, рифампицин), может потребоваться коррекция дозы цинакальцета.
В экспериментальных исследованиях in vitro показано, что цинакальцет частично метаболизируется при участии изофермента CYP1A2. Курение стимулирует активность CYP1A2. Клиренс цинакальцета на 36-38% выше у курящих, чем у некурящих. Влияние ингибиторов CYP1A2 (флувоксамина, ципрофлоксацина) на концентрацию цинакальцета в плазме не изучался. Может потребоваться коррекция дозы, если во время терапии препаратом пациент начинает/прекращает курение или начинает/прекращает одновременный прием мощных ингибиторов CYP1A2.
Цинакальцет является мощным ингибитором CYP2D6. Сочетанное применение цинакальцета и препаратов с узким терапевтическим диапазоном и/или вариабельной фармакокинетикой, метаболизирующихся изоферментом CYP2D6 (например, флекаинид, пропафенон, метопролол, дезипрамин, нортриптилин, кломипрамин), может потребовать коррекции дозы этих препаратов.
При одновременном приеме цинакальцета в дозе 90 мг 1 раз/сут с дезипрамином (трициклический антидепрессант, метаболизирующийся CYP2D6) в дозе 50 мг повышается уровень экспозиции дезипрамина в 3.6 раза у пациентов с активным метаболизмом CYP2D6.
Реклама
Все аналоги
Аналоги препарата
ЦИНАКАЛЬЦЕТ
(ФАРМЛЭНД, СП ООО, Республика Беларусь)
Аналоги КФУ
ПАРСАБИВТМ
(AMGEN EUROPE B.V., Нидерланды)
ЦИНАКАЛЬЦЕТ
(ФАРМЛЭНД, СП ООО, Республика Беларусь)
Другие препараты этого производителя
ВЕЗИФИКС
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
ВИЛАДОН
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
ТЕРФАЛИН
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
СЕФПОТЕК
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
КЛОВИКС
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
МАСИПАХ
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
ПИРФЕКТ
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
ПРЕФИКС
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
МЕЛБЕК®
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
ЭТОДИН ФОРТ
(NOBEL ILAC SANAYII VE TICARET, A.S., Турция)
Реклама
Цинесет: инструкция по применению

Форма выпуска: Таблетки
Цены в аптеках: Минск
109,76 — 116,60 р.
Содержание
- Описание
- Состав
- Фармакотерапевтическая группа
- Показания к применению
- Способ применения и дозы
- Противопоказания
- Меры предосторожности
- Лекарственные взаимодействия
- Период беременности и лактации
- Влияние на способность управлять транспортными средствами и другими механизмами
- Побочное действие
- Передозировка
- Условия хранения
- Срок годности
- Условия отпуска из аптек
- Упаковка
Описание
зеленые овальные таблетки, покрытые пленочной оболочкой, с гравировкой «30» на одной стороне.
Таблетки, покрытые пленочной оболочкой, 60 мг:
зеленые овальные таблетки, покрытые пленочной оболочкой, с гравировкой «60» на одной стороне.
Состав
содержит:
активное вещество: цинакальцет 30 мг (в виде цинакальцета гидрохлорида);
вспомогательные вещества: крахмал прежелатинизированный, микрокристаллическая целюллоза pH 102, L-гидроксипропилцелюллоза-LH 11, кросповидон, кремния диоксид коллоидный, магния стеарат;
Состав материала пленочной оболочки №65 (Опадрай II зеленый 32F210000): гидроксипропилметилцелюллоза 2910, лактозы моногидрат, титана диоксид, макрогол, Индигокармин алюминиевый лак, Тартразин (Е102) алюминиевый лак, Закатный желтый (Е110) FCF алюминиевый лак;
Состав материала пленочной оболочки №66 (Опадрай прозрачный 03F190003): гидроксипропилметилцелюллоза 2910, макрогол.
1 таблетка, покрытая пленочной оболочкой, 60 мг
содержит:
активное вещество: цинакальцет 60 мг (в виде цинакальцета гидрохлорида);
вспомогательные вещества: крахмал прежелатинизированный, микрокристаллическая целюллоза pH 102, L-гидроксипропилцелюллоза-LН 11, кросповидон, кремния диоксид коллоидный, магния стеарат;
Состав материала пленочной оболочки №65 (Опадрай II зеленый 32F210000): гидроксипропилметилцелюллоза 2910, лактозы моногидрат, титана диоксид, макрогол, Индигокармин алюминиевый лак, Тартразин (Е102) алюминиевый лак, Закатный желтый (Е110) FCF алюминиевый лак;
Состав материала пленочной оболочки №66 (Опадрай прозрачный Q3F190003): гидроксипропилметилцелюллоза 2910, макрогол.
Фармакотерапевтическая группа
Гормоны для лечения заболеваний паращитовидной железы. Антипаратиреоидные гормоны. Прочие антипаратиреоидные препараты.
Код АТХ: Н05ВХ01.
Показания к применению
Вторичный гиперпаратиреоз
Взрослые
Лечение вторичного гиперпаратиреоза (ГПТ) у пациентов с терминальной стадией болезни почек (ТСХПН), находящихся на поддерживающем гемодиализе.
Педиатрические пациенты
Лечение вторичного гиперпаратиреоза (ГПТ) у детей от 3 лет и старше с терминальной стадией болезни почек (ТСХПН), находящихся на поддерживающем гемодиализе, у которых вторичный ГПТ не адекватно контролируется при помощи стандартной поддерживающей терапии (см. Раздел «Меры предосторожности»). Цинакальцет можно назначать в составе комбинированной терапии, включающей препараты, связывающие фосфаты и / или витамин D в зависимости от обстоятельств.
Карцинома паращитовидных желез и первичный гиперпаратиреоз у взрослых
Снижение гиперкальциемии у пациентов с:
• карциномой паращитовидных желез;
• первичным ГПТ, для которого показана паратиреоидэктомия на основании уровня кальция в сыворотке крови (в соответствии с признанными схемами лечения), но по состоянию пациента паратиреоидэктомия клинически нецелесообразна или противопоказана.
Способ применения и дозы
Таблетки следует принимать целиком, не измельчать, не разжевывать и не делить.
Вторичный гиперпаратиреоз
Взрослые и пожилые (> 65 лет)
Рекомендуемая начальная доза препарата Цинесет для взрослых составляет 30 мг один раз в день. Коррекцию дозы Цинесет следует проводить каждые 2-4 недели до максимальной дозы 180 мг (один раз в сутки), при которой у пациентов на диализе достигается целевая концентрация ПТГ в диапазоне 150-300 пг/мл (15.9-31.8 пмоль/л), определяемая по концентрации интактного ПТГ (иПТГ).
Определение концентраций ПТГ должно проводиться не раньше, чем через 12 часов после приема препарата Цинесет. При оценке концентрации ПТГ следует придерживаться современных рекомендаций. Определение концентрации ПТГ следует проводить через 1-4 недели после начала терапии или коррекции дозы препарата Цинесет. При приеме поддерживающей дозы, мониторинг концентрации ПТГ должен проводиться примерно раз в 1-3 месяца. Для определения концентрации ПТГ можно использовать содержание иПТГ или биоинтактного ПТГ (биПТГ); терапия препаратом Цинесет не меняет соотношения между иПТГ и биПТГ.
Коррекция дозы в зависимости от уровня кальция в крови
Уровень кальция в сыворотке крови с поправкой на содержание альбумина (далее – «уровень кальция») следует измерять и контролировать, он должен находиться на уровне или ниже нижнего предела нормального диапазона до введения первой дозы Цинесета (см. Раздел «Меры предосторожности»). Нормальный диапазон кальция может отличаться в зависимости от методов, используемых местной лабораторией.
Измерение уровня кальция в сыворотке крови следует проводить в течение 1 недели после начала применения препарата Цинесет или изменения дозы. После определения поддерживающей дозы измерение уровня кальция в сыворотке крови следует производить приблизительно каждые 4 недели. В случае клинически значимого снижения концентрации альбумин-корригированного кальция в сыворотке крови ниже 8,4 мг/дл (2,1ммоль/л) и/или появления симптомов гипокальциемии, рекомендуется следующая тактика ведения:
| Уровень кальция в сыворотке крови или клинические симптомы гипокальциемии | Рекомендации |
| <8,4 мг/дл (2,1 ммоль/л) и >7,5 мг/дл (1,9 ммоль/л) или при наличии клинических симптомов гипокальциемии | Кальцийсодержащие фосфатные соединения, стеролы витамина D и/или коррекция уровня кальция в диализной жидкости могут использоваться для повышения уровня кальция в сыворотке крови в соответствии с клинической оценкой. |
| <8,4 мг/дл (2,1 ммоль/л) и >7,5 мг/дл (1,9 ммоль/л) или стойкие симптомы гипокальциемии, несмотря на попытки повысить уровень кальция в сыворотке крови | Уменьшить дозу или прекратить применение цинакальцета. |
| <7,5 мг/дл (1,9 ммоль/л) или стойкие симптомы гипокальциемии и невозможность повысить уровень витамина D | Прекратить прием цинакальцета, пока уровень кальция в сыворотке крови не достигнет уровня 8,0 мг/дл (2,0 ммоль/л) и/или не исчезнут симптомы гипокальциемии. Терапию следует восстановить, используя следующую самую низкую дозу цинакальцета. |
Педиатрические пациенты
Уровень кальция в сыворотке крови должен находиться в верхнем диапазоне или выше соответствующего возрасту контрольного интервала до введения первой дозы Цинесета, и должен тщательно контролироваться (см. Раздел «Меры предосторожности»). Нормальный диапазон кальция варьируется в зависимости от методов, используемых местной лабораторией, и возраста ребенка / пациента.
Рекомендуемая начальная доза для детей в возрасте от 3 лет до <18 лет составляет ≤ 0,20 мг / кг один раз в день в пересчете на сухой вес пациента (см. Таблицу 1).
Дозу можно увеличить, чтобы достичь желаемого целевого диапазона иПТГ. Дозу следует увеличивать последовательно через доступные уровни дозировки (см. Таблицу 1) не чаще, чем каждые 4 недели. Дозу можно увеличить до максимальной дозы 2,5 мг/кг/день, не превышая общую суточную дозу 180 мг.
Таблица 1. Ежедневная доза Цинесета для педиатрических пациентов
| Сухой вес пациента (кг) | Начальная доза (мг) | Доступные последовательные уровни дозирования (мг) |
| от 10 до <12.5 | 1 | 1, 2.5, 5, 7.5, 10, и 15 |
| от ≥ 12.5 до <25 | 2,5 | 2.5, 5, 7.5, 10, 15, и 30 |
| от ≥ 25 до <36 | 5 | 5, 10, 15, 30, и 60 |
| от ≥ 36 до <50 | 5, 10, 15, 30, 60, и 90 | |
| от ≥ 50 до <75 | 10 | 10, 15, 30, 60, 90, и 120 |
| ≥ 75 | 15 | 15, 30, 60, 90, 120, и 180 |
Коррекция дозы, основанная на уровнях ПТГ
Уровни ПТГ следует оценивать по меньшей мере через 12 часов после дозирования с помощью Цинесета, а иПТГ следует измерять от 1 до 4 недель после начала или коррекции дозы Цинесета.
Дозу следует откорректировать в зависимости иПТГ, как показано ниже:
• Если иПТГ составляет < 150 пг/мл (15,9 пмоль/л) и > 100 пг/мл (10,6 пмоль/л), уменьшите дозу Цинесета до следующей более низкой дозы.
• Если иПТГ < 100 пг/мл (10,6 пмоль/л) прекратите лечение Цинесетом, начните заново прием Цинесета при следующей более низкой дозе, когда иПТГ > 150 пг/мл (15,9 пмоль/л). Если лечение Цинесетом прекратилось на период более 14 дней, начните его заново в рекомендуемой начальной дозе.
Коррекция дозы, основанная на уровне кальция в сыворотке
Уровень кальция в сыворотке следует измерять в течение 1 недели после начала лечения или коррекции дозы Цинесета.
После того, как поддерживающая доза была установлена, рекомендуется недельное измерение урвоня кальция в сыворотке. Уровень кальция в сыворотке крови у педиатрических пациентов должен поддерживаться в нормальном диапазоне. Если уровень кальция в сыворотке снижается ниже нормального диапазона или появляются симптомы гипокальциемии, следует предпринять соответствующие шаги по коррекции дозы, как показано в таблице 2 ниже:
Таблица 2. Коррекция дозы у педиатрических пациентов от ≥ 3 до <18 лет
| Уровень кальция в сыворотке крови или клинические симптомы гипокальциемии |
Рекомендации |
| Уровень кальция в сыворотке крови находится ниже или ниже установленного по возрасту нижнего предела нормы или если симптомы гипокальциемии происходят независимо от уровня кальция. |
Прекратите лечение с помощью препарата Цинесет.* Применение добавок кальция, кальцийсодержащих фосфатных связующих и/или стеринов витамина D, как показано клинически. |
| Уровень кальция в сыворотке выше установленного по возрасту нижнего предела нормы, и устранены симптомы гипокальциемии. |
Возобновите прием препарата в более низкой дозе. Если лечение Цинесетом было прекращено на период более 14 дней, возобновите его в рекомендуемой начальной дозе. Если пациент получал самую низкую дозу (1 мг/день) до прекращения приема, возобновите его лечение в той же дозе (1 мг/день). |
| * Если доза была установлена, уровень кальция в сыворотке следует измерять в течение 5-7 дней |
Безопасность и эффективность Цинесета у детей в возрасте менее 3 лет для лечения вторичного гиперпаратиреоза не установлены. Недостаточно данных.
Карцинома паращитовидных желез и первичный гиперпаратиреоз
Взрослые и пожилые (> 65 лет)
Рекомендуемая начальная доза препарата Цинесет для взрослых составляет 30 мг, кратность приема: два раза в сутки. Коррекцию дозы Цинесет следует проводить с шагом в 2-4 недели, увеличивая дозу препарата следующим образом: 30 мг два раза в сутки, 60 мг два раза в сутки, 90 мг два раза в сутки и 90 мг три или четыре раза в сутки по мере необходимости для снижения концентрации кальция в сыворотке крови до верхнего предела нормального диапазона или ниже. Максимальная доза, применявшаяся в ходе клинических исследований, составляла 90 мг при кратности приема четыре раза в сутки.
Уровень кальция в сыворотке крови должна определяться через 1 неделю после начала терапии или после коррекции дозы препарата Цинесет. При достижении целевой концентрации ПТГ, сывороточные концентрации кальция должны оцениваться каждые 2-3 месяца. По завершении периода коррекции до максимальной дозы, следует проводить периодический мониторинг уровня кальция в сыворотке крови; если клинически значимое снижение уровня кальция в сыворотке крови не достигается на поддерживающей дозе, следует решить вопрос о прекращении терапии препаратом Цинесет (см. раздел «Фармакодинамика»).
Дети и подростки
Цинесет не показан к применению у детей и подростков в связи с отсутствием данных по безопасности и эффективности (см. раздел «Меры предосторожности»).
Печеночная недостаточность
У пациентов с печеночной недостаточностью не требуется коррекции начальной дозы. Препарат Цинесет следует назначать с осторожностью пациентам с печеночной недостаточностью средней и тяжелой степеней. Необходимо тщательное клиническое наблюдение пациента в период титрования дозы и при продолжении терапии (см. разделы «Меры предосторожности», «Фармакокинетика»).
Способ применения
Для приема внутрь. Препарат Цинесет рекомендуется принимать во время еды или вскоре после приема пищи, поскольку в ходе исследований было показано, что биодоступность цинакальцета увеличивается при приеме препарата с пищей (см. раздел «Фармакокинетика»).
Цены в аптеках Минск
Цинесет, таблетки, 30 мг ×28
покрытые пленочной оболочкой, Нобель Илач, Турция • По рецепту
МНН: Цинакальцет
Производитель: Нобел Алматинская Фармацевтическая Фабрика АО
Анатомо-терапевтическо-химическая классификация: Cinacalcet
Номер регистрации в РК:
РК-ЛС-5№022877
Информация о регистрации в РК:
08.04.2021 — 08.04.2031
- русский
- қазақша
- Скачать инструкцию медикамента
Торговое наименование
ЦИНЕСЕТ®
Международное непатентованное название
Цинакальцет
Лекарственная
форма, дозировка
Таблетки,
покрытые пленочной оболочкой, 30
мг, 60 мг, 90 мг
Фармакотерапевтическая группа
Фармакотерапевтическая группа: Гормональные препараты
системного действия, исключая половые гормоны и инсулин. Гармоны для
лечения заболеваний паращитовидной железы. Антипаратиреоидные
гормоны. Прочие антипаратиреоидные препараты.
Цинакальцет.
Код АТХ: H05BX01.
Показания к применению
—
вторичный гиперпаратиреоз у пациентов с терминальной стадией почечной
недостаточности, находящихся на диализе. ЦИНЕСЕТ® может также
назначаться в составе комбинированной терапии, включающей препараты,
связывающие фосфаты, и/или витамин D;
—
гиперкальциемия у пациентов (с целью снижения выраженности),
вызванная следующими заболеваниями: карцинома паращитовидных желез и
первичный гиперпаратиреоз, если, несмотря на сывороточные
концентрации кальция, паратиреоидэктомия клинически неприемлема
или противопоказана.
Перечень
сведений, необходимых до начала применения
Противопоказания
— детский
возраст до 18 лет (эффективность и безопасность не изучены)
—
повышенная чувствительность к компонентам препарата.
—
гипокальцемия
—
противопоказано лицам с наследственной непереносимостью галактозы,
галактоземией или мальабсорбцией глюкозогалактозы
Необходимые
меры предосторожности при применении
В ходе трех исследований с участием пациентов с ХБП,
находящихся на диализе, у 5% пациентов в каждой из групп, получавшей
препарат ЦИНЕСЕТ® или
плацебо, на момент начала терапии были зафиксированы сведения о
приступах судорог. При проведении этих исследований судороги
отмечались у 1.4% пациентов, получавших ЦИНЕСЕТ®,
и у 0.4% пациентов из группы плацебо. Хотя причины сообщаемых
различий по судорогам неясны, порог возникновения судорожных
припадков понижается при существенном снижении уровня кальция в
сыворотке крови.
У пациентов с сердечной недостаточностью, принимающих
цинакальцет, в ходе постмаркетинговых исследований регистрировались
отдельные случаи идиосинкразии артериальной гипотензии и/или
ухудшения течения сердечной недостаточности, в которых
причинно-следственная связь с цинакальцетом не может быть полностью
исключена и может быть обусловлена снижением концентрации кальция в
сыворотке крови. Данные клинических исследований показали, что
артериальная гипотензия возникала у 7% пациентов, принимавших
цинакальцет, и у 12% пациентов, получавших плацебо, а сердечная
недостаточность — у 2% пациентов, получавших цинакальцет или плацебо.
Терапию препаратом ЦИНЕСЕТ®
не следует проводить при концентрации кальция в
сыворотке крови (с поправкой на альбумин) ниже минимального предела
нормального диапазона. Поскольку цинакальцет понижает концентрацию
кальция в сыворотке крови, необходимо проводить тщательный мониторинг
пациентов в отношении развития гипокальциемии. У пациентов с
диагнозом ХБП, находящихся на диализе, при приеме препарата ЦИНЕСЕТ®
концентрация кальция в сыворотке крови в 4%
случаев был ниже 7.5 мг/дл (1.875 ммоль/л). В случае гипокальциемии,
для повышения уровня кальция в сыворотке крови, можно использовать
кальцийсодержащие фосфат связывающие препараты, витамин D и/или
провести коррекцию концентрации кальция в растворе при диализе. При
устойчивой гипокальциемии следует снизить дозу или прекратить прием
ЦИНЕСЕТ®. Потенциальными
признаками развития гипокальциемии могут быть парестезии, миалгии,
судороги, тетания.
Цинакальцет не показан пациентам с диагнозом ХБП, не
находящимся на диализе, в связи с возрастанием риска развития
гипокальциемии (концентрация сывороточного кальция <8.4 мг/дл или
<2.1 ммоль/л) по сравнению с пациентами, находящимися на диализе,
что может быть обусловлено более низким начальным уровнем кальция
и/или наличием остаточной функции почек.
При хроническом подавлении концентрации ПТГ ниже
концентрации, составляющей приблизительно 1.5% от ВГН по результатам
анализа иПТГ, может развиться адинамическая болезнь кости. Если
концентрация ПТГ снижается ниже рекомендуемого диапазона, следует
уменьшить дозу препарата ЦИНЕСЕТ®
и/или витамина D, или прекратить терапию.
Концентрация тестостерона часто бывает ниже нормы у
пациентов с терминальной стадией почечной недостаточности. Данные
клинического исследования с участием пациентов с терминальной стадией
почечной недостаточности, находящихся на диализе, показали, что
концентрация свободного тестостерона снижалась, в среднем, на 31.3% у
пациентов, принимающих ЦИНЕСЕТ®,
и на 16.3% у пациентов в группе плацебо через 6 месяцев после начала
терапии. Открытая продленная фаза данного исследования не показала
дальнейшего снижения в концентрации свободного и общего тестостерона
у пациентов за 3-летний период лечения препаратом ЦИНЕСЕТ®.
Поскольку у пациентов с печеночной недостаточностью
средней и тяжелой степени (по шкале Чайлд-Пью), уровень цинакальцета
в плазме крови может быть в 2-4 раза выше, таким пациентам следует с
осторожностью принимать препарат ЦИНЕСЕТ®
и проводить тщательный мониторинг функции печени
во время лечения.
В составе пленочной оболочки ЦИНЕСЕТ®
содержится 28.00 % лактоза моногидрата.
Пациенты с редкой наследственной непереносимостью галактозы,
дефицитом лактазы lapp или нарушением всасывания глюкозы/галактозы не
должны принимать препарат.
Взаимодействия
с другими лекарственными препаратами
Цинакальцет
частично метаболизируется изоферментом CYP3A4. Одновременный прием
кетоконазола (сильный ингибитор CYP3A4) в дозе 200 мг 2 раза/сут
приводил к повышению концентрации цинакальцета примерно в 2 раза. При
необходимости одновременного приема мощных ингибиторов (например,
кетоконазол, итраконазол, телитромицин, вориконазол, ритонавир) или
индукторов CYP3A4 (например, рифампицин), может потребоваться
коррекция дозы препарата ЦИНЕСЕТ®.
В экспериментальных исследованиях in vitro показано, что
цинакальцет частично метаболизируется при участии изофермента CYP1A2.
Курение стимулирует активность CYP1A2. Клиренс цинакальцета на 36-38%
выше у курящих, чем у некурящих. Влияние ингибиторов CYP1A2
(флувоксамина, ципрофлоксацина) на концентрацию цинакальцета в плазме
не изучался. Может потребоваться коррекция дозы, если во время
терапии препаратом пациент начинает/прекращает курение или
начинает/прекращает одновременный прием мощных ингибиторов CYP1A2.
Фармакокинетика цинакальцета не изменялась при
одновременном применении с кальция карбоната (однократная доза 1500
мг), севеламером (2400 мг 3 раза/сут), пантопразолом (80 мг 1
раз/сут).
Кальция
карбонат: одновременное применение
кальция карбоната (однократная доза 1500 мг) не изменяло
фармакокинетику цинакалцета.
Севеламер: одновременное
применение севеламера (2400 мг 3 раза в день) не оказывало
влияния на фармакокинетику цинакалцета.
Пантопразол: одновременное
применение пантопразола (80 мг 1 раз в день) не изменяло
фармакокинетику цинакалцета.
Влияние
цинакалцета на другие лекарственные препараты
Цинакальцет
является мощным ингибитором CYP2D6. Сочетанное применение
цинакальцета и препаратов с узким терапевтическим диапазоном и/или
вариабельной фармакокинетикой, метаболизирующихся изоферментом CYP2D6
(например, флекаинид, пропафенон, метопролол, дезипрамин,
нортриптилин, кломипрамин), может потребовать коррекции дозы этих
препаратов.
Дезипрамин:
при одновременном приеме цинакалцета в дозе 90 мг
1 раз/сут с дезипрамином (трициклический антидепрессант,
метаболизирующийся CYP2D6) в дозе 50 мг повышается уровень экспозиции
дезипрамина в 3.6 раза (90% CI3.0, 4.4) у пациентов с активным
метаболизмом CYP2D6.
Варфарин:
многократный пероральный прием
цинакальцета не влиял на фармакокинетику или фармакодинамику
варфарина (измерялись протромбиновое время и фактор VII).
Отсутствие
влияния цинакальцета на фармакокинетику R- и S-варфарина и отсутствие
аутоиндукции ферментов у пациентов после многократного приема
указывает на то, что цинакальцет не является индуктором CYP3A4,
CYP1A2 или CYP2C9 у человека.
Мидазолам: одновременное
применение цинакалцета в дозе 90 мг и перорального мидазолама в дозе
2 мг, субстрата CYP3A4 и CYP3A5, не влияет на фармакокинетику
мидазолама. Эти данные указывают на то, что цинакальцет не влияет на
фармакокинетику лекарственных средств, метаболизирующихся
изоферментами CYP3A4 и CYP3A5, таких как некоторые
иммуннодепрессанты, включая циклоспорин и такролимус.
Специальные
предупреждения
В
ходе трех исследований с участием пациентов с ХБП, находящихся на
диализе, у 5% пациентов в каждой из групп, получавшей препарат
ЦИНЕСЕТ® или
плацебо, на момент начала терапии были зафиксированы сведения о
приступах судорог. При проведении этих исследований судороги
отмечались у 1.4% пациентов, получавших ЦИНЕСЕТ®,
и у 0.4% пациентов из группы плацебо. Хотя причины сообщаемых
различий по судорогам неясны, порог возникновения судорожных
припадков понижается при существенном снижении уровня кальция в
сыворотке крови.
У пациентов с сердечной недостаточностью, принимающих
цинакальцет, в ходе постмаркетинговых исследований регистрировались
отдельные случаи идиосинкразии артериальной гипотензии и/или
ухудшения течения сердечной недостаточности, в которых
причинно-следственная связь с цинакальцетом не может быть полностью
исключена и может быть обусловлена снижением концентрации кальция в
сыворотке крови. Данные клинических исследований показали, что
артериальная гипотензия возникала у 7% пациентов, принимавших
цинакальцет, и у 12% пациентов, получавших плацебо, а сердечная
недостаточность — у 2% пациентов, получавших цинакальцет или плацебо.
Терапию препаратом ЦИНЕСЕТ®
не следует проводить при концентрации кальция в
сыворотке крови (с поправкой на альбумин) ниже минимального предела
нормального диапазона. Поскольку цинакальцет понижает концентрацию
кальция в сыворотке крови, необходимо проводить тщательный мониторинг
пациентов в отношении развития гипокальциемии. У пациентов с
диагнозом ХБП, находящихся на диализе, при приеме препарата ЦИНЕСЕТ®
концентрация кальция в сыворотке крови в 4%
случаев был ниже 7.5 мг/дл (1.875 ммоль/л). В случае гипокальциемии,
для повышения уровня кальция в сыворотке крови, можно использовать
кальцийсодержащие фосфат связывающие препараты, витамин D и/или
провести коррекцию концентрации кальция в растворе при диализе. При
устойчивой гипокальциемии следует снизить дозу или прекратить прием
ЦИНЕСЕТ®. Потенциальными
признаками развития гипокальциемии могут быть парестезии, миалгии,
судороги, тетания.
Цинакальцет не показан пациентам с диагнозом ХБП, не
находящимся на диализе, в связи с возрастанием риска развития
гипокальциемии (концентрация сывороточного кальция <8.4 мг/дл или
<2.1 ммоль/л) по сравнению с пациентами, находящимися на диализе,
что может быть обусловлено более низким начальным уровнем кальция
и/или наличием остаточной функции почек.
При хроническом подавлении концентрации ПТГ ниже
концентрации, составляющей приблизительно 1.5% от ВГН по результатам
анализа иПТГ, может развиться адинамическая болезнь кости. Если
концентрация ПТГ снижается ниже рекомендуемого диапазона, следует
уменьшить дозу препарата ЦИНЕСЕТ®
и/или витамина D, или прекратить терапию.
Концентрация тестостерона часто бывает ниже нормы у
пациентов с терминальной стадией почечной недостаточности. Данные
клинического исследования с участием пациентов с терминальной стадией
почечной недостаточности, находящихся на диализе, показали, что
концентрация свободного тестостерона снижалась, в среднем, на 31.3% у
пациентов, принимающих ЦИНЕСЕТ®,
и на 16.3% у пациентов в группе плацебо через 6 месяцев после начала
терапии. Открытая продленная фаза данного исследования не показала
дальнейшего снижения в концентрации свободного и общего тестостерона
у пациентов за 3-летний период лечения препаратом ЦИНЕСЕТ®.
Поскольку у пациентов с печеночной недостаточностью
средней и тяжелой степени (по шкале Чайлд-Пью), уровень цинакальцета
в плазме крови может быть в 2-4 раза выше, таким пациентам следует с
осторожностью принимать препарат ЦИНЕСЕТ®
и проводить тщательный мониторинг функции печени
во время лечения.
В составе пленочной оболочки ЦИНЕСЕТ®
содержится 28.00 % лактоза моногидрата.
Пациенты с редкой наследственной непереносимостью галактозы,
дефицитом лактазы lapp или нарушением всасывания глюкозы/галактозы не
должны принимать препарат.
Применение
в педиатрии
По
соображениям безопасности ЦИНЕСЕТ®
не применяется у пациентов младше 18 лет.
Во
время беременности или лактации
Клинические
данные о применении цинакальцета при беременности отсутствуют.
Препарат ЦИНЕСЕТ® не
следует применять во время беременности за исключением случаев, когда
потенциальная польза для матери оправдывает потенциальный риск для
плода.
До настоящего времени не изучена возможность выведения
цинакальцета в грудное молоко. После тщательной оценки соотношения
риск/польза, следует принять решение о прекращении грудного
вскармливания или приема препарата ЦИНЕСЕТ®.
Особенности
влияния препарата на способность управлять транспортным средством или
потенциально опасными механизмами
Исследования
по изучению влияния препарата на способность управлять автомобилем
или работать со сложными механизмами не проводились. Однако некоторые
нежелательные реакции могут влиять на способность управлять
автомобилем или работать со сложными механизмами.
Рекомендации
по применению
Режим
дозирования
Препарат рекомендуется принимать внутрь во время еды или
вскоре после приема пищи, поскольку биодоступность цинакальцета
увеличивается при приеме препарата с пищей. Таблетки следует
принимать целиком, не разжевывая и не деля их.
Метод
и путь введения
Внутрь, во время приема пищи.
Особые
группы пациентов
Дети
По соображениям безопасности ЦИНЕСЕТ®
не применяется у пациентов младше 18 лет.
Пациенты пожилого возраста
Вторичный
гиперпаратиреоз
Рекомендуемая
начальная доза препарата ЦИНЕСЕТ®
составляет 30 мг 1 раз/сут.
Титрование
дозы следует проводить каждые 2-4 недели до максимальной дозы 180 мг
1 раз/сут, при которой у пациентов, находящихся
на диализе, достигается
требуемая концентрация ПTГ в диапазоне 150-300 пг/мл (15.9-31.8
ммоль/л), определяемый по содержанию иПТГ. Определение концентрации
ПТГ следует проводить не раньше, чем через 12 ч после приема
препарата. При оценке концентрации ПТГ необходимо придерживаться
современных рекомендаций.
Измерение концентрации ПТГ следует проводить через 1-4
недели после начала терапии или коррекции дозы. При
приеме поддерживающей дозы мониторинг концентрации ПТГ должен
проводиться примерно раз в 1-3 месяца. Для определения концентрации
ПТГ можно использовать содержание иПТГ или биоинтактного ПТГ (биПТГ).
Терапия препаратом ЦИНЕСЕТ®
не меняет соотношения между иПТГ и биПТГ.
Во
время титрования дозы необходимо часто проводить мониторинг
концентрации кальция в сыворотке крови, в т.ч. через 1 неделю после
начала терапии или коррекции дозы. При достижении целевой
концентрации ПТГ и переходе на поддерживающую дозу, концентрации
кальция в сыворотке крови должны оцениваться примерно раз в месяц.
Если концентрация кальция в сыворотке крови снижается ниже
нормального диапазона, необходимо предпринять соответствующие меры,
включая коррекцию сопутствующей терапии.
Карцинома
паращитовидных желез и первичный гиперпаратиреоз
Рекомендуемая
начальная доза препарата ЦИНЕСЕТ®
составляет 30 мг 2 раза/сут.
Титрование
дозы следует проводить каждые 2-4 недели в следующей
последовательности изменений дозировки: 30 мг 2 раза/сут, 60 мг 2
раза/сут, 90 мг 2 раза/сут и 90 мг 3-4 раза/сут по мере необходимости
для снижения концентрации кальция в сыворотке крови до ВГН или ниже
этого уровня. Максимальная доза, применявшаяся в ходе клинических
исследований, составляла 90 мг 4 раза/сут.
Определение концентрация кальция в сыворотке крови
следует проводить через 1 неделю после начала терапии или коррекции
дозы. При достижении целевой концентрации ПТГ и переходе на
поддерживающую дозу, концентрации кальция в сыворотке крови должны
оцениваться каждые 2-3 месяца. По завершению периода титрования до
максимальной дозы, следует проводить периодический мониторинг
концентрации кальция в сыворотке крови. Если клинически значимое
снижение концентрации кальция в сыворотке крови не достигается при
приеме поддерживающей дозы, следует решить вопрос о прекращении
терапии препаратом ЦИНЕСЕТ®.
Пациенты с печеночной недостаточностью
При лечении пациентов
с печеночной
недостаточностью начальную дозу менять не
требуется. С осторожностью назначать препарат пациентам
с печеночной недостаточностью средней и тяжелой
степени. Следует тщательно наблюдать за лечением
во время титрования дозы и при длительной терапии.
Меры,
которые необходимо принять в случае передозировки
Дозы,
титрованные до уровня до 300 мг (1 раз/сут), безопасны для больных,
находящихся на диализе.
Передозировка
препаратом ЦИНЕСЕТ® может
привести к гипокальциемии. В случае передозировки у пациентов следует
мониторировать концентрацию кальция, для своевременного выявления
гипокальциемии. Следует проводить симптоматическую и поддерживающую
терапию. Поскольку степень связывания цинакальцета с белками высокая,
цинакальцет не выводится при гемодиализе, т.е. гемодиализ при
передозировке не эффективен.
Указание
на наличие риска симптомов отмены
Симптомы: никаких
специфических симптомов передозировки у пациентов, получавших
цинакальцет, не сообщалось.
Лечение: в случае
передозировки, пациенты должны контролироваться, показана
соответствующая симптоматическая и поддерживающая терапия.
Рекомендации по обращению за
консультацией к медицинскому работнику для разъяснения способа
применения лекарственного препарата
Описание нежелательных реакций, которые проявляются
при стандартном применении ЛП и меры, которые следует принять в этом
случае
Вторичный гиперпаратиреоз
В
ходе контролируемых клинических исследований были получены данные у
656 пациентов, принимавших препарат ЦИНЕСЕТ®,
и 470 пациентов, принимавших плацебо длительностью до 6 месяцев.
Наиболее часто наблюдались тошнота (31% в группе цинакальцета; 19% в
группе плацебо) и рвота (27% в группе цинакальцета; 15% в группе
плацебо). Тошнота и рвота были легкой и умеренной степени
выраженности и в большинстве случаев носили кратковременный характер.
Прекращение терапии в результате развития нежелательных эффектов было
вызвано, главным образом, тошнотой (1% в группе плацебо; 5% в группе
цинакальцета) и рвотой (<1% в группе плацебо; 4% цинакальцета).
Нежелательные
реакции, связанные с применением цинакальцета и встречавшиеся чаще в
группе ЦИНЕСЕТ® по сравнению с группой плацебо, в двойных слепых
клинических исследованиях, приведены ниже с соблюдением следующей
последовательности: очень часто (>1/10); часто (>1/100, <1/10);
иногда (>1/1000, <1/100); редко (>1/10 000, <1/1000);
очень редко (<1/10 000).
Со
стороны иммунной системы:
иногда —
реакции гиперчувствительности.
Со
стороны пищеварительной системы:
часто
— анорексия;
Со
стороны ЦНС и периферической нервной системы:
часто
— головокружение, парестезии; иногда — судороги.
Со
стороны ЖКТ:
очень
часто — тошнота, рвота; иногда — диспепсия,
диарея.
Со
стороны кожи и подкожной ткани:
часто —
сыпь.
Со
стороны скелетной мускулатуры, соединительной ткани и костной
системы: часто — миалгия.
Общие
нарушения и реакции на прием препарата:
часто —
астения.
Лабораторные
показатели:
часто —
гипокальциемия, снижение уровня тестостерона
Карцинома
паращитовидных желез и первичный гиперпаратиреоз
Профиль безопасности ЦИНЕСЕТ®
в этой группе пациентов в целом соответствует картине, наблюдаемой у
пациентов с хроническим заболеванием почек. Наиболее часто
встречающимися побочными эффектами были тошнота и рвота.
Постмаркетинговые наблюдения
При применении препарата ЦИНЕСЕТ®
в рутинной практике, были установлены следующие нежелательные
реакции, частота которых не может быть оценена на основании имеющихся
данных:
-
у
пациентов с сердечной недостаточностью и принимающих цинакальцет
регистрировались отдельные идиосинкразические случаи снижения АД
и/или ухудшения течения сердечной недостаточности; -
аллергические
реакции, включая ангионевротический отек и крапивницу.
При возникновении нежелательных
лекарственных реакций обращаться к медицинскому работнику,
фармацевтическому работнику или напрямую в информационную базу данных
по нежелательным реакциям (действиям) на лекарственные препараты,
включая сообщения о неэффективности лекарственных препаратов
РГП
на ПХВ «Национальный Центр экспертизы лекарственных средств и
медицинских изделий» Комитет контроля качества и безопасности
товаров и услуг Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные сведения
Состав лекарственного препарата
Одна
таблетка содержит
активное вещество —
цинакальцета гидрохлорид (эквивалетно
цинакальцету) 33.06 мг (30.00 мг), 66.12 мг (60.00 мг) или 99.18 мг
(90.00 мг);
вспомогательные вещества:
крахмал
прежелатинизированный, микрокристаллическая целлюлоза РН 102, L—
гидроксипропилцеллюлоза LH
11, кремния диоксид коллоидный безводный (Аэросил 200), кросповидон,
магния стеарат.
cостав
пленочной оболочки Опадрай II
зеленый 32F210000:
HPMC
2910/Гипромеллоза, лактозы моногидрат, титана диоксид (Е171),
макрогол/ПЭГ, FD&C
синий №2/индигокармин AL
3 % — 5 % (E
132), FD&C
желтый №6/сансет желтый FCF
алюминиевый лак (Е 110), FD&C
желтый №5/тартразин алюминиевый лак (Е 102);
cостав
пленочной оболочки Опадрай Clear
03F190003:
HPMC
2910/Гипромеллоза, макрогол/ПЭГ.
Описание
внешнего вида, запаха, вкуса
Таблетки
овальной формы, покрытые пленочной оболочкой
от светло зеленого до зеленого цвета, с
надписью «30», «60» или «90» на
одной стороне.
Форма выпуска и упаковка
По
14 таблеток (для дозировки 30 мг) или по 7 таблеток
(для дозировок 60 мг и 90 мг) помещают
в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги
алюминиевой печатной.
По
2 (для 14 таблеток) или 4
(для 7 таблеток) контурных ячейковых упаковок вместе с инструкцией по
медицинскому применению на государственном и русском языках помещают
в пачку картонную с голограммой фирмы – производителя.
Срок хранения
Срок
годности 3 года
Не
применять по истечении срока годности!
Условия хранения
Хранить
при температуре не выше 25 ºС в сухом, защищённом от света месте
Хранить в недоступном для детей месте!
Условия отпуска из аптек
по
рецепту
Сведения о производителе
АО «Нобел Алматинская Фармацевтическая Фабрика»
Республика Казахстан, г. Алматы, ул. Шевченко 162 Е.
Номер
телефона: (+7 727)
399-50-50
Номер
факса: (+7 727)
399-60-60
Адрес
электронной почты nobel@nobel.kz
Держатель
регистрационного удостоверения
АО «Нобел Алматинская Фармацевтическая Фабрика»
Республика Казахстан, г. Алматы, ул. Шевченко 162 Е.
Номер
телефона: (+7 727)
399-50-50
Номер
факса: (+7 727)
399-60-60
Адрес
электронной почты nobel@nobel.kz
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории
Республики Казахстан, принимающей претензии (предложения) по
качеству лекарственных средств от потребителей и
ответственной за
пострегистрационное наблюдение за безопасностью лекарственного
средства
АО «Нобел Алматинская Фармацевтическая Фабрика»
Республика Казахстан, г. Алматы, ул. Шевченко 162 Е.
Номер
телефона: (+7 727)
399-50-50
Номер
факса: (+7 727)
399-60-60
Адрес
электронной почты nobel@nobel.kz
| ЦИНЕСЕТ_каз.docx | 0.04 кб |
| ЦИНЕСЕТ_рус.docx | 0.05 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Описание препарата Ларипронт (таблетки для рассасывания) основано на официальной инструкции, утверждено компанией-производителем в 1996 году
Дата согласования: 31.07.1996
Особые отметки:
Содержание
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав и форма выпускa
- Фармакологическое действие
- Показания
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
ATX
Фармакологическая группа
Состав и форма выпускa
1 таблетка для рассасывания содержит лизоцима гидрохлорида 10 мг и деквалиния хлорида 0,25 мг; в контурной ячейковой упаковке 10 шт., в коробке 2 упаковки.
Фармакологическое действие
Показания
Бактериальные и грибковые инфекционно-воспалительные заболевания полости рта, глотки и гортани (стоматит, фарингит, ларингит, тонзиллит, ангина, молочница и др.); до и после стоматологических и ЛОР-операций.
Противопоказания
Гиперчувствительность.
Способ применения и дозы
Внутрь, за 30 мин до еды по 1 табл. (держат во рту или под языком до полного растворения) каждые 2–3 ч; в течение 30 мин после приема таблетки следует воздержаться от приема пищи или жидкости.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Аллергические реакции.
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Дата обновления: 08.11.2022
Аналоги (синонимы) препарата Ларипронт
Аналоги по действующему веществу не найдены.
Заказ в аптеках
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.

ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.
Автор статьи
Профессия: провизор
Название вуза: Пермская государственная фармацевтическая академия (ПГФА)
Специальность: фармация
Стаж работы: 2 года 8 месяцев
Диплом о фармацевтическом образовании: 105924 3510926 , рег. номер 32018
Места работы: провизор в аптеке, провизор сервиса Мегаптека
Все авторы
Содержание
- РЛС
- Состав
- Действующее вещество
- От чего принимать препарат?
- Дозировка
- Противопоказания
- Ларипронт: совместимость с алкоголем
- Побочное действие
- Ларипронт или Лизобакт: что лучше?
- Краткое содержание
Резкая боль в горле, «лающий» кашель и потеря голоса – симптомы ларингита. Это одна из самых распространенных форм ОРВИ у детей. В структуре ежегодных обращений к педиатрам и в отделения неотложной помощи до 6% визитов приходится на долю детей с обструктивным ларингитом – ложным крупом.
За возникновение болезни ответственны вирусы и бактерии. Поэтому составляющей терапии ларингита, а также других инфекционно-воспалительных поражений гортани, зачастую являются местные антисептики. Об одном из них и пойдет речь в статье.
Провизор расскажет о препарате Ларипронт: ознакомит с его составом, показаниями к применению, а также сравнит с аналогом – препаратом Лизобакт.
РЛС
Ларипронт зарегистрирован в Государственном реестре лекарственных средств России (ГРЛС). Это комбинированный препарат, который является антисептиком для местного применения в ЛОР-практике и стоматологии. Из аптек лекарство отпускается без рецепта.
Состав
Таблетки для рассасывания Ларипронт – противовоспалительное средство с противовирусным и противомикробным действием. В составе Ларипронта два активных вещества:
- Лизоцим – фермент, который предотвращает проникновение вируса в клетки организма, образуя с ними комплекс. Вещество также разрушает клетки бактерий, уменьшает воспаление, разжижает мокроту и обладает местным кровоостанавливающим действием.
- Деквалиния хлорид – антисептик, который воздействует на бактериальных и грибковых возбудителей, а также способствует проникновению лизоцима в более глубокие слои слизистой оболочки.
Таблетки Ларипронт, как и другие лекарства, произведены с использованием вспомогательных веществ. Одно из них требует внимания – это сахароза. Людям с сахарным диабетом нужно соблюдать осторожность.
Действующее вещество
В состав таблеток Ларипронт входят два действующих вещества: деквалиния хлорид (антисептик) и лизоцим (природный фермент).
От чего принимать препарат?
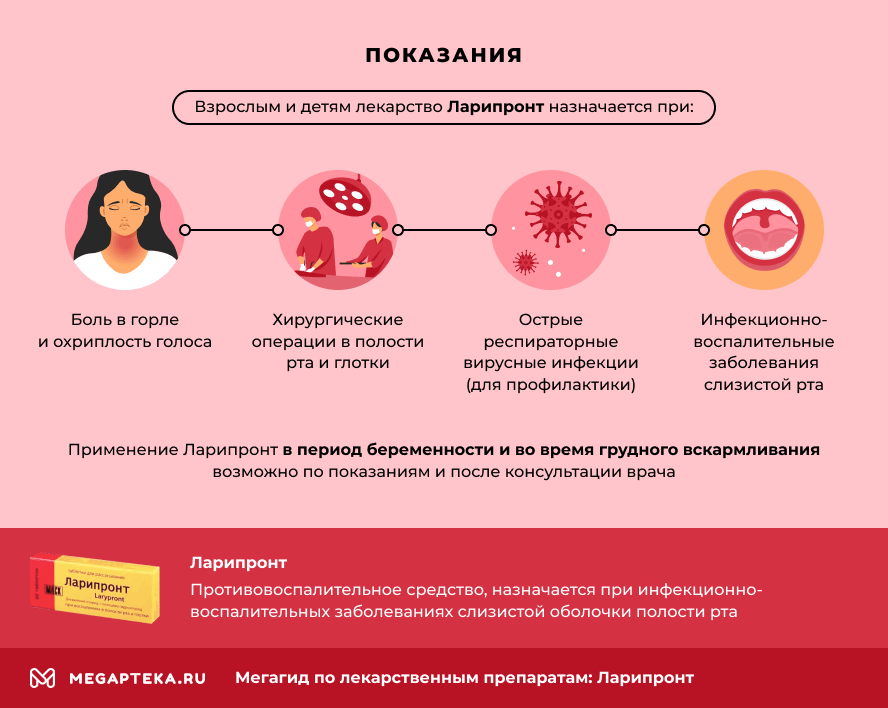
Многие пациенты знают, что Ларипронт – таблетки от горла. Однако список показаний к применению препарата шире. Согласно источнику «Инструкция по применению: Ларипронт», взрослым и детям лекарство назначается при:
- Инфекционно-воспалительных заболеваниях слизистой оболочки полости рта, глотки и гортани: ангине, ларингите, гингивите, пародонтите, стоматите и других;
- Острых респираторных вирусных инфекциях (для профилактики);
- Боли в горле и охриплости голоса;
- Хирургических операциях в полости рта и глотки (до и после процедуры).
Ларипронт: с какого возраста
Инструкция на таблетки Ларипронт не дает возрастных ограничений. Тем не менее с физиологической точки зрения ребенок может рассасывать таблетку начиная с 3 лет. Перед применением Ларипронт детям рекомендуется проконсультироваться с врачом.
Ларипронт: при беременности
Применение Ларипронт в период беременности и во время грудного вскармливания возможно по показаниям и после консультации врача.
Дозировка
Таблетки Ларипронт рекомендуется держать во рту до полного растворения. Пациентам показано по 1 таблетке каждые 2-3 часа, если врачом не предписано иное. После приема таблетки рекомендуется воздержаться от употребления пищи или жидкости в течение получаса.
Противопоказания
Таблетки для рассасывания Ларипронт противопоказаны пациентам с повышенной чувствительностью к компонентам препарата.
Ларипронт: совместимость с алкоголем
В инструкции по применению лекарства Ларипронт нет информации о совместимости с алкоголем. Для эффективного лечения и снижения риска побочных реакций врачи рекомендуют отказаться от спиртных напитков во время терапии.
Побочное действие
На фоне приема таблеток Ларипронт могут развиваться аллергические реакции. При ухудшении состояния или появлении симптомов аллергии рекомендуется обратиться за медицинской помощью.
Ларипронт или Лизобакт: что лучше?
Лизобакт – комбинированный препарат на основе лизоцима и пиридоксина (витамина В6). Последний отвечает за защиту слизистой полости рта. При этом главного компонента (лизоцима) в составе Лизобакта в два раза больше.
В отличие от Ларипронта, Лизобакт:
- Применяется при стоматите, гингивите, катаральных явлениях в верхних дыхательных путях (насморк, продуктивный кашель), а также при герпетических поражениях слизистых оболочек полости рта, эрозиях и язвах;
- Противопоказан детям до 3 лет.
Таким образом, за счет наличия дополнительного антисептического компонента (деквалиния хлорида) Ларипронт преимущественно применяют для лечения инфекционно-воспалительных заболеваний глотки и гортани – ангины, ларингита и фарингита. Лизобакт же чаще назначается в стоматологии: для лечения стоматита и других поражений слизистой оболочки полости рта.
Краткое содержание
- Таблетки для рассасывания Ларипронт – противовоспалительное средство с противовирусным и противомикробным действием.
- Ларипронт назначается при инфекционно-воспалительных заболеваниях слизистой оболочки полости рта, глотки и гортани, острых респираторных вирусных инфекциях (для профилактики), боли в горле и охриплости голоса, а также при хирургических операциях в полости рта и глотки.
- Лизобакт чаще назначается в стоматологии: для лечения стоматита и других поражений полости рта.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же вы можете поделиться своим опытом с другими читателями Мегасоветов.
от 337 ₽
от 267,90 ₽
