ХИТАБИС – это комплексное соединение хитозана, растворенного в Абисибе
Хитозан – аминосахарид, получаемый из панцирей ракообразных, оказывает гипохолестеринемическое и дезинтоксикационное действие.
Хитабис способствует улучшению пищеварения, снижению уровня мочевой кислоты, холестерина и глюкозы (на фоне сахарного диабета) в крови, улучшает усвоение кальция из пищи, а также обладает противогрибковыми и антибактериальными свойствами. Одним из основных свойств ХИТАБИСаявляется способность связывать и выводить ионы различных металлов. Это относится как к радиоактивным изотопам, так и к токсичным элементам, он наиболее эффективен в качестве сорбента. Обладает способностью связываться с молекулами жира в пищеварительном тракте, поэтому его можно использовать для снижения веса.
Применяется при: сахарном диабете, нарушении пищеварения (поносы, запоры), при отравлениях, эффективен при заболеваниях печени, поджелудочной железы. Принимать по 1ст.ложке 3 раза в день перед едой.
УДК 57+61]:: 539.1.04, 612.014.4, 591.044
Е.С. Гулик, Н.я. Костеша, Г.А. Борило
Обособленное структурное подразделение «Научно-исследовательский институт биологии и биофизики Томского государственного университета» (г. Томск)
влияние хитабиса и его компонентов на структурно-функциональное состояние тонкого кишечника и кроветворения облученных крыс
Исследовано влияние биологически активных веществ природного происхождения: водного экстракта пихты сибирской — абисиба, хитозана, выделенного из панциря крабовых, и их комплекса — хитабиса — на состояние кроветворной системы и надэпителиального слизистого слоя тонкого кишечника облученных крыс в дозе 5,5 Гр. Установлено, что наибольшее противолучевое действие по исследуемым показателям проявляет хитабис: ослабление выраженности лейкопении, большая сохранность клеточности костного мозга, формирование более устойчивого к разрушению слизистого геля тонкого кишечника по сравнению с облученным контролем.
Ключевые слова: общее рентгеновское излучение; крысы; кроветворная система; слизистый слой тонкого кишечника; абисиб; хитозан; хитабис.
Введение
Поиск эффективных средств профилактики и предотвращения лучевых поражений человека и животных остается актуальной проблемой радиобиологии, так как сохраняется опасность радиационного поражения при техногенных и природных катастрофах. Последним свидетельством является авария на АЭС «Фукусима-1» в Японии (2011 г.). Многочисленными исследованиями установлено, что биологически активные вещества природного происхождения повышают неспецифическую резистентность организма и успешно используются для профилактики и терапии различных патологий [1—3], в том числе и лучевых поражений [4-6]. В последние годы ведутся интенсивные исследования хитозана (сополимера D-глюкозамина и К-ацетил-D-глюкозамина), выделенного из панциря крабовых, установлены его сорбционные, детоксицирующие, антимикробные, антиоксидантные свойства [7-12], обнаружено выраженное противолучевое действие этого препарата при внутривенном введении как до, так и после облучения [13]. В лаборатории радиационной физиологии и биохимии НИИ биологии и биофизики Томского государственного университета ранее был изучен водный экстракт пихты сибирской — абисиб, обнаружены его бактерицидные, противовоспалительные, гемо- и иммуностимулирующие свойства [14]. При исследова-
нии комплексного препарата хитабис, представляющего собой раствор хитозана в абисибе, установлена его антиоксидантная активность [15]. Кроме того, хитабис повышает выживаемость и среднюю продолжительность жизни облученных в дозе LD90/30 экспериментальных крыс в большей степени, чем его компоненты — абисиб и хитозан [16]. Известно, что наиболее радиочувствительными системами организма являются кроветворная система и тонкий кишечник, которым свойственная высокая активность физиологической пролиферации [17].
Цель данной работы — изучение действия хитабиса и его компонентов -абисиба и хитозана — на состояние кроветворения и тонкого кишечника облученных животных.
Материалы и методики исследования
Эксперименты проведены на 104 белых беспородных крысах-самцах массой 180-220 г. Животных подвергали однократному общему воздействию рентгеновского излучения на аппарате РУМ-17 в дозе 5,5 Гр (напряжение 220 кВ, сила тока 15 мА, фильтры 0,5 мм Cu + 1 мм Al, фокусное расстояние 60 см). После облучения опытным животным вводили абисиб (производство ООО НПЦ «БИОЭПЛ», Томск), 0,1%-ный водный раствор хитозан-гидрохлорида с ММ 23 кДа (производство ВНИТИ биологической промышленности, Щелково) и 0,1%-ный раствор хитозана в абисибе — хитабис. Препараты в объеме 1 мл вводили перорально через зонд непосредственно сразу после облучения и затем в течение 10 дней. Контрольные животные получали по 1 мл дистиллированной воды в эти же сроки.
На 7, 14 и 26-е сут после облучения животных показатели периферической крови (количество эритроцитов, лейкоцитов, содержание гемоглобина) оценивали по стандартным клиническим методикам. Клеточность костного мозга определяли, вымывая костный мозг из бедренной кости и рассчитывая количество клеток на бедро.
Структурно-функциональное состояние пристеночного надэпителиаль-ного слизистого слоя (НэСС) тонкого кишечника исследовали в соответствии с модифицированной методикой Н.А. Кривовой [18]. Нативную слизь со стенок тонкого кишечника подвергали очистке, в результате которой получали фракцию очищенных гликопротеинов (Гп) и супернатант, содержащий внеклеточные компоненты слизистого слоя. Полученную фракцию очищенных гликопротеинов слизи и супернатант подвергали ступенчатому гидролизу, в гидролизатах определяли концентрацию моносахаров — гексо-заминов [19], галактозы [20], фукозы [21] и N-ацетилнейраминовой кислоты [22]. Рассчитывали суммарное содержание всех моносахаров в 1 мл слизи, парциальное содержание отдельных моносахаров в структурных Гп.
Статистическая обработка полученных результатов выполнена в программе StatSoft Statistica 6.0. Результаты исследований представлены в виде сред-
ней арифметической с ошибкой. Статистическую значимость различий между сравниваемыми выборками показателей оценивали с помощью непараметрического и-критерия Манна — Уитни с уровнем значимости р < 0,05 [23].
Результаты исследования и обсуждение
Результаты исследований показали, что облучение крыс в дозе 5,5 Гр (контрольная группа) приводило к выраженным и стойким изменениям картины периферической крови, вызванным, главным образом, опустошением кроветворных органов (табл. 1).
Т а б л и ц а 1
Показатели периферической крови и клеточности костного мозга крыс, облученных в дозе 5,5 Гр, после 10-дневного введения абисиба, хитозана, хитабиса
Время после облу- чения Группа Количество эритроцитов, х 1012/л Количество лейкоцитов, X 109/л Содержание гемоглобина, г/л Клеточность костного мозга, х 106/бедро
— Интактный контроль п = 10 6,00 ± 0,22 13,19 ± 0,86 142,1 ± 6,6 108,75 ± 5,16
7-е сут Контроль (облучение) п = 8 4,49 ± 0,04* 0,95 ± 0,06* 144,0 ± 9,0 72,40 ± 3,47*
Облучение + абисиб п = 8 3,81 ± 0,11* /** 1,29 ± 0,04* /** 115,6 ± 6,0* /** 66,96 ± 6,09*
Облучение + хитозан п = 8 3,07 ± 0,21* /** 1,20 ± 0,03* /** 116,4 ± 6,6* /** 69,56 ± 3,07*
Облучение + хитабис п = 8 4,80 ± 0,19* 1,58 ± 0,08* /** 152,9 ± 7,8 56,16 ± 3,07* /**
14-е сут Контроль (облучение) п = 8 2,96 ± 0,28* 1,36± 0,11* 85,5 ± 10,1* 58,70±3,10*
Облучение + абисиб п = 8 2,64 ± 0,20* 1,99 ± 0,27* /** 70,8 ± 6,1* 60,76±6,33*
Облучение + хитозан п = 8 3,70 ± 0,25* 2,31 ± 0,28* /** 114,1 ± 4 7* /** 82,50 ± 2,61* /**
Облучение + хитабис п = 8 3,68 ± 0,32* 2,77 ± 0,32* /** 101,4 ± 8,4* 80,72 ± 9,81* /**
26-е сут Контроль (облучение) п = 7 4,40 ± 0,07* 4,14 ± 0,34* 130,7 ± 1,7 117,26 ± 1,79
Облучение + абисиб п = 8 3,69 ± 0,23* /** 3,28 ± 0,48* 152,5±5,1** 103,96 ± 1,47**
Облучение + хитозан п = 8 3,61 ± 0,15* /** 3,09 ± 0,16* /** 123,7 ± 1,5* 97,86 ± 3,67**
Облучение + хитабис п = 7 3,38 ± 0,09* /** 3,78 ± 0,33* 127,7 ± 3,6 109,66 ± 5,52**
* Статистически значимые отличия показателей от интактного контроля (р < 0,05).
** Статистически значимые отличия показателей от соответствующего облученного контроля (р < 0,05).
На 7-е сут после облучения наблюдали ярко выраженную лейкопению (количество лейкоцитов было в 14 раз ниже, чем у интактных животных), которая сохранялась на 14-е и 26-е сут после облучения. Несмотря на то
что клетки эритроцитарного ряда также высокорадиочувствительны [24], количество эритроцитов снижалось медленнее, что связано прежде всего с большим сроком жизни красных кровяных телец. Наименьшее содержание гемоглобина и эритроцитов отмечено на 14-е сут после облучения: к этому времени количество эритроцитов составило 50%, а содержание гемоглобина — 60% от интактного уровня. Также отмечено максимальное опустошение костного мозга (клеточность костного мозга в 2 раза ниже, чем в интактной группе животных). К 26-м сут клеточность костного мозга восстанавливалась до интактного уровня, повышалось содержание эритроцитов и гемоглобина в крови облученных крыс.
Действие абисиба, хитозана, хитабиса, вводимых в течение 10 дней после облучения, проявляется на показателях красного кровяного ростка в разные сроки после облучения. На 7-е сут после применения абисиба и хитозана отмечено достоверное снижение количества эритроцитов и содержания гемоглобина облученных животных, при введении хитабиса не выявлено статистически значимых различий между опытной и контрольной группами (см. табл. 1). В разгар лучевой болезни (14-е сут) количество эритроцитов и содержание гемоглобина были наименьшими по сравнению с интактным контролем как в опытных группах, так и в контрольной. У животных, получавших хитозан, в этот срок содержание гемоглобина в крови было достоверно выше, чем у соответствующего облученного контроля. На 26-е сут после облучения количество эритроцитов во всех опытных группах снижено по сравнению с показателями как интактного, так и облученного контроля. В этот срок отмечено достоверное увеличение гемоглобина в периферической крови у крыс, получавших абисиб (см. табл. 1). Гемостимулирующее действие абисиба в восстановительный период острой лучевой болезни (ОЛБ) было зарегистрировано также в исследованиях Н.Я. Костеши [25] и
З.К. Вымятниной и др. [26]. Авторы связывают данный эффект с влиянием абисиба на интенсификацию процессов регенерации в костном мозге и усиление функциональной активности щитовидной железы, играющей важную роль в постлучевом восстановлении организма.
Таким образом, хитозан проявляет гемостимулирующее действие в разгар лучевой болезни (14-е сут после облучения), а абисиб — в восстановительный период (26-е сут после облучения), что, безусловно, сказывается на исходе ОЛБ.
В группах животных, получавших хитозан и абисиб, наблюдали большую сохранность лейкоцитов, чем в контрольной группе облученных крыс. Еще более выраженный эффект отмечен у крыс, получавших хитабис. Так, на 7-е сут после облучения число лейкоцитов периферической крови в опытной группе было в 1,5 раза больше, чем в контрольной, а на 14-е сут после облучения — более, чем в 2 раза. К концу наблюдения разница в содержании лейкоцитов нивелировалась (см. табл. 1).
В разгар лучевой болезни (14-е сут), когда клеточность костного мозга в контрольной группе составила 54% от интактного контроля, у животных,
получавшж xm^ra, этот показатель снижался лишь до 74% от интактного контроля (см. табл. 1). Клеточность костного мозга у крыс, получавшж абисиб, практически не отличалась от контрольный, тогда как в группе, получавшей xитозан, составляла 76% от интактного контроля, что на 22% выше уровня этого показателя у контрольный: облученныгс животные.
Анализ полученный результатов позволяет заключить, что для всеx групп облученныгс животные наиболее xарактерными изменениями в системе ге-мопоэза можно считать опустошение костного мозга, лейкопению, а в более поздние сроки — эритропению.
Количественные изменения со стороны форменный элементов периферической крови после облучения отражают процессы, происxодящие в костном мозге, функциональные и репаративные особенности каждого клеточного пула. Клеточность костного мозга наиболее адекватно xаракте-ризует степень лучевого поражения организма [27]. В нашж эксперимен-таx через 7 дней после облучения отмечено существенное снижение кле-точности костного мозга (до 66% от интактного контроля). Минимальное значение клеточности костного мозга у облученныгс крыс зарегистрировано через 2 недели (50% от интактного контроля). Процессы регенерации кроветворный клеток в контрольной группе животные отмечены на 26-е сут после облучения. В группаx животные, получавшж xитозан и к^абис, процессы восстановления начинались раньше (через 2 недели после облучения) и были более выражены. Это может быть связано как с усилением пролиферативной активности выжившж стволовый клеток, так и с миграцией в костный мозг клеток (в первую очередь лимфоцитов) из периферической крови и тимуса. Исследованиями К.Д. Жоголева и соавт. [28] показано, что xитозан стимулирует процессы миграции, пролиферации и дифференцировки стволовый гемопоэтическж клеток, способствуя более быстрой репарации костного мозга облученныи животные. Таким образом, введение xитозана после облучения оказывает противолучевое действие, проявляющееся в увеличении содержания гемоглобина и количества лейкоцитов в периферической крови, клеточности костного мозга опытный крыс по сравнению с соответствующими показателями у контрольный животные в разгар лучевой болезни. Абисиб проявляет гемостимулирующее действие в восстановительный период. Противолучевая активность комплексного препарата китабис наиболее выражена по отношению к белому кровяному ростку в разгар лучевой болезни и является результатом синергизма его отдельный компонентов.
Известно, что кроветворная и пищеварительная системы, в частности тонкий кишечник, являются наиболее радиочувствительными системами организма. Структурно-функциональное состояние тонкого кишечника отражает степень лучевого поражения организма [29]. Структурные Гп НэСС обладают протекторными свойствами благодаря вязкости и эластичности формируемого геля, а продукты распада ГП обладают антирадикальной
активностью, по-видимому, благодаря большому числу свободных радикалов на моносахаридных остатках [30]. Выполнение основной функции Гп слизи — образование слизистого геля — определяется строением боковых олигосахаридных цепочек молекулы [31]. Благодаря присутствию олигосахаридов гликозилированные участки полипептидов недоступны протеолизу. В Гп НэСС желудочно-кишечного тракта присутствуют следующие моносахара: ацетил-Д-глюкозамин, ацетил-Д-галактозамин, галактоза, фукоза и ацетилнейраминовая (сиаловая) кислота [32].
Облучение крыс в дозе 5,5 Гр приводило к снижению в слизи (структурные ГП) фукозы и галактозы во все сроки наблюдения (табл. 2), что свидетельствует о происходящих в облученном кишечнике деструктивных процессах. Подобный эффект отмечен во всех экспериментальных группах, за исключением животных, получавших хитозан. В этой группе на 14-е и 26-е сут после облучения содержание фукозы и галактозы было достоверно выше, чем у контрольных облученных животных, что является свидетельством активных репаративных процессов, происходящих в кишечнике. Содержание гексозаминов на 7-е сут после облучения оставалось неизменным, кроме группы крыс, получавших хитозан. На 14-е и 26-е сут во всех экспериментальных группах содержание гексозаминов было снижено по сравнению с соответствующим показателем у интактного контроля. Лишь в группе крыс, получавших абисиб, содержание гексозаминов было достоверно выше соответствующего показателя у облученного контроля и почти приближалось к значению интактного контроля. У животных, получавших хитабис, наблюдали увеличение фукозы и галактозы, при небольшом снижении гексозаминов, на 14-е сут после облучения. На 26-е сут после воздействия зарегистрированы небольшое снижение галактозы и увеличение нейраминовой кислоты в слизи кишечника крыс, получавших хитабис (табл. 2).
Защитную функцию слизи косвенно характеризует суммарное содержание моносахаров структурных Гп [33]. Резкое снижение концентрации моносахаров при облучении указывает на ослабление защитной функции слизи во все сроки наблюдения у крыс после облучения в дозе 5,5 Гр. В группе животных, получавших хитабис, отмечено достоверное увеличение суммарного содержания моносахаров на 7-е и 14-е сут после облучения.
На 14-е и 26-е сут после облучения в группе крыс, получавших хитозан, отмечено увеличение суммарного содержания моносахаров Гп НэСС, что обусловлено достоверным увеличением содержания фукозы и галактозы в этот период наблюдения (табл. 2).
Таким образом, введение хитабиса после облучения усиливает защитную функцию НэСС в разгар лучевой болезни, а применение хитозана после облучения усиливает защитную функцию НэСС в разгар и восстановительный период лучевой болезни, увеличивая суммарное содержание моносахаров структурных гликопротеинов.
Т а б л и ц а 2
Состав структурных гликопротеинов пристеночного слизистого слоя тонкого кишечника крыс, облученных в дозе 5,5 Гр
е я лия си поен С р « ^ ол рб Со Группа Гексоза- мины, мкмоль/мл Галактоза, мкмоль/мл Фукоза, мкмоль/мл Нейрами- новая кислота, мкмол/мл Сумма моноса- харов, мкмоль/мл
Интактный контроль п = 10 5,31 ± 0,81 23,3 ± 4,0 18,1 ± 5,3 0,966 ± 0,133 47,7 ± 5,2
Контроль (облучение) п = 8 5,30 ± 0,30 14,43 ± 1,11* 7,21 ± 1,18* 0,999 ± 0,004 27,9 ± 1,16*
7-е Облучение + абисиб п = 8 5,60 ± 0,21 14,71± 1,49* 5,62 ± 0,63* 0,866 ± 0,100 26,8 ± 1,46*
сут Облучение + хитозан п = 8 4,20 ± 0,25*/** 8,38 ± 0,97*/** 11,41 ± 2,07 1,099 ± 0,230 25,1 ± 2,01*
Облучение + хитабис п = 8 5,30 ± 0,21 16,71 ± 1,63* 9,62 ± 1,76* 1,265 ± 0,110 32,6 ± 1,60*/**
Контроль (облучение) п = 8 3,75 ± 0,21 7,05 ± 0,69* 2,77 ± 0,23* 1,216 ± 0,180 14,8 ± 0,50*
14-е Облучение + абисиб п = 8 4,93 ± 0,38** 8,49 ± 1,30* 3,65 ± 0,30* 1,485 ± 0,110 18,6 ± 1,20*/**
сут Облучение + хитозан п = 8 3,07 ± 0,15*/** 14,21 ± 2,38* /** 3,93 ± 0,26*/** 1,698 ± 0,180* 22,9 ± 2,20*/**
Облучение + хитабис п = 8 3,25 ± 0,10* 10,66 ± 1,31*/** 4,12 ± 0,16*/** 1,375 ±0,070 19,4 ± 1,30*/**
Контроль (облучение) п = 7 3,39 ± 0,15* 8,38 ± 1,17* 4,46 ± 0,51* 1,399 ± 0,100 17,6 ± 1,10*
26-е Облучение + абисиб п = 8 3,25 ± 0,14* 9,27 ± 0,94* 4,03 ± 0,31* 1,765 ± 0,030*/** 18,3 ± 0,80*
сут Облучение + хитозан п = 8 3,35 ± 0,34* 43,0 ± 3,32*/** 12,42 ± 0,58** 0,902 ± 0,100** 59,7 ± 3,20**
Облучение + хитабис п = 7 2,71 ± 0,27* 5,00 ± 0,34*/** 4,69 ± 0,55* 1,775 ± 0,120*/** 14,2 ± 0,30*
* Статистически значимые отличия показателей от интактного контроля (р < 0,05).
** Статистически значимые отличия показателей от соответствующего облученного контроля (р < 0,05).
Для характеристики строения олигосахаридных цепочек структурных Гп было рассчитано парциальное содержание отдельных моносахаров. Известно, что основной функцией структурных Гп НэСС является образование слизистого геля, который образуется за счет нековалентных взаимодействий между гликозилированными участками разных молекул Гп [34, 35]. Эти взаимодействия осуществляются благодаря терминально расположенным остаткам фукозы и нейраминовой кислоты, а также наличию дисульфидных
связей [30]. По количеству терминально расположенных фукозы и нейра-миновой кислоты, по-видимому, можно судить об устойчивости слизистого геля к разрушению. Суммарное содержание терминальных моносахаров у интактных животных составляет 40% в общем пуле углеводных компонентов слизи. Увеличение или уменьшение их процентного содержания может свидетельствовать об увеличении или уменьшении защитных свойств НэСС тонкого кишечника.
Облучение контрольных животных приводит к изменению парциального состава углеводных компонентов олигосахаридных цепочек Гп. Суммарное содержание фукозы и нейраминовой кислоты снижается как в облученном контроле, так и после применения абисиба.
Введение хитозана и хитабиса существенно изменяет соотношение углеводных компонентов слизи по сравнению с соответствующими показателями у облученного контроля. На 7-е сут после облучения у животных, получавших хитозан, суммарное содержание терминальных углеводных компонентов составляет 49,9%, что превышает их содержание в интактном контроле, а на 14-е и 26-е сут оно значительно снижено (до 24,6 и 22,3% соответственно). Такая динамика, вероятно, связана с тем, что защитное действие хитозана проявлялось только в период введения препарата (10 сут). По-видимому, этот эффект можно объяснить сорбционными свойствами хитозана и малым его проникновением из ЖКТ в кровоток. Большое количество водородных связей, которые способен образовывать хитозан, определяют его способность связывать большое количество органических водорастворимых веществ, в том числе бактериальные токсины и токсины, образующиеся в кишечнике в процессе пищеварения. Первичные аминогруппы хитозана обеспечивают связывание ионов тяжелых металлов и радионуклидов, в десятки раз превосходя по эффективности ионообменные смолы [36].
При введении хитабиса суммарное содержание концевых углеводных компонентов во все сроки наблюдения выше, чем соответствующие показатели в облученном контроле, и на 26-е сут составляет 45,5% по сравнению с 33,2% в облученном контроле. Полученные данные свидетельствуют о пролонгированном действии хитабиса, что может быть связано с сорбционными, гемо- и иммуностимулирующими эффектами абисиба и хитозана, возможным увеличением проникающей способности хитабиса и большей степенью его накопления в различных органах по сравнению с раздельным применением компонентов препарата. Исследованиями Б.А. Комарова и соавт. [36] показана тенденция увеличения содержания хитозана (при его введении в виде раствора в настое сбора лекарственных растений — фитохи-тодеза) в крови на 40% по сравнению с контрольным опытом (введение водных подкисленных растворов), что может быть обусловлено несколькими факторами. Во-первых, некоторые лектины растительного происхождения -сложные металлсодержащие белковые комплексы — способны выполнять роль хитиназы. Такие лектины могут быть в фитохитодезах и участвовать
в деструкции хитозана, что в свою очередь может приводить к частичному его усваиванию [37]. Во-вторых, хитозан, поступая в желудочно-кишечный тракт вместе с экстрактом фитосбора, может активизировать ферменты человека типа хитотриозидаз [38] лизоцима. Кроме этого, хитозан может разрушаться Н2О2 и активными формами кислорода [39], особенно если в хи-тозансодержащем фитопрепарате имеется повышенное содержание железа, меди и других металлов с переменной валентностью. Абисиб представляет собой многокомпонентную систему, содержащую витаминные комплексы, органические кислоты [40], макро- и микроэлементы. Среди макроэлементов обнаружено наибольшее количество магния (1,7 г/л), калия (0,6 г/л), натрия (0,3 г/л), железа (19,8 мг/л) и цинка (4,2 мг/л); рН абисиба находится в пределах 2,6-4,6 [25]. Все это может приводить к расщеплению хитозана по Р-(1-4)-гликозидной связи и накоплению легко усвояемой олигомерной фракции хитозана [39].
Таким образом, введение хитозана крысам после облучения способствует повышению защитных свойств НэСС тонкого кишечника путем формирования более устойчивого к разрушению слизистого геля тонкого кишечника на 7-е сут после облучения и увеличения суммарного содержания структурных гликопротеинов в разгар лучевой болезни и в восстановительный период. Курсовое применение хитабиса также повышает защитные свойства НэСС тонкого кишечника путем формирования более устойчивого к разрушению слизистого геля тонкого кишечника в течение всего периода наблюдения (7, 14, 26-е сут после облучения крыс в дозе 5,5 Гр).
Под действием радиации активируется свободнорадикальное окисление, нарушается деятельность быстро обновляющихся тканей, в частности системы кроветворения и желудочно-кишечного тракта, выработка антиоксидант-ных факторов этими органами подавляется, и устойчивость экспериментальных животных резко снижается [41]. Поэтому введение веществ, которые могут выступать перехватчиками образующихся под действием ионизирующего излучения радикалов, должно способствовать снижению поражающего действия радиации на организм облученных животных. Совокупность литературных и собственных данных позволяет предположить, что противолучевой эффект хитабиса и его компонентов является системным проявлением ряда механизмов. По-видимому, можно говорить об антистрессорном (адаптоген-ном) действии хитабиса и его компонентов, включающем стабилизирующее влияние на определенные звенья гемопоэза и нормализующем воздействии на НэСС тонкого кишечника. Еще один возможный механизм противолучевого действия хитабиса и его компонентов — их антиоксидантная активность.
Мы использовали известную схему патогенеза острой лучевой болезни П.Д. Горизонтова [42], адаптировав ее для костномозговой формы, для указания возможных путей физиологического действия хитабиса и его компонентов — абисиба и хитозана (рис. 1). Абисиб, обладая гемо- и иммуностимулирующим действием, оказывает прямое влияние на нервногор-
Рис. 1. Схема патогенеза костномозговой формы острой лучевой болезни с указанием возможных путей воздействия абисиба, хитозана, хитабиса
и*
и*
Влияние хитабиса и его компонентов
мональную регуляцию. В ранее проведенных исследованиях показано усиление синтетических процессов в аденогипофизе, снижение гиперсекреции коркового слоя надпочечников [25]. Формирование определенных взаимосвязей в гипоталамо-гипофизарно-надпочечниковой системе под влиянием абисиба способствует включению защитных механизмов, определяющих резистентность организма к радиационному воздействию. Для кроветворной системы это проявляется в большей сохранности костного мозга, для гастродуоденальной системы — более ранним развитием репаративных процессов в слизистой тонкого кишечника и формированием устойчивого слизистого слоя.
Более выраженная противолучевая активность хитабиса по сравнению с его компонентами может быть связана с влиянием абисиба на изменение динамики распределения и содержания хитозана в крови и различных органах опытных животных. Гетерогенность комплексного препарата (хитабис) дает увеличение противолучевого действия — гемо- и иммуностимулирующее действие абисиба усиливается сочетанием с сорбционными свойствами хитозана. Полученные результаты позволяют сделать заключение о выраженном противолучевом действии комплексного препарата хитабис.
Литература
1. Брехман И.И. Человек и биологически активные вещества. Л. : Наука, 1980. 120 с.
2. Лекарственные растения Сибири для лечения сердечно-сосудистых заболеваний. Но-
восибирск : Наука, 1991. 345 с.
3. Замощина Т.А., Никифиров Л.А., Просекина Е.Ю., Томова Т.А. Биологическая активность спиртовых извлечений из ряски малой (Lemna minor L.) в отношении процесса воспаления // Вестник Томского государственного университета. Биология. 2011. № 2(14). С. 73-80.
4. Барабой В.А. Растительные фенолы и здоровье человека. М. : Наука, 1984. 160 с.
5. Алехина С.М., Бурмистров А.Н., Макаров Р.Н. Антиоксидантные препараты, которые
используются для коррекции нарушений окислительного гомеостаза при действии ионизирующего излучения // Вестник МНАПЧАК. 2003. Т. 10, № 1. С. 79-82.
6. Овсянникова Л.М., Алехина С.М., Бурмистров А.Н. Антиоксидантная терапия наруше-
ний окислительного гомеостаза у потерпевших вследствие аварии на ЧАЭС // Вестник Международной академии проблем человека в авиации и космонавтике. 2007. № 1 (24).
7. Комаров Б.А., Албулов А.И., Эстрина Г.А. и др. Исследование хитодеза и фитохитоде-
за как перспективных биологически активных пищевых добавок // Материалы 6-й Международной конференции «Новые достижения в исследовании хитина и хитозана». СПб., 2001. С. 195-198.
8. Червинец В.М., Бондаренко В.М., Албулов А.И., Комаров Б.А. Антимикробная актив-
ность хитозана с разной молекулярной массой // Материалы 6-й Международной конференции «Новые достижения в исследовании хитина и хитозана». М. : Изд-во ВНИРО, 2001. С. 252-254.
9. Xie W., Xu P., Liu Q. Antioxidant activity of water-soluble chitosan derivatives // Bioorganic
and Medicinal Chemistry Letters. 2001. Vol. 11, № 13. P. 1699-1701.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
10. Feng T., Du Y, Li J., Wei Y., Yao P. Antioxidant activity of half N-acetylated water-soluble chitosan in vitro // European Food Research and Technology. 2007. Vol. 225, № 1. P. 133-138.
11. Sun T., Zhou D., Xie J., MaoF. Preparation of chitosan oligomers and antioxidant activity // European Food Research and Technology. 2007. Vol. 225, № 3-4. P. 451-456.
12. Sun T., Yao Q., ZhouD., MaoF. Antioxidant activity ofN-carboxymethyl chitosan oligosaccharides // Bioorganic & Medicinal Chemistry Letters. 2008. Vol. 18, is. 21. P. 5774-5776.
13. Андрианова И.Е. Противолучевые свойства хитозана // Материалы 6-й Международной конференции «Новые достижения в исследовании хитина и хитозана». СПб., 2001. С. 126-127.
14. Костеша Н.Я., Стрелис А.К., Лукьяненок П.И. и др. Экстракт пихты сибирской Аби-сиб и его применение в медицине и ветеринарии. Томск : Scientific Technical Translations ; Издательский дом «Полдень», 2004. Т. II. 140 с.
15. Гулик Е.С., Костеша Н.Я., Заева О.Б., Борило Г.А. Влияние хитозана и хитабиса на антиоксидантную активность биологических жидкостей // Материалы 10-й Международной конференции «Современные перспективы в исследовании хитина и хитоза-на. РосХит2010». Нижний Новгород, 2010. С. 177-180.
16. Гулик Е.С., Костеша Н.Я. Противолучевая активность хитозана, растворенного в экстракте пихты сибирской // Радиационная биология. Радиоэкология. 2004. Т. 44, вып. 5. С. 563-565.
17. Даренская Н.Г. Реакция основных систем организма // Теоретические основы радиационной медицины. М. : Изд. АТ, 2004. Т. 1. С. 294-314.
18. Кривова Н.А. Механизмы образования и деградации надэпителиального слизистого слоя пищеварительного тракта : дис. … д-ра биол. наук. Томск, 1994. 228 с.
19. HandelD.U., Kittlak W. Vergleichende untersuchung zur metodik der bestimmung des ei-wei gebudenen suckers // Z. Med. Labor. Techn. 1963. № 4. S. 163-169.
20. Dische Z., Shettles L. A specific color reaction of methylpentoses and spectrophotometric micromethod for their determination // J. of Biol. Chemistry. 1948. Vol. 175, № 2. P. 595-603.
21. Blix G. The determination of Hexosamines According to Elson and Morgan // Acta Chem-ica Scandinavica. 1948. Vol. 2, № 5-6. P. 467-473.
22. Warren L. The thiobarbituric acid assay of sialic acid // J. Biol. Chemistry. 1959. Vol. 234, № 8. P. 1971-1975.
23. Лакин Г.Ф. Биометрия. М. : Высшая школа, 1990. 352 с.
24. Белоусова О.И., Горизонтов П.Д., Федотова М.И. Радиация и система крови. М. : Атомиздат, 1979. 128 с.
25. Костеша Н.Я. Некоторые пути повышения резистентности организма при действии ионизирующего излучения : дис. … д-ра биол. наук. Томск, 2000. С. 143, 145.
26. Вымятнина З.К., Костеша Н.Я., Лопухова В.В., Борило Г.А. Влияние хвойного экстракта Abies sibirica Ledeb. на гемопоэз облученных крыс // Растительные ресурсы. 2000. Вып. 4. С. 83-89.
27. Горизонтов П.Д., Белоусова О.И., Федотова М.И. Стресс и система крови. М. : Медицина, 1983. 213 с.
28. Жоголев К.Д., Никитин В.Ю., Цыган В.Н. Некоторые аспекты противолучевого действия препаратов хитозана // Медицинские аспекты радиационной и химической безопасности. СПб., 2001.
29. Федоровский Л.Л. Патофизиологический анализ кишечной формы лучевой болезни // Радиационное поражение организма. М. : Атомиздат, 1976. С. 22-39.
30. Кривова Н.А., Дамбаев Г.Ц., Хитрихеев В.Е. Надэпителиальный слизистый слой желудочно-кишечного тракта и его функциональное значение. Томск : РАСКО, 2002. 316 с.
31. Gad A. Pathophysiology of gastrointestinal mucins // Adv. Physiol. Sci. 1981. Vol. 29. P. 161-184.
32. Allen A., Bell A., Mantle M., Pearson J.P. The structure and physiology of gastrointestinal mucus // Mucus in Health and Disease. 1982. P. 115-133.
33. Тарасенко Л.М., Петрушенко Т.А., Гребенникова В.Ф. Роль слизистого барьера в патогенезе стрессорных язв желудка // Физиологический журнал. 1991. № 6. С. 88-91.
34. Slomiany B., Laszewicz W., SlomianyA. In vitro inhibition of peptic degradation of porcine gastric mucus glycoprotein by sucralfate // Scand. J. Gastroenterol. 1985. Vol. 20, № 7. P. 1191-1196.
35. Sellers L.A., Allen A., Morris E.R. Mucus glycoprotein gels. Role of glycoprotein polymeric structure and carbohydrate side-chains in gel-formation // Carbohydr. Res. 1988. Vol. 178 (15). P. 93-110.
36. Комаров Б.А., Албулов А.И., Эстрина Г.А. и др. Исследование хитодеза и фитохито-деза как перспективных биологически активных пищевых добавок // Материалы 6-й Международной научной конференции «Новые достижения в исследовании хитина и хитозана». СПб., 2001. С. 195-198.
37. Комаров Б.А., Албулов А.И., Трескунов К.А., Погорельская Л.В. Некоторые аспекты фитохитодезтерапии и ее развитие // Практическая фитотерапия. 2000. № 3. С. 31-33.
38. Fusetti F., Von Moeller Y., Houston D. et al. Structure of human chitotriosidase. Implications specific inhibitor design and function of mammalian chitinase-like lectins // J. Biol. Chem. 2002. Vol. 277, is. 28. P. 25537-25544.
39. КомаровБ.А., Албулов А.И., Шинкарев С.М., Фоменко А.С. Качество хитозансодержа-щих фитопрепаратов для фитохитодезтерапии // Материалы 5-й Международной научной конференции «Фитотерапия, биологически активные вещества естественного происхождения», 22-23 января 2004 г., Черноголовка. С. 279-289.
40. Костеша Н.Я., Гулик Е.С., Борило Г.А., Зибарева Л.Н. Биологическая активность светлой фракции экстракта пихты сибирской // Вестник Томского государственного университета. 2007. № 299. С. 204-206.
41. Оганесян А.С., ГеворкянЖ.С., Татевосян А.Т., Минасян Г.М. Новые антиоксидантные факторы, секретируемые желудочно-кишечным трактом // Бюллетень экспериментальной биологии и медицины. 1990. Т. 109, № 4. С. 348-349.
42. Горизонтов П.Д. Экстремальные состояния, вызванные внешним ионизирующим излучением // Патологическая физиология экстремальных состояний / под ред. П.Д. Го-ризонтова, Н.Н. Сиротинина. М. : Медицина, 1973. С. 120.
Поступила в редакцию 15.12.2011 г.
Tomsk State University Journal of Biology. 2012. № 3 (19). P. 146-159
Elena S. Gulik, Nickolai Ya. Kostesha, Galina A. Borilo
Research Institute of Biology and Biophysics of Tomsk State University, Tomsk, Russia
INFLUENCE OF CHITABIS AND ITS COMPONENTS ON THE FUNCTIONAL STATE OF THE SMALL INTESTINE AND BLOOD INDICES OF IRRADIATED ANIMALS
The influence of aqueous extract of Abies sibirica fir-needles — abisib, chitosan-hydrochlorid (MM 23kDa, 0.1% aqueous solution) and their complex — chitabis (0.1% solution of chitosan in abisib) on the blood system andfunctional state ofsmall intestine of X-irradiated rats (dose 5.5 Gr) has been studied. Solutions of tested substances (5 ml/ kg) were administrated per os immediately after irradiation and then within 10 days. Control animals received distilled water at the same dose. On the 7-th, 14th and 26th day after exposure the blood indices (erythrocytes, leukocytes, hemoglobin) and the
number of cells in the bone marrow were estimated. Also the mucous layer carbohydrate structure of the small intestine was determined. It was shown that chitosan enhances the protective properties of mucous layer of the small intestine by forming a more stable gel on the 7-th day after exposure and increasing the total summary of structural glycoproteins in the midst of radiation sickness and recovery period. Chitabis has a more considerable influence on processes of safety and repair of mucous layer of the small intestine during the observation period. Also, chitabis increases the safety of bone marrow cells and decreases the manifestation of leucopenia. A more pronounced radioprotective activity of chitabis may be related to the influence of abisib on chitosan distribution and content in blood and in various organs of experimental animals.
Key words: X-ray irradiation; rats; small intestine; blood; abisib; chitosan; chitabis.
Received December 15, 2011
Абисиб (экстракт для приема внутрь жидкий), инструкция по медицинскому применению РУ № Р N001124/01
Дата последнего изменения: 06.09.2007
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Нозологическая классификация (МКБ-10)
- Фармакологическая группа
- Лекарственная форма
- Описание лекарственной формы
- Фармакологические свойства
- Фармако-терапевтическая группа
- Показания
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Производитель
- Аналоги (синонимы) препарата Абисиб
Действующее вещество
ATX
Фармакологическая группа
Лекарственная форма
Экстракт для приема внутрь [жидкий]
Описание лекарственной формы
Прозрачная жидкость от розового до светло-оранжевого цвета с характерным запахом хвои пихты.
Фармакологические свойства
Препарат растительного происхождения — водный экстракт хвои пихты сибирской. Ускоряет процессы регенерации тканей (изъязвлений слизистой оболочки желудочно-кишечного тракта). Обладает противовоспалительным и некоторым общетонизирующим действием.
Фармако-терапевтическая группа
Стимулятор репарации тканей растительного происхождения
Показания
Язвенная болезнь желудка и двенадцатиперстной кишки (в составе комплексной терапии).
Противопоказания
Повышенная индивидуальная чувствительность к препарату.
Способ применения и дозы
Внутрь, по одной столовой ложке 3 раза в день за 20–30 минут до приема пищи. При повышенной кислотности желудочного сока препарат следует принимать через 30 минут после приема пищи. Курс лечения 3 недели. Повторный курс — после консультации с врачом.
Возможно применение беременным женщинам на протяжении всего срока беременности и лактации.
Детям от 1 до 11 лет по 1 чайной ложке 1–2 раза в день после кормления или приема пищи через 40 минут.
Детям с 12 лет по 1–2 столовой ложки 2–3 раза в день за 30 минут до приема пищи.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Возможны аллергические реакции.
Форма выпуска
Экстракт для приема внутрь [жидкий].
450 мл во флаконе, укупоренном пробкой из резины и обжатом колпачком алюминиевым. Каждый флакон вместе с инструкцией по применению помещают в пачку картонную.
Условия отпуска из аптек
Условия хранения
В сухом, защищенном от света месте при температуре от +4 °С до +18 °С.
Хранить в недоступном для детей месте.
Срок годности
1,5 года. Не применять по истечении срока годности, указанного на упаковке.
Производитель
ООО НПЦ «БИОЭПЛ»
634009, г. Томск, ул. Р. Люксембург, 31
Тел.: (3822) 51-20-92, факс: (3822) 51-44-84
Описание проверено
-
Комкова Людмила Александровна
(Провизор)
Опыт работы: более 12 лет
Дата обновления: 06.10.2021
Аналоги (синонимы) препарата Абисиб
Аналоги по действующему веществу не найдены.
Над описанием клинического случая, представленного доктором
работали
литературный редактор
Юлия Липовская,
научный редактор
Сергей Федосов
Гастроэнтеролог
Cтаж — 23 года
Доктор наук
Медицинский центр «Афло-центр» на Володарского
Поликлиника №7
Дата публикации 17 декабря 2021 г.Обновлено 17 декабря 2021
Вступление
В декабре 2017 года в поликлинику № 7 города Кирова обратилась женщина 32 лет. Она пришла сделать плановое ультразвуковое исследование (УЗИ) брюшной полости, так как около года назад у неё выявили желчнокаменную болезнь (ЖКБ).
Жалобы
Жалоб у пациентки не было. Каких-либо симптомов, в том числе связанных с желудочно-кишечным трактом (например, изжогу, горечь во рту или расстройство стула), она не отмечала
Несмотря на отсутствие жалоб, женщину беспокоило наличие камня в желчном пузыре.
Анамнез
Камень выявили случайно в конце 2016 года, когда впервые провели УЗИ брюшной полости без каких-либо показаний для этого.
Анамнез жизни у пациентки без особенностей. Вес нормальный, питается обычно. Наследственность по ЖКБ не отягощена.
Обследование
При осмотре и физикальном обследовании никаких отклонений от нормы не выявлено.
Показатели общего и биохимического анализов крови в пределах нормы: АЛТ — 23 Ед/л, АСТ — 28 Ед/л, общий билирубин — 12,5 мкмоль/л.
По данным УЗИ, размеры желчного пузыря 33×29×64 мм, толщина стенки до 3 мм. В желчном пузыре определяется подвижное однородное образование овальной формы с чётким, ровным контуром размером 14×16×19 мм (рис. 1). В других органах брюшной полости патологий не выявили.
На рентгенограмме желчного пузыря камень не обнаружили. Это указывает на то, что камень, вероятнее всего, холестериновый.
Диагноз
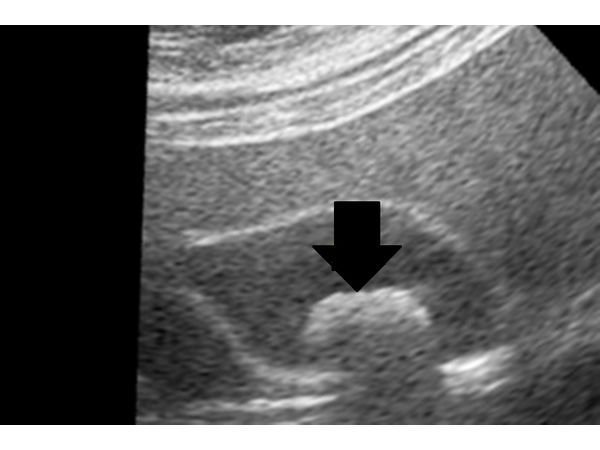
УЗИ от 23.12.2017. Камень желчного пузыря размерами 14×16×19 мм.
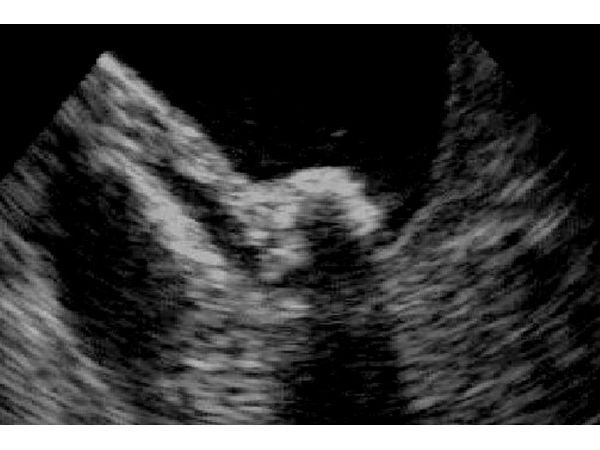
УЗИ от 19.09.2018. Камень желчного пузыря размерами 5×7×11 мм.
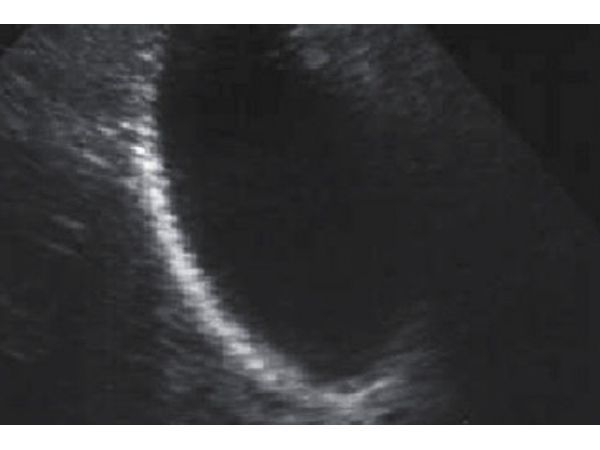
УЗИ от 12.03.2019 Желчный пузырь без признаков камня.
Лечение
Показаний для операции не было, так как болезнь никак себя не проявляла. Пациентке сообщили, что холестериновый камень можно пролечить урсодезоксихолевой кислотой и предупредили о возможных рецидивах ЖКБ после окончания курса терапии. Женщина согласилась на лечение.
Пациентка весила 67 кг, поэтому ей назначили 750 мг урсодезоксихолевой кислоты в сутки, т. е. три капсулы по 250 мг.
При применении урсодезоксихолевой кислоты более месяца в первые 3 месяца нужно контролировать уровень печёночных ферментов (АСТ и АЛТ), щелочной фосфатазы (ЩФ), гамма-глутамилтрансферазы (ГГТ) и билирубина в крови каждые 4 недели. Далее 1 раз в 3 месяца.
УЗИ желчного пузыря нужно делать 1 раз в 3 месяца. Промежуточное обследование необходимо, чтобы исключить обызвествление камней (отложение солей кальция). В случае обызвествления лечение следует прекратить.
По разным причинам контроль АЛТ, АСТ и билирубина у этой пациентки провели только в сентябре 2018 года. Анализы по-прежнему были в норме.
Контрольное УЗИ тоже сделали не в рекомендованные сроки, а только 19.09.2018. В динамике у камня в желчном пузыре были те же характеристики, но он приобрёл округлую форму и уменьшился до 5×7×11 мм, т. е. на 88 % (рис. 2).
Следующие контрольные исследования и биохимические анализы провели 12.03.2019. Лабораторные тесты были в норме. В желчном пузыре камней либо эхогенной взвеси выявлено не было (рис. 3). Пациентка по-прежнему ни на что не жаловалась, лечение она перенесла хорошо, побочных явлений не отмечала. Результатом лечения была довольна.
Заключение
Никогда нельзя полностью быть уверенным, что камень именно холестериновый. И даже в случае холестериновых камней нет гарантии, что терапия будет эффективной. В этом случае камень полностью растворился. Всего в моей практике за 4 года было четыре пациента, получавших урсодезоксихолевую кислоту по поводу ЖКБ: у двоих камни растворились полностью, у двоих терапия не подействовала.
Учёные утверждают, что урсодезоксихолевая кислота является гепатопротектором с относительно доказанной эффективностью, который хорошо себя зарекомендовал при лечении гепатозов и гепатитов. Поэтому его целесообразно назначать пациентам, у которых обнаружен холестериновый камень или есть показания к лечению неалкогольной жировой болезни печени.
Инхибейс® (Inhibace®) инструкция по применению
📜 Инструкция по применению Инхибейс®
💊 Состав препарата Инхибейс®
✅ Применение препарата Инхибейс®
📅 Условия хранения Инхибейс®
⏳ Срок годности Инхибейс®
Препарат отпускается по рецепту
Температура хранения: от 2 до 25 °С
⚠️ Государственная регистрация данного препарата отменена
Описание лекарственного препарата
Инхибейс®
(Inhibace®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2008
года, дата обновления: 2020.12.14
Владелец регистрационного удостоверения:
Код ATX:
C09AA08
(Цилазаприл)
Лекарственные формы
|
Препарат отпускается по рецепту |
Инхибейс® |
Таблетки, покрытые пленочной оболочкой, 1 мг: 15, 28, 30, 50, 98 или 100 шт. рег. №: П N015295/01 |
|
Таблетки, покрытые пленочной оболочкой, 2.5 мг: 15, 28, 30, 50, 98 или 100 шт. рег. №: П N015295/01 |
||
|
Таблетки, покрытые пленочной оболочкой, 5 мг: 15, 28, 30, 50, 98 или 100 шт. рег. №: П N015295/01 |
Форма выпуска, упаковка и состав
препарата Инхибейс®
Таблетки, покрытые оболочкой бледно-желтого цвета, овальные, двояковыпуклые; с гравировкой «CIL 1» с одной стороны таблетки и риской — с другой стороны.
Вспомогательные вещества: лактоза, крахмал кукурузный, гидроксипропилметилцеллюлоза, тальк, натрия стеарилфумарат, титана диоксид (Е171), оксид железа красный (Е172), железа оксид желтый (Е172).
7 шт. — блистеры (4) — пачки.
7 шт. — блистеры (14) — пачки.
10 шт. — блистеры (3) — пачки.
15 шт. — флаконы темного стекла (1) — пачки.
30 шт. — флаконы темного стекла (1) — пачки.
50 шт. — флаконы темного стекла (1) — пачки.
100 шт. — флаконы темного стекла (1) — пачки.
Таблетки, покрытые оболочкой блекло-красного цвета, овальные, двояковыпуклые; с гравировкой «CIL 2.5» с одной стороны таблетки и риской — с другой стороны.
Вспомогательные вещества: лактоза, крахмал кукурузный, гидроксипропилметилцеллюлоза, тальк, натрия стеарилфумарат, титана диоксид (Е171), оксид железа красный (Е172), железа оксид желтый (Е172).
7 шт. — блистеры (4) — пачки.
7 шт. — блистеры (14) — пачки.
10 шт. — блистеры (3) — пачки.
15 шт. — флаконы темного стекла (1) — пачки.
30 шт. — флаконы темного стекла (1) — пачки.
50 шт. — флаконы темного стекла (1) — пачки.
100 шт. — флаконы темного стекла (1) — пачки.
Таблетки, покрытые оболочкой от красновато-коричневого до коричневого цвета, овальные, двояковыпуклые; с гравировкой «CIL 5» с одной стороны таблетки и риской — с другой стороны.
Вспомогательные вещества: лактоза, крахмал кукурузный, гидроксипропилметилцеллюлоза, тальк, натрия стеарилфумарат, титана диоксид (Е171), оксид железа красный (Е172), железа оксид желтый (Е172).
7 шт. — блистеры (4) — пачки.
7 шт. — блистеры (14) — пачки.
10 шт. — блистеры (3) — пачки.
15 шт. — флаконы темного стекла (1) — пачки.
30 шт. — флаконы темного стекла (1) — пачки.
50 шт. — флаконы темного стекла (1) — пачки.
100 шт. — флаконы темного стекла (1) — пачки.
Фармакологическое действие
Ингибитор АПФ длительного действия. Подавляет ренин-ангиотензин-альдостероновую систему и, тем самым, превращение неактивного ангиотензина I в ангиотензин II , который обладает сильным сосудосуживающим действием. В рекомендуемых дозах эффект Инхибейса у пациентов с артериальной гипертензией и у больных хронической сердечной недостаточностью сохраняется в течение 24 ч.
У пациентов с нормальной функцией почек во время лечения Инхибейсом концентрация калия в сыворотке крови обычно остается в пределах нормы. У больных, одновременно принимающих калийсберегающие диуретики, возможно повышение уровня калия.
Артериальная гипертензия
Инхибейс снижает систолическое и диастолическое АД как в вертикальном, так и в горизонтальном положении, обычно без ортостатических реакций. Препарат эффективен на всех стадиях артериальной гипертензии, а также при почечной гипертензии. Антигипертензивный эффект Инхибейса обычно проявляется в течение первого часа после приема внутрь и достигает максимума через 3-7 ч. Рефлекторной тахикардии не возникает, хотя могут наблюдаться небольшие изменения частоты сердечных сокращений, не имеющие клинического значения. У некоторых пациентов снижение АД может уменьшаться к моменту следующего приема препарата.
При длительном лечении антигипертензивное действие Инхибейса сохраняется. После внезапной отмены препарата быстрого повышения АД не происходит.
У больных с артериальной гипертензией, имеющих умеренную или тяжелую почечную недостаточность, скорость клубочковой фильтрации и почечный кровоток при лечении Инхибейсом, как правило, не меняются, несмотря на клинически значимое снижение артериального давления.
Как и в случае других ингибиторов АПФ, антигипертензивное действие Инхибейса у больных негроидной расы может быть менее выражено, чем у больных других рас. Если, однако, Инхибейс применяется в комбинации с гидрохлоротиазидом, различий в действии препарата у больных разных рас не наблюдается.
Хроническая сердечная недостаточность
При хронической сердечной недостаточности активность ренин-ангиотензин-альдостероновой системы, а также симпатической нервной системы обычно повышена, что приводит к увеличению системной вазоконстрикции и к усилению задержки натрия и воды в организме. У пациентов, получающих диуретики и/или препараты наперстянки, Инхибейс, подавляя ренин-ангиотензин-альдостероновую систему, уменьшает нагрузку на сердце, снижая системное сосудистое сопротивление (постнагрузку) и давление в легочных капиллярах (преднагрузку). Кроме того, у этих больных значительно улучшается переносимость физической нагрузки, что повышает качество их жизни. Гемодинамические и клинические эффекты достигаются быстро и сохраняются в течение длительного времени.
Фармакокинетика
Всасывание
После приема внутрь цилазаприл хорошо всасывается и быстро превращается в активную форму — цилазаприлат. Прием пищи непосредственно перед приемом препарата несколько задерживает и уменьшает всасывание, что не имеет терапевтического значения. После приема внутрь цилазаприла биодоступность цилазаприлата составляет около 60%, судя по результатам определения его в моче. Cmax в плазме крови достигаются в течение 2 ч после приема и прямо пропорциональны дозе.
Выведение
Цилазаприлат выводится в неизмененном виде почками. T1/2 при приеме внутрь 1 раз/сут составляет 9 ч.
Фармакокинетика в особых клинических случаях
У пациентов с почечной недостаточностью концентрации цилазаприлата в плазме крови выше, чем у больных с нормальной функцией почек, т.к. клиренс препарата снижается при низком КК. У больных с терминальной стадией почечной недостаточности элиминация отсутствует вообще, однако посредством гемодиализа можно в некоторой степени понизить концентрации как цилазаприла, так и цилазаприлата.
У больных старческого возраста с нормальной для их возраста почечной функцией концентрации цилазаприлата в плазме крови могут быть на 40% выше, а клиренс — на 20% ниже, чем у молодых. Аналогичные изменения фармакокинетики наблюдаются у больных с умеренным или тяжелым циррозом печени.
У больных с хронической сердечной недостаточностью клиренс цилазаприлата коррелирует с КК. Поэтому какой-либо дополнительной коррекции дозы, помимо той, которая рекомендуется для пациентов с нарушениями функции почек, не требуется.
Показания препарата
Инхибейс®
- артериальная гипертензия (в т.ч. реноваскулярная);
- в качестве вспомогательного средства при хронической сердечной недостаточности (в комбинации с сердечными гликозидами и/или диуретиками).
Режим дозирования
Инхибейс следует принимать в 1 раз/сут. Поскольку прием пищи не оказывает клинически значимого влияния на всасывание, препарат можно принимать до или после еды, всегда примерно в одно и то же время суток.
При артериальной гипертензии рекомендуемая начальная доза составляет 1-1.25 мг 1 раз/сут. Дозу следует подбирать индивидуально в зависимости от динамики АД. Стандартный диапазон доз Инхибейса — от 2.5 до 5 мг 1 раз/ сут. Если при дозе 5 мг 1 раз/сут АД снижается недостаточно, для усиления гипотензивного эффекта одновременно можно назначить калийвыводящий диуретик в малой дозе.
При реноваскулярной гипертензии лечение Инхибейсом следует начинать с дозы 500 мкг или менее 1 раз/сут, поскольку у этих больных ингибиторы АПФ могут вызывать более выраженное снижение АД, чем у больных артериальной гипертензией другого генеза. Поддерживающую дозу подбирают индивидуально.
Больные с артериальной гипертензией, получающие диуретики: чтобы снизить вероятность возникновения симптоматической гипотензии, диуретик следует отменить за 2-3 дня до начала лечения Инхибейсом. При необходимости его прием можно потом возобновить. Рекомендуемая начальная доза для этих больных составляет 500 мкг 1 раз/сут.
Хроническая сердечная недостаточность: лечение Инхибейсом следует начинать с дозы 500 мкг 1 раз/сут под тщательным врачебным наблюдением. В зависимости от переносимости препарата и клинического состояния дозу повышают до наименьшей поддерживающей дозы в 1 мг в сутки. Дальнейший подбор дозы в пределах обычной поддерживающей дозы 1-2.5 мг/сут производится на основании реакции больного на лечение, его клинического состояния и переносимости препарата. Максимальная доза составляет 5 мг 1 раз/сут.
Результаты клинических исследований показали, что клиренс цилазаприлата у больных с хронической сердечной недостаточностью коррелирует с КК. Поэтому при лечении больных с хронической сердечной недостаточностью и нарушением функции почек следует корректировать режим дозирования в соответствии с приведенными ниже рекомендациями.
Пациентам с почечной недостаточностью может потребоваться снижение дозы в зависимости от КК. Рекомендуемый режим дозирования приведен в таблице.
Если в исключительных случаях пациентам с циррозом печени требуется лечение цилазаприлом, то препарат следует назначать с осторожностью в начальной дозе 250-500 мкг 1 раз/сут, поскольку может развиться выраженная артериальная гипотензия.
При артериальной гипертензии для пациентов старческого возраста начальная доза Инхибейса составляет от 0.5-1.25 мг/сут. Поддерживающую дозу подбирают индивидуально в зависимости от переносимости препарата, реакции больного на лечение и его клинического состояния.
При хронической сердечной недостаточности пациентам старческого возраста, принимающим диуретики в высоких дозах, при назначении препарата следует строго придерживаться рекомендуемой начальной дозы 500 мкг.
Побочное действие
Со стороны ЦНС: наиболее часто — головная боль и головокружение.
Со стороны сердечно-сосудистой системы: менее 2% — слабость, артериальная гипотензия. При лечении ингибиторами АПФ имеются отдельные сообщения о симптоматической артериальной гипотензии, особенно у пациентов с гипонатриемией и гиповолемией, вызванными рвотой, диареей, предшествующим лечением диуретиками, бессолевой диетой или диализом.
Со стороны пищеварительной системы: менее 2% — диспепсия. Как и при применении других ингибиторов АПФ, при лечении Инхибейсом описаны отдельные случаи панкреатита, иногда с летальным исходом.
Аллергические реакции: как и при лечении другими ингибиторами АПФ, описаны случаи ангионевротического отека, хотя и редкие. При распространении отека на лицо, губы, язык, голосовой аппарат и/или гортань Инхибейс следует отменить и немедленно назначить соответствующее лечение.
Прочие: менее 2% — сыпь и кашель.
Со стороны лабораторных показателей: редко — небольшое, чаще обратимое, увеличение содержания креатинина и мочевины в сыворотке крови (такие изменения происходят в основном у больных со стенозом почечной артерии или с почечной недостаточностью, но иногда — у пациентов с нормальной функцией почек, особенно у тех, которые одновременно получают диуретики).
У больных, у которых функция почек зависит, главным образом, от ренин-ангиотензин-альдостероновой системы, например, при тяжелой недостаточности кровообращения, стенозе почечной артерии и других заболеваниях почек, лечение Инхибейсом, как и другими ингибиторами АПФ, может привести к повышению концентраций азота мочевины крови и креатинина сыворотки. Хотя после отмены Инхибейса и/или диуретиков эти изменения обычно обратимы, описаны случаи тяжелого нарушения функции почек и, редко, острой почечной недостаточности.
Иногда наблюдалось уменьшение уровня гемоглобина, гематокрита и/или лейкоцитов, однако причинная связь этих изменений с приемом Инхибейса не установлена.
В большинстве случаев побочные реакции легкой или умеренной степени тяжести, имеют преходящий характер и не требуют прекращения лечения.
Противопоказания к применению
- ангионевротический отек в анамнезе (в т.ч. наследственный, идиопатический, а также ангионевротический отек, вызванный применением других ингибиторов АПФ);
- двусторонний стеноз почечных артерий или стеноз артерии единственной почки;
- гиперкалиемия;
- порфирия;
- беременность;
- период лактации (грудное вскармливание);
- гемодиализ через высокопроизводительные мембраны из полиакрилонитритметаллилсульфата (например, AN69), гемофильтрация или ЛПНП-аферез;
- повышенная чувствительность к цилазаприлу или другим ингибиторам АПФ.
С осторожностью следует применять препарат при хронической почечной недостаточности (протеинурия более 1 г/сут), при тяжелой недостаточности кровообращения, тяжелых аутоиммунных заболеваниях (в т.ч. системная красная волчанка, склеродермия), при артериальной гипотензии, митральном стенозе, стенозе устья аорты, при ИБС, угнетении костномозгового кроветворения, состоянии после трансплантации почек, у пациентов, находящихся на гемодиализе, при сахарном диабете, подагре, гиперурикемии, на фоне диеты с ограничением соли, при циррозе печени, состояниях, сопровождающихся снижением ОЦК (в т.ч. диарея, рвота), при обструктивных заболеваниях легких, у детей и подростков в возрасте до 18 лет (безопасность и эффективность применения не изучены).
Применение при беременности и кормлении грудью
Адекватных и строго контролируемых клинических исследований по безопасности применения препарата при беременности не проводилось. Применение других ингибиторов АПФ у беременных было связано со случаями маловодия, гипотензии у новорожденных и/или анурии.
В экспериментальных исследованиях на животных ингибиторы АПФ оказывали токсическое действие на плод. Хотя соответствующие данные по Инхибейсу отсутствуют, необходимо информировать беременных о возможном риске для плода.
Неизвестно, выделяется ли цилазаприл с грудным молоком у человека, но поскольку исследования показали его присутствие в молоке крыс, назначать Инхибейс кормящим матерям не следует.
Применение при нарушениях функции печени
С осторожностью следует применять препарат при циррозе печени.
Применение при нарушениях функции почек
С осторожностью следует применять препарат при хронической почечной недостаточности (протеинурия более 1 г/ сут), состоянии после трансплантации почек.
У пациентов с почечной недостаточностью концентрации цилазаприлата в плазме крови выше, чем у больных с нормальной функцией почек, т.к. клиренс препарата снижается при низком КК. У больных с терминальной стадией почечной недостаточности элиминация отсутствует вообще, однако посредством гемодиализа можно в некоторой степени понизить концентрации как цилазаприла, так и цилазаприлата.
Противопоказано применение препарата при двустороннем стенозе почечных артерий или стенозе артерии единственной почки.
Особые указания
Как и другие ингибиторы АПФ, Инхибейс с осторожностью назначают больным аортальным стенозом.
В случае острой артериальной гипотензии больного следует уложить горизонтально; ему может потребоваться вливание физиологического раствора или препарата, увеличивающего ОЦК. После возмещения ОЦК лечение Инхибейсом можно продолжить. Однако если симптомы не исчезают, следует уменьшить дозу или отменить препарат.
У пациентов с хронической недостаточностью кровообращения, получающих ингибиторы АПФ, возможно значительное снижение АД. Однако, в клинических исследованиях, в которых больные с хронической недостаточностью кровообращения принимали Инхибейс в дозе 500 мкг, симптомы артериальной гипотензии не возникали.
Артериальную гипотензию может вызвать применение ингибиторов АПФ в ходе хирургических вмешательств в сочетании с анестетиками, также обладающими гипотензивным действием. В таких случаях больному может быть показано увеличение ОЦК путем в/в инфузии или — если эта мера не помогает — инфузии ангиотензина II.
При почечной недостаточности, а также при тяжелой сердечной недостаточности необходимо контролировать функцию почек в первые недели терапии.
Одновременное применение калийсберегающих диуретиков может вызывать увеличение уровня калия в сыворотке крови, особенно у больных с почечной недостаточностью. Поэтому если показано одновременное применение этих препаратов, в начале лечения Инхибейсом их дозу следует уменьшить, тщательно контролируя концентрацию калия в сыворотке крови и функцию почек.
Гемодиализ через высокопроизводительные мембраны из полиакрилонитритметаллилсульфата (например, AN 69), гемофильтрация или ЛПНП-аферез могут вызывать у больных, принимающих ингибиторы АПФ, включая цилазаприл, анафилаксию или анафилактоидные реакции, в том числе угрожающий жизни шок. Механизм данного явления точно неизвестен. Поэтому указанных процедур у таких пациентов следует избегать.
Анафилактические реакции могут возникать у больных, проходящих гипосенсибилизацию с применением осиного или пчелиного яда и получающих одновременно ингибитор АПФ. Поэтому прием Инхибейса следует прекратить до начала гипосенсибилизации. Кроме того, в данной ситуации Инхибейс нельзя заменять бета-адреноблокаторами.
Применение ингибиторов АПФ у больных сахарным диабетом может потенцировать гипогликемизирующий эффект пероральных гипогликемических препаратов.
Использование в педиатрии
Переносимость и эффективность Инхибейса у детей не установлены, поэтому применять препарат в педиатрии не рекомендуется.
Передозировка
Симптомы: данных о передозировке препарата у больных очень мало. У здоровых добровольцев, принимавших однократные дозы до 160 мг, нежелательного действия на АД не отмечалось. Наиболее вероятным симптомом является выраженное снижение АД.
Лечение: при выраженном снижении АД – меры, направленные на увеличение ОЦК. По показаниям цилазаприлат можно частично удалить из организма посредством гемодиализа.
Лекарственное взаимодействие
Если Инхибейс применяется в комбинации с другими антигипертензивными средствами, может наблюдаться аддитивное действие, и повышается риск развития артериальной гипотензии.
Инхибейс применялся одновременно с дигоксином, нитратами, фуросемидом, тиазидами, антикоагулянтами кумаринового ряда и блокаторами гистаминовых Н2-рецепторов. При этом увеличения концентрации дигоксина в плазме, а также другого клинически значимого или фармакокинетического взаимодействия не отмечалось.
Комбинированное применение калийсберегающих диуретиков с Инхибейсом может привести к увеличению уровня калия в сыворотке, особенно у больных с почечной недостаточностью.
При одновременном применении с НПВС возможно уменьшение гипотензивного эффекта Инхибейса, как и других ингибиторов АПФ. Этого не наблюдается у больных, получавших Инхибейс до назначения НПВС.
Условия хранения препарата Инхибейс®
Список Б. Препарат следует хранить в недоступном для детей месте при температуре до 25°С.
Срок годности препарата Инхибейс®
Условия реализации
Препарат отпускается по рецепту.
Адрес производителя
|
F.Hoffmann-La Roche , Ltd |
Швейцария |
Grenzacherstrasse 124, CH-4070 Basel, Switzerland |
|
ROCHE FARMA , S.A. |
Испания |
Severo Ochoa, 13 (Pol. Ind. De Leganes), Leganes 28914, Madrid, Spain |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
