Сыворотка против яда гадюки обыкновенной лошадиная очищенная концентрированная жидкая (раствор для инъекций, 150 АЕ/доза), инструкция по медицинскому применению РУ № Р N002482/01
Дата последнего изменения: 10.02.2023
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Нозологическая классификация (МКБ-10)
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакологические свойства
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Производитель
- Аналоги (синонимы) препарата Сыворотка против яда гадюки обыкновенной лошадиная очищенная концентрированная жидкая
- Заказ в аптеках Москвы
Действующее вещество
ATX
Фармакологическая группа
Лекарственная форма
Состав
В
1 дозе содержится:
Действующее вещество:
Специфические
иммуноглобулины, нейтрализующие яд гадюки обыкновенной, 150 АЕ.
Описание лекарственной формы
Представляет
собой прозрачную или слегка опалесцирующую жидкость с желтоватым оттенком, без
осадка.
Фармакологические свойства
Препарат
представляет собой иммуноглобулиновую фракцию сыворотки крови лошадей,
иммунизированных ядом гадюки, очищенную и концентрированную методом
пептического переваривания и солевого фракционирования, содержащую
специфические антитела. Антитела, содержащиеся в сыворотке, нейтрализуют яд
гадюки обыкновенной.
Показания
Лечение
людей, укушенных гадюкой.
Противопоказания
Противопоказанием
к продолжению применения сыворотки является только развитие анафилактического
шока при введении 0,1–0,25 мл сыворотки.
Применение при беременности и кормлении грудью
При
беременности возможно применение по жизненным показаниям с учетом пользы для
матери и возможного риска для плода. Период лактации не является
противопоказанием к применению.
Способ применения и дозы
Сыворотку
вводят подкожно, внутримышечно или внутривенно в максимально ранние сроки после
укуса змеи.
Оказание первой помощи укушенному на месте
Пострадавшего
укладывают в тень и дают обильное питье: чай, кофе, молоко, бульон, воду (употребление алкогольных напитков запрещается)
и вводят 1 лечебную дозу сыворотки независимо от массы тела укушенного. Во
избежание анафилактического шока или других аллергических осложнений, перед
введением сыворотки пострадавшему дают внутрь 1–2 таблетки любого
антигистаминного препарата (димедрол, пипольфен, тавегил и др.). Сыворотку
вводят подкожно дробно (по Безредка) в любой участок тела пострадавшего:
вначале 0,1 мл, при отсутствии реакции через 10–15 мин вводят
0,25 мл и затем через 15 мин при отсутствии побочных реакций всю
оставшуюся сыворотку. Вскрытую ампулу следует прикрывать стерильным бинтом или
ватным тампоном.
После
оказания первой помощи необходимо обеспечить неотложную госпитализацию
пострадавшего в ближайшее медицинское учреждение, где продолжат лечение.
Транспортируют больного в лежачем положении. Укушенную ногу прибинтовывают к
здоровой, придавая слегка возвышенное положение. При укусе в руку ее фиксируют
в согнутом положении с помощью ткани, перекинутой через шею.
Помощь в медицинском учреждении
Общую
вводимую дозу сыворотки устанавливает врач в зависимости от степени
интоксикации: при легкой степени внутримышечно 1–2 дозы,
при тяжелой 4–5 доз,
с учетом дозы, введенной до госпитализации.
В
случае особо тяжелой интоксикации сыворотку рекомендуется вводить внутривенно
медленно капельно после разведения (1/5–1/10) стерильным, подогретым до
температуры (37 ± 1) °С
0,9% раствором натрия хлорида для инъекций. Скорость введения: вначале 1 мл
в течение 5 мин,
затем по 1 мл
в мин. В исключительных случаях, при невозможности осуществления капельной
инфузии, допускается медленное струйное введение лечебной дозы сыворотки без
разведения шприцем. Во избежание возможных аллергических реакций до начала
внутривенного вливания сыворотки больному струйно вводят 60–90 мг
преднизолона.
Внутривенное введение сыворотки разрешается только
медицинскому персоналу!
У
детей используется тот же принцип дозирования, что и у взрослых, независимо от
веса и возраста.
В
некоторых случаях при загрязнении места укуса землей, наличии ран, некроза
тканей любого типа необходимо проведение мероприятий по экстренной профилактике
столбняка в соответствии с инструкцией по профилактике столбняка.
Введение
сыворотки должно быть зарегистрировано в установленных учетных формах с
обязательным указанием даты, способа и времени введения, реакции больного,
предприятия-производителя и номера серии препарата.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Введение
сыворотки против яда гадюки может сопровождаться развитием различных
аллергических реакций: немедленной, наступающей сразу после введения или через
несколько часов и проявляющейся симптомами анафилактического шока, ранней — на
2‑е сутки после введения и отдаленной — на 5–10 сутки.
Последние сопровождаются симптомокомплексом сывороточной болезни (повышение
температуры, появление зуда и высыпаний на коже, болей в суставах и т. д.).
При появлении анафилактической реакции введение сыворотки приостанавливают.
Подкожно вводят адреналин (эпинефрин) (0,3–1 мл),
кордиамин (1,5–2 мл),
преднизолон 25 мл
или гидрокортизон (50–100 мл),
строфантин (0,5 мл
0,04%) с глюкозой (20 мл
40% раствора). Учитывая возможность возникновения шока при введении сыворотки
за каждым привитым необходимо обеспечить медицинское наблюдение в течение 1 часа
после окончания введения препарата.
Взаимодействие
Необходимо
учитывать совместимость с другими лекарственными средствами, содержащими в
своем составе чужеродный белок.
Передозировка
Симптомы
передозировки не установлены.
Особые указания
Ампулы
с сывороткой перед вскрытием тщательно просматривают. Препарат не подлежит
применению при:
—
изменении
физических свойств (мутное содержимое ампулы, наличие не разбивающихся
хлопьев);
—
любом
повреждении целостности ампул (трещины и т. д.).
Препарат
для оказания первой помощи, хранившийся в условиях экспедиций с нарушением
температурного режима, по окончании экспедиции к применению не пригоден.
Влияние на способность управлять
транспортными средствами, механизмами
Сведения
о возможном влиянии препарата на способность управлять транспортными
средствами, механизмами отсутствуют.
Форма выпуска
Раствор
для инъекций 150 АЕ.
В
ампулах по 1 лечебной
дозе (150 АЕ
— в объеме не более 3 мл).
По
5 ампул
в картонной пачке или по 1 ампуле
в коробке из пластмассы в комплекте со стерильным шприцем одноразового
применения на 5 мл
и иглой.
В
пачку или коробку вкладывают скарификатор ампульный и инструкцию по применению.
При
использовании ампул с насечками, кольцом излома или точкой для вскрытия
скарификатор ампульный не вкладывают.
Условия транспортирования
В
соответствии с СанПиН 3.3686‑21 при температуре от 2 до 8 °C.
Условия отпуска из аптек
Условия хранения
В
соответствии с СП 3.3.2.3332‑16 при температуре от 2 до 8 °С в
недоступном для детей месте.
Срок годности
Срок
годности 2 года.
Препарат
с истекшим сроком годности применению не подлежит.
Производитель
Владелец регистрационного удостоверения
АО «НПО «Микроген»
Россия,
115088, г. Москва, ул. 1‑я Дубровская, д. 15, стр. 2
Производитель
АО «НПО «Микроген»
Россия,
115088, г. Москва, ул. 1‑я Дубровская, д. 15, стр. 2
Тел.:
(495) 710‑37‑87
Факс:
(495) 783‑88‑04
E‑mail:
info@microgen.ru
Адрес производства:
Россия,
355019, Ставропольский край,
г.
Ставрополь, ул. Биологическая, д. 20
Тел.:
(8652) 24‑40‑84
Организация, уполномоченная держателем (владельцем)
регистрационного удостоверения лекарственного препарата для медицинского
применения на принятие претензий от потребителей
АО «НПО «Микроген»
Россия,
115088, г. Москва, ул. 1‑я Дубровская, д. 15, стр. 2
Тел.:
(495) 710‑37‑87
Факс:
(495) 783‑88‑04
E‑mail:
info@microgen.ru
Описание проверено
-
Комкова Людмила Александровна
(Провизор)
Опыт работы: более 12 лет
Дата обновления: 28.05.2024
Аналоги (синонимы) препарата Сыворотка против яда гадюки обыкновенной лошадиная очищенная концентрированная жидкая
Аналоги по действующему веществу не найдены.
Заказ в аптеках
| Название препарата | Цена за упак., руб. | Аптеки |
|---|---|---|
|
Сыворотка против яда гадюки обыкновенной лошадиная очищенная концентрированная жидкая, раствор для инъекций, |
||
|
536.00 |
||
|
540.00 |
||
|
Сыворотка против яда гадюки обыкновенной лошадиная очищенная концентрированная жидкая, раствор для инъекций, |
||
|
569.00 |
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Ферковен
Fercovenum
Аналоги (дженерики, синонимы)
Актиферрин, Гемофер, Железа лактат, Гемостимулин, Ферроплекс, Ферлатум, Ферро-Фольгамма, Фербитол, Сорбифер дурулес, Актиферрин композитум, Ферро-фольгамма, Бебе-тардиферон, Каферид, Конферон, Оксиферрискорбон натрия, Ферамид, Ферро-градумент, Феррокаль, Ферроцерон, Фитоферролактол, Гемоферон, Гино-тардиферон
Действующее вещество
Фармакологическая группа
Из этой же фармакологической группы
Рецепт
Международный:
Rp.: Sol. Fercoveni 5,0
D. t. d. № 10 in amp.
S. Вводят в вену 1 раз в день ежедневно в течение 10-15 дней.
Россия:
Препарат не зарегистрирован в России
Фармакологическое действие
Гемопоэтическое
Фармакодинамика
Стимулирует эритропоэз. Из-за наличия в комбинированном препарате кобальта улучшается утилизация железа, синтез гема, ускоряется включение железа в эритроциты. Существует мнение, что кобальт блокирует сульфгидрильные группы цистеина, вызывая нарушение тканевого дыхания, особенно в клетках почек, с последующим образованием эритропоэтинов, которые и влияют на эритропоэз.
Фармакокинетика
Нет данных
Способ применения
Для взрослых:
Вводят в вену 1 раз в день ежедневно в течение 10-15 дней: первые 2 инъекции — по 2 мл, затем — по 5 мл. Вводят медленно (в течение 8-10 мин). Раствор не должен попадать под кожу. Применяют только в стационаре (больнице).
Дефицит железа в организме и количество препарата на курс лечения можно рассчитать по формуле: дефицит железа в мг равен: масса больного в кг * 2,5 * [16,5 — (1,3 * содержание гемоглобина в крови больного в г/100 мл)]. Сверх тех количеств, которые получаются при расчете, вводить препарат не следует. Для поддержания эффекта, достигнутого введением ферковена, в дальнейшем применяют препараты железа внутрь.
Показания
— при лечении гипохромных анемий (снижения содержания гемоглобина в крови) различной этиологии (причины).
— особо при плохой переносимости и недостаточной всасываемости продуктов железа, принимают вовнутрь, также в случаях, когда требуется быстро ликвидировать дефицит железа в организме. Наличие в продукте кобальта способствует усилению эритропоэза (процесса образования эритроцитов).
Противопоказания
— Хронические и острые заболевания печени
— Гипертоническая болезнь II и III степени
— Стенокардия, коронарная недостаточность.
Особые указания
Для поддержания эффекта, достигнутого в/в введением, в дальнейшем применяют препараты Fe внутрь. В период лечения необходим систематический контроль показателей сывороточного Fe и Hb. Окрашивает кал в черный цвет (не имеет клинического значения).
Побочные действия
— Гиперемия лица
— Боли в пояснице
— Чувство сжатия в груди.
Передозировка
Нет данных
Лекарственное взаимодействие
При одновременном назначении ГКС возможно усиление стимуляции эритропоэза.
Форма выпуска
Выпускают ампулы и герметически закрытые флаконы по 5 мл. Прозрачная жидкость красновато-коричневого цвета; в 1 мл препарата содержится 0,020 г (20 мг) железа в виде сахарата железа и 0,00009 г (0,09 мг) кобальта в виде глюконата кобальта, а также раствор углеводов.
Эта информация оказалась полезной?
Установи allmed.pro на телефон:

Венофер — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
Торговое название:
Венофер® (Venofer®)
Международное непатентованное или группировочное название:
железа(III) гидроксид сахарозный комплекс
Лекарственная форма:
раствор для внутривенного введения
Состав:
1 мл препарата содержит:
Активное вещество:
железо(Ш) 20 мг
в виде железа(Ш) гидроксид сахарозного комплекса 510-570 мг
Вспомогательные вещества:
натрия гидроксид 0-5 мг
в виде 10 % раствора натрия гидроксида q.s. до доведения pH 10,5-11,0
вода для инъекций 580-640 мг
Описание
Водный раствор коричневого цвета.
Фармакотерапевтическая группа:
противоанемическое средство, препарат железа для парентерального введения.
Код АТХ:
В03АС
Фармакологические свойства
Фармакодинамика
Механизм действия
Активный компонент препарата Венофер® — железо-сахарозный комплекс — состоит из ядра многоядерного гидроксида железа(Ш), окруженного большим количеством нековалентно связанных молекул сахарозы. Средняя молекулярная масса этого комплекса примерно равна 43 кДа. Структура многоядерного железосодержащего ядра сходна со структурой ядра белка ферритина — физиологического депо железа. Этот комплекс предназначен для создания управляемого источника утилизируемого железа для белков, отвечающих за транспорт и депонирование железа в организме (соответственно трансферрина и ферритина).
После внутривенного введения многоядерное железосодержащее ядро этого комплекса захватывается преимущественно ретикулоэндотелиальной системой печени, селезенки и костного мозга. На следующем этапе железо используется для синтеза гемоглобина, миоглобина и других железосодержащих ферментов, либо хранится преимущественно в печени в форме ферритина.
Фармакокинетика
Распределение
Феррокинетика железо-сахарозного комплекса, меченного 52Fe и 59Fe, оценивалась у пациентов с анемией и хронической почечной недостаточностью. В течение первых 6-8 часов 52Fe захватывался печенью, селезенкой и костным мозгом. Считается, что захват радиоактивной метки селезенкой, богатой макрофагами, является типичным для захвата железа ретикулоэндотелиальной системой.
После внутривенного введения однократной дозы препарата Венофер®, содержащей 100 мг железа, здоровым добровольцам максимальные суммарные концентрации железа в сыворотке достигались через 10 минут после инъекции, при этом средняя концентрация составляла 538 μ моль/л. Объем распределения центральной камеры полностью соответствовал объему плазмы (около 3 л).
Биотрансформация
После инъекции сахароза по большей части распадается, а многоядерное железосодержащее ядро захватывается преимущественно ретикулоэндотелиальной системой печени, селезенки и костного мозга. Через 4 недели после введения утилизация железа эритроцитами составляет от 59 до 97 %.
Выведение
Средняя молекулярная масса железо-сахарозного комплекса примерно равна 43 кДа, что достаточно много для предотвращения выведения через почки.
Выведение железа почками в первые 4 часа после инъекции дозы препарата Венофер®, содержащей 100 мг железа, составляло менее 5 % от введенной дозы. Через 24 часа суммарная концентрация железа в сыворотке снижалась до уровня перед введением. Выведение сахарозы почками составляло около 75 % от введенной дозы.
Показания к применению
Венофер® применяется для лечения железодефицитных состояний в следующих случаях:
- при клинической потребности в быстром восполнении запасов железа;
- у пациентов, которые не переносят пероральные препараты железа или не соблюдают режим лечения;
- при наличии активного воспалительного заболевания кишечника, когда пероральные препараты железа неэффективны.
Противопоказания
Применение препарата Венофер® противопоказано в следующих случаях:
- повышенная чувствительность к железо-сахарозному комплексу, раствору железосахарозного комплекса или к любому из компонентов данного лекарственного препарата;
- анемия, не обусловленная дефицитом железа;
- наличие признаков перегрузки железом или врожденные нарушения процессов его утилизации;
- I триместр беременности.
С осторожностью
Пациентам с бронхиальной астмой, экземой, поливалентной аллергией, аллергическими реакциями на иные парентеральные препараты железа и лицам, имеющим низкую железосвязывающую способность сыворотки и/или дефицит фолиевой кислоты Венофер® нужно назначать с осторожностью. Также осторожность требуется при введении препаратов железа пациентам с печеночной недостаточностью, с острыми или хроническими инфекционными заболеваниями и лицам, у которых повышены показатели ферритина сыворотки крови в связи с тем, что парентерально вводимое железо может оказывать неблагоприятное действие при наличии бактериальной или вирусной инфекции.
Применение во время беременности и в период грудного вскармливания
Умеренное количество данных по применению препарата Венофер® беременными женщинами во II и III триместрах беременности не выявило каких-либо угроз для матери или новорожденного.
Однако Венофер® следует применять во время II и III триместра беременности только тогда, когда потенциальная польза для матери превышает потенциальный риск для плода.
Применение препарата в первом триместре беременности противопоказано.
Результаты исследований на животных не выявили прямых или опосредованных вредных воздействий на течение беременности, развитие эмбриона/плода, роды или постнатальное развитие.
Количество данных по выделению железа с грудным молоком человека после внутривенного введения железо-сахарозного комплекса ограничено. В рамках небольшого клинического исследования здоровые, кормящие грудью матери с дефицитом железа получали 100 мг железа в виде железо-сахарозного комплекса. Через 4 дня после лечения содержание железа в грудном молоке не повышалось, и разницы в сравнении с контрольной группой (n=5) не наблюдалось. Нельзя исключить тот факт, что железо из препарата Венофер® может поступать новорожденному/младенцу с молоком матери, поэтому следует проводить оценку соотношения риска и пользы.
Способ применения и дозы
Применение
Препарат Венофер® вводится только внутривенно: путем капельной инфузии, или медленной инъекции, или непосредственно в венозный участок диализной системы.
Перед использованием ампулы/флаконы следует осмотреть на предмет отсутствия осадка или повреждений. Использовать следует только ампулы/флаконы с однородным, не содержащим осадка раствором коричневого цвета.
Каждая ампула/флакон препарата Венофер® предназначены исключительно для одноразового использования. Любые остатки неиспользованного лекарственного препарата или его отходы следует утилизировать в соответствии с локальными требованиями.
Введение препарата Венофер® должно осуществляться под наблюдением медицинского персонала, имеющего опыт диагностики и лечения анафилактических реакций, в условиях специализированного отделения. Должна быть обеспечена возможность проведения противошоковой терапии, включающая 0,1 % раствор эпинефрина (адреналина), антигистаминные и/или кортикостероидные препараты. Тест-доза не является надежным прогностическим фактором развития в последующем реакций гиперчувствительности, в связи с чем ее предварительное введение не рекомендуется.
Во время введения препарата и непосредственно после введения пациенты должны находиться под наблюдением врача. При появлении первых признаков анафилактических реакций применение препарата должно быть немедленно прекращено.
Необходимо наблюдать за каждым пациентом в течение как минимум 30 минут после каждого введения препарата Венофер® в терапевтической дозе на предмет отсутствия нежелательных явлений.
Внутривенная капельная инфузия
Венофер® разводится только стерильным 0,9 % (масса/объем) раствором натрия хлорида (NaCl). Разведенный раствор должен быть прозрачным, коричневого цвета. Разведение следует производить непосредственно перед инфузией, а полученный раствор следует вводить следующим образом:

Разведение препарата до более низких концентраций железа недопустимо по причинам, связанным со стабильностью раствора.
Внутривенная инъекция
Венофер® может вводиться путем медленной внутривенной инъекции со скоростью 1 мл неразведенного раствора в минуту и его доза не должна превышать 10 мл (200 мг железа) на инъекцию.
Инъекция в венозный участок диализной системы
Венофер® можно вводить во время сеанса гемодиализа непосредственно в венозный участок диализной системы при соблюдении тех же условий, что и для внутривенной инъекции.
Дозы
Для каждого пациента следует индивидуально рассчитывать кумулятивную дозу препарата Венофер®, которую нельзя превышать.
Расчет дозы
Общая кумулятивная доза препарата Венофер®, эквивалентная общему дефициту железа (мг), определяется на основании содержания гемоглобина (Hb) и массы тела (МТ). Дозу препарата Венофер® следует индивидуально рассчитывать для каждого пациента в соответствии с общим дефицитом железа, рассчитанным по нижеприведенной формуле Ганзони, например:
Общий дефицит железа [мг] = масса тела [кг] х (целевое содержание гемоглобина -фактическое содержание гемоглобина) [г/л] х 0,24* + депонированное железо [мг]
При массе тела менее 35 кг: целевое содержание гемоглобина = 130 г/л, а количество депонированного железа = 15 мг/кг массы тела
При массе тела 35 кг и больше: целевое содержание гемоглобина = 150 г/л, а количество депонированного железа = 500 мг
* Коэффициент 0,24 = 0,0034 (содержание железа в гемоглобине = 0,34 %) х 0,07 (масса крови ~ 7 % от массы тела) х 1000 (перевод [г] в [мг])
Общее количество препарата Венофер®, которое следует ввести (в мл) = Общий дефицит железа [мг] / 20 мг железа/мл
Общее количество препарата Венофер® (мл), которое следует ввести, в зависимости от массы тела, фактического содержания гемоглобина и целевого содержания гемоглобина* :
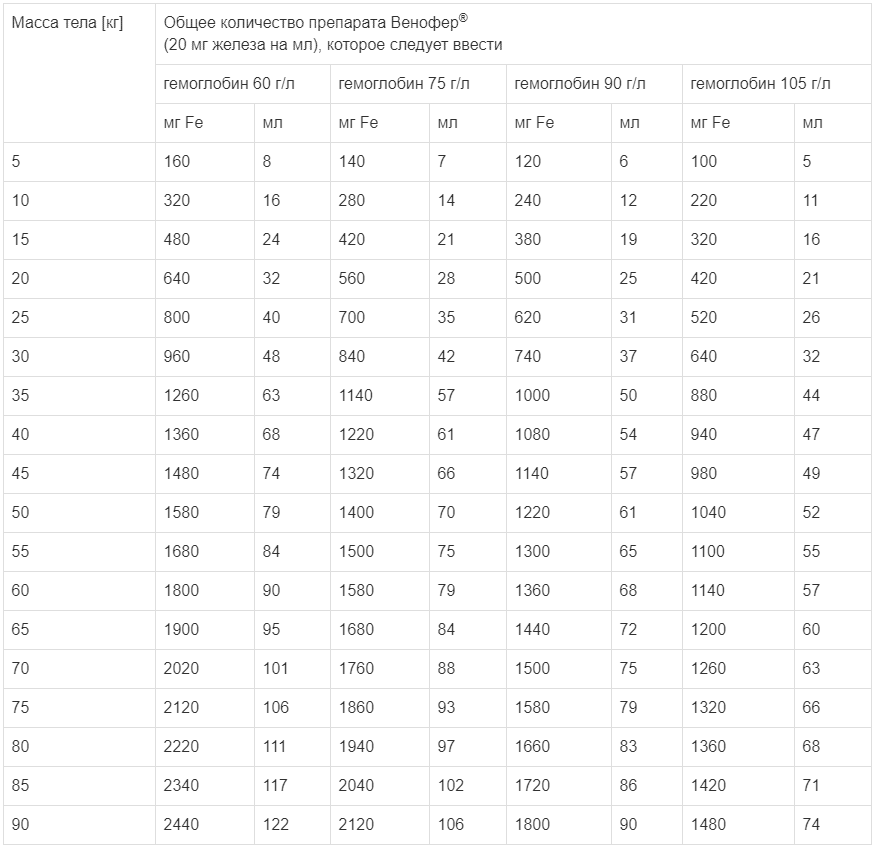
* При массе тела менее 35 кг: Целевое содержание гемоглобина = 130 г/л
При массе тела 35 кг и больше: Целевое содержание гемоглобина = 150 г/л
Для перевода гемоглобина (ммоль) в гемоглобин (г/л) умножьте первое значение на 16. Если общая необходимая доза превышает максимальную дозволенную однократную дозу, ее следует разделить на несколько введений.
Если через 1-2 недели не наблюдается ответа со стороны гематологических параметров, первоначальный диагноз следует пересмотреть.
Расчет дозы для восполнения запасов железа после кровопотери или при сдаче аутологичной крови
Дозу препарата Венофер®, необходимую для компенсации дефицита железа, можно рассчитать по следующим формулам:
Если количество потерянной крови известно: введение 200 мг железа (10 мл препарата Венофер®) должно приводить приблизительно к такому же повышению концентрации гемоглобина, что и переливание 1 порции крови (400 мл с концентрацией гемоглобина = 150 г/л).
Количество железа, которое необходимо восполнить [мг] = количество порций потерянной крови х 200 мг
или
Необходимый объем препарата Венофер® [мл] = количество порций потерянной крови х 10 мл
Если содержание гемоглобина ниже желаемого: формула предполагает, что депо железа пополнять не требуется.
Количество железа, которое необходимо восполнить [мг] = масса тела [кг] х 0,24 х (целевое содержание гемоглобина — фактическое содержание гемоглобина) [г/л]
Пример:
При массе тела = 60 кг и снижении содержания гемоглобина = 10 г/л
⇒≈150 мг железа необходимо восполнить
⇒ необходимо 7,5 мл препарата Венофер®
Максимальная переносимая разовая и недельная дозы указаны ниже в разделах «Стандартные дозы» и «Максимальная переносимая разовая и недельная дозы».
Стандартные дозы
Пациенты взрослого и пожилого возраста
5-10 мл препарата Венофер® (100-200 мг железа) 1-3 раза в неделю.
Время введения препарата и способ разведения указаны в разделе «Применение».
Дети
Имеется лишь умеренное количество данных о применении препарата у детей в рамках исследований. В случае клинической необходимости применения не рекомендуется превышать дозу 0,15 мл препарата Венофер® (3 мг железа) на кг массы тела не чаще 3 раз в неделю.
Время введения препарата и способ разведения указаны в разделе «Применение».
Максимально переносимая разовая и недельная дозы
Пациенты взрослого и пожилого возраста
Максимальная переносимая доза в сутки, вводимая в виде инъекции не чаще 3 раз в неделю:
- 10 мл препарата Венофер® (200 мг железа), вводимые в течение минимум 10 минут.
Максимальная переносимая доза в сутки, вводимая в виде инфузии не чаще 1 раза в неделю:
- Пациенты с массой тела более 70 кг: 500 мг железа (25 мл препарата Венофер®), вводимые в течение минимум 3,5 часов.
- Пациенты с массой тела 70 кг и менее: 7 мг железа/кг массы тела, вводимые в течение минимум 3,5 часов.
Следует строго придерживаться времени инфузии, указанного в разделе «Применение», даже если пациент не получил максимальной переносимой разовой дозы.
Побочное действие
Наиболее частой нежелательной лекарственной реакцией (НЛР), регистрировавшейся в рамках клинических исследований препарата Венофер®, являлось изменение вкусовых ощущений, которое наблюдалось с частотой 4,5 явления на 100 субъектов. Наиболее важными серьезными нежелательными лекарственными реакциями, связанными с применением препарата Венофер®, являлись реакции гиперчувствительности, которые наблюдались в рамках клинических исследований с частотой 0,25 явления на 100 субъектов.
В таблице ниже представлены нежелательные лекарственные реакции, зарегистрированные после применения препарата Венофер® в рамках клинических исследований, а также в пострегистрационном периоде.
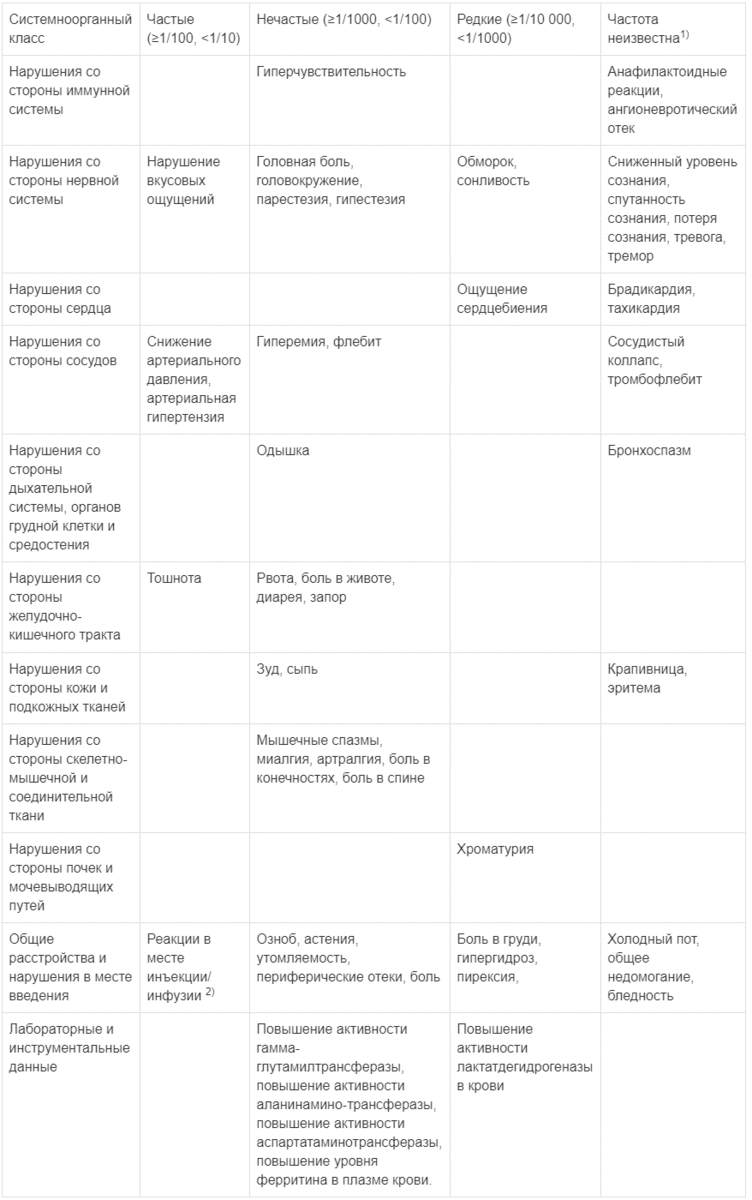
1)Спонтанные сообщения, полученные в пострегистрационном периоде
2)Наиболее частые: боль в месте инъекции/инфузии, экстравазация в месте инъекции/инфузии, раздражение в месте инъекции/инфузии, реакция в месте инъекции/инфузии, изменение окрашивания кожи в месте инъекции/инфузии, кровоподтек в месте инъекции/инфузии, зуд в месте инъекции/инфузии.
Передозировка
Передозировка может вызывать перегрузку железом, которая может проявляться симптомами гемосидероза. Передозировку следует лечить с использованием хелатирующего средства для связывания железа или в соответствии со стандартами медицинской практики.
Взаимодействие с другими лекарственными средствами
Как и при применении всех парентеральных препаратов железа, препарат Венофер® не рекомендуется применять одновременно с пероральными препаратами железа, поскольку всасывание перорального железа может снижаться, поэтому терапию пероральными препаратами железа следует начинать не ранее, чем через 5 дней после последней инъекции.
Венофер можно смешивать только со стерильным 0,9 % (масса/объем) раствором натрия хлорида. При смешивании с другими растворами или лекарственными препаратами имеется риск выпадения осадка и/или взаимодействия. Совместимость с контейнерами из других материалов, помимо стекла, полиэтилена и поливинилхлорида, не изучена.
Особые указания
Парентерально вводимые препараты железа могут вызывать аллергические или анафилактоидные реакции, которые потенциально могут быть летальными, поэтому в наличии должны иметься противоаллергические препараты, а также оборудование для проведения сердечно-легочной реанимации и соответствующих процедур. После предшествовавших неосложненных введений парентеральных комплексов железа также отмечались реакции гиперчувствительности. После каждой инъекции препарата Венофер® за всеми пациентами следует наблюдать на предмет отсутствия нежелательных явлений в течение как минимум 30 минут.
Пациентам, имеющим в анамнезе бронхиальную астму, экзему, другие виды атопических аллергий или аллергические реакции на другие парентеральные препараты железа, препарат Венофер® следует применять с осторожностью, поскольку такие пациенты в особенности могут иметь риск развития аллергической реакции.
Пациентам с нарушением функции печени парентеральное железо следует применять только после тщательной оценки соотношения риска и пользы. Пациентам с нарушением функции печени, когда перегрузка железом является провоцирующим фактором, не следует применять парентеральное железо. Для того чтобы избежать перегрузки железом, рекомендуется проводить тщательный мониторинг уровня железа в организме.
Парентеральное железо следует применять с осторожностью при наличии острой или хронической инфекции. Пациентам с бактериемией рекомендуется прекратить применение препарата Венофер®. У пациентов с хронической инфекцией следует провести оценку соотношения риска и пользы.
Следует избегать проникновения препарата в околовенозное пространство, поскольку это может привести к появлению боли, развитию воспаления и окрашиванию кожи в коричневый цвет. В случаях непреднамеренного проникновения препарата в околовенозное пространство лечение следует проводить в соответствии со стандартами медицинской практики.
Венофер® следует применять только в тех случаях, когда показание к применению подтверждено результатами соответствующих исследований (например, уровень ферритина в сыворотке, уровень насыщения трансферрина, содержание гемоглобина (Hb), эритроцитарные показатели — MCV, MCH, MCHC).
Срок годности после первого вскрытия контейнера
С микробиологической точки зрения, препарат следует использовать незамедлительно.
Срок годности после разведения 0,9 % раствором натрия хлорида (NaCl)
Химическая и физическая стабильность после разведения при комнатной температуре (15-25 °С) составляет 12 часов. Однако с микробиологической точки зрения, препарат следует использовать сразу после разведения. Если препарат не был использован сразу же после разведения, тот, кто использует данный раствор, несёт ответственность за условия и время хранения после разведения, которое в любом случае не должно превышать 3 часов при комнатной температуре, кроме тех случаев, когда разведение было выполнено в контролируемых и надлежащих асептических условиях.
Влияние на способность управлять транспортными средствами или работать с другими механизмами
Данных о влиянии на способность управлять транспортными средствами или работать с другими механизмами не имеется. Однако некоторые нежелательные реакции (такие, как головокружение, спутанность сознания и прочие (указаны в разделе «Побочное действие»)) могут оказывать негативное влияние на способность управлять транспортными средствами или работать с другими механизмами. Пациентам, у которых отмечаются данные нежелательные реакции, рекомендовано воздержаться от управления транспортными средствами или работы с другими механизмами до полного исчезновения данных симптомов.
Форма выпуска
Раствор для внутривенного введения 20 мг/мл.
По 5 мл препарата в бесцветные, прозрачные стеклянные ампулы (тип I по Евр. Ф.), имеющие насечку на шейке ампулы и технические цветные метки в виде одного или двух ободков и точки.
По 5 мл препарата в бесцветные, прозрачные стеклянные флаконы (тип I по Евр. Ф.), закрытые эластичной пробкой и алюминиевым колпачком с отрывным элементом.
По 5 ампул или флаконов в контурной ячейковой упаковке из поливинилхлорида вместе с инструкцией по применению упаковывают в картонную пачку.
Условия хранения
В оригинальной упаковке при температуре не выше 25 °С.
Препарат не подлежит замораживанию.
Хранить в местах, недоступных для детей.
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска
По рецепту.
Юридическое лицо, на имя которого выдано регистрационное удостоверение / Компания, осуществляющая выпускающий контроль качества
Вифор (Интернэшнл) Инк.
Рехенштрассе 37, 9014 Ст. Галлен, Швейцария
Vifor (International) Inc.
Rechenstrasse 37, 9014 St. Gallen, Switzerland
Производитель
БИПСО ГмбХ, Роберт-Гервиг-Штрассе 4, 78224 Зинген, Германия
(BIPSO GmbH, Robert-Gerwig-Strasse 4, 78224 Singen, Germany)
АйДиТи Биологика ГмбХ, Ам Фармапарк, 06861 Дессау-Росслау, Германия
(IDT Biologika GmbH, Am Pharmapark, 06861 Dessau-Rosslau, Germany)
Организация, принимающая претензии потребителей
ООО «Такеда Фармасьютикалс»
119048, г. Москва, ул. Усачева, д. 2, стр. 1
Купить Венофер в ГорЗдрав
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Фервекс® (Fervex) инструкция по применению
📜 Инструкция по применению Фервекс®
💊 Состав препарата Фервекс®
✅ Применение препарата Фервекс®
📅 Условия хранения Фервекс®
⏳ Срок годности Фервекс®
Описание лекарственного препарата
Фервекс®
(Fervex)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2020 года.
Дата обновления: 2019.12.10
Код ATX:
N02BE51
(Парацетамол в комбинации с другими препаратами, кроме психолептиков)
Активные вещества
-
аскорбиновая кислота
(ascorbic acid)
Rec.INN
зарегистрированное ВОЗ -
парацетамол
(paracetamol)
Rec.INN
зарегистрированное ВОЗ -
фенирамин
(pheniramine)
Rec.INN
зарегистрированное ВОЗ
Лекарственные формы
|
Без рецепта |
Фервекс® |
Порошок для приготовления раствора для приема внутрь (малиновый с сахаром) 500 мг+25 мг+200 мг/1 пак.: пак. 12.75 г 8 шт. рег. №: П N015947/01 |
|
Порошок для приготовления раствора для приема внутрь (лимонный с сахаром) 500 мг+25 мг+200 мг/1 пак.: пак. 13.1 г 4, 8 или 12 шт. рег. №: П N015947/01 |
Форма выпуска, упаковка и состав
препарата Фервекс®
Порошок для приготовления раствора для приема внутрь (лимонный с сахаром) светло-бежевого цвета; допускаются вкрапления коричневого цвета; приготовленный раствор светло-желтого с сероватым оттенком цвета, опалесцирующий.
Вспомогательные вещества: сахароза — 11.555 г, лимонная кислота — 0.2 г, акации камедь — 0.1 г, натрия сахарината дигидрат — 0.02 г, ароматизатор лимонно-ромовый* — 0.5 г.
13.1 г — пакетики из комбинированного материала (4) — пачки картонные.
13.1 г — пакетики из комбинированного материала (8) — пачки картонные.
13.1 г — пакетики из комбинированного материала (12) — пачки картонные.
Порошок для приготовления раствора для приема внутрь (малиновый с сахаром) от светло-розового до светло-бежевого цвета; допускаются вкрапления темно-розового цвета; приготовленный раствор розового цвета, слегка опалесцирующий.
Вспомогательные вещества: сахароза — 11.555 г, лимонная кислота — 0.2 г, акации камедь — 0.1 г, натрия сахарината дигидрат — 0.02 г, ароматизатор малиновый** — 0.15 г.
12.75 г — пакетики из комбинированного материала (8) — пачки картонные.
* состав ароматизатора лимонно-ромового: мальтодекстрин, камедь акации, α-пинен, β-пинен, лимонен, γ-терпинен, линалоол, нераль, α-терпинеол, гераниаль, декстроза, кремния диоксид, бутилгидроксианизол.
** состав ароматизатора малинового: этилацетат, изоамилацетат, уксусная кислота, бензиловый спирт, триацетин, ванилин, p-гидрокси-бензилацетон, мальтодекстрин, E1450 модифицированный кукурузный крахмал, E129 краситель красный очаровательный, E133 краситель бриллиантовый голубой, E110 краситель солнечный закат желтый, пермастабил 505528 RI, малина 054428 A, хлорид натрия и/или сульфат натрия.
Фармакологическое действие
Фервекс® — комбинированный препарат, который содержит парацетамол, фенирамин и аскорбиновую кислоту.
Парацетамол — ненаркотический анальгетик, блокирует циклооксигеназу, преимущественно в ЦНС, воздействуя на центры боли и терморегуляции; оказывает анальгезирующее и жаропонижающее действие.
Фенирамин — блокатор гистаминовых H1-рецепторов, снижает ринорею и слезотечение, устраняет спастические явления, отечность и гиперемию слизистой оболочки полости носа, носоглотки и придаточных пазух носа.
Аскорбиновая кислота является ко-фактором некоторых реакций гидроксилирования и амидирования — переносит электроны на ферменты, снабжая их восстановительным эквивалентом. Участвует в реакциях гидроксилирования пролиновых и лизиновых остатков проколлагена с образованием гидроксипролина и гидроксилизина (посттрансляционная модификация коллагена), окислении боковых цепей лизина в белках с образованием гидрокситриметиллизина (в процессе синтеза карнитина), окислении фолиевой кислоты до фолиновой, метаболизме лекарственных средств в микросомах печени и гидроксилировании дофамина с образованием норадреналина. Повышает активность амидирующих ферментов, участвующих в синтезе окситоцина, адренокортикотропного гормона и холецистокинина. Участвует в стероидогенезе в надпочечниках.
Фармакокинетика
Парацетамол
Абсорбция — высокая. Время, необходимое для достижения максимальной концентрации (ТСmax) — 30-60 мин; максимальная концентрация (Сmax) — 5-20 мкг/мл. Связывание с белками плазмы — 15%. Проникает через гематоэнцефалический барьер (ГЭБ).
Метаболизируется в печени по трем основным путям: конъюгация с глюкуронидами, конъюгация с сульфатами, окисление микросомальными ферментами печени. В последнем случае образуются токсичные промежуточные метаболиты, которые впоследствии конъюгируют с глутатионом, а затем с цистеином и меркаптуровой кислотой. Основными изоферментами цитохрома Р450 для данного пути метаболизма являются изофермент CYP2E1 (преимущественно), CYP1A2 и CYP3A4 (второстепенная роль). При дефиците глутатиона эти метаболиты могут вызывать повреждение и некроз гепатоцитов.
Дополнительными путями метаболизма являются гидроксилирование до 3-гидроксипарацетамола и метоксилирование до 3-метоксипарацетамола, которые впоследствии конъюгируют с глюкуронидами или сульфатами.
Конъюгированные метаболиты парацетамола (глюкурониды, сульфаты и конъюгаты с глутатионом) обладают низкой фармакологической (в т.ч. токсической) активностью. Т1/2 — 1-4 ч. Выводится почками в виде метаболитов, преимущественно конъюгатов, только 3% в неизмененном виде.
У пожилых пациентов снижается клиренс препарата и увеличивается Т1/2.
Фенирамин
Хорошо всасывается в пищеварительном тракте. Т1/2 из плазмы крови составляет от 1 до 1.5 ч. Выводится из организма преимущественно через почки.
Аскорбиновая кислота
Хорошо всасывается в пищеварительном тракте. Время создания максимальной терапевтической концентрации (ТСmax) после приема внутрь — 4 ч. Метаболизируется преимущественно в печени. Выводится почками, через кишечник, с потом, в неизмененном виде и в виде метаболитов.
Связывание с белками плазмы — 25%. Легко проникает в лейкоциты, тромбоциты, а затем — во все ткани; наибольшая концентрация достигается в железистых органах, лейкоцитах, печени и хрусталике глаза; проникает через плацентарный барьер. Концентрация аскорбиновой кислоты в лейкоцитах и тромбоцитах выше, чем в эритроцитах и в плазме. При дефицитных состояниях концентрация в лейкоцитах снижается позднее и более медленно и рассматривается как лучший критерий оценки дефицита, чем концентрация в плазме.
Метаболизируется преимущественно в печени в дезоксиаскорбиновую и далее в щавелевоуксусную кислоту и аскорбат-2-сульфат.
Выводится почками, через кишечник, с потом, грудным молоком в неизмененном виде и в виде метаболитов. Выводится при гемодиализе.
Показания препарата
Фервекс®
В качестве симптоматической терапии при острых респираторных вирусных инфекциях для облегчения следующих симптомов:
- ринорея, заложенность носа;
- головная боль;
- повышенная температура тела;
- слезотечение;
- чиханье.
Режим дозирования
Внутрь, по 1 пакетику 2-3 раза/сут. Перед применением содержимое пакетика необходимо растворить в стакане (200 мл) теплой воды. Максимальная продолжительность лечения — 5 дней.
Максимальная суточная доза парацетамола при массе тела более 50 кг не должна превышать 4 г (или 8 пакетиков препарата Фервекс®); у детей или пациентов с массой тела 40-50 кг максимальная суточная доза парацетамола не должна превышать 3 г, при массе тела менее 40 кг — не более 2 г.
Интервал между приемами препарата должен быть не менее 4 ч.
У пациентов с нарушениями функции почек (клиренс креатинина (КК) <10 мл/мин) интервал между приемами препарата должен составлять не менее 8 ч.
У пациентов с хроническими или декомпенсированными заболеваниями печени, у пациентов с печеночной недостаточностью, хроническим алкоголизмом, у истощенных больных и при обезвоживании суточная доза парацетамола не должны превышать 3 г.
Не следует принимать препарата более 3 дней в качестве жаропонижающего средства и более 5 дней в качестве обезболивающего средства.
Если не наблюдается облегчения симптомов в течение 5 дней после начала приема препарата, сохраняется повышенная температура тела или после первоначального снижения она внезапно повышается снова, пациенту необходимо обратиться к врачу.
Побочное действие
Препарат хорошо переносится в рекомендованных дозах. При применении препарата отмечались указанные ниже побочные эффекты (частота не установлена).
Со стороны системы кроветворения: анемия, лейкопения, агранулоцитоз, тромбоцитопения.
Со стороны иммунной системы: аллергические реакции (эритема, кожная сыпь, зуд, отек Квинке, анафилактический шок).
Со стороны нервной системы: сонливость, спутанность сознания, галлюцинации, нарушение концентрации внимания (чаще — у пожилых пациентов), возбуждение, нервозность, бессонница, координационная дисфункция, тремор.
Со стороны органа зрения: нарушение аккомодации.
Со стороны сердечно-сосудистой системы: ощущение сердцебиения, ортостатическая гипотензия, головокружение.
Со стороны пищеварительной системы: сухость во рту, тошнота, рвота, боль в животе, запор.
Со стороны мочевыделительной системы: нарушение мочеиспускания.
При появлении побочных реакций пациенту необходимо прекратить прием препарата и обратиться к врачу.
Противопоказания к применению
- эрозивно-язвенные поражения ЖКТ (в фазе обострения);
- печеночная недостаточность;
- закрытоугольная глаукома;
- задержка мочи, связанная с заболеваниями предстательной железы и нарушениями мочеиспускания;
- портальная гипертензия;
- алкоголизм;
- фенилкетонурия;
- глюкозо-галактозная мальабсорбция, дефицит сахаразы/изомальтазы, непереносимость фруктозы;
- детский возраст (до 15 лет);
- беременность (безопасность не изучена);
- период лактации (безопасность не изучена);
- повышенная чувствительность к парацетамолу, аскорбиновой кислоте, фенирамину или любому другому компоненту препарата.
С осторожностью: почечная недостаточность, врожденные гипербилирубинемии (синдромы Жильбера, Дубина-Джонсона и Ротора), вирусный гепатит, алкогольный гепатит, пожилой возраст, сахарный диабет.
Применение при беременности и кормлении грудью
Адекватных и хорошо контролируемых исследований препарата Фервекс® у беременных женщин не проводилось, поэтому применение препарата у данной группы пациентов не рекомендуется.
Неизвестно, проникают ли активные вещества препарата в грудное молоко. Препарат не следует применять в период лактации.
Применение при нарушениях функции печени
С осторожностью следует применять препарат при печеночной недостаточности, врожденных гипербилирубинемиях (синдромы Жильбера, Дубина-Джонсона и Ротора), при вирусном гепатите, алкогольном гепатите.
Применение при нарушениях функции почек
С осторожностью следует применять препарат при почечной недостаточности.
Применение у детей
Противопоказано применение препарата в детском возрасте до 15 лет.
Применение у пожилых пациентов
С осторожностью следует применять препарат у пациентов пожилого возраста.
Особые указания
Фервекс® не следует применять одновременно с другими препаратами, содержащими парацетамол.
Во избежание токсического поражения печени парацетамол не следует сочетать с приемом алкогольных напитков, а также принимать лицам, склонным к хроническому потреблению алкоголя.
Риск развития повреждений печени возрастает у больных с алкогольным гепатозом.
При превышении рекомендованных доз и при длительном применении может появиться психическая зависимость от препарата.
Во избежание передозировки парацетамола следует убедиться, что суммарная суточная доза парацетамола, содержащегося во всех лекарственных препаратах, принимаемых пациентом, не превышает 4 г.
Аскорбиновая кислота как восстановитель может искажать результаты различных лабораторных тестов (содержание в крови и моче глюкозы, билирубина, активности печеночных трансаминаз и ЛДГ).
В случае приема препарата пациентами с сахарным диабетом или находящимися на диете с пониженным содержанием сахара, следует учитывать, что в каждом пакетике содержится 11.555 г сахарозы, что соответствует 0.9 ХЕ.
Влияние на способность к управлению транспортными средствами и механизмами
Учитывая возможность развития таких нежелательных эффектов, как сонливость и головокружение, в период лечения препаратом рекомендуется воздержаться от управления автомобилем и механизмами.
Передозировка
Симптомы, обусловленные действием парацетамола
При передозировке возможна интоксикация, особенно у пожилых пациентов, детей, пациентов с заболеваниями печени (вызванных хроническим алкоголизмом), у пациентов с нарушением питания, а также у пациентов, принимающих индукторы микросомальных ферментов печени, при которой может развиться молниеносный гепатит, печеночная недостаточность, холестатический гепатит, в указанных выше случаях — иногда с летальным исходом. Порог передозировки у этих категорий пациентов может быть ниже. Клиническая картина острой передозировки развивается в течение 24 ч после приема парацетамола.
Симптомы: желудочно-кишечные расстройства (тошнота, рвота, снижение аппетита, ощущение дискомфорта в брюшной полости и (или) абдоминальная боль), бледность кожных покровов. При одномоментном введении взрослым 7.5 г и более или детям более 140 мг/кг происходит цитолиз гепатоцитов с полным необратимым некрозом печени, развитием печеночной недостаточности, метаболического ацидоза и энцефалопатии, которые могут привести к коме и летальному исходу. Через 12-48 ч после введения парацетамола отмечается повышение активности микросомальных ферментов печени, ЛДГ, концентрации билирубина и снижение концентрации протромбина. Клинические симптомы повреждения печени проявляются через 2 сут после передозировки препарата и достигают максимума на 4-6 день.
Лечение: немедленная госпитализация. Определение количественного содержания парацетамола в плазме крови перед началом лечения в как можно более ранние сроки после передозировки. Введение донаторов SH-групп и предшественников синтеза глутатиона — метионина и ацетилцистина — наиболее эффективно в первые 8 ч. Необходимость в проведении дополнительных терапевтических мероприятий (дальнейшее введение метионина, в/в введение ацетилцистеина) определяется в зависимости от концентрации парацетамола в крови, а также времени, прошедшего после его введения. Симптоматическое лечение. Лабораторные исследования активности микросомальных ферментов печени следует проводить в начале лечения и затем — каждые 24 ч. В большинстве случаев активность микросомальных ферментов печени нормализуется в течение 1-2 недель. В очень тяжелых случаях может потребоваться пересадка печени.
Симптомы, обусловленные действием аскорбиновой кислоты
Симптомы: тошнота, диарея, раздражение слизистой оболочки ЖКТ, метеоризм, абдоминальная боль спастического характера, учащенное мочеиспускание, нефролитиаз, бессонница, раздражительность, гипогликемия.
Лечение: немедленно прекратить применение препарата и обратиться к врачу. Лечение симптоматическое, форсированный диурез.
Симптомы, обусловленные действием фенирамина
Симптомы: судороги, нарушения сознания, кома.
Лечение: немедленно прекратить применение препарата и обратиться к врачу. Рекомендуется промывание желудка, прием энтеросорбентов (активированный уголь, лигнин гидролизный), в/в или пероральное введение антидота ацетилцистеина (при возможности, в первые 10 ч после передозировки), симптоматическое лечение.
Лекарственное взаимодействие
Этанол усиливает седативное действие антигистаминных препаратов (фенирамин), поэтому следует избегать его приема в период лечения препаратом Фервекс®. Кроме того, этанол при одновременном применении с фенирамином способствует развитию острого панкреатита.
Фенирамин усиливает действие седативных препаратов: производных морфина, барбитуратов, бензодиазепиновых и других транквилизаторов, нейролептиков (мепробамат, производные фенотиазина), антидепрессантов (амитриптилин, миртазапин, миансерин), гипотензивных препаратов центрального действия, седативных средств, относящихся к группе блокаторов гистаминовых H1-рецепторов, баклофена; при этом не только возрастает седативный эффект, но и повышается риск развития побочных эффектов препарата (задержка мочи, сухость во рту, запоры).
Следует учитывать возможность усиления центральных м-холиноблокирующих эффектов при применении в комбинации с другими препаратами, обладающими м-холиноблокирующей активностью (другие блокаторы гистаминовых Н1-рецепторов, трициклические антидепрессанты, нейролептики фенотиазинового ряда, спазмолитические и противопаркинсонические средства с м-холиноблокирующей активностью, дизопирамид).
При использовании препарата вместе с индукторами микросомального окисления: барбитуратами, трициклическими антидепрессантами, противосудорожными средствами (фенитоин), флумецинолом, фенилбутазоном, рифампицином и этанолом, значительно повышается риск гепатотоксического действия (за счет входящего в состав парацетамола).
ГКС при одновременном применении увеличивают риск развития глаукомы.
Прием одновременно с салицилатами повышает риск нефротоксического действия.
При одновременном применении с хлорамфениколом (левомицетином) токсичность последнего возрастает.
Парацетамол усиливает действие антикоагулянтов непрямого действия и снижает эффективность урикозурических препаратов.
Аскорбиновая кислота повышает концентрацию в крови бензилпенициллина и тетрациклинов; в дозе 1 г/сут повышает биодоступность этинилэстрадиола (в т.ч. входящего в состав пероральных контрацептивов).
Аскорбиновая кислота улучшает всасывание в кишечнике препаратов железа (переводит трехвалентное железо в двухвалентное); может повышать выведение железа при одновременном применении с дефероксамином.
Аскорбиновая кислота снижает эффективность гепарина и непрямых антикоагулянтов.
При одновременном применении с ацетилсалициловой кислотой (АСК) повышается выведение с мочой аскорбиновой кислоты и снижается выведение АСК. АСК снижает абсорбцию аскорбиновой кислоты примерно на 30%. Увеличивает риск развития кристаллурии при лечении салицилатами и сульфаниламидами короткого действия, замедляет выведение почками кислот, увеличивает выведение лекарственных средств, имеющих щелочную реакцию (в т.ч. алкалоидов), снижает концентрацию в крови пероральных контрацептивов.
Аскорбиновая кислота повышает общий клиренс этанола, который, в свою очередь, снижает концентрацию аскорбиновой кислоты в организме.
Лекарственные средства хинолинового ряда, кальция хлорид, салицилаты, ГКС при длительном применении истощают запасы аскорбиновой кислоты.
При одновременном применении аскорбиновая кислота уменьшает хронотропное действие изопреналина.
При длительном применении или применении в высоких дозах аскорбиновая кислота может препятствовать взаимодействию дисульфирама и этанола.
В высоких дозах аскорбиновая кислота повышает выведение мексилетина почками.
Барбитураты и примидон повышают выведение аскорбиновой кислоты с мочой.
Аскорбиновая кислота уменьшает терапевтическое действие нейролептиков — производных фенотиазина, канальцевую реабсорбцию амфетамина и трициклических антидепрессантов.
Условия хранения препарата Фервекс®
Препарат следует хранить в недоступном для детей месте при температуре от 15° до 25°C.
Срок годности препарата Фервекс®
Срок годности — 3 года. Не использовать препарат после истечения срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается без рецепта.
БРИСТОЛ-МАЙЕРС СКВИББ
(США)
|
BRISTOL-MYERS SQUIBB Представительство в России |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
-
Антигриппин-Экспресс
(ФармФирма Сотекс, Россия) -
ОРВИС® Флю
(ЭВАЛАР, Россия) -
Ринза® кидс
(ДЖЕЙТНЛ, Россия) -
Сафистон Флю
(АТОЛЛ, Россия) -
Фасторик
(ДЖОДАС ЭКСПОИМ, Россия) -
Фервекс® (без сахара)
(UPSA, Франция) -
Фервекс® для детей
(UPSA, Франция) -
Флювикс детский
(Березовский фармацевтический завод, Россия) -
Флювикс Колд
(Березовский фармацевтический завод, Россия)
Все аналоги
30.05.2010г.
Препарат железа для внутривенного введения. Состоит из сахарата железа, глюконата кобальта и раствора углеводов. В 1 мл содержит 0,02 г железа и 0,00009 г (0,09 мг) кобальта. Прозрачная жидкость красновато-коричневого цвета, сладкого вкуса. Применяют при лечении гипохромных анемий различной этиологии, особенно при плохой переносимости и недостаточной всасываемости препаратов железа, вводимых per os.
Наличие в препарате кобальта способствует усилению эритропоэза. Вводят ферковен в вену по одному разу в день ежедневно в течение 10—15 дней; в первые 2 инъекции вводят по 2 мл, затем — по 5 мл. Введение производят медленно (в течение 8—10 минут). Дефицит железа в организме и количество препарата, необходимое на курс лечения, можно рассчитать более точно, исходя из следующей формулы: дефицит железа в миллиграммах равен [вес больного в килограммах * 2,5] * [16,5 — (1,3 * содержание гемоглобина в крови больного в граммах на 100 мл)].
При определении гемоглобина по Сали расчет в граммах производят следующим образом. Так как в 1 мл раствора содержится 20 мг железа, то больной должен получить на курс 67,5 мл.
Сверх тех количеств, которые получаются при расчете по указанной формуле, вводить препарат не следует. Для поддержания эффекта, достигнутого введением ферковена, в дальнейшем применяют препараты железа per os.
При первых введениях в вену ферковена и при передозировке препарата могут наблюдаться побочные явления: гиперемия лица, шеи, чувство сжатия в грудной клетке, боли в пояснице; побочные явления снимаются при введении под кожу 1 мл 1% раствора омнопона и 0,5 мл 0,1% атропина. Ферковен следует применять только в стационаре.
Препарат противопоказан при заболеваниях печени, коронарной недостаточности, гипертонической болезни II и III стадии.
Форма выпуска: ампулы и герметически закрытые флаконы по 5 мл. Сохраняют в защищенном от света месте при комнатной температуре.
Rp. Fercoveni 5,0
D. t. d. N. 6 in amp.
S. По 2—5 мл в вену (вводить медленно!).
«Лекарственные средства», М.Д.Машковский
Читайте далее:
- Малые дозы йода
- Препараты, содержащие кобальт
- Йод (Рецепт)
- Йодид калия
- Таблетки йодида калия
- Настойка йодная 5%
- Раствор люголя (Solutio Lugoli)
- Сайодин (Saiodinum)
- Йод-гиперсол (Iod-hypersolum)
- Препараты, содержащие железо
- Железо восстановленное (При секреторной недостаточности желудка)
- Феррогематоген (Ferrohaematogenum)
- Гемостимулин (Haemostimulinum)
- Карбонат закиси железа с сахаром
- Сульфат закиси железа
- Настойка железа яблочнокислого (Tinctura ferri pomati)
- Сироп алоэ с железом (Sirupus Aloes cum ferro)
