Технические характеристики — Сетал-1В Электрокардиостимулятор наружный однокамерный
Предназначен для генерирования импульсов электрического тока с целью навязывания искусственного ритма сердцу. Основной областью применения электрокардиостимулятора является практическая медицина, то есть стационарные лечебные учреждения, реанимационные кардиологические отделения.
Кардиостимулятор позволяет проводить следующие виды стимуляции в эндокардиальном режиме:
— асинхронный (AOO, VOO);
— деманд (AAI, VVI).
Электрокардиостимулятор позволяет проводить два вида стимуляции в эндокардиальном режиме:
— Лечебная электрокардиостимуляция:
— временная стимуляция желудочков при угрожающих жизни брахикардиях, а также при А-V блокадах;
— Диагностическая электрокардиостимуляция:
— подбор медикаментозных средств при различных видах нарушений ритма сердца; определение параметров стимулирующих импульсов при имплантации постоянного водителя ритма.
Технические характеристики
| Диапазон частот импульсов в асинхронном режиме: | от 30 до 250 имп/мин +0,1 имп/мин. |
| Диапазон частот импульсов в режиме деманд: | от 30 до 180 имп/мин +0,1 имп/мин. |
| Шаг установки частоты | 1 имп/мин +0,1 имп/мин. |
| Длительность импульсов: | 1,5 мс ±0.01 мс. |
| Амплитуда импульсов тока: | от 0 до 15мА, +0,4 ма. |
| Шаг установки амплитуды тока: | 1 мА. |
| Форма импульсов: | прямоугольная, однополярная; |
| Порог срабатывания кардиостимулятора в режиме деманд: | от 0,5 мВ до 10 мВ. |
| В режиме деманд осуществляется подсчет количества навязанных стимулирующих импульсов по отношению к общему числу сердечных сокращений. Результат выводится на индикатор в виде процентов. Каждую минуту значения обновляются | |
| Когда батарея питания разряжается, прибор запускает звуковое оповещение через каждые 5 минут. Даже при разряженной батарее электрокардиостимулятор может функционировать не менее 6 часов. | |
| Время непрерывной работы | 300 ч |
| Питание | 2 батареи типа АА напряжением по 1,5В, емкостью 2400 мАч. |
| Конструкция кардиостимулятора обеспечивает: | |
| — В режиме деманд осуществляется подсчет количества навязанных стимулирующих сердечных сокращений по отношению их к общему числу и вывод результата на дисплей, каждую минуту значения обновляются. | в виде % |
| — Автоматическое включение энергосберегающего режима с фиксацией параметров стимуляции, и пробуждением по нажатию любой клавиши | |
| — Контроль расхода питания батареи; | |
| — Блокировка от случайного отключения электрокардиостимулятора. | |
| Габариты: | 150мм х 75мм х 30 мм. |
| Масса: | 250 г |
| При разряде батареи кардиостимулятор выдает звуковое предупреждение каждые 5 мин, при этом сохраняет свою работоспособность | не менее 6 ч |
| Рефрактерный период: | 320 мс±0.1 мс. |
Для этого товара отзывов пока нет.
Будьте первыми.
К этому товару дополнений нет
В ПОМОЩЬ ПРАКТИЧЕСКОМУ ВРАЧУ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ (ЭКС) Состав рабочей группы по разработке рекомендаций: Л.А.Бокерия, А.Ш.Ревишвили, О.Л.Гордеев, А.Ю.Григорьев, К.В.Давтян, Д.Ф.Егоров, А.М.Жданов, С.А.Зенин, В.А.Кузнецов, В.В.Купцов, Д.С.Лебедев, Н.Н.Ломидзе, Н.М.Неминущий, А.В.Певзнер, Е.А.Покушалов, С.В.Попов, Ф.Г.Рзаев
Исходя из понимания исключительной важности наличия номенклатурных документов, относящихся к разработке показаний к имплантации электрокардиостимуляторов и антиаритмических устройств, рабочая группа ВНОА (Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции) разработала рекомендации по имплантации кардиостимуляторов и антиаритмических устройств при приобретенной атрио-вентрикулярной (АВ) блокаде, при АВ-блокаде после инфаркта миокарда, хронической би- и трифасцику-лярной блокаде, дисфункции синусно-предсердного узла, синдроме повышенной чувствительности каро-тидного синуса и нейрососудистых синдромах, а также показания для проведения электрофизиологических процедур и деструкции аритмогенных очагов у взрослых пациентов и детей с тахиаритмиями.
При разработке рекомендаций авторы использовали свой более чем 35-летний опыт по имплантации антиаритмических устройств и проведения электрофизиологических исследований (ЭФИ) в специализированных лабораториях, а также рекомендации по проведению подобных операций в странах Европы и Северной Америки. В основу данных рекомендаций по имплантации кардиостимуляторов и антиаритмических устройств легли рекомендации Комитета экспертов Минздрава РФ и РАМН по имплантируемым антиаритмическим устройствам и электрофизиологии (1993, 1998, 2005 годы), а также рекомендации по проведению данных процедур рабочих групп Всероссийского научного общества аритмологов, ассоциации сердечно-сосудистых хирургов, Всероссийского научного общества кардиологов, Европейского общества кардиологов, Европейского общества аритмологов, Французского общества кардиологов, Канадского общества аритмологов, Национального общества сердца Великобритании, Американского колледжа кардиологов, Американской ассоциации сердца (1984, 1991, 1998, 2002, 2007 и 2008 годы).
Предлагаемые рекомендации определяют показания и противопоказания к имплантации современных моделей антиаритмических устройств и проведению ЭФИ, определяют тактику поведения специалиста при отборе на процедуру и операцию больных с тахи- и брадиаритмиями, что предполагает обязательную сертификацию центров, проводящих имплантацию антиаритмических устройств, и лабораторий для проведения интервенционных процедур при аритмиях сердца.
До внедрения в клиническую практику методов постоянной электрокардиостимуляции ежегодная смертность больных с приобретенной полной пред-сердножелудочковой блокадой превышала 50% [1, 2]. Первый электрокардиостимулятор (ЭКС) был имплан-
тирован А.Сенингом в 1958 году, и эта дата стала точкой отсчета для клинического внедрения высокоэффективного и жизнеспасающего метода лечения больных с брадиаритмиями, так как электрокардиостимуляция позволяет снизить летальность, число госпитализаций в стационары, устранить симптомы болезни и резко улучшить качество жизни больных с брадиаритмиями. В СССР первый серийный имплантируемый ЭКС был разработан и имплантирован в клинике факультетской хирургии Второго Московского медицинского института им. Н.И.Пирогова [1, 2].
В связи с широким распространением в ряде стран мира ЭКС, работающих в бифокальном режиме (DDD) (так называемая физиологическая стимуляция), и обнадеживающим клиническим опытом применения ЭКС, меняющих частоту ритмовождения в ответ на физическую или эмоциональную нагрузку (УУШ, DDDR) (так называемая частотно-адаптированная стимуляция), актуальность проблемы показаний к имплантации и выбора режима стимуляции сердца существенно расширилась [16,17]. Можно констатировать, что современные показания более индивидуализированы, чем предыдущие. Поэтому во многих странах мира в начале XXI века рабочими группами по аритмиям сердца были пересмотрены или вновь сформулированы показания и выбор режима стимуляции в зависимости от вида кардиальной патологии.
Данные рекомендации включают в себя расширенные разделы по выбору ЭКС приборов для сердечной ресинхронизации и ИКД, оптимизации технологий, стоимости, последующего наблюдения. Раздел последующего наблюдения короткий и включен с целью полноты рекомендаций, хотя по ряду обстоятельств характер и частота последующих наблюдений зависят от типа имплантируемого устройства. Важность наблюдения за пациентом после имплантации антиаритмического устройства трудно переоценить, так как оптимальную пользу имплантированное устройство приносит, когда подстраивается под меняющиеся клинические условия [28].
НОМЕНКЛАТУРА И СОВРЕМЕННАЯ ТЕХНОЛОГИЯ ЭКС
В международной практике используется 5-бук-венный номенклатурный код, который представляет собой совместную разработку рабочих групп Североамериканского общества по стимуляции и электрофизиологии (NASPE) и Британской группы по стимуляции и электрофизиологии (BPEG), известный как общий код NBG-NASPE/BPEG (таблица 1а). Как правило, используют первые 3 буквы, а буква R (IV позиция) используется для программируемых ЭКС с изменяющейся частотой ритмовождения — VVIR, DDDR
(адаптация по частоте). 5-я буква в коде NBG связана с антитахикардитическими функциями.
В октябре 2001 г. рабочие группы Североамериканского общества по стимуляции и электрофизиологии (NASPE) и Британской группы по стимуляции и электрофизиологии (BPEG) приняли обновленный 5-буквенный номенклатурный код для антибрадикарди-тических устройств, приведенный в таблица 1б (D.L. Hayes et al., 2001).
Первые модели ЭКС работали в асинхронном режиме (VOO) и проводили стимуляцию с фиксированной частотой. В 1965 году появились первые модели ЭКС, способные определять собственную деятельность сердца и работать в режиме demand, т. е. «по требованию» (VVI). Мультипрограммируемые стимуляторы обеспечили широкий набор характеристик, необходимых для изменения электрических параметров ЭКС при изменяющемся взаимодействии мышцы сердца и самого ЭКС. Следующее поколение стимуляторов обеспечило физиологический характер электрокардиостимуляции (режимы VAT, VDD, AAI и DDD) путем автоматического контроля частоты и/или увеличения степени наполнения желудочков сердца за счет синхронного сокращения предсердий (вклад предсердий) [15-18]. Физиологическая стимуляция нормализует сердечный выброс и значительно увеличивает функциональные возможности пациента. Интересно, что первый клинический опыт приме-
нения физиологических стимуляторов относится к 1962 году, когда пытались использовать Р-синхрони-зированные ЭКС. Однако бывшие тогда в наличии и работавшие в режиме VAT стимуляторы не обладали способностью определять желудочковую активность. Поэтому желудочковая экстрасистола вполне могла привести к желудочковой стимуляции в уязвимый период. Для исключения возможных проблем, связанных со стимуляцией в режиме VAT, были созданы более совершенные ЭКС, работающие в режиме VDD. Недостатком такого режима стимуляции является отсутствие возможности стимуляции предсердий при отсутствии предсердной активности. Последнее исключает положительный фактор предсердно-желу-дочковой синхронизации.
В настоящее время наиболее совершенная система стимуляции — это полностью автоматизированная электростимуляция сердца в режиме DDD, позволяющая сохранить предсердно-желудочковую синхронизацию при урежении ритма сердца ниже установленного предела. Однако и этот режим недостаточен при хро-нотропной некомпетентности сердца. Таким примером является синдром слабости синусно-предсердного узла (СССУ), когда не отмечается спонтанного учащения сердечного ритма в ответ на физиологическую нагрузку. Только включение в электронную систему ЭКС специальных детекторов (сенсоров), реагирующих на различные сигналы, отличные от Р-волны, и увеличи-
Таблица 1а.
Единый код ЭКС — номенклатура NBG-NASPE/BPEG (1987 г.)
Позиция буквы в номенклатуре кода
I II III IV V
Функциональное значение буквы в номенклатуре кода
Камера (ы) стимулируемая (ые) Камера (ы) воспринимающая (ие) Ответ на восприятие Программируемость Антитахиаритми-ческие функции
0 — нет А — предсердие V — желудочек D — обе камеры (Л+У) 0 — нет А — предсердие V — желудочек D — обе камеры (Л+У) 0 — нет Т — триггер I — подавление D — обе функции (Т +1) 0 — нет Р — простое программирование С — коммуникативность К — модуляция частоты 0 — нет Р — антитахикардити-ческая стимуляция Б — дефибрилляция D — двойная функция (Р+Б)
Таблица 1б.
Обновленный единый код ЭКС — номенклатура NBG-NASPE/BPEG (2001 г.)
Позиция буквы в номенклатуре кода
I II III IV V
Функциональное значение буквы в номенклатуре кода
Камера (ы) стимулируемая (ые) Камера (ы) воспринимающая (ие) Ответ на восприятие Модуляция частоты Многокамерная стимуляция
0 — нет А — предсердие V — желудочек D — обе камеры (Л+У) 0 — нет А — предсердие V — желудочек D — обе камеры (Л+^ 0 — нет Т — триггер I — подавление D — обе функции (Т +1) 0 — нет R — модуляция частоты 0 — нет А — предсердие V — желудочек D- обе камеры (Л+^
Б — однокамерная (Л или V) Б — однокамерная (Л или V)
вающие соответственно частоту, оптимизируют физиологическую стимуляцию.
Ряд зарубежных фирм используют или использовали сенсоры, реагирующие на нагрузку (механические сотрясения — «Medtronic»), частоту дыхания и минутный объем дыхания («Telectronics»), коэффициент dp/dt правого желудочка («Medtronic»), изменение температуры центральной венозной крови («Biotronik»), вызванный интервал Q-Т («Vitatron») и другие параметры. Появились ЭКС, имеющие по два сенсора в одном устройстве, что позволяет нивелировать недостатки односенсорного ЭКС. Новым в этом направлении стало использование сочетания функции адаптации по частоте с двухкамерным (секвенциальным) режимом стимуляции. Комбинация сенсора, работающего по нагрузке и позволяющего быстро достичь оптимальной частоты, и второго сенсора, работающего по интервалу Q-Т или минутному объему вентиляции (при продолжении нагрузки или в фазе восстановления), позволяют добиться оптимальной частоты ритма в любую фазу нагрузки [16, 24, 25].
Самые последние модели ЭКС, работающие в режиме DDDR, способны определять наличие у больного фибрилляции и трепетания предсердий и автоматически переключаться на другой, безопасный и тоже
Рекомендации по выбору модели ЭКС согласно опреде
частотно адаптирующийся (желудочковый) режим стимуляции (VVIR) — так называемый режим «switch mode» («переключение режима»). Таким образом, исключается возможность поддержания наджелудочко-вой тахиаритмии [24, 25].
Данные рекомендации посвящены правильному подходу к имплантации кардиостимуляторов и кар-диовертеров-дефибрилляторов, но не к терапии аритмий. Тот факт, что применение ЭКС попадает в класс I рекомендаций (полезно и эффективно), не исключает других методов лечения, которые могут быть так же эффективны, как и другие клинические рекомендации [16, 17]. Данный документ обобщает основные подходы к лечению пациента с конкретным нарушением ритма сердца. Сопутствующие заболевания или прогноз по сопутствующим заболеваниям, а также ряд других условий, могут изменяться, и окончательный выбор остается за лечащим врачом.
ВЫБОР КАРДИОСТИМУЛЯТОРА
После принятия решения об имплантации ЭКС конкретному пациенту вторая главная задача клинициста — выбор оптимального стимулирующего устройства среди богатства электрокардиостимуляторов и электродов. Предстоит выбрать между одно- и двухкамер-
Таблица 2.
нным показаниям к электрокардиостимуляции
Дисфункция СПУ АВ-блокада Нейрогенные синкопе или синдром гиперчувствитель-нсти каротидного синуса
Окамерная предсердная стимуляция (ААГ) Интактность АВ-прове-дения и отсутствие риска развития АВ-блокады в будущем. Поддержание АВ-синхронизации во время стимуляции. Наличие частотной адаптации (при необходимости.) Неприемлема Неприемлема
Однокамерная желудочковая стимуляция (УУГ) Нет необходимости поддержания АВ-синхронизации во время стимуляции. Наличие частотной адаптации (при необходимости). Хроническая фибрилляция предсердий или другие предсердные тахиаритмии или нет необходимости поддержания АВ-синхрони-зации. Наличие частотной адаптации (при необходимости). Хроническая фибрил-ляция предсердий или другие предсердные тахиаритмии. Наличие частотной адаптации (при необходимости).
Двухкамерная стимуляция (DDD) Поддержание АВ-синх-ронизации Подозрение на нарушение АВ-проведения или высокий риск развития АВ-блокады в будущем. Наличие частотной адаптации (при необходимости). Наличие частотной адаптации (при желании). Поддержание АВ-синхронизации. Стимуляция предсердий. Наличие синусовогоритма. Наличие частотной адаптации (при необходимости).
Моноэлектродные желудочковые ЭКС с детекцией предсердной активности (VDD) Неприемлема Нормальная функция СПУ, и нет необходимости в стимуляции предсердий. Желание ограничить количество эндокардиальных электродов. Неприемлема
ным ЭКС, униполярной и биполярной конфигурацией электрода, наличием и типом сенсора для частотной адаптации, некоторыми дополнительными функциями, например автоматическая смена режима, размер ЭКС, емкость батареи, стоимость, диагностические возможности. Для выбора электрода следует отдать предпочтение той или иной полярности, типу изоляционного материала, механизму фиксации (активный или пассивный) и наличию стероидного включения. Некоторые модели электродов обладают низким (300-500 Ом) сопротивлением (импедансом), другие — высоким (более 1000 Ом), что требует подбора ЭКС с той или иной емкостью батареи. Другие обстоятельства, влияющие на выбор стимулирующей системы, — это умение и возможности врача при программировании, а также техническое оснащение стационара [24, 25].
После имплантации ЭКС врачу предстоит подбор и программирование некоторых параметров ЭКС. В современных однокамерных ЭКС программируемые параметры включают выбор режима стимуляции, нижний уровень частоты, длительности импульса, амплитуды, чувствительности и рефрактерного периода. В двухкамерных ЭКС кроме этого программируется максимальный уровень частоты, АВ-задержка и так далее. Частотноадаптивные ЭКС содержат программу для регуляции соотношения чувствительности и частоты стимуляции и ограничения по максимальной детектируемой частоте стимуляции. С появлением более сложных систем электрокардиостимуляции оптимальное программирование становится еще более сложным и специфичным, что требует особых знаний врача [16, 18, 28].
Подробности программирования ЭКС в этом документе не обсуждаются. Фундаментальная проблема врача — оптимальный выбор стимулирующей системы: однокамерная стимуляция желудочка, однокамерная стимуляция предсердия или двухкамерная стимуляция.
В таблице 2 кратко изложены принципы выбора различных ЭКС в зависимости от показаний к электрокардиостимуляции. Важная задача в выборе стимулирующей системы — предупредить прогрессирование нарушения автоматизма и проводимости, выбрать систему, которая наилучшим образом предотвратит эти нарушения. В связи с этим целесообразен подбор ЭКС с большими возможностями программирования, чем это необходимо на момент имплантации. Так, у пациента с дисфункцией СПУ и па-роксизмальной фибрилляцией предсердий в дальнейшем может развиться АВ-блокада (результат прогрессирования заболевания,
приема препаратов или катетерной абляции), а при наличии двухкамерного ЭКС возможно переключение режима стимуляции.
МОНОЭЛЕКТРОДНЫЕ СИСТЕМЫ УББ
Несмотря не преимущества частотноадаптивных стимулирующих систем, нормально функционирую-
Дисфункция СПУ
Синусовая брадикардия
блокада АВУ
Да
Нет
Имеется хронотропная дисфункция
Имеется предсердная тахиаритмия
Существует или отсутствует хронотропная дисфункция
Существует или отсутствует хронотропная дисфункция
Отсутствует предсердная тахиаритмия
ОООН+функция минимизация желудочковой стимуляции (класс На, доказанность С)
□ □ЕШ+функция
минимизация желудочковой стимуляции + функция антитахи (класс ИЬ, доказанность С)
Отсутствует предсердная тахиаритмия
ДАШ
(класс I, доказанность С)
ОООИ+функция минимизация желудочковой стимуляции
(класс На, доказанность С)
ОООЛ+функция минимизация желудочковой стимуляции (класс I, доказанность С)
Схема №1. Выбор типа электрокардиостимулятора у пациентов с СССУ.
Схема №2. Выбор типа электрокардиостимулятора у пациентов с приобретенной атриовентрикулярной блокадой, хронической бифасцикулярной и трифасцикулярной блокадами.
щий СПУ осуществляет наилучшую хронотропную реакцию ритма сердца на физиологический стресс и нагрузку. Наиболее часто в этих целях используют двухкамерные ЭКС с отдельным предсердным электродом, детектирующим деполяризацию предсердий, и с желудочковым электродом. Моноэлектродные трансвенозные стимулирующие системы, способные осуществлять детекцию деполяризации предсердий, все больше приобретают популярность. Дистальный конец электрода устанавливается в правый желудочек, где осуществляется детекция желудочковой активности и стимуляция, а пара электродов, объединенная в проксимальной части единого электрода, располагается в полости правого предсердия для детекции его активности. Современные моноэлектродные системы в режиме VDD в 100% случаев не способны стимулировать предсердия, так как детектируемый предсердный сигнал меньшей амплитуды, чем в двухкамерных системах, и варьирует в зависимости от положения тела [24]. Поэтому моноэлектродные ЭКС в режиме VDD, с более простой техникой имплантации, являются альтернативой двухкамерной электрокардиостимуляции у пациентов с АВ-блокадой, не требующей стимуляции предсердий (нормальная хронотропная функция предсердий).
АВТОМАТИЧЕСКОЕ ПЕРЕКЛЮЧЕНИЕ РЕЖИМА СТИМУЛЯЦИИ (MODE SWITCH)
При появлении пароксизмов предсердной та-хиаритмии (трепетания, фибрилляции предсердий) у пациента со стимуляцией в режиме DDD или DDDR тахиаритмия может восприниматься как максимальная частота в запрограммированном диапазоне, что вызовет нежелательное учащение желудочковой стимуляции. В новые поколения двухкамерных ЭКС включены алгоритмы детекции частого, нефизиологичного пред-сердного ритма и автоматического включения другого режима стимуляции (например, DDI или DDIR). По окончании тахиаритмии ЭКС автоматически переключается на исходный режим стимуляции (DDD или DDDR). Эта функция особенно полезна у пациентов с АВ-блокадой и пароксизмальной фибрилляцией предсердий и позволяет использовать двухкамерные стимулирующие системы у этих пациентов. Большинство двухкамерных ЭКС, имплантируемых на данный момент в США, содержат в себе функцию автоматического переключения режима [16, 24].
ЭЛЕКТРОДЫ ДЛЯ СТИМУЛИРУЮЩИХ СИСТЕМ
При имплантации электрокардиостимуляторов чаще всего используются трансвенозные эндокарди-альные электроды, реже — эпикардиальные. Трансвенозные электроды могут быть биполярной или униполярной конфигурации. Преимуществом биполярных электродов является возможность избежать эпизодов миопотенциального ингибирования и стимуляции скелетных мышц, а наиболее ценное их свойство — совместимость с кардиовертерами-дефибрилляторами.
В качестве изоляционного материала при изготовлении электрода используется силиконовая резина или
полиуретан. Как показала практика, некоторые биполярные электроды с полиуретановой изоляцией часто выходили из строя из-за разрушения изоляции. По этой причине при изготовлении современных полиуретано-вых электродов стали использовать другие полимеры и изменили производственный процесс.
Электроды с активной фиксацией, содержащие на дистальном кончике электрода спиралеобразный винт для фиксации к эндокарду, являются альтернативой электродам с пассивной фиксацией. Активная фиксация позволяет использовать разные зоны эн-домиокарда для стимуляции. Например, если желудочковый электрод с пассивной фиксацией обычно помещается в верхушку желудочка, электрод с активной фиксацией может быть помещен в верхушку, в выводной тракт, приточный отдел правого желудочка, в межжелудочковую перегородку. Другое преимущество электродов с активной фиксацией — облегчение экстракции после давней имплантации. Недостаток такого электрода по сравнению с пассивной фиксацией — его более высокий хронический порог стимуляции, хотя использование стероидного включения эту разницу нивелирует.
Разработка новых электродов с более низким порогом стимуляции снижает затраты энергии батареи при стимуляции. Электроды со стероидным пропитыванием на дистальном конце содержат небольшую емкость с кортикостероидом, который постепенно высвобождается в пространство между электродом и эндокардом, тем самым уменьшая зону воспаления и фиброза. Таким образом, электроды со стероидным покрытием значительно снижают хронический порог стимуляции. Выгода использования стероидного пропитывания была продемонстрирована при использовании как эндокардиальных электродов с пассивной и активной фиксацией, так и эпикардиальных электродов. Подобные успехи по снижению порога стимуляции были достигнуты после модификации формы, размеров и состава электродов.
НАБЛЮДЕНИЕ ПАЦИЕНТОВ
С КАРДИОСТИМУЛЯТОРАМИ
После имплантации ЭКС требуется тщательное, динамическое наблюдение за пациентом [10, 28]. Ниже будут указаны лишь некоторые опубликованные формулировки и рекомендации NASPE, которое опубликовало серию сообщений о наблюдениях за пациентами с антибрадикардитическими устройствами [19, 27]. Канадская рабочая группа по электрокардиостимуляции также опубликовала свой подход о наблюдении за пациентами с электрокардиостимуляторами. Кроме того, администрация финансирования здравоохранения (HCFA, в настоящее время — центр правительственной программы медицинской помощи и медицинских услуг) разработала руководство по наблюдению за пациентами с устройствами, включенными в программу Medicare [15-19]. Динамическое наблюдение, лечение и реабилитация пациентов с непрерывно совершенствующимися имплантируемыми антиаритмическими устройствами становится совершенно новым направлением в кардиологии [28].
Много общих моментов выделено для наблюдения за электрокардиостимуляторами и кардиоверте-рами-дефибрилляторами. Перед выпиской пациента необходимо тестирование параметров, программированных во время имплантации. Эти параметры должны быть изменены в случае необходимости при последующих визитах пациента, с учетом результатов прочтения исходных данных, их тестирования и жалоб пациента. Программирование амплитуды, длины импульса и проведение диагностических функций, влияющих на состояние батареи ЭКС, не должно подвергать риску безопасность пациента. Оптимизирование функции ЭКС должно проводиться у каждого пациента индивидуально.
Частота и способ наблюдения зависят от множества факторов, в том числе от различных сердечно-сосудистых заболеваний и медицинских проблем, возраста ЭКС, географической отдаленности пациента от медицинского центра. Некоторые центры предпочитают использование транстелефонного монито-рирования для общего наблюдения с эпизодическим исследованием клинических данных. Другие центры выполняют большинство манипуляций для наблюдения за пациентами в условиях клиники. Автоматические функции, например автоматическая оценка порога стимуляции, широко используются в новых моделях электрокардиостимуляторов и облегчают наблюдение за отдаленно живущими пациентами. Однако автоматические функции неуниверсальны и не могут заменить индивидуальное программирование и тестирование, особенно сопровождающееся сбором анамнеза и осмотром пациента.
Наблюдение в условиях клиники включает в себя оценку клинического статуса пациента, состояния батареи, порогов стимуляции и длительности импульса, функцию чувствительности, целостность электрода, а также оптимизацию P-управляемой и сенсорной частоты сердечного ритма. Расписание осмотров в условиях клиники составляется на усмотрение врачей, наблюдающих этих пациентов. В руководстве, согласно документу HCFA от 1984 г., рекомендуется: пациентам с однокамерными ЭКС после имплантации необходимо явиться дважды в течение полугода, затем ежегодно. Пациентам с двухкамерными ЭКС после имплантации проводится осмотр дважды в течении 6 месяцев, затем один раз в полгода. Детям может потребоваться более частый контроль — каждые 3-4 месяца [28].
Руководство по транстелефонному мониторироваш
Руководство для транстелефонного мониториро-вания (ТТМ) эволюционировало с появлением новых стимулирующих систем и транстелефонных технологий. Законодательство в отношении ТТМ не пересматривалось с 1984 г. Цели ТТМ, как коммерческой, так и некоммерческой услуги, состоят в регистрации ЭКГ в покое и во время проведения магнитного теста. При ТТМ регистрации ЭКС в покое выявляют спонтанный ритм, перемежающуюся или постоянную электрокардиостимуляцию. Определяют ритм в предсердиях, например фибрилляция предсердий или синусовый ритм.
При наличии спонтанного ритма определяют адекватность функции чувствительности определенной камеры (или обеих камер сердца), в зависимости от вида ЭКС и режима стимуляции. Цели ТТМ при регистрации ЭКГ во время магнитного теста — выявление эффективности стимуляции определенной камеры (или обеих камер) в зависимости от вида ЭКС и режима стимуляции. Оценивают также магнитный тест, сравнивают частоту стимуляции с данными предыдущего ТТМ и выявляют изменения. Пациент должен знать о значениях частоты магнитного теста, характерной для появления признаков истощения батареи.
Если в модели ЭКС индикатором истощения батареи служит длительность импульса, этот параметр также оценивается во время ТТМ и сравнивается с предыдущим значением.
Если в модели ЭКС предусмотрена возможность транстелефонного исследования порога, например включение функции ТТМ-тестирование предельного порога, эта программа выполняется и анализируется.
Если во время магнитного теста двухкамерного ЭКС изменяется АВ-интервал, эти изменения должны быть продемонстрированы и верифицированы.
Распределение по классам предназначено для расположения показаний в таком порядке: Класс I: Условия, для которых имеются доказательства и/или общее мнение о полезности и эффективности диагностической процедуры или метода лечения. Класс II: Условия, для которых имеются противоречивые свидетельства и/или расхождение мнений относительно полезности/эффективности диагностической процедуры или метода лечения.
Класс IIa: Доказательства или мнения в пользу процедуры или метода лечения.
Класс IIb: Меньше данных за полезность/эффективность.
Таблица 3.
(1984 г.)
Руководство 1 Месяцы после имплантации ЭКС
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Однокамерная ЭКС 1 каждые 2 недели 2-36 каждые 8 недель 37 — истощение батареи каждые 4 недели
Двухкамерная ЭКС 1 каждые 2 недели 2-6 каждые 4 недели 7-36 каждые 8 недель 37 — истощение батареи каждые 4 недели
Руководство 2 Месяцы после имплантации ЭКС
Однокамерная ЭКС 1 каждые 2 недели 2-48 каждые 12 недель 49 — истощение батареи каждые 4 недели
Двухкамерная ЭКС 1 каждые 2 недели 2-30 каждые 12 недель 31-48 каждые 8 недель 49 — истощение батареи каждые 4 недели
Класс III: Условия, для которых имеются доказательства и/или общее согласие о том, что данная процедура или метод лечения не является полезным/эффективным, а в некоторых случаях может приносить вред. Класс А — доказательность считается наивысшей при наличии данных большого количества рандомизированных клинических исследований. Класс В — доказательность считается средней при ограниченном количестве рандомизированных исследований, нерандомизированных исследованиях или данных публикаций в журналах.
Класс С — доказательность считается низшей на основании мнения экспертов.
КАРДИОСТИМУЛЯЦИЯ ПРИ ПРИОБРЕТЕННОЙ АТРИОВЕНТРИКУЛЯРНОЙ БЛОКАДЕ У ВЗРОСЛЫХ
Атриовентрикулярная блокада подразделяется на первую, вторую и третью степень. Анатомически: на супра-, интра- и инфрагисовскую. Первая степень АВ-блокады определяется как аномальное удлинение PR-интервала более 0,2 сек. Вторая степень АВ-блокады подразделяется на первый и второй тип. Первый тип АВ-блокады второй степени характеризуется прогрессивным удлинением PR-интервала до блокированного сокращения и обычно ассоциирован с узким комплексом QRS. Второй тип АВ-блокады второй степени характеризуется фиксированным PR-интервалом до и после блокированных комплексов, обычно ассоциирован с широким QRS-комплексом. Когда отмечается проведение 2:1, блок не может быть классифицирован на первый или второй тип, хотя это можно предполагать по ширине QRS. При далеко зашедшей АВ-блока-де второй степени не проводятся две или более последовательных Р-волны, но некоторые волны проводятся, демонстрируя наличие частичного АВ-проведения. При третьей степени АВ-блокады (полной поперечной блокаде) АВ-проведение отсутствует (отмечается предсердно-желудочковая диссоциация).
Пациенты с нарушением АВ-проведения могут быть асимптомны или предъявлять серьезные жалобы вследствие брадикардии, желудочковых аритмий или их сочетания. Решение относительно необходимости имплантации кардиостимулятора во многом зависит от наличия или отсутствия симптоматики, непосредственно связанной с брадикардией. Более того, многие показания к кардиостимуляции, выработанные за последние 50 лет, базируются на клиническом опыте, без проведения сравнительных рандомизированных клинических исследований, в том числе потому, что не существует приемлемой альтернативы лечения большинства брадиаритмий.
Нерандомизированные исследования с высокой вероятностью полагают, что постоянная стимуляция улучшает выживаемость пациентов с АВ-блокадой третьей степени, особенно при наличии синкопе. Несмотря на незначительное количество доказательств, что ЭКС улучшают выживаемость пациентов с изолированной АВ-блокадой первой степени, сейчас известно, что значимая АВ-блокада первой степени (PR более 300 мс), может вызывать симптоматику в отсутствие
более высоких степеней блокады. Подобная значимая АВ-блокада первой степени может быть следствием катетерной абляции быстрого пути АВ-соединения с сохраняющимся проведением по медленному пути. Когда значимая АВ-блокада первой степени любой этиологии вызывает сокращение предсердий в непосредственной близости от систолы желудочков, могут наступить гемодинамические последствия и симптомы, как при ретроградном (вентрикулоатриальном) проведении (пейсмекерном синдроме). При значимой АВ-блокаде первой степени сокращения предсердий происходит до их полного наполнения, нарушается наполнение желудочков, повышается давление в легочных капиллярах, что ведет к снижению сердечного выброса. Небольшие, неконтролируемые исследования говорят об уменьшении симптомов и улучшении функции сердца на фоне кардиостимуляции у пациентов с PR-интервалом более 300 мс при уменьшении времени АВ-проведения. Наконец, длинный PR-интервал может составлять подгруппу пациентов с дисфункцией левого желудочка, состояние которых может улучшиться при двухкамерной стимуляции с укороченной АВ-за-держкой. Эти же самые принципы могут также быть применены к пациентам с первым типом АВ-блокады второй степени, гемодинамика которых ухудшается в силу утраты АВ-синхронизации, даже при отсутствии брадикардии. Хотя для оценки улучшения гемодинамики могут использоваться эхокардиографические или инвазивные методы, такие исследования не являются необходимыми.
Первый тип АВ-блокады второй степени обычно вызван задержкой проведения в АВ-узле, вне зависимости от продолжительности QRS. Поскольку переход в далеко зашедший АВ-блок в этой ситуации не является частым, стимуляция обычно не показана, за исключением случаев, когда имеется выраженная симптоматика. Тем не менее, существует противоположное мнение, что стимуляция в этой ситуации показана. С другой стороны, второй тип АВ-блокады второй степени обычно инфранодальный (интра- или инфрагисов-ский), особенно когда комплекс QRS расширен. У этих пациентов часто присутствует симптоматика, хуже прогноз, нередко наблюдается переход в блокаду третьей степени. Таким образом, второй тип блокады второй степени и широкий комплекс QRS говорят о диффузном поражении проводящей системы и диктуют показания к кардиостимуляции, даже если симптоматика отсутствует. Однако не всегда возможно определить уровень АВ-блокады без электрофизиологического исследования, так как АВ-блокада второй степени первого типа может быть инфранодальной, даже при узком QRS. Если при электрофизиологическом исследовании выявляется первый тип АВ-блокады второй степени с узкими или широкими QRS на уровне или ниже пучка Гиса, показана постоянная стимуляция [15-17].
Поскольку как для пациента, так и для врача может быть сложно связать неоднозначные симптомы, такие как утомляемость при появлении брадикардии, должно быть обращено особое внимание на то, связаны ли жалобы пациента с редким ритмом. У пациента с АВ-блокадой третьей степени кардиостимуляция
Таблица 4.
Рекомендации для постоянной электрокардиостимуляции у взрослых при приобретенной атриовентрикулярной блокаде
Класс Г
1. АВ-блокада 3 степени и прогрессирующая АВ-блокада 2 степени любого анатомического уровня, сочетающаяся с симптоматической брадикардией (включая сердечную недостаточность) и желудочковыми аритмиями, обусловленными АВ-блокадой. (Уровень доказанности: С).
2. АВ-блокада 3 степени и прогрессирующая АВ-блокада 2 степени любого анатомического уровня, сочетающаяся с аритмиями и другими медицинскими условиями, требующими медикаментозного лечения, вызывающего симптоматическую брадикардию. (Уровень доказанности: С).
3. АВ-блокада 3 степени и прогрессирующая АВ-блокада 2 степени любого анатомического уровня с документированными периодами асистолии более или равными 3.0 секундам, либо любой выскальзывающий ритм <40 ударов в минуту, либо выскальзывающий ритм ниже уровня АВ-узла в бодрствующем состоянии у бессимптомных пациентов с синусовым ритмом. (Уровень доказанности: С)
4. АВ-блокада 3 степени и прогрессирующая АВ-блокада 2 степени любого анатомического уровня у бессимптомных пациентов с ФП и документированной, по крайне мере, одной (или более) паузой 5 секунд и более. (Уровень доказанности: С)
5. АВ-блокада 3 степени и прогрессирующая АВ-блокада 2 степени любого анатомического уровня у пациентов после катетерной абляции АВ-узла или пучка Гиса. (Уровень доказанности: С).
6. АВ-блокада 3 степени и прогрессирующая АВ-блокада 2 степени любого анатомического уровня у пациентов с послеоперационной АВ блокадой, если ее разрешение после кардиохирургического вмешательства не прогнозируется. (Уровень доказанности: С)
7. АВ-блокада 3 степени и прогрессирующая АВ-блокада 2 степени любого анатомического уровня у пациентов с нейромышечными заболеваниями с АВ-блокадой, такими как миотоническая мышечная дистрофия, синдром Кернс-Сэйра, дистрофия Лейдена, перонеальная мышечная атрофия, с симптомами или без них. (Уровень доказанности: В)
8. АВ блокада 2 степени, вне зависимости от типа и места блокады, с сопутствующей симптомной брадикар-дией. (Уровень доказанности: В).
9. Персистентная АВ блокада 3 степени любого анатомического уровня с выскальзывающим ритмом > 40 ударов в минуту в бодрствающем состоянии — у пациентов с кардиомегалией, дисфункцией ЛЖ либо выскальзывающим ритмом ниже уровня АВ узла, не имеющих клинических проявлений брадикардии. (Уровень доказанности: В).
10. АВ блокада 2 либо 3 степени, возникающая при тесте с физической нагрузкой при условии отсутствия признаков ИБС. (Уровень доказанности: С)
Класс ГГа
1. Бессимптомная персистентная АВ-блокада 3 степени любой анатомической локализации, при частоте желудочковых сокращений в состоянии бодрствования > 40 ударов в минуту, без кардиомегалии. (Уровень доказанности: С).*
2. Бессимптомная АВ блокада 2 степени ГГ типа на интра- или инфра-Гисовском уровне, выявленная при ЭФИ. (Уровень доказанности: В).
3. Бессимптомная АВ блокада 2 степени II типа с узким QRS. Если бессимптомная АВ блокада 2 степени возникает с расширенным QRS, включая изолированную блокаду ПНПГ, показания к кардиостимуляции переходят в класс I рекомендаций (см. следующий раздел о хронической двух- и трехпучковой блокаде). (Уровень доказанности: В)
4. АВ-блокада 1 или 2 степени с симптомами, присущими пейсмейкерному синдрому или нарушениям гемодинамики. (Уровень доказанности: В).
Класс ГГб
1. Нейромышечные заболевания, такие как миотоническая мышечная дистония, синдром Кернс-Сэйра, дистрофия Лейдена, перонеальная мышечная атрофия с АВ-блокадой любой степени (включая АВ-блокаду 1 степени), с симптомами или без, т.к. может быть непредсказуемое прогрессирование заболевания и ухудшение предсердножелудочковой проводимости. (Уровень доказанности: В)
Продолжение таблицы 4 см. на стр. 68.
где, * — в рекомендациях 2005 года было «Бессимптомная персистентная АВ-блокада 3 степени в любой анатомической локализации, при средней частоте желудочковых сокращений в состоянии бодрствования > 40 ударов в минуту, особенно при кардиомегалии или дисфункции левого желудочка. (Уровень доказанности: В,С)»; эти изменения представляют концепцию о том, что кардиомегалия и дисфункция левого желудочка не имеют принципиального значения при имплантации водителей ритма пациентам с АВ-блокадой 3 степени или другими «допустимыми» брадиаритмиями при отсутствии симптомов; ** — отсутствует в рекомендациях Европейского общества кардиологов и Американской ассоциации сердца; новые рекомендации включают пациентов с дисфункцией левого желудочка, у которых предсердный вклад имеет принципиальное значение в клиническом состоянии и самочувствии пациента.
Продолжение таблицы 4, начало см. на стр. 67.
2. При возникновении АВ-блокады в связи с применением препаратов и/или их токсическим воздействием, когда разрешение блокады не ожидается, даже в условиях отмены данного препарата. (Уровень доказанности: В).
3. АВ-блокада 1 степени с интервалом PR >0.30 сек у пациентов с дисфункцией левого желудочка и симптомами застойной сердечной недостаточности, у которых более короткий интервал A-V приводит к гемоди-намическому улучшению, предположительно за счет уменьшения давления в левом предсердии. (Уровень доказанности: С).**
Класс III
1. Бессимптомная АВ-блокада 1 степени. (Уровень доказанности: В)
2. Бессимптомная АВ-блокада 2 степени I типа при блокаде проведения на уровне атриовентрикулярного узла), или неясно каком: интра- или инфра-Гисовском. (Уровень доказанности: С)
3. Ожидаемое разрешение АВ-блокады или маловероятный ее рецидив (например, лекарственная токсичность, болезнь Лайма, повышение вагального тонуса, ночное апноэ при отсутствии симптоматики). (Уровень доказанности: В)
обязательно должна обсуждаться в качестве метода лечения даже при частоте желудочкового ритма более 40 ударов в 1 мин, так как условная граница в 40 ударов в мин, приведенная в данных рекомендациях, не определялась клиническими исследованиями. Конечно, не частота выскальзывающего ритма определяет безопасность пациента, а, скорее, уровень возникновения замещающего ритма (например, АВ-узел, пучок Гиса или ниже пучка Гиса).
АВ-блокада может иногда провоцироваться физической нагрузкой. Если АВ-блокада не является вторичной по отношению к ишемии миокарда, блокада в этих ситуациях обычно связана с заболеванием системы Гиса-Пуркинье и ассоциируется с плохим прогнозом, то есть стимуляция показана. Напротив, длинные синусовые паузы и АВ-блокада могут случиться при апноэ во время сна. При отсутствии симптомов эти аномалии обратимы и не требуют стимуляции. Если симптоматика выражена и не исчезает, стимуляция показана, как и в других ситуациях.
Рекомендации по имплантации постоянных кардиостимуляторов у пациентов с АВ-блокадой при остром инфаркте миокарда, врожденной АВ-блокадой и вследствие повышенного вагусного тонуса обсуждаются в отдельных разделах. У молодых пациентов должна рассматриваться нейрокардиогенная этиология АВ-блокад до начала постоянной стимуляции. Физиологическая АВ-блокада при наджелудочковых тахиа-ритмиях не означает, что показана стимуляция, за исключением особых случаев, рассматриваемых ниже.
В общем, решение об имплантации постоянного ЭКС должно приниматься в зависимости от того, будет ли блокада постоянной. В первую очередь должны быть корригированы обратимые причины АВ-блока-
ды, такие как электролитные нарушения. Некоторые заболевания имеют спонтанное разрешение (например, болезнь Лайма), при некоторых блокадах можно надеяться на разрешение (например, гиперваготония вследствие известных и предотвратимых физиологических факторов, периоперационная блокада вследствие гипотермии или воспаления в области АВ-узла после хирургических вмешательств). Напротив, некоторые условия могут оправдывать имплантацию стимулятора вследствие возможности прогрессирования заболевания, даже когда АВ-блокада транзиторно разрешается (например, саркоидоз, амилоидоз, нейромус-кулярные заболевания). Наконец, АВ-блокада после пластики или протезирования клапанов сердца имеет разное течение, и решение о постоянной стимуляции принимается врачом в каждом конкретном случае.
КАРДИОСТИМУЛЯЦИЯ ПРИ ХРОНИЧЕСКИХ БИФАСЦИКУЛЯРНЫХ И ТРИФАСЦИКУЛЯРНЫХ БЛОКАДАХ
Бифасцикулярная блокада относится к ситуациям с доказанными по ЭКГ нарушениями проводимости ниже АВ-узла в двух ветвях правой или левой ножек пучка Гиса. Альтернирующая блокада ножек (известная также как билатеральная блокада ножек) относится к ситуациям, в которых имеются явные ЭКГ доказательства блокады во всех трех ветвях. Например, блокада правой и блокада левой ножки по ЭКГ или блокада правой ножки в сочетании с блокадой передней ветви левой ножки п. Гиса на одной ЭКГ и с блокадой задней ветви левой ножки пучка Гиса — на другой. При четко определенной трифасцикулярной блокаде блок документирован во всех трех ветвях, либо последовательно, либо в разное время. Альтернирующая блока-
да ножек также соответствует этому критерию. Этот термин также используется для описания АВ-блокады первой степени с бифасцикулярным блоком. Пациенты с подобными ЭКГ аномалиями и симптоматичной далеко зашедшей АВ-блокадой имеют высокий уровень летальности и значительную частоту внезапной смерти. Хотя бифасцикулярный блок наиболее часто предшествует АВ-блокаде третьей степени, существуют доказательства, что переход бифасцикулярного блока в АВ-блокаду третьей степени происходит постепенно и длительно. Более того, ни один из клинических или лабораторных признаков, включая бифасцикулярный блок, не выявляет пациентов высокого риска внезапной смерти от брадиаритмии, вследствие блокады в области ножек пучка Гиса [19].
У пациентов с бифасцикулярным блоком часто отмечаются синкопе. Несмотря на то, что синкопе могут повторяться, это не связано с повышением риска внезапной смерти. Электрокардиостимуляция освобождает от преходящих неврологических симптомов, но не снижает частоту внезапной смерти [16]. Для оценки и подбора терапии по поводу индуцируемых желудочковых аритмий, которые часто присутствуют у пациентов с бифасцикулярными и трифасцикулярными блокадами, может быть полезным электрофизиологическое исследование. Существуют убедительные доказательства, что при наличии постоянной или преходящей АВ-блокады третьей степени синкопе ассоциировано с повышенным риском внезапной смерти вне зависимости от результатов ЭФИ. Наконец, если при бифас-
Рекомендации для постоянной электрокардиостиму. и трифасцикулярной блокадах
цикулярной или трифасцикулярной блокаде имеются синкопе неясного генеза или используется терапия (лекарства), которая может вызвать АВ-блокаду, показана профилактическая постоянная ЭКС, особенно если потери сознания могут вызываться преходящей АВ-блокадой третьей степени.
Из множества данных обследования лишь PR- и КУ-интервалы могут быть возможными предикторами АВ-блокады третьей степени и внезапной смерти. Хотя удлинение PR-интервала часто встречается у пациентов с бифасцикулярным блоком, задержка проведения часто происходит на уровне АВ-узла. Не существует корреляции между PR- и КУ-интервала-ми, между продолжительностью PR и наступлением АВ-блокады третьей степени и внезапной смерти. Хотя у большинства пациентов с хронической или интермиттирующей АВ-блокадой третьей степени отмечается удлинение Н^интервала при антеградном проведении, некоторые исследователи полагают, что асимптомным пациентам с бифасцикулярным блоком показана постоянная стимуляция, особенно когда HV интервал превышает или равен 100 мс. Несмотря на то, что удлинение HV встречается нередко, частота перехода в АВ-блокаду третьей степени невысока. Так как удлинение Н^интервала свойственно тяжелым заболеваниям сердца с повышенной летальностью, смерть чаще не бывает внезапной или вызванной АВ-блока-дой, а обусловлена основным сердечным заболеванием и неаритмическими причинами. Использование предсердной стимуляции при ЭФИ у асимптомных
Таблица 5.
ции при хронической бифасцикулярной
Класс I
1. Прогрессирующая АВ-блокада 2 степени либо интермиттирующая АВ-блокада 3 степени. (Уровень доказанности: В)
2. АВ-блокада 2 степени II типа. (Уровень доказанности: В)
3. Перемежающаяся (альтернирующая) блокада ножек пучка Гиса. (Уровень доказанности: С)
Класс 11а
1. Синкопе (потери сознания) при отсутствии доказательств их связи с АВ-блокадой и при исключении их связи с желудочковой тахикардией (ЖТ). (Уровень доказанности: В)*
2. Случайное выявление во время инвазивного ЭФИ явно удлиненного интервала HV >100 мс у пациентов при отсутствии симптомов.(Уровень доказанности: В)
3. Выявление во время инвазивного электрофизиологического исследования нефизиологической АВ-блокады ниже пучка Гиса, развивающейся при проведении стимуляции. (Уровень доказанности: В)
Класс 11б
1. Нейромышечные заболевания, такие как миотоническая мышечная дистония, синдром Кернс-Сэйра, дистрофия Лейдена, перонеальная мышечная атрофия с фасцикулярной блокадой любой степени, с симптомами или без, т.к. может быть непредсказуемое нарастание нарушения предсердножелудочковой проводимости. (Уровень доказательности: С)
Класс III
1. Блокада ножек без нарушений АВ-проводимости, а также бессимптомная блокада ножек (Уровень доказанности: В)
2. Бессимптомная блокада ножек при наличии АВ-блокады I степени. (Уровень доказанности: В)
где, * — в рекомендациях 2005 года было «Отсутствие видимой связи синкопе с АВ-блокадой при исключении их связи с желудочковой тахикардией (ЖТ). (Уровень доказанности: В)»; изменение слова «видимая связь » на «доказательства », т.к. необходимо задокументированние клинического состояния с брадикардией.
пациентов для выявления блокады высокой степени является спорным. Вероятность получения блокады дистальнее АВ-узла (интра- или инфрагисовской) при помощи частой предсердной стимуляции невысока. Невозможность достижения дистальной блокады при стимуляции не может быть доказательством того, что в будущем не наступит АВ-блокада третьей степени. Тем не менее, получение при предсердной стимуляции нефизиологической инфрагисовской блокады рассматривается некоторыми специалистами как показание к стимуляции [7, 14, 21].
КАРДИОСТИМУЛЯЦИЯ ПРИ ОСТРОМ ИНФАРКТЕ МИОКАРДА
Показания к постоянной стимуляции после инфаркта миокарда у пациентов, перенесших АВ-блокаду, относятся в большей мере к нарушениям внутрижелу-дочкового проведения. В отличие от других показаний к постоянной стимуляции, критерии для пациентов с инфарктом миокарда и АВ-блокадой не обязательно зависят от наличия симптомов. Более того, потребность во временной стимуляции при остром инфаркте миокарда сама по себе не определяет показаний к постоянной стимуляции.
Долговременный прогноз у перенесших ОИМ, имевших АВ-блокаду, зависит в большей мере от размеров повреждения миокарда и характера нарушений внутрижелудочковой проводимости, чем от самой АВ-блокады. Пациенты с острым инфарктом миокарда, имеющие нарушения внутрижелудочкового проведения, за исключением изолированной блокады передней ветви левой ножки, имеют неблагоприятный краткосрочный и долговременный прогноз и повышенный риск внезапной смерти. Этот неблагоприятный прогноз необязательно связан с развитием АВ-блокады
высокой степени, хотя встречаемость блокад выше у постинфарктных пациентов с нарушенным внутриже-лудочковым проведением [17, 21].
Когда атриовентрикулярная или внутрижелудоч-ковая блокада проведения осложняет острый инфаркт миокарда, при рассмотрении показаний к постоянной стимуляции должны учитываться тип нарушения проводимости, локализация инфаркта и связь электрических нарушений с инфарктом. Даже когда имеются все данные, решение не всегда однозначно, так как встречаемость и значимость нарушений проводимости по данным литературы сильно варьирует. Несмотря на использование тромболитической терапии и первичной ангиопластики, которые снижают частоту АВ-блокад при остром инфаркте миокарда, летальность при возникновении АВ-блокады остается высокой [15-18].
Хотя наиболее тяжелые нарушения проводимости в общем ассоциированы с большей смертностью, влияние ранее существовавшей блокады ножек пучка Гиса на летальность при остром инфаркте миокарда является спорным. Особенно неблагоприятный прогноз связан с наличием блокады левой ножки в сочетании с далеко зашедшей блокадой второй или третьей степени или с наличием блокады правой ножки в сочетании с блокадой передней или задней ветви левой ножки. Вне зависимости от передней или нижней локализации инфаркта развитие нарушений внутрижелудочко-вой проводимости отражает обширное повреждение миокарда, а не отдельную «электрическую» проблему. Хотя АВ-блокада, возникающая при нижнем инфаркте миокарда, связана с лучшим долговременным клиническим исходом, госпитальная выживаемость снижается вне зависимости от временной или постоянной стимуляции. Более того, стимуляторы не должны имплантироваться, если периинфарктная блокада должна
Класс I
1. АВ-блокада III степени на уровне пучка Гиса или ниже, а также стойкая АВ-блокада II степени ниже пучка Гиса в сочетании с бифасцикулярной блокадой. (Уровень доказанности: В)
2. Преходящая АВ-блокада II-III степени с уровнем поражения ниже АВ-соединения в сочетании с блокадой ножки пучка Гиса. Если локализация блокады неизвестна, возможно проведение электрофизиологического исследования. (Уровень доказанности: В)
3. Стойко сохраняющаяся АВ-блокада II-III степени сопровождающаяся клинической картиной. (Уровень доказанности: С)
Класс II6
1. Стойко сохраняющаяся АВ-блокада II-III степени проксимального типа, даже при отсутствии симптоматики. (Уровень доказанности: В)
Класс III
1. Преходящая АВ-блокада при отсутствии нарушений внутрижелудочковой проводимости. (Уровень доказанности: В)
2. Преходящая АВ-блокада при наличии изолированной блокады передней ветви левой ножки пучка Гиса. (Уровень доказанности: В)
3. Приобретенная блокада передней ветви левой ножки при отсутствии АВ-блокады. (Уровень доказанности: В)
4. Стойкая АВ-блокада I степени, развившаяся на фоне ранее существовавшей блокады ножки. (Уровень доказанности: В)
Таблица 6.
Рекомендации по постоянной кардиостимуляции после острой фазы инфаркта миокарда
разрешиться или не имеет отрицательного влияния на долговременный прогноз, как при нижнем инфаркте миокарда [18, 19].
КАРДИОСТИМУЛЯЦИЯ ПРИ ДИСФУНКЦИИ СИНУСНО-ПРЕДСЕРДНОГО УЗЛА
Дисфункция синусно-предсердного узла (синдром слабости СПУ) объединяет целый спектр аритмий, включающий в себя синусовую брадикардию, отказ синусового узла, синоатриальную блокаду и пароксиз-мальные наджелудочковые тахиаритмии (фибрилляция и трепетание предсердий), сменяющиеся периодами брадикардии и/или асистолии. Эти пациенты могут иметь симптомы тахикардии, брадикардии или те и другие одновременно. Связь симптомов с аритмией устанавливается при помощи ЭКГ. Определение этой связи может быть затруднительным в связи с преходящим характером эпизодов аритмий. В электрофизиологической лаборатории нарушенная функция СПУ может быть характеризована удлинением корригированного времени восстановления функции синусно-предсер-дного узла (КВВФСУ) или времени синоатриального проведения (ВСАП). Однако информативность электрофизиологических исследований ограничена чувствительностью и специфичностью метода.
Дисфункция СПУ может проявляться хронотроп-ной недостаточностью с неадекватным ответом СПУ на нагрузку или стресс. Частотноадаптивные ЭКС
Рекомендации по постоянной кардиостимуляции при
помогают пациентам восстановить физиологическую частоту ритма во время физической активности.
Синусовая брадикардия допускается как физиологическая находка у тренированных атлетов. Они нередко имеют ЧСС от 40 до 50 в мин во время отдыха и пробуждения. ЧСС до 30 в мин отмечается у них во время сна, с синусовыми паузами или АВ-блокадой второй степени первого типа, дающими асистоличес-кие интервалы до 2,8 сек. Эти особенности обусловлены повышенным тонусом блуждающего нерва.
Хотя дисфункция СПУ часто является первичным показанием для имплантации постоянного ЭКС [13], постоянная стимуляция у этих пациентов необязательно приводит к улучшению выживаемости, тогда как симптомы брадикардии могут исчезать. При мониторировании паузы чаще наблюдаются во время сна, хотя продолжительность пауз и их клиническая значимость однозначно не определены. Если они связаны с апноэ во время сна — необходимо лечить апноэ. Небольшое ретроспективное исследование частой (overdrive) предсердной стимуляции в лечении апноэ во время сна показало снижение частоты эпизодов центрального или обструктивного апноэ во время сна без уменьшения времени сна [17, 18]. Хотя это исследование обнадеживает, пока преждевременно предлагать рекомендации до появления большего количества клинических наблюдений. С другой стороны, нет убедительных доказательств, позволяющих разделить
Таблица 7.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
дисфункции синусно-предсердного узла
Класс I
1. Дисфункция СПУ с документированной брадикардией или паузами, сопровождающимися симптоматикой. (Уровень доказанности: С)
2. Проявляющаяся клинически хронотропная некомпетентность.(Уровень доказанности: C)
3. Синусовая брадикардия с симптоматикой, являющаяся результатом длительной медикаментозной терапии, которая не может быть прекращена или заменена другой терапией. (Уровень доказанности: С)
Класс Па
1. Спонтанная или медикаментозно обусловленная дисфункция синусового узла с ЧСС < 40 ударов в минуту, сопровождающаяся симптоматикой, но при отсутствии документального подтверждения наличия более значимой брадикардии. (Уровень доказанности: 0)
2. Синкопе (потеря сознания) по непонятным причинам в случае, когда основные отклонения от норм функции СПУ выявлены или спровоцированы электрофизиологическим исследованием. (Уровень доказанности: С)
Класс Пб
1. Минимально выраженная симптоматика при ЧСС в состоянии бодрствования меньше 40 ударов в минуту. (Уровень доказанности: С)
Класс III
1. Дисфункция синусового узла у бессимптомных больных, включая и тех, у кого синусовая брадикардия менее 40 ударов в минуту, является последствием долгосрочной лекарственной терапии.*
2. Дисфункция синусового узла с симптоматикой, которая могла бы быть обусловлена брадикардией, но имеется четкая документация того, что клиника не связана с редким ритмом.
3. Симптоматическая дисфункция СПУ, развившаяся на фоне лекарственных препаратов, от которых можно отказаться без последствий для больного.
где, * — в рекомендациях 2005 года было «Дисфункция синусового узла у бессимптомных больных, у которых синусовая брадикардия является последствием долгосрочной лекарственной терапии»; данная поправка имеет значение для пациентов принимающих медикаменты в связи с хроническим заболеванием и не имеющих клинических проявлений, связанных с брадикардией.
физиологическую и патологическую ночную бради-кардию.
ПРЕДОТВРАЩЕНИЕ И ПРЕКРАЩЕНИЕ ТАХИАРИТМИЙ МЕТОДОМ ЭЛЕКТРОКАРДИОСТИМУЛЯЦИИ
В силу определенных обстоятельств имплантированный стимулятор может быть полезен для лечения пациентов с возвратными симптомными желудочковыми и наджелудочковыми тахикардиями [15-17]. Стимуляция может быть полезна для предотвращения и купирования аритмий. Рецидивирующие аритмии, такие как трепетание предсердий, пароксизмальные реципрокные наджелудочковые тахикардии и ЖТ, могут быть купированы различными режимами стимуляции, включая программированную стимуляцию и короткие залпы частой стимуляции (burst, ramp). Антиаритмические устройства могут детектировать тахикардию и автоматически активировать стимуляцию или отвечать на внешний запуск (например, поднесение магнита).
Профилактика аритмий при помощи кардиостимуляции продемонстрирована в ряде ситуаций. У некоторых пациентов с синдромом удлиненного интервала QT рецидивирующая, брадизависимая ЖТ может быть
предотвращена overdrive стимуляцией. Описано, что комбинация предсердной стимуляции и бета-блокато-ров укорачивает QT-интервал и помогает предотвращать внезапную смерть [14]. ИКД-терапия в сочетании со стимуляцией должна рассматриваться у пациентов высокого риска по ВСС.
Синхронизированная с предсердиями желудочковая стимуляция может предотвращать наджелудоч-ковые реципрокные тахикардии, хотя эта методика редко используется в связи с возможностями катетер-ной абляции или других видов лечения. Хотя желудочковая эктопическая активность также может быть подавлена подобной стимуляцией, серьезные и симптоматичные аритмии редко поддаются профилактике. У некоторых пациентов с брадизависимой ФП предсердная стимуляция может быть эффективной в качестве снижения частоты рецидивов. В исследовании MOST (Mode Selection Trial) 2001 г. пациенты с дисфункцией синусового узла были поделены на 2 группы по типу стимуляции: на DDDR- и VVIR-режи-мы. После 33 месячного периода наблюдения отмечалось снижение риска ФП на 21% (р=0,008) в группе с режимом DDDR по сравнению с группой VVIR. Роль алгоритмов предсердной стимуляции в профилактике фибрилляции предсердий пока остается неопре-
Таблица 8.
Рекомендации по установке постоянных водителей ритма, автоматически распознающих и предотвращающих тахикардии
Класс 11а
1. Симптоматическая рецидивирующая наджелудочковая тахикардия, купируемая кардиостимуляцией, в тех редких случаях, когда катетерная абляция и/или медикаментозная терапия не помогают контролировать аритмию или влекут за собой нежелательные побочные эффекты. (Уровень доказанности: С)
Класс III
1. Наличие дополнительных проводящих путей со способностью быстрой антероградной проводимости, вне зависимости от того, участвуют ли проводящие пути в механизме тахикардии или нет. (Уровень доказанности: С)
2. Рецидивирующая наджелудочковая тахикардия или трепетание предсердий, купируемая кардиостимуляцией, как альтернатива медикаментозной терапии или абляции. (Уровень доказанности: С)*
где * — отсутствует в рекомендациях Европейского общества кардиологов и Американской ассоциации сердца; этот пункт добавлен, что бы показать высокую значимость, на сегодняшний день, методик радикального лечения тахиаритмий.
Таблица 9.
Рекомендации по кардиостимуляции для профилактики возникновения тахикардии
Класс I
1. Продолжительная паузозависимая желудочковая тахикардия, с удлинением интервала QT или без него, когда эффективность кардиостимуляции документирована. (Уровень доказанности: С)
Класс 11а
1. Пациенты высокого риска с врожденным синдромом удлиненного интервала QT. (Уровень доказанности: С)
Класс 11б
1. Предотвращение проявляющейся клинически, рефрактерной к медикаментозной терапии, рецидивирующей фибрилляции предсердий с сопутствующей дисфункцией СПУ. (Уровень доказанности: В)
Класс III
1. Частая или комплексная желудочковая эктопическая активность без длительной желудочковой тахикардии при отсутствии синдрома удлиненного интервала QT. (Уровень доказанности: С)
2. Двунаправленная желудочковая тахикардия, вызванная обратимыми причинами. (Уровень доказанности: А)
деленной. Однако недавнее многоцентровое рандомизированное клиническое исследование SAFARI продемонстрировало безопасность и эффективность превентивных алгоритмов стимуляции, предназначенных для профилактики ФП у пациентов с бради-кардией и пароксизмальной формой ФП. Наибольшая эффективность была достигнута при исходно частых пароксизмах ФП [29]. Бифокальная стимуляция правого предсердия или альтернативная монофокальная стимуляция из нетрадиционных точек (например, межпредсердной перегородки или пучка Бахмана) могут давать дополнительные преимущества по сравнению с монофокальной стимуляцией ушка правого предсердия у пациентов с симптомной медикаментоз-но-резистентной фибрилляцией предсердий и сопутствующими брадиаритмиями. У пациентов с СССУ и внутрипредсердной блокадой проведения (Р больше 160 мс) биатриальная стимуляция может снизить частоту рецидивов ФП [22].
Потенциальные реципиенты антиаритмических устройств, прерывающих аритмии, должны подвергаться расширенному тестированию перед имплантацией для того, чтобы убедиться, что аппарат безопасно и надежно купирует механизм аритмии без ее ускорения и индукции фибрилляции желудочков. Пациенты, которым рекомендуется антитахикардитический стимулятор, обычно рефрактерны к антиаритмической терапии. Когда постоянный антитахикардитический прибор детектирует и прерывает наджелудочковую тахикардию, в связи с описанными побочными эффектами при применении желудочковой стимуляции, необходима только предсердная стимуляция. Постоянная антитахикардитическая стимуляция как монотерапия ЖТ неприемлема, эти алгоритмы возможны при последовательных режимах терапии ИКД, имеющих возможность кардиоверсии и дефибрилляции в случаях, когда антитахикардитическая стимуляция неэффективна, или в случаях ускорения тахикардии.
КАРДИОСТИМУЛЯЦИЯ ПРИ ГИПЕРЧУВСТВИТЕЛЬНОСТИ КАРОТИДНОГО СИНУСА И НЕЙРОКАРДИОГЕННОМ СИНКОПЕ
Синдром гиперчувствительности каротидного синуса (ГКС) проявляется синкопальными (полная потеря сознания) или пресинкопальными состояниями в результате повышенного рефлекторного ответа на стимуляцию каротидного синуса. Эта весьма редкая причина синкопе представлена двумя компонентами рефлекторного ответа:
1) кардиоингибиторный — вследствие повышения парасимпатического тонуса, приводящего к манифестации синусовой брадикардии или удлинению интервала PR с появлением АВ-блокады, или к их комбинации;
2) вазодепрессорный — в результате снижения симпатической активности, проявляющейся снижением тонуса сосудистой стенки и гипотонией. Этот эффект возникает независимо от изменений ритма сердца.
Для определения показаний к постоянной кардиостимуляции в подобных случаях необходимо выяснить, какова степень участия того или ино-
го компонента в симптомокомплексе синкопального состояния у пациента. Гиперчувствительность каро-тидного синуса может проявляться в виде эпизодов асистолии длительностью более 3 сек вследствие отказа синусового узла или АВ-блокады, в виде симп-томного падения систолического АД, а также в форме сочетания этих симптомов. В норме, у здоровых людей и у больных ИБС, при проведении пробы с массажем каротидного синуса паузы не превышают 3 сек. Выяснение причинноследственных связей в случае диагностирования синдрома ГКС является первостепенной задачей. Само по себе появление синкопальных состояний при стимуляции каротид-ного синуса подразумевает наличие этого синдрома. Незначительное давление на зону каротидного синуса у пожилых людей и пациентов, принимающих препараты дигиталиса, также может привести к изменениям ритма и артериального давления, которые не являются признаками синдрома ГКС. Постоянная кардиостимуляция весьма эффективно устраняла симптомы при кардиоингибиторном типе синдрома ГКС. У 10-20% пациентов с синдромом ГКС кардио-ингибиторный тип сочетается в разном процентном соотношении с вазодепрессорным компонентом. Эффективность кардиостимуляции у таких пациентов зависит от верификации причины синкопальных состояний. Поэтому необходимо убедиться, что оно вызвано именно эпизодом асистолии.
Практика показывает, что большинство син-копальных состояний неясного генеза у пациентов пожилого возраста обусловлено синдромом ГКС. В исследовании, включившем 175 пожилых пациентов с синкопальными состояниями в анамнезе и положительными результатами пробы с массажем каротид-ного синуса, проведена рандомизация по принципу проводимой терапии. За время наблюдения в группе с проводимой электрокардиостимуляцией вероятность эпизодов потери сознания у пациентов была значительно меньше [15-17]. Нейрокардиогенные синкопе и синдромы происходят по различным сценариям, однако и брадикардия, и периферическая вазодилятация могут приводить к преходящей системной гипотонии. Нейрокардиогенные синкопе составляют около 1040% всех причин синкопальных состояний. Термин «вазовагальные» синкопе подразумевает наиболее распространенный сценарий синкопального состояния и также относится к категории нейрокардиоген-ных синкопальных синдромов. Как правило, у этих пациентов предшествуют продромальные симптомы — тошнота, потливость (у пожилых они могут отсутствовать), причем нередко эти проявления передаются по наследству. Эти приступы могут провоцироваться болью, беспокойством, стрессовыми ситуациями, пребыванием в душном помещении. Обычно структурных изменений сердца у таких пациентов не наблюдается и исключены другие причины синкопаль-ных состояний — обструкция выводного тракта левого желудочка, брадиаритмии, тахиаритмии. В диагностических целях эффективна ортостатическая проба на столе с изменяемым углом наклона — тилт-тест (tilt-test) [15-17].
Таблица 10.
Рекомендации по постоянной электрокардиостимуляции при синдроме гиперчувствительного каротидного синуса и нейрокардиогенной потере сознания
Класс I
1. Рецидивирующие синкопе, вызванные стимуляцией каротидного синуса; минимальное давление каротидного синуса индуцирует желудочковую асистолию длительностью более 3 секунд. (Уровень доказанности:С)*
Класс Па
1. Рецидивирующие синкопе без провокаций и гиперчувствительной кардиоингибиторной реакции в течение 3 секунд и более. (Уровень доказанности: С)
Класс III
1. Гиперчувствительная кардиоингибиторная реакция на стимуляцию каротидного синуса при отсутствии симптоматики. (Уровень доказанности: С)**
2. Гиперчувствительная кардиоингибиторная реакция на стимуляцию каротидного синуса при таких симптомах, как головокружение, легкая дезориентация или то и другое. (Уровень доказанности: С)***
где * — в рекомендациях 2005 года было «Рецидивирующие синкопе, вызванные стимуляцией каротидного синуса; минимальное давление каротидного синуса индуцирует желудочковую асистолию длительностью более 3 секунд, при отсутствии медикаментозного влияния на СПУ или предсердно-желудочковую проводимость (Уровень доказанности: С)»; удалена фраза про влияние препаратов на проводящую систему, т.к. при их воздействии данные критерии сохраняют свою актуальность; ** — рекомендация Класса III «симптоматичная нейрокардиогенная потеря сознания, связанная с брадикардией, зафиксированная спонтанно или во время йк-теста. (Уровень доказанности: В)» разделена на рекомендации 1 и 2; *** — рекомендация 2005 года «рецидивирующая потеря сознания, головокружение или легкая дезориентация при отсутствии гиперчувствительной кардиоингибиторной реакции, (Уровень доказанности: С)» удалена так как необходимо выяснение истинных причин синкопальных состояний; рекомендация 2005 года «Ситуативный вазовагальный обморок, при котором эффективны предотвращающие меры, (Уровень доказанности: С)» удалена так как только лишь при отсутствии альтернативных методов лечения нужно думать о постоянной электрокардиостимуляции.
Роль постоянной кардиостимуляции при рефрактерных нейро-кардиогенных синкопальных состояниях, сочетаемых с выраженной брадикардией и асистолией, противоречива. Приблизительно у 25% пациентов с доминирующим вазодепрессорным эффектом выраженная брадикардия может не регистрироваться. Кроме того, большую часть составляют пациенты с сочетанием компонентов. По данным одних исследователей, отмечена некоторая эффективность кардиостимуляции у этой категории пациентов, в других работах показано, что стимуляция с частотой, на 20% превышающей спонтанный ритм, не предотвращала появления синкопе, и фармакотерапия не уступала в эффективности лечения. Полученные результаты объяснялись тем, что брадикардия появлялась вторично, на фоне падения давления. Двухкамерная кардиостимуляция при кардиоингибиторном типе синдрома ГКС, подтвержденного йН-тестом, показала себя эффективным методом лечения. По данным рандомизированных исследований [25] постоянная кардиостимуляция у пациентов с выраженной симп-томной брадикардией значительно увеличивала сроки появления синкопальных состояний. По данным одного из исследований, рецидивы синкопе в течение года встречались у 18,5% пациентов на фоне кардиостимуляции и у 59,7% пациентов контрольной группы.
Изучались и различные виды стимуляции у этой категории пациентов. В одном из исследований продемонстрирована эффективность DDD стимуляции с функцией частотной адаптации по сравнению с терапией бета-блокаторами для предотвращения рецидивов у пациентов с симптомными вазовагальными синкопе
и умеренной брадикардией во время йЬ-теста. В целом у таких пациентов прогноз в отсутствии кардиостимуляции достаточно благоприятный. Ряд исследователей подчеркивает эффективность электрокардиостимуляции у пациентов с синдромом ГКС, в основе которого лежит симптомная брадикардия, которая, кроме того, подтверждается электрофизиологическим исследованием [17, 24].
При обследовании данных пациентов важно не упустить другие, более опасные причины обморочных состояний, такие как желудочковые тахиаритмии.
КАРДИОСТИМУЛЯЦИЯ У ДЕТЕЙ, ПОДРОСТКОВ И ПАЦИЕНТОВ С ВРОЖДЕННЫМИ ПОРОКАМИ СЕРДЦА
Показаниями для имплантации постоянного электрокардиостимулятора детям, подросткам и пациентам молодого возраста с врожденными пороками сердца являются: 1) симптомная синусовая брадикардия, 2) синдром брадикардии-тахикардии, 3) врожденная полная АВ-блокада и 4) хирургическая или приобретенная АВ-блокада 2 или 3 степени. Хотя показания к имплантации у детей и взрослых сходны, следует отметить несколько моментов. Во-первых, возрастает количество пациентов, которым выполняются сложные паллиативные хирургические вмешательства, не направленные на полную коррекцию порока сердца. Сохраняющееся нарушение функции желудочков может привести к развитию симптомов брадикардии при частоте, которая при сохраненной физиологии кровообращения не сопровождалась бы симптоматикой. Таким образом, у
Таблица 11.
Рекомендации по применению постоянной кардиостимуляции у детей, подростков и пациентов с врожденными пороками сердца
Класс I
1. Прогрессирующая атриовентрикулярная блокада 2 или 3 степени, в сочетании с симптомной брадикардией, дисфункцией желудочков сердца или снижением сердечного выброса. (Уровень доказанности: С)
2. Нарушение функции СПУ с корреляцией симптомов во время несоответствующей возрасту брадикардии. Определение брадикардии варьирует в зависимости от возраста пациента и ожидаемой ЧСС. (Уровень доказанности: В)
3. Послеоперационная прогрессирующая атриовентрикулярная блокада 2 или 3 степени, если не прогнозируется ее разрешение после операции на сердце или если она не разрешается в течение 7 дней. (Уровень доказанности: В)
4. Врожденная атриовентрикулярная блокада 3 степени с ширококомплексным замещающим ритмом, поли-топной желудочковой эктопией или дисфункцией желудочков. (Уровень доказанности: В)
5. Врожденная атриовентрикулярная блокада 3 степени у грудного ребенка с желудочковым ритмом менее 5055 ударов в минуту или с врожденным пороком сердца и желудочковым ритмом менее 70 ударов в минуту. (Уровень доказанности: С)
6. Устойчивая паузозависимая желудочковая тахикардия, с увеличением интервала QT или без него, при которой эффективность кардиостимуляции доказана. (Уровень доказанности: В)*
Класс IIa
1. Пациенты с врожденным пороком сердца и синусовой брадикардией для профилактики повторяющихся эпизодов внутрипредсердной реципрокной тахикардии; при этом синусовая дисфункция может быть как первичной, так и медикаментозной. (Уровень доказанности: С)
2. Врожденная атриовентрикулярная блокада 3 степени после первого года жизни при среднем ЧСС менее 50 ударов в минуту или внезапных паузах в желудочковом ритме, превышающих длительность базового цикла в 2 или 3 раза, или симптоматичная хронотропная недостаточность. (Уровень доказанности: В)
3. Бессимптомная синусовая брадикардия у детей со сложным врожденным пороком сердца при ЧСС в покое менее 40 ударов в минуту или паузах в желудочковом ритме более 3 секунд. (Уровень доказанности: С)
4. Пациенты с врожденным пороком сердца и нарушением гемодинамики вследствие синусовой брадикардии или предсердножелудочковой диссинхронии. (Уровень доказанности: С)
5. Синкопальные состояния неясного генеза у пациентов после хирургической коррекции порока сердца осложненные кратковременной АВ-блокадой 3 степени и остаточной блокадой ножек пучка Гиса при отсутствии иных причин синкопальных состояний. (Уровень доказанности: В)
6. Синдром брадикардии-тахикардии при необходимости длительной антиаритмической терапии без применения препаратов дигиталиса. (Уровень доказанности: С)**
7. Синдром удлиненного интервала QT с атриовентрикулярной блокадой 2:1 или АВ-блокадой 3 степени. (Уровень доказанности: В)***
Класс II6
1. Преходящая послеоперационная атриовентрикулярная блокада 3 степени, которая возвращается к синусовому ритму с остаточной бифасцикулярной блокадой. (Уровень доказанности: С)
2. Врожденная атриовентрикулярная блокада 3 степени у новорожденного, ребенка, подростка юноши и девушки без проявления симптомов, с приемлемой ЧСС, узким комплексом QRS и нормальной функцией желудочков. (Уровень доказанности: В)
3. Бессимптомная синусовая брадикардия у подростков после гемодинамической коррекции врожденного порока сердца при ЧСС в покое менее 40 ударов в минуту или паузах между желудочковыми комплексами более 3 секунд. (Уровень доказанности: С)
3. Нейромышечные расстройства с любой степенью атриовентрикулярной блокады (включая первую степень блокады), с наличием симптомов или без симптомов, поскольку возможно непредсказуемое прогрессирова-ние нарушения атриовентрикулярной проводимости.****
Класс III
1. Преходящая послеоперационная атриовентрикулярная блокада с возвратом нормальной атриовентрикулярной проводимости. (Уровень доказанности: В)
2. Бессимптомные послеоперационные бифасцикулярные блокады с/без атриовентрикулярной блокады первой степени при отсутствии транзиторной АВ-блокады 3 степени. (Уровень доказанности: C)
Продолжение таблицы 11 см. на стр. 76.
Продолжение таблицы 11, начало см. на стр. 75.
3. Бессимптомная атриовентрикулярная блокада второй степени I типа. (Уровень доказанности: C)
4. Бессимптомная синусовая брадикардия у подростков с паузами менее 3 секунд и минимальной ЧСС более 40 ударов в минуту. (Уровень доказанности: C)
где, * — отсутствует в рекомендациях Европейского общества кардиологов и Американской ассоциации сердца; для пациентов, у которых имеются паузы в ритме, не достаточные для постановки кардиостимулятора, но при этом эти паузы являются пусковым механизмом желудочковых нарушений ритма сердца; ** — отсутствует в рекомендациях Европейского общества кардиологов и Американской ассоциации сердца; при подобранной оптимальной терапии и отсутствии альтернативных методов лечения тахиаритмии;*** — отсутствует в рекомендациях Европейского общества кардиологов и Американской ассоциации сердца; у данного контингента пациентов кардиостимуляция уменьшает вероятность развития желудочковых нарушений ритма сердца; **** — отсутствует в рекомендациях Европейского общества кардиологов и Американской ассоциации сердца; рекомендация класса IIb для кардиостимуляции у детей и подростков с нейромышечными расстройствами и любой степенью атриовен-трикулярной блокады, аналогична рекомендации с такими нарушениями у взрослых.
таких пациентов показания к имплантации основываются на сочетании симптомов с уровнем частоты сердечных сокращений. Во-вторых, клиническая значимость брадикардии носит возрастзависимый характер, например ЧСС 50 в минуту у подростка может быть вариантом нормы, тогда как у новорожденных — выраженной брадикардией.
Брадикардия и ассоциированные с ней симптомы у детей часто бывают преходящими (например, преходящая А-В блокада или остановка синусового узла), что затрудняет их выявление. Дисфункция синусно-предсердного узла (СССУ) часто регистрируется в педиатрической практике. Однако лишь при наличии синкопального состояния и брадикардии (ЧСС менее 40 в минуту или асистолии длительностью более 3 сек) этим пациентам показана имплантация ЭКС [1517]. Связь появления симптомов с брадикардией устанавливается с помощью 24-часового холтеровского мониторирования или транстелефонной электрокардиографией. Только после исключения других причин появления симптомов — припадки, задержка дыхания, апноэ или нейрокардиогенные синкопе — принимается решение об имплантации ЭКС.
Синдром брадикардии-тахикардии (синусовая брадикардия в сочетании с трепетанием/фибрилляцией предсердий или предсердной реципрокной тахикардией) нередко встречается у молодых пациентов после хирургии врожденных пороков сердца. Большой процент заболеваемости и смертности наблюдается среди молодых пациентов с персистирующим или хроническим трепетанием/фибрилляцией предсердий, а синусовая брадикардия является независимым предиктором развития трепетания/фибрилляции предсердий. Фармакотерапия имеет ряд ограничений: длительный прием одних препаратов (соталол или амиодарон) при трепетании/фибрилляции предсердий может привести к симптомной брадикардии, а прием других (препараты 1 класса — хинидин, ритмонорм) увеличивает риск развития желудочковых аритмий или выраженной брадикардии, опасной развитием внезапной смерти пациента [12]. В некоторых случаях при врожденных пороках сердца альтернативным способом терапии является радиочастотная катетер-ная абляция и модификация анатомического субстрата тахикардии.
Показания к имплантации ЭКС у молодых пациентов с врожденной полной поперечной блокадой со временем претерпели изменения, которые базировались как на наблюдении за естественным течением заболевания, так и на успехах диагностики и появлении современных технологий электрокардиостимуляции. В нескольких исследованиях было показано, что кардиостимуляция у пациентов с асимптомной полной блокадой увеличивала их долгосрочную выживаемость и предотвращала синкопальные состояния. Всем этим пациентам, в том числе и после имплантации, необходимо контролировать функцию левого желудочка. У асимптомных пациентов с полной АВ-блокадой обязательно исследование среднесуточной ЧСС, выявление пауз при спонтанном ритме, структурных аномалий, измерение интервала QT и исследование толерантности к физическим нагрузкам.
Многими наблюдениями подчеркивается целесообразность использования бета-блокаторов на фоне кардиостимуляции у пациентов с врожденным синдромом удлиненного интервала QT. Наиболее оптимальный эффект от электрокардиостимуляции наблюдается у пациентов с брадизависимыми желудочковыми тахикардиями и у лиц с синусовой брадикардией или АВ-блокадой в сочетании с врожденным синдромом удлиненного интервала QT. Имплантация ЭКС у таких пациентов снижает количество симптомов, таким образом обеспечивая снижение риска внезапной остановки сердца.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Гораздо хуже прогноз у пациентов с послеоперационной АВ-блокадой без постоянной электрокардиостимуляции. Сохраняющаяся АВ-блокада 2 или 3 степени в течение 7-10 суток после операции является показанием класса I к имплантации ЭКС. Необходимость электрокардиостимуляции у пациентов с преходящей АВ- и бифасцикулярной блокадой не столь очевидна, тогда как у пациентов после нормализации АВ-проведения прогноз улучшается.
Для принятия решения об имплантации ЭКС пациентам с сохраненными интракардиальными дефектами необходимо учитывать риск парадоксальной эмболии тромботическими массами, локализованными на эндокардиальном электроде и выбор варианта имплантации (трансвенозный или эпикардиальный).
КАРДИОСТИМУЛЯЦИЯ ПРИ СПЕЦИФИЧЕСКИХ СОСТОЯНИЯХ
Гипертрофическая обструктивная
кардиомиопатия
В ранних нерандомизированных исследованиях было продемонстрировано снижение градиента между левым желудочком и его выводным трактом при двухкамерной кардиостимуляции с укороченной АВ-задерж-кой и уменьшение симптоматики у некоторых пациентов с гипертрофической обструктивной кардиомиопатией (ГКМП) [15-17]. Одно продолжительное исследование, включившее 8 человек с двухкамерной кардиостимуляцией в течение значительного времени выявило снижение этого градиента даже после прекращения стимуляции. Это позволило предположить, что благодаря стимуляции произошло ремоделирование желудочков. Два рандомизированных исследования показали субъективное улучшение качества жизни приблизительно у 50% исследуемых, которое, однако, не было связано со снижением градиента и выраженным эффектом плацебо. Третье рандомизированное исследование не показало какого-либо улучшения качества жизни у пациентов при кардиостимуляции, хотя было высказано предположение, что стимуляция у пожилых больных (старше 65 лет) была более эффективна [15-18].
У небольшой группы пациентов с обструктивной ГКМП проводилась VDD-стимуляция с преждевременным возбуждением желудочков, то есть короткой АВ-задержкой. У этой группы наблюдали повышение толерантности к физическим нагрузкам, сердечно-
го резерва и улучшение клинической симптоматики. Двухкамерная стимуляция может уменьшить градиент выводного тракта и в педиатрической практике. Однако у некоторых пациентов эффективность кардиостимуляции снижается при высокой частоте предсердного ритма, быстром АВ-проведении и врожденных аномалиях митрального клапана.
В настоящее время практически отсутствуют доказательства, что электрокардиостимуляция останавливает дальнейшее прогрессирование заболевания и улучшает выживаемость или качество жизни. Кроме того, рутинная имплантация двухкамерного ЭКС не рекомендуется абсолютно всем пациентам с симп-томной гипертрофической обструктивной кардиомио-патией. Эффективность кардиостимуляции определяется главным образом выраженностью градиентов (более 30 мм рт. ст. в покое и более 50 мм рт. ст. при нагрузке) [16].
У крайне симптомных пациентов вместо двухкамерной кардиостимуляции предпочтительна септаль-ная миотомия или внутрикоронарная септальная спиртовая деструкция. Врачам-клиницистам необходимо выбрать оптимальный в перспективе метод лечения между имплантацией ЭКС и установкой кардиовер-тера-дефибриллятора пациентам с гипертрофической обструктивной кардиомиопатией с высоким риском внезапной смерти, несмотря на четкие показания к двухкамерной стимуляции [23].
Трансплантация сердца
Частота развития брадикардии после трансплантации сердца варьирует от 8% до 23% [15-17]. Боль-
Таблица 12.
Рекомендации для постоянной электрокардиостимуляции при гипертрофической кардиомиопатии
Класс I
1. Показания Класс I для дисфункции СПУ или атриовентрикулярной блокады, как описано выше. (Уровень доказанности: С)
Класс 11б
1. Устойчивая к медикаментозной терапии, проявляющаяся клинически гипертрофическая кардиомиопатия со значительным снижением фракции выброса ЛЖ в покое или при нагрузке. (Уровень доказанности: А)
Класс III
1. Пациенты с бессимптомным течением или при успешном медикаментозном контроле. (Уровень доказанности: С)
2. Пациенты, у которых есть симптомы, но отсутствуют признаки обструкции выводного отдела ЛЖ. (Уровень доказанности: С)
Таблица 13. Рекомендации по постоянной электрокардиостимуляции после трансплантации сердца
Класс I
1. Клинически проявляющиеся брадиаритмии/хронотропная некомпетентность, без прогноза к разрешению и другие показания Класса I для постоянной кардиостимуляции. (Уровень доказанности: С)
Класс 11б
1. Клинически проявляющиеся брадиаритмии/хронотропная некомпетентность, которые, несмотря на преходящий характер, могут персистировать и продолжаются после реабилитационного и восстановительного периодов. (Уровень доказанности: C)
2. При возникновении синкопальных состояний в послеоперационном периоде, если даже брадикардия не документирована. (Уровень доказанности: C)
шинство брадиаритмий связаны с дисфункцией СПУ. Некоторые программы по трансплантации предлагают использовать электрокардиостимуляцию у таких пациентов, так как с появлением симптомов затягивается восстановительный и реабилитационный период. В течение последующих 6-12 месяцев у 50% пациентов наблюдали разрешение брадиаритмий, поэтому многим пациентам постоянная электрокардиостимуляция необязательна. Выраженные брадиаритмия и асистолия нередко служили причиной внезапной смерти.
Предикторов развития послеоперационной брадикар-дии не выявлено. Некоторым пациентам требуется временная электрокардиостимуляция. Полноценный предсердный вклад обеспечивает эффективный сердечный выброс и хронотропную функцию, что улучшает состояние больного. Назначение таких препаратов, как теофиллин [15], может снизить необходимость в электростимуляции. После трансплантации лицам с необратимой дисфункцией СПУ и АВ-блокадой применимы показания класса I для имплантации ЭКС.
ЛИТЕРАТУРА
1. Бельгов В.С, Рихтер А.А., Савельев В.С, Савчук Б.Д. Имплантируемый электрокардиостимулятор. А. с. 169141, 5.04.65 СССР.
2. Бокерия Л.А., Ревишвили А.Ш., Левант А.Д. и др. Рекомендации для имплантации электрокардиостимуляторов при брадикардиях, 1993. УДК 616.12-008.314089.844
3. Бокерия Л.А., Ревишвили А.Ш. Катетерная абла-ция тахиаритмий: современное состояние проблемы и перспективы развития // Вестник аритмологии — 1998.-№8.- С.70.
4. Ревишвили А.Ш. Электрофизиологическая диагностика и хирургическое лечение наджелудочковых тахиаритмий// Кардиология 1990, №11- с. 56-59.
5. Akhtar M, Garan H, Lehmann MH, Troup PJ. Sudden cardiac death: management of high-risk patients. Ann Intern Med 1991; 114:499-512.
6. Amiodarone Trials Meta-Analysis Investigators. Effect of prophylactic amiodarone on mortality after acute myocardial infarction and in congestive heart failure: meta-analysis of individual data from 6500 patients in randomised trials. Lancet 1997; 350:1417-24.
7. Auricchio A, Stellbrink C, Block M, et al, for the Pacing Therapies for Congestive Heart Failure Study Group and the Guidant Congestive Heart Failure Research Group. Effect of pacing chamber and atrioventricular delay on acute systolic function of paced patients with congestive heart failure. Circulation 1999; 99:2993-3001.
8. Bardy GH, Yee R, Jung W, for the Active Can Investigators. Multicenter experience with a pectoral unipolar implantable cardioverter-defi brillator. J Am Coll Cardiol 1996;28:400-10.
9. Beller GA, Bonow RO, Fuster V. ACC revised recommendations for training in adult cardiovascular medicine: Core Cardiology Training II (COCATS 2). (Revision of the 1995 COCATS training statement.) J Am Coll Cardiol 2002;39:1242-6.
10. Bernstein AD, Fletcher RD, Hayes DL et al. The NASPE/BPEG generic pacemaker code for antibrady-cardia, adaptive-rate multisite pacing. PACE 2002; Vol. 25:260-264.
11. Buxton AE, Lee KL, Fisher JD, Josephson ME, Prys-towsky EN, Hafl ey G, for the Multicenter Unsustained Tachycardia Trial Investigators. A randomized study of the prevention of sudden death in patients with coronary artery disease. N Engl J Med 1999;341:1882-90.
12. Cairns JA, Connolly SJ, Roberts R, Gent M, for the Canadian Amiodarone Myocardial Infarction Arrhythmia Trial Investigators. Randomised trial of outcome after
myocardial infarction in patients
with frequent or repetitive ventricular premature depolari-sations: CAMIAT. Lancet 1997;349:675-82.
13. Cardiac Arrest in Seattle: Conventional versus Amiodarone Drug Evaluation (the CASCADE study). Am J Cardiol 1991;67:578-84.
14. Connolly SJ, Gent M, Roberts RS, et al. Canadian Implantable Defi brillator Study (CIDS) : a randomized trial of the implantable cardioverter defi brillator against amiodarone. Circulation 2000; 101:1297-302.
15. Fraser JD, Gillis AM, Irwin ME, Nishimura S, Tyers GF, Philippon F. Guidelines for pacemaker follow-up in Canada: a consensus statement of the Canadian Working Group on Cardiac Pacing. Can J Cardiol 2000;16:355-76.
16. Epstein A., DiMarco J., Ellenbogen K. et al. ACC/AHA/ HRS 2008 guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities: a Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation 2008;117:2820-2840.
17. Vardas P., Auricchio A. et al. Guidelines for cardiac pacing and cardiac recynchronization therapy. The Task Force for Cardiac Pacing and Cardiac Recynchronization Therapy of the European Society of Cardiology. Developed in Collaboration with the European Heart Rhythm Association. European Heart Journal (2007) 28, 2256-2295.
18. Hayes DL, Barold SS, Camm AJ, Goldschlager NF. Evolving indications for permanent cardiac pacing: an appraisal of the 1998 American College of Cardiology/ American Heart Association Guidelines. Am J Cardiol 1998;82:1082-6, A6.
19. Hayes DL, Naccarelli GV, Furman S, Parsonnet V. Report of the NASPE policy conference on training requirements for permanent pacemaker selection, implantation, and follow-up. North American Society of Pacing and Electrophysiology. PACE Pacing Clin Electrophysiol 1994;17:6-12.
20. Hunt SA, Baker DW, Chin MH, et al. ACC/AHA guidelines for the evaluation and management of chronic heart failure in the adult: executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Revise the 1995 Guidelines for the Evaluation and Management of Heart Failure), developed in collaboration with the International Society for Heart and Lung Transplantation, endorsed by the Heart Failure Society of America. J Am Coll Cardiol 2001;38:2101-13.
21. Julian DG, Camm AJ, Frangin G, et al, for the European Myocardial Infarct Amiodarone Trial Investigators. Randomized trial of effect of amiodarone on mortality in
patients with left-ventricular dysfunction after recent myocardial infarction: EMIAT. Lancet 1997;349:667-74.
22. Lamas GA, Lee K, Sweeney M, et al. The Mode Selection Trial (MOST) in sinus node dysfunction: design, rationale, and baseline characteristics of the fi rst 1000 patients. Am Heart J 2000; 140:541-51.
23. Maron BJ, Nishimura RA, McKenna WJ, Rakowski H, Josephson ME, Kieval RS. Assessment of permanent dual-chamber pacing as a treatment for drug-refractory symptomatic patients with obstructive hypertrophic car-diomyopathy: a randomized, doubleblind, crossover study (M-PATHY). Circulation 1999;99:2927-33.
24. John G.F. Cleland, M.D., Jean-Claude Daubert, M.D., Erland Erdmann, M.D., Nick Freemantle, Ph.D., Daniel Gras, M.D., Lukas Kappenberger, M.D., and Luigi Tavazzi,
M.D., for the Cardiac Resynchronization — Heart Failure (CARE-HF) Study Investigators. The Effect of Cardiac Resynchronization on Morbidity and Mortality in Heart Failure. N Engl J Med 2005; 352.
25. Recommendations for pacemaker prescription for symptomatic bradycardia: report of a working party of the British Pacing and Electrophysiology Group. Br Heart J 1991;66:185-91.
26. Ryan TJ, Antman EM, Brooks NH, et al. 1999 update: ACC/AHA guidelines for the management of patients with acute myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on Management of Acute Myocardial Infarction). J Am Coll Cardiol 1999;34:890-911.
Электрокардиостимулятор наружный ЭКСТАЙМ 2
Наружный двухкамерный электрокардиостимулятор DDD предназначен для стимуляции предсердий и желудочков и восприятия управляющих сигналов из обеих камер, обеспечивая при этом синхронизированную с предсердной активностью стимуляцию желудочков.
Может использоваться как однокамерный стимулятор в режиме VVI/AAI (demand) и режиме VOO/AOO (асинхронный).
Имеется светодиодная индикация, которая отображает статус чувствительности и стимуляции.
Если сопротивление электрода выходит за пределы оптимальных значений, то выдается звуковой и визуальный сигнал.
Экстайм-2 имеет цанговые зажимы, позволяющие использовать электроды диаметром от 0,9 до 2,0 мм. Для подсоединения к стимулятору постоянных электродов с коннектором IS-1 прилагается набор переходных кабелей с клипсами.
Специальные зажимы позволяют использовать временные электроды с диаметром контакта от 0,9 до 2,0 мм.
Индикация, измерение и статистика стимуляций и воспринятых событий.
Подсветка дисплея позволяет работать с прибором в условиях плохой видимости.
Блокировка клавиш исключает случайное нажатие.
Средний срок службы в стандартном режиме составляет не менее пяти лет.
Стимулятор надежно защищен чехлом из натуральной кожи.
Характеристики:
— Цанговые зажимы
— Совместимость с временными электродами с диаметром контактной части, мм от 0,9 мм до 2,0 мм.
— Индикация стимуляции и воспринятых событий;
— Подсветка дисплея для работы в затемненном помещении.
— Сигнал тревоги при отключении или повреждении электрода.
— Статистика стимуляции и воспринятых событий
— Измерение частоты стимуляции и воспринятых событий
— Блокировка клавиш от случайного нажатия
— Индикация разряда батареи
— Имеется в наличии защитный чехол, ремень для крепления на руке стимулятора и фиксации электрода, кабель пациента длиной 180 см
Режим стимуляции: DDD, VDD, DOO, AAI, AOO, VVI, VOO;
Частота стимулирующих импульсов, имп/мин: от 30 до 150 имп/мин с шагом 5 имп/мин;
Амплитуда A/V-стимулов, В: 0,5, 1,0, 1,5, 2,0, 2,5, 3,0, 3,5, 4,0, 5,0, 6,0, 7,0, 8,0, 10,0, 12,0, 14,0, 16,0.
Длительность A/V-стимулов, мс: 0,6
Чувствительность по А-каналу, мВ: от 0,3 до 4,8 мВ с шагом 0,3 мВ
Чувствительность по V-каналу, мВ: от 0,6 до 9,6 мВ с шагом 0,6 мВ
Рефрактерный период А канала, мс: от 200 до 660 мс с шагом 20 мс
Рефрактерный период V канала, мс: от 200 до 500 мс с шагом 20 мс
A-V задержка, мс: от 40 до 340 мс с шагом 20 мс
Диапазон частот функция быстрой стимуляции предсердий, имп/мин от 300 до 600 с шагом 10 имп/мин
Экстренный режим: VVI, 70 имп/мин, 8,0 В,
Временные функции:
— Маркеры стимулов и воспринятых сокращений
— Измерение импеданса электрода
— Измерение частоты стимуляции и воспринятых событий
— Быстрая стимуляция предсердий: от 300 до 600 имп/мин с шагом 10 имп/мин.
Габаритные размеры стимулятора: 130х75х26 мм.
Масса стимулятора без чехла: 170 г.
Cредний срок службы в режиме Стандарт D: не менее 5 лет
Электрокардиостимулятор носимый наружный СОБОЛЬ-1НМ
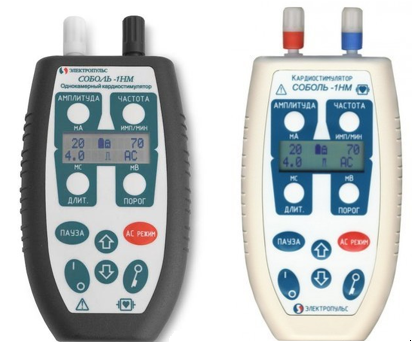
Предназначение:
Профилактики нарушений ритма сердца и проводимости у больных в раннем послеоперационном периоде после хирургических вмешательств на открытом сердце
Лечения пациентов с жизнеугрожающими брадикардиями вызванными синдромом синусового узла, A-V блокадой и другими заболеваниями
Соболь-1НМ обеспечивает электрокардиостимуляцию в режимах SOO, SSI по единому коду номенклатуры NGB-NASPE/BPEG
Параметры стимулирующих импульсов:
Амплитуда — 1-20мА. Дискретность установки амплитуды — 1 мА.;
Длительность — 0,5-4 мс. Дискретность установки длительности — 0,5 мс.;
Частота — 40-200 имп/мин. Дискретность установки частоты — 5 имп/мин.;
Время непрерывной работы Соболь-1НМ не менее 150 часов
Экстренное включение асинхронного режима стимуляции
Степень защиты от поражения электрическим током CF по ГОСТ МЭК 60601-1-2010
Защита от случайного изменения параметров
Электрокардиостимулятор эндокардиальной стимуляции наружный «ЭКС-Сетал-1В»
Электрокардиостимулятор эндокардиальной стимуляции наружный «ЭКС-Сетал-1В», предназначен для генерирования импульсов электрического тока с целью навязывания искусственного ритма сердцу в режимах: асинхронный ( AOO, VOO), деманд ( AAI, VVI).
Электрокардиостимулятор позволяет проводить два вида стимуляции в эндокардиальном режиме:
● лечебная электрокардиостимуляция: временная стимуляция желудочков при угрожающих жизни брадикардиях, а также при А-V блокадах;
● диагностическая электрокардиостимуляция: подбор медикаментозных средств при различных видах нарушений ритма сердца; определение параметров стимулирующих импульсов при имплантации постоянного водителя ритма.
Кардиостимулятор обеспечивает:
в режиме деманд осуществление подсчета количества навязанных стимулирующих сердечных сокращений по отношению их к общему числу и отображение результата на ЖК дисплее в виде процентов;
автоматическое включение энергосберегающего режима с фиксацией параметров стимуляции, и пробуждением по нажатию любой клавиши;
встроенный контроль расхода батареи питания;
звуковое предупреждение при разряде батареи каждые 5 мин (при этом сохранение работоспособности — не менее 6 часов);
блокировку случайного отключения прибора.
По устойчивости к воздействию внешних климатических факторов в процессе эксплуатации ЭКС соответствует требованиям категории 4.2 исполнения УХЛ по ГОСТ 15150
По устойчивости к механическим воздействиям в процессе эксплуатации ЭКС соответствует требованиям, предъявляемым для изделий группы 3 по ГОСТ Р 50444
Основные характеристики
Режимы работы: деманд (AAI,VVI) (*по требованию), асинхронный (A00,V00)
Частота стимуляции в режиме деманд (по требованию), [имп/мин]: 30-180 (с шагом 1 — обычное нажатие, с шагом 10 — непрерывное нажатие)
Порог срабатывания кардиостимулятора в режиме деманд, [мВ]: 0.5-10
Частота стимуляции в асинхронном режиме, [имп/мин]: 30-250 (с шагом 1 — обычное нажатие, с шагом 10 — непрерывное нажатие)
Амплитуда тока, [мА]: 0-15 (с шагом 1 — обычное нажатие, с шагом 2 — непрерывное нажатие)
Длительность импульса, [мс]: 1.5 ±0.01
Форма импульсов: прямоугольная, однополярная
Чувствительность, [мВ]: 0.5-10 (с шагом 1 — обычное нажатие, с шагом 2 — непрерывное нажатие)
Рефракторный период, [мс]: 280 ±0.1
Время готовности ЭКСк работе, [c] (не более): 1
Габаритные размеры, [мм] (не более): 150х75х30
Масса, [г] (не более): 250
Рабочая температура, [°C]: 20 ±5
Температура хранения, [°C]: 20
Влажность при хранении, [%]: 60 ±15
Атмосферное давление, [кПа]: от 84 до 106.7 (от 630 до 800 мм.рт.ст)
Тип элементов питания: MN 1500 / LR 6 / АА, 1.5 В
Время работы от элементов питания, [час] (не менее): 300 (*при рабочей частоте 60имп/мин и амплитуде 1мА)
Электрокардиостимулятор временный носимый одно – двухкамерный ЭКС-ВН-12 «Вектор-МС
Предназначен:
— Для проведения временной эндокардиальной стимуляции одной либо двух камер сердца у пациентов с нарушениями ритма.
Особенности:
— Определение качества установки электрода в камерах сердца без применения дополнительного оборудования — «интраоперационный тестер
— Отображение электрограммы для позиционирования электрода в камерах сердца без применения дополнительного оборудования.
— Оперативное определение возможности возникновения нежелательной стимуляции диафрагмального нерва или грудных мышц при высоких амплитудах импульсов стимуляции
Возможности:
— Стимуляция осуществляется бифазными асимметричными импульсами стабилизированного напряжения амплитудой от 0,1 В до 17 В.
— Режимы стимуляции S00 (A00, V00), SST (AAT, VVT), SSI (AAI, VVI), D00, VDD, DVI, DDD, экстренный и режим купирования.
Базовая частота, имп/мин: 30 — 250
Частота купирования, имп/мин: 60 — 1000
AV-задержка, мс: 15 — 400
— Для предотвращения ненамеренного изменения параметров, изменения режима или прекращения стимуляции в аппарате предусмотрен переключатель блокировки клавиатуры. Нажатия любой кнопки обрабатывается только при отключении блокировки клавиатуры.
— Индикация импульсов стимуляции осуществляется с помощью жёлтых светодиодов.
— Детектированные сигналы спонтанной активности сердца индицируются с помощью зелёных светодиодов.
— Низкий остаточный заряда батареи индицируется с помощью мерцания красного светодиода и звукового сигнала.
— Масса аппарата вместе с элементом питания не более 230 — 250 граммов (в зависимости от модели элемента питания)
Электропитание
— Осуществляется от стандартного элемента питания типа 6F22
— Время замены элемента питания без остановки стимуляции не более 30 секунд.
Электрод эндокардиальный временный для наружных электрокардиостимуляторов ЭЛВИ без стилета
Конфигурация дистального конца обеспечивает легкое проведение электрода и удаление при деимплантации, а также оптимальное позиционирование в правом желудочке. Атравматическим кончик особой формы обеспечивает надежный и безопасный контакт с сердечной мышцей. Несмываемые метки по всей длине и трубка, прекрасно видная под рентгеном, обеспечивает полный контроль имплантации. Защитные колпачки обеспечивают безопасность от попадания на электрод статического электричества. Рабочие контакты электрода совместимы с разъемом большинства моделей наружных электрокардиостимуляторов. Общая длина электрода дает возможность доступа в эндокард через бедренную вену.
Электрод эндокардиальный временный для наружных электрокардиостимуляторов ЭЛВИ со стилетом
Использование направителя и хорошая рентгеноконтрастность обеспечивают легкое проведение и оптимальное позиционирование электрода. Водонепроницаемый клапан обеспечивает безопасную работу электрода при попадании на него жидкости. Защитные колпачки обеспечивают безопасность от попадания на электрод статического электричества. Рабочие контакты электрода совместимы с разъемом большинства моделей наружных электрокардиостимуляторов.
Провод-электрод временный индифферентный ПЭВИ-5
Длина, мм: 700
Диаметр рабочей головки, мм: 1.5
Диаметр провода, мм: 0.75
Электрическое сопротивление электрода постоянному току в нормальных климатических условиях, Ом: 50
Материал токопроводящей жилы: сплав CoCrNi
Материал изоляции: полиэтилен
Электрод эндокардиальный монополярный для временной стимуляции сердечной деятельности ЭПВП
Электрод ЭПВП предназначен для кратковременной стимуляции сердечной деятельности, передачи стимулирующего электрического сигнала от наружного кардиостимулятора на внутреннюю часть сердца (эндокарда).
Вводится в полость сердца трансвенозно через пункционную иглу или вводное устройство.
Для непосредственной передачи электрического сигнала на участок мышечной ткани служит головка (*1), выполненная из биологически инертного материала и соединенная герметично с токопроводящей жилой механическим обжатием или сваркой.
Провод (*2) служит для передачи электрического сигнала от кардиостимулятора к головке и представляет собой спираль из двух проволок, заправленную в изоляционную полиэтиленовую трубку.
Спиральная жила имеет внутренний канал для прохождения специального направителя (*4), с помощью которого придается жесткость электроду при его введении.
Дистальный наконечник (*3) служит для подключения к кардиостимулятору.
Концентрическая выточка обеспечивает надежное соединение и предохраняет от случайного выдергивания провода.
После введения электрода в сердце и достижения надежного контакта головки с областью сердца, направитель удаляется, дистальный наконечник вставляется в гнездо зажима таким образом, чтобы концентрическая веточка наконечника вошла в выступ контактной части.
Стерилизация: выдержка в 6% р-ре перекиси водорода ГОСТ 177-88 при температуре
50±2°С в течение 180±5 мин. согласно ОСТ 42-21-2-85
Характеристики
Длина, мм: 900
Диаметр рабочей головки, мм: 1.5
Площадь контактного электрода, мм: 32
Номинальное напряжение, В: 6
Электрическое сопротивление электрода постоянному току в нормальных клЭлектрод ЭЛВИ 214-100 предназначен для проведения временной эндокардиальной лечебной стимуляции желудочка сердца. Электрод используется совместно с наружным кардиостимулятором. Электрод не предназначен для повторного использования.
Использование направителя (стилета) и чёткая ренгеноконтрастность обеспечивают лёгкое проведение и оптимальное позиционирование электрода.
Защитные колпачки на штекерах и водонепроницаемый клапан для введения направителя обеспечивают повышенную безопасность.
Изодиаметрическая форма дистального конца электрода обеспечивает легкое удаление при деимплантации.
Характеристики
Длина, мм: 1000
Длина для имплантации, мм: 800
Диаметр электрода, F: 5.4
Коннектор: установленные постоянно однополюсные штекеры Ø2 мм с разноцветными корпусами «-» чёрный, «+» красный
Катод «-«: цилиндр с полусферой (5.7 F)
Площадь, мм2: 12
Анод «+»: цилиндр (5.4 F)
Площадь, мм2: 22
Расстояние между катодом и анодом, мм: 10
Электрическое сопротивление (не менее), Ом: 50
Материал токопроводящей жилы: Cr Ni Fe
Материал изоляции: полиэтилен ренгеноконтрастный
Рекомендуемый интродюсер, F: 6-7иматических условиях, Ом: 100
Материал токопроводящей жилы: сплав CoCrNi
Материал изоляции: полиэтилен
Температурный диапазон использования электродов, °C: +20 — +50
Электрод эндокардиальный биполярный временный для наружных электрокардиостимуляторов ЭЛВИ 214–100
Провод-электрод для кардиостимуляции деятельности чреспищеводный ПЭДCП-2
ПЭДСП-2 предназначен для диагностики сердечной проводимости и проведения бифокальной электростимуляции сердца через пищевод. Область применения кардиологические и кардио-хирургические отделения больниц и клиник.
Провод-электрод состоит из неподвижного и подвижного электродов.
Подвижный электрод представляет собой отрезок провода, армированного с одного конца контактным элементом шаровидной формы (*1), а с другого- штырем для подключения к электростимулятору. Провод имеет канал для введения направителя (*7).
Неподвижный электрод выполнен из провода, армированного контактным элементом шаровидной формы (*2) и штырем (*8) для подключения к электро-кардиостимулятору.
Провод-электрод снабжен двумя фиксирующими устройствами,первое из которых (*4) фиксирует за-данное положение подвижного электрода вовремя записи ЭКГ или электрокардиостимуляции. Второе фиксирующее устройство (*6) необходимо для разборки провода-электрода с целью промывки от слизи.
Вспомогательные принадлежности: Направитель – 1 шт.
Характеристики
Длина рабочей части подвижного электрода, мм: 700±5
Длина рабочей части неподвижного электрода, мм: 500± 5
Диаметр контактного элемента подвижного и неподвижногоэлектродов, мм: 4, 5
Электрическое сопротивление провода-электрода постоянному току ,Ом: 180
Материал токопроводящей жилы: сплав Сo Cr Ni
Материал изоляции: полиэтилен
Средний ресурс, ч: 500
Провод-электрод диагностический многоконтактный кардиологический ПЭДМ-2
ПЭДМ-2 предназначен для проведения внутрисердечных исследований.
ПЭДМ-2 представляет собой отрезок провода, армированный с одного конца контактами, а c другой на конце расположен распределитель со штырями. В канал распределителя введен направитель, служащий для проведения провода-электрода по венам к сердцу.
Характеристики
Рабочая длина, мм: 1200
Наружный диаметр, мм: 2.3
Диаметр штекера, мм: 2
Расстояние между контактами, мм: 10
Количество электрических контактов, шт: 2
Электрическое сопротивление электрода постоянному току, Ом: 250
Материал токопроводящей жилы: сплав Co Cr Ni
Материал изоляции: полиэтилен
Провод-электрод диагностический многоконтактный кардиологический ПЭДМ-6
Провод-электрод ПЭДМ-6 предназначен для проведения внутрисердечных исследований.
ПЭДМ-6 представляет собой отрезок провода, армированный с одного конца контактами, а c другой на конце расположен распределитель со штырями. В канал распределителя введен направитель, служащий для проведения провода-электрода по венам к сердцу.
Характеристики
Рабочая длина, мм: 1200
Наружный диаметр, мм: 2.3
Диаметр штекера, мм: 2
Расстояние между контактами, мм: 10
Количество электрических контактов, шт: 6
Электрическое сопротивление электрода постоянному току, Ом: 250
Материал токопроводящей жилы: сплав Co Cr Ni
Материал изоляции: полиэтилен
Провод-электрод диагностический многоконтактный кардиологический ПЭДМ-9
ПЭДМ-9 предназначен для проведения внутрисердечных исследований.
Электрод представляет собой отрезок провода, армированный с одного конца контактами, а c другой в конце расположен распределитель со штырями.
В канал распределителя введен направитель, служащий для проведения провода-электрода по венам к сердцу.
Электрод ПЭДМ-9 имеет 9 полюсов, 2 из которых используются для стимуляции, а остальные 7 для регистрации с помощью электрокардиографа (кабель отведений должен иметь штырьковые 4 мм выводы).
Провод-электрод ПЭДМ соответствует ТУУ 33.1-00217107-016:2007 и признан годным к эксплуатации.
Характеристики
Рабочая длина, мм: 1200
Наружный диаметр, мм: 2.3
Диаметр штекера, мм: 2
Расстояние между контактами, мм: 10
Количество электрических контактов, шт: 9
Электрическое сопротивление электрода постоянному току, Ом: 250
Материал токопроводящей жилы: сплав Co Cr Ni
Материал изоляции: полиэтилен
Купить электрокардиостимуляторы, Наружные электрокардиостимуляторы, медицинское оборудование у нас на сайте вы можете заполнив заявку в свободной форме на почту Этот адрес электронной почты защищён от спам-ботов. У вас должен быть включен JavaScript для просмотра. или же позвонив по телефону +7 (343) 361-44-98.
электрокардиостимуляторы, Наружные электрокардиостимуляторы, медицинское оборудование и другие медицинские товары в разделе каталоги
Об операции
Электрокардиостимулятор – это небольшой прибор (искусственный водитель ритма), который создает электрические импульсы и направляет их в камеры сердца, заставляя сокращаться в определённом порядке, синхронизируя работу предсердий и желудочков. Кардиостимулятор устраняет редкий ритм сердца и препятствует его остановке.
Прибор состоит из генератора и электродов. Генератор формирует электрические импульсы. Электроды проводят импульсы от генератора к камерам сердца, на которые необходимо воздействовать. В зависимости от ЭКС, электродов может быть от одного до трёх. Аппарат весит 30-50 грамм, оснащён аккумулятором и микросхемой. Устанавливается хирургом-аритмологом через небольшой разрез в верхней части грудной клетки. Корпус состоит из титанового покрытия, поэтому риск отторжения минимален. Вся информация из ЭКС направляется на стационарный компьютер лечебного учреждения, где устанавливали прибор. С его помощью врач отслеживает самочувствие пациента, работу ЭКС, при необходимости производит изменения в настройках аппарата.
Электрокардиостимуляторы бывают нескольких видов:
- Однокамерный – контролирует и стимулирует только одну полость сердца (предсердие или желудочек). Не способен имитировать физиологическое сокращение сердечной мышцы;
- Двухкамерный – соединяет генератор через электроды одновременно с предсердием и желудочком. При возникновении потребности в стимуляции, генератор последовательно направляет импульсы от предсердия к желудочкам, восстанавливая нормальное сокращение миокарда;
- Трехкамерный – предназначен для синхронизации желудочков сердца. Электроды направляют в правое предсердие и оба желудочка. В основном применятся при лечении хронической сердечной недостаточности.
По функциональности ЭКС выделяют:
- кардиостимуляторы – задают сердцу правильный ритм;
- дефибрилляторы-кардиовертеры – помимо навязывания правильного ритма, могут купировать приступы аритмии и фибрилляцию желудочков.
В современных электрокардиостимуляторах установлен тип работы «по требованию». Прибор автоматически отслеживает сердечный ритм. Если частота сердечных сокращений в норме, прибор не посылает импульсы. В случае затянувшейся паузы (свыше пороговой величины), прибор подает сигнал в миокард.
Также существуют временные ЭКС, которые используют при угрожающих жизни состояниях. В такой ситуации генератор не вшивается под кожу, а располагается вне тела пациента. Также временный ЭКС могут использовать до установки постоянного водителя ритма или для снятия приступа, который может исчезнуть (например, при передозировке лекарственными препаратами). Процедура проводится только в стационаре под постоянным присмотром специалистов.
В некоторых случаях установка ЭКС – единственная возможность сохранить здоровье и жизнь пациента.
Преимущества имплантации электрокардиостимулятора
снижение риска смерти из-за неправильной работы сердца
восстановление нормального ритма сердца
восстановление работоспособности
возможность избежать инвалидности
Показания к имплантации
Когда медикаментозного лечения недостаточно, кардиолог рекомендует имплантацию электрокардиостимулятора. Операция предназначена для лечения заболеваний:
- брадикардия, сопровождающаяся постоянными обмороками, потерей сознания, головокружением, низким пульсом при физических нагрузках;
- мерцательная аритмия;
- АВ-блокады сердца с клиническими проявлениями;
- синдром слабости синусового узла;
- кардиомиопатия с нарушением сократительной функции миокарда;
- хроническая сердечная недостаточность.
К относительным показаниям относятся:
- АВ-блокады сердца без клинических проявлений;
- обморочные состояния, не связанные с полной поперечной блокадой или желудочковыми тахикардиями, но другой причины состояния установить не удается.
В данном случае решение об имплантации принимается врачом индивидуально по каждому пациенту с учётом физиологических особенностей и наличия сопутствующих патологий.
Фактически противопоказаний к установке ЭКС нет. Отложить операцию могут из-за вирусных или инфекционных заболеваний. После лечения сопутствующей патологии операция проводится в плановом режиме после проведения обследований.
Подготовка к операции
Перед операцией больному необходимо пройти полное обследование и сдать перечень анализов. Наш кардиологический центр ФНКЦ ФМБА предлагает своим пациентам плановую госпитализацию. Во время пребывания в отделении сердечно-сосудистой хирургии вам проведут все необходимые исследования. В перечень обследования входит:
- клинический и биохимический анализ крови (общий белок, креатинин, мочевина, общий билирубин, прямой билирубин, глюкоза, панкреатическая амилаза);
- определение группы крови и резус-фактора;
- развёрнутая коагулограмма;
- показатель АДФ агрегации тромбоцитов;
- маркеры инфекций: ВИЧ, гепатит В, гепатит С, сифилис;
- общий анализ мочи;
- рентген органов грудной клетки;
- ЭКГ;
- ЭхоКГ;
- ЭГДС;
- УЗДС брахиоцефальных артерий;
- УЗДС артерий нижних конечностей и вен нижних конечностей;
- ФВД;
- УЗИ внутренних органов;
- ЧПЭхоКГ;
- коронарографию.
Если во время обследования врач обнаружит сопутствующую патологию, вам могут назначить дополнительные анализы и консультацию смежных специалистов (невролог, офтальмолог, эндокринолог и др.).
В нашем Центре установлено высокоточное современное оборудование. Благодаря большому опыту и многолетнему стажу работы врачи гарантируют максимально точную диагностику и расшифровку показателей. Собственный клинико-диагностический центр отвечает за точность результатов анализов. Проходя у нас обследование перед имплантацией ЭКС, вы можете быть уверены в качестве оказываемых услуг и скорости их предоставления. Сбор всех необходимых исследований может занять месяцы, в то время как мы подготовим вас к операции всего за 1 день.
Перед операцией пациенту необходимо подготовиться, для этого достаточно придерживаться простых рекомендаций:
- за несколько дней до операции врач может отменить приём лекарственных препаратов. Алкоголь необходимо исключить (желательно за неделю);
- в день перед имплантацией ЭКС пациент завтракает и обедает, как обычно. Вечером приносят лёгкий ужин, последний приём пищи должен быть не позднее, чем за 6-8 часов до операции. Пить воду можно в неограниченном количестве;
- на ночь пациенту ставят очистительную клизму;
- с утра пациент принимает душ и подготавливает операционное поле: необходимо сбрить волосы в области груди.
Перед тем, как пациента отвозят в операционную, его осматривает хирург и анестезиолог. Может быть введено мягкое седативное средство для успокоения и снятия тревожности.
Проведение имплантации электрокардиостимулятора
Операция по имплантации электрокардиостимулятора проводится под местным наркозом. Время установки кардиостимулятора зависит от его вида. Процедура может занять около получаса при установке однокамерного ЭКС, при установке трёхкамерного – до 2,5 часов. Если пациент правша, кардиостимулятор устанавливают в левую подключичную область, если левша – в правую. Это позволяет снизить влияние ЭКС на рабочую руку.
Кардиохирург и ассистирующий персонал проводят следующие действия:
- хирургическое поле обрабатывается антисептиками и обезболивается;
- хирург проводит небольшой разрез около 5 см под ключицей, формирует карман для имплантации ЭКС. Карман может находиться под большой грудной мышцей или над ней, место определяет хирург;
- из разреза специальной иглой пунктируют (прокалывают) подключичную вену;
- в вену через иглу вводят проводник в полость сердца, врач контролирует движение проводника с помощью рентгенологической установки;
- игла удаляется и по проводнику в вену вставляется интрадьюсер (пластиковая трубка). В зависимости от вида ЭКС (при необходимости ввести два или три электрода) дополнительный интрадьюсер проводится по тому же пути или через прокол другой вены;
- проводник удаляется;
- по интрадьюсеру в полость сердца заводят один или несколько электродов. Электроды крепятся к внутренней оболочке сердца с помощью крючков на конце электрода или с помощью специального крепления, которое напоминает штопор (электрод будто вкручивается во внутреннюю оболочку);
- когда электроды установлены в нужном месте, интрадьюсер удаляется;
- врач подключает другой конец электродов к кардиостимулятору;
- кардиостимулятор имплантируется в сформированный ранее карман под ключицей;
- рана зашивается;
- накладывается асептическая повязка;
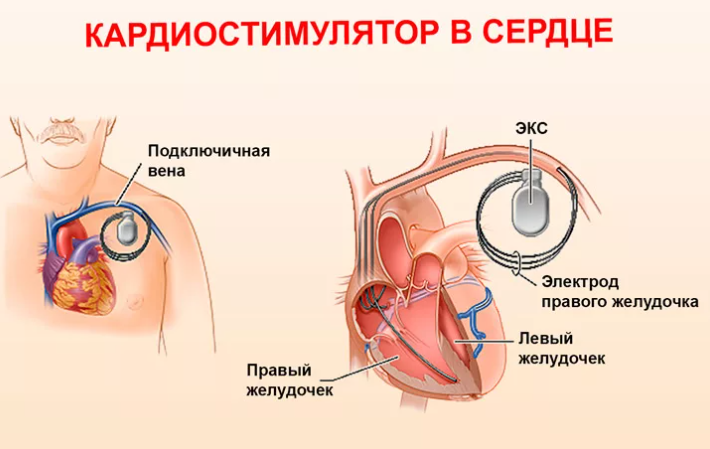
После операции
Пациент в течение недели находится под присмотром медицинского персонала. За это время швы заживают, их можно снимать. Пациент готовится к выписке. Перед тем, как отпустить пациента домой, его осматривает врач: делает назначения и выдает памятку о том, как вести себя в период реабилитации и после.
После выписки пациент встает на учёт по месту жительства и своевременно посещает врача. В первые три месяца важно соблюдать рекомендации:
- временно отказаться от физической активности;
- нельзя поднимать тяжести;
- нельзя садиться за руль;
- нельзя делать МРТ;
- избегать радиолокационную технику;
- отказаться от тепловых процедур;
- о любых недомоганиях сообщать врачу.
Следующие полгода необходимо планово посещать кардиолога. Разрешено пользоваться бытовыми приборами. Включать их нужно противоположной рукой к установленному кардиостимулятору, в том числе при разговоре по телефону, прикладывать телефон к противоположной стороне от установленного ЭКС. Необходимо избегать металлодетекторов в магазине, аэропортах, концертных залах.
Пожизненные правила после имплантации ЭКС:
- ежемесячное посещение кардиолога;
- ежедневное измерение давления и пульса, желательно вести дневник и помечать данные;
- полный отказ от пагубных привычек;
- носить при себе паспорт электрокардиостимулятора.
Стоимость имплантации ЭКС
Стоимость зависит от исходного состояния пациента, наличия сопутствующих заболеваний, объёма предстоящего оперативного вмешательства.
Окончательная стоимость складывается из:
- предоперационных обследований и анализов, если пациент не сделал их самостоятельно до госпитализации;
- стоимости самой операции (указана в прайсе ниже);
- вида необходимого электрокардиостимулятора (устройство стоит от 80 000 до 450 000 рублей);
- количества расходных материалов и инструментов для проведения операции;
- анестезии;
- медикаментозного лечения и лекарственных препаратов;
- категории выбранной палаты и количества дней, проведенных в клинике.
Многофункциональный центр ФНКЦ ФМБА предлагает своим пациентам услуги по удалённому контролю за работой электрокардиостимулятора.
Наша клиника гарантирует своим пациентам многопрофильную помощь при лечении сердечно-сосудистых заболеваний по индивидуальным программам. Инновационное оснащение Центра позволяет провести качественную диагностику и предоставить эффективное лечение. Операции проводятся высококвалифицированными врачами с большим практическим опытом. В своей работе мы используем высокоточное и современное оборудование, расходные материалы европейских производителей.
Обратитесь за консультацией к нашим специалистам или запишитесь на приём с помощью специальной формы на сайте или по телефону центра.
Электрокардиостимуля́тор (ЭКС) или просто кардиостимулятор, также иску́сственный води́тель ри́тма (ИВР) — медицинский прибор, предназначенный для воздействия на ритм сердца.
| Электрокардиостимулятор | |
|---|---|
| Состояние здоровья | аритмия, атриовентрикулярная блокада и брадикардия |
| Код в Гармонизированной системе | 902150[1] |
| Медиафайлы на Викискладе |
Основной задачей кардиостимулятора (водителя ритма) является поддержание или навязывание частоты сердечных сокращений пациенту, у которого сердце бьётся недостаточно часто или имеется электрофизиологическое разобщение между предсердиями и желудочками (атриовентрикулярная блокада). Также имеются специальные (диагностические) наружные кардиостимуляторы для проведения нагрузочных функциональных проб.
История создания электрокардиостимуляторов
править
Впервые способность импульсов электрического тока вызвать сокращения мышцы заметил итальянец Гальвани. Позднее советские физиологи В. Ю. Чаговец и Н. Е. Введенский изучили особенности воздействия электрического импульса на сердце и предположили возможность использования их для лечения некоторых заболеваний сердца. В 1932 году Альберт Хаймен (Albert Hyman) создал первый в мире наружный электрокардиостимулятор и применил его в клинике для лечения больного, страдающего редким пульсом и потерями сознания. Это сочетание известно как синдром Морганьи — Адамса — Стокса (МЭС).
В 1951 году американские кардиохирурги Каллаган и Бигелоу использовали кардиостимулятор для лечения больной после операции, так как у неё развилась полная поперечная блокада сердца с редким ритмом и приступами МЭС. Однако у данного прибора имелся большой недостаток — он находился вне тела пациента, и импульсы к сердцу проводились по проводам через кожу.
В 1958 году шведские учёные (в частности, Руне Элмквист) создали имплантируемый, то есть полностью находящийся под кожей, кардиостимулятор (Siemens-Elema). Первые стимуляторы были недолговечными: их срок службы составлял от 12 до 24 месяцев.
В СССР история кардиостимуляции ведёт отсчёт с 1960 года, когда академик А. Н. Бакулев обратился к ведущим конструкторам страны с предложением о разработке медицинских аппаратов. И тогда в конструкторском бюро точного машиностроения (КБТМ) — ведущем предприятии оборонной отрасли, возглавлявшемся А. Э. Нудельманом, — начались первые разработки имплантируемых ЭКС (А. А. Рихтер, В. Е. Бельгов). В декабре 1961 года первый созданный в СССР стимулятор, ЭКС-2 («Москит»), был имплантирован академиком А. Н. Бакулевым больной с полной атриовентрикулярной блокадой.
- Аритмия сердца
- Синдром слабости синусового узла (СССУ)
- Атриовентрикулярная блокада
Наружная кардиостимуляция может быть использована для первичной стабилизации больного, но она не исключает имплантацию постоянного кардиостимулятора. Методика заключается в размещении двух пластин стимулятора на поверхности грудной клетки. Один из них обычно располагается на верхней части грудины, второй — слева сзади практически на уровне последних ребер. При прохождении электрического разряда между двумя пластинами он вызывает сокращение всех мышц, расположенных на его пути, в том числе сердца и мышц грудной стенки.
Пациент с наружным стимулятором не может быть оставлен без присмотра на длительное время. Если пациент находится в сознании, применение этого вида стимуляции вызовет у него дискомфорт вследствие частого сокращения мышц грудной стенки. К тому же стимуляция мышц грудной стенки ещё не означает стимуляцию сердечной мышцы. В целом метод недостаточно надёжен, поэтому применяется редко.
Временная эндокардиальная стимуляция (ВЭКС)
править
Стимуляция производится через зонд-электрод, проведённый по центральному венозному катетеру в полость сердца. Операция установки зонда-электрода проводится в стерильных условиях, наилучшим вариантом является использование для этого одноразовых стерильных наборов, включающих собственно зонд-электрод и средства его доставки. Дистальный конец электрода устанавливается в правом предсердии или правом желудочке. Проксимальный конец снабжен двумя универсальными клеммами для подключения к любому пригодному наружному стимулятору.
Временная кардиостимуляция часто используется для спасения жизни пациента, в том числе как первый этап перед имплантацией постоянного водителя ритма. При определённых обстоятельствах (например в случае острого инфаркта миокарда с преходящими нарушениями ритма и проводимости или в случае временных нарушений ритма/проводимости вследствие передозировки медикаментов) пациент после осуществления временной стимуляции не будет переведён на постоянную.
Имплантация постоянного кардиостимулятора
править
Имплантация постоянного водителя ритма — это малое оперативное вмешательство, оно проводится в рентгеноперационной. Пациенту не осуществляется наркоз, производится только местное обезболивание в области операции. Операция включает несколько этапов: разрез кожи и подкожной клетчатки, выделение одной из вен (чаще всего — латеральной подкожной вены руки, она же v. cephalica), проведение через вену одного или более электродов в камеры сердца под рентгеновским контролем, проверку параметров установленных электродов с помощью наружного прибора (определение порога стимуляции, чувствительности и др.), фиксацию электродов в вене, формирование в подкожной клетчатке ложа для корпуса кардиостимулятора, подключение стимулятора к электродам, ушивание раны.
Обычно корпус стимулятора располагают под подкожной жировой клетчаткой грудной клетки. В России принято имплантировать стимуляторы слева (правшам) или справа (левшам и в ряде других случаев — например при наличии рубцов кожи слева), хотя вопрос о размещении решается в каждом случае индивидуально. Наружная оболочка стимулятора крайне редко вызывает отторжение, так как её изготавливают из титана или специального сплава, являющегося инертным для тела.
Чреспищеводная кардиостимуляция
править
Для диагностических целей иногда применяется также метод чреспищеводной электрокардиостимуляции (ЧПЭС) В зависимости от целей исследования можно выделить два варианта проведения исследования:
- стресс-тест для сердечно-сосудистой системы (цель — выявление ИБС);
- неинвазивное электрофизиологическое исследование сердца.
Зачастую оба варианта проведения исследования могут выполняться последовательно одному и тому же пациенту.
Стресс тест для сердечно сосудистой системы проводится как замена нагрузочной велоэргометрической или тредмил-пробы. Смысл данного исследования состоит в том, что с помощью стимуляции сердцу навязывается более высокая частота ритма, большая, чем естественная частота работы сердца пациента в покое. Обычно это последовательные включения стимулятора длительностью от 20 до 60 сек. с частотой, соответственно, 100, 120, 140, и 160 в 1 мин. Таким образом, сердце работает с повышенной частотой, вследствие чего имитируется совершение пациентом физической нагрузки, что позволяет выявить наличие ИБС и определить предположительную тяжесть заболевания.
Неинвазивное электрофизиологическое исследование сердца применяется у пациентов с подозрением на нарушения функции синусового узла, у пациентов с преходящими нарушениями атривентрикулярной проводимости, пароксизмальными нарушениями ритма, подозрением на наличие дополнительных проводящих путей (ДПП).
Пациент лежит на кушетке. Через нос (реже — через рот) ему вводят в пищевод специальный двух- или трёхполюсный зонд-электрод, устанавливают этот зонд в пищеводе на уровне, где с пищеводом соприкасается левое предсердие. В этой позиции осуществляют стимуляцию импульсами напряжением, как правило, от 5 до 15 В, близость левого предсердия к пищеводу позволяет навязать таким образом ритм сердцу.
В качестве водителя ритма используются специальные наружные приборы-кардиостимуляторы, например ЧЭЭКСП. В настоящее время все большее распространение получают не отдельные стимуляторы,а комплексные системы на базе ПК, включающие стимуляторы и систему наблюдения ЭКГ.
Стимуляция проводится по разным методикам с разной целью. Принципиально существует учащающая стимуляция (частоты близки к частотам собственного ритма), частая (от 140 до 300 имп./мин.), сверхчастая (от 300 до 1000 имп./мин.), а также программированная (в этом случае выдается не «сплошной ряд» стимулов, а их группы («пачки», «залпы», в англоязычной терминологии burst) с разной частотой, запрограммированные по специальному алгоритму).
Чреспищеводная стимуляция является относительно безопасным методом диагностики, так как воздействие на сердце происходит кратковременно и мгновенно прекращается при выключении стимулятора. Стимуляция с частотами более 170 имп./мин. производится в течение 1—2 сек., что также вполне безопасно.
Тем не менее, в процессе выполнения исследования в некоторых случаях возможно развитие осложнений, таких например как индукция тяжелых аритмий в виде желудочковых тахикардий или фибрилляции предсердий с высокой частотой проведения к желудочкам. Последнее особенно опасно у пациентов с WPW-синдромом, имеющих высокоактивные ДПЖС (дополнительные предсердно-желудочковые соединения), так как может привести к развитию фибрилляции желудочков, остановке кровообращения и смерти пациента. Именно поэтому кабинет для проведения ЧПЭС должен быть в обязательном порядке оснащен дефибриллятором.
Могут также развиваться и менее тяжелые осложнения, такие, как носовые кровотечения, ущемление зонда-электрода в носовых ходах, затянувшийся приступ стенокардии, редко — ОНМК вследствие повышения АД в связи с негативной эмоциональной реакцией пациента на исследование.
Диагностическая эффективность ЧПЭС при различных заболеваниях различна. Поэтому исследование проводится только по строгим показаниям. В случаях, когда ЧПЭС не дает полной и/или исчерпывающей информации, пациенту приходится проводить инвазивное ЭФИ сердца, что существенно труднее и дороже, проводится в условиях рентгеноперационной и сопряжено с введением катетера-электрода в полость сердца.
Методом чреспищеводной электростимуляции иногда осуществляется и лечение: купирование пароксизмального трепетания предсердий (но не мерцательной аритмии) или некоторых видов наджелудочковых пароксизмальных тахикардий, также может использоваться в качестве временной электрокардиостимуляции при брадиаритмиях, сопровождающихся редким пульсом, таких, как синдром слабости синусового узла и полная AV-блокада (III степени). В последнем случае должна выполняться чреспищеводная желудочковая стимуляция, которая, в отличие от предсердной, требует большей энергии стимуляции и более глубокого положения зонда в пищеводе.
Основные функции кардиостимулятора
править
Кардиостимулятор представляет собой прибор в герметичном металлическом корпусе небольшого размера. В корпусе располагается батарея и микропроцессорный блок. Все современные стимуляторы воспринимают собственную электрическую активность (ритм) сердца, и если возникает пауза либо иное нарушение ритма/проводимости в течение определенного времени, прибор начинает генерировать импульсы для стимуляции миокарда. В противном случае — при наличии адекватного собственного ритма — кардиостимулятор импульсов не генерирует. Эта функция ранее называлась «по требованию» или «on demand».
Энергия импульсов измеряется в джоулях, однако на практике применяется шкала напряжения (в вольтах) для имплантируемых кардиостимуляторов и шкалы напряжения (в вольтах) или тока (в амперах) — для наружных стимуляторов.
Существуют имплантируемые кардиостимуляторы с функцией частотной адаптации. Они снабжены сенсором, воспринимающим физическую активность пациента. Чаще всего сенсор — это акселерометр, датчик ускорений. Однако встречаются также сенсоры, определяющие физическую активность в соответствии с минутной вентиляцией легких или по изменению параметров электрокардиограммы (интервала QT) и некоторые другие. Информация о движении тела человека, полученная с сенсора, после обработки процессором стимулятора управляет частотой стимуляции, позволяя адаптировать её к потребностям пациента во время физической нагрузки.
Некоторые модели кардиостимуляторов могут отчасти предупреждать возникновение аритмии (фибрилляцию и трепетание предсердий, пароксизмальные наджелудочковые тахикардии и др.) за счет специальных режимов стимуляции, в том числе overdrive pacing (принудительного учащения ритма относительно собственного ритма пациента) и прочих. Но показано, что эффективность этой функции невелика, следовательно, наличие кардиостимулятора в общем случае не гарантирует устранения аритмии.
Современные электрокардиостимуляторы могут накапливать и сохранять данные о работе сердца. В последующем врач с помощью специального компьютерного аппарата — программатора — может считать эти данные и проанализировать ритм сердца, его нарушения. Это помогает назначить грамотное медикаментозное лечение и подобрать индивидуальные параметры стимуляции. Проверка работы имплантированного кардиостимулятора с программатором должна производиться не реже 1 раза в 6 месяцев, иногда — и чаще.
Система маркировки стимуляторов
править
Кардиостимуляторы бывают однокамерные (для стимуляции только желудочка или только предсердия, один провод), двухкамерные (для стимуляции и предсердия и желудочка, два провода) и трёхкамерные (для проведения стимуляции правого предсердия и обоих желудочков, три провода). Кроме того применяются имплантируемые кардиовертеры-дефибрилляторы.
В 1974 году была выработана система трёхбуквенных кодов для описания функций стимуляторов. По разработчику код назван ICHD (Intersociety Commission on Heart Disease).
В последующем создание новых моделей ЭКС привело к появлению пятибуквенного кода ICHD и его трансформации затем в пятибуквенный код имплантируемых систем электрического воздействия на ритм сердца —- ЭКС, кардиовертеров и дефибрилляторов в соответствии с рекомендациями Британской группы по изучению электрокардиостимуляции и электрофизиологии (British Pacing and Electrophysiology Group — BREG) и Северо-Американского общества электрокардиостимуляции и электрофизиологии (North American Society of Pacing and Electrophysiology — NASPE). Окончательный действующий ныне код называется NASPE/BREG (NBG).
В России традиционно применяется нечто вроде комбинированной кодировки: для режимов стимуляции, не имеющих частотной адаптации, применяется трехбуквенный код ICHD, а для режимов с частотной адаптацией — первые 4 буквы кода NASPE/BREG (NBG).
Согласно коду NBG:
| Номер позиции | 1 | 2 | 3 | 4 | 5 |
| Категория | Стимулируемая камера | Детектируемая камера | Ответ на воспринятый импульс | Параметры частотной адаптации | Параметры ответа на тахикардию |
| Код | O = нет, A = предсердие, V = желудочек, D = (A + V) | O = нет, A = предсердие, V = желудочек, D = (A + V) | O = нет, T = стимулирование, I = подавление, D = (T + I) | O = нет, R = частотная адаптация | O = нет, D = (Pacing + Shock) |
| Маркировка производителя | S = одно из (A или V) | S = одно из (A или V) |
Обозначения в данной таблице — это сокращения английских слов.
А — atrium, V — ventricle, D — dual, I — inhibition, S — single (в позициях 1 и 2), T — triggering, R — rate-adaptive.
Например, согласно этой системе VAT будет означать: стимулятор в режиме детекции ритма предсердия и стимуляции желудочка в режиме биоуправления, без частотной адаптации.
Наиболее распространённые режимы стимуляции:
- VVI — однокамерная желудочковая стимуляция по требованию (по старой российской номенклатуре «R-запрещаемая стимуляция желудочка»);
- VVIR — то же с частотной адаптацией;
- AAI — однокамерная предсердная стимуляция по требованию (по старой российской номенклатуре «P-запрещаемая стимуляция предсердия»);
- AAIR — то же с частотной адаптацией;
- DDD — двухкамерная предсердно-желудочковая биоуправляемая стимуляция;
- DDDR — то же с частотной адаптацией.
Последовательная стимуляция предсердия и желудочка называется секвенциальной.
VOO/DOO — асинхронная стимуляция желудочка/асинхронная секвенциальная стимуляция (в клинической практике как постоянная не применяется, возникает в особых случаях работы стимулятора, например при магнитном тесте или при наличии внешних электромагнитных помех. Чреспищеводная кардиостимуляция чаще всего проводится в режиме AOO (формально это не противоречит стандартным обозначениям, хотя предсердие при эндокардиальной стимуляции имеется в виду правое, а при ЧПЭС — левое).
Совершенно очевидно, что, например, стимулятор типа DDD принципиально возможно программно перевести в режим VVI или VAT. Таким образом, код NBG отражает и принципиальную способность данного кардиостимулятора и режим работы прибора в каждый момент времени (например, ИВР типа DDD, работающий в режиме AAI). Двухкамерные стимуляторы зарубежных и некоторых отечественных производителей обладают кроме всего прочего функцией «переключения режимов» (switch mode — стандартное международное наименование). Так, например, при развитии у пациента с имплантированным ИВР в режиме DDD мерцательной аритмии, стимулятор переключается в режим DDIR и т. д. Это сделано для обеспечения безопасности пациента.
Ряд производителей ИВР расширяет данные правила кодирования для своих стимуляторов. Так например Sorin Group применяет для ИВР типа Symphony режим, обозначаемый как AAIsafeR (а также AAIsafeR-R). Принципиально похожий режим фирма Medtronic для своих ИВР Versa и Adapta обозначает AAI<=>DDD и т. д..
Двухжелудочковая стимуляция (BVP, biventricular pacing)
править
При некоторых заболеваниях сердца возможна ситуация, когда предсердия, правый и левый желудочки сокращаются несинхронно. Такая асинхронная работа приводит к снижению производительности сердца как насоса и ведёт к развитию сердечной недостаточности, недостаточности кровообращения.
При данной методике (BVP) стимулирующие электроды помещаются в правое предсердие и к миокарду обоих желудочков. Один электрод располагается в правом предсердии, в правом желудочке электрод находится в его полости, а к левому желудочку он подводится через венозный синус.
Такой вид стимуляции называется также кардиоресинхронизирующей терапией (CRT).
Путём подбора параметров последовательной стимуляции предсердия и левого и правого желудочка в ряде случаев удаётся устранить диссинхронию и улучшить насосную функцию сердца. Как правило для подбора действительно адекватных параметров у таких приборов требуется не только перепрограммирование и наблюдение за пациентом, но и контроль одновременно эхокардиографии (с определением параметров сердечного выброса, в том числе VTI — интеграла объемной скорости кровотока).
В наше время могут быть применены и комбинированные устройства, обеспечивающие РСТ, функции ИКД, ну и конечно стимуляцию при брадиаритмиях. Однако стоимость подобных устройств до сих пор весьма велика, что сдерживает их применение.
Имплантируемые кардиовертеры-дефибрилляторы (ИКД, ИКВД)
править
Остановка кровообращения у пациента может произойти не только при остановке водителя ритма сердца или развитии нарушений проведения (блокад), но и при фибрилляции желудочков или при желудочковой тахикардии.
Если человек по этой причине имеет высокий риск остановки кровообращения, ему имплантируют кардиовертер-дефибриллятор. Кроме функции стимуляции при брадисистолических нарушениях ритма он имеет функцию прерывания фибрилляции желудочков (а также трепетания желудочков, желудочковой тахикардии). С этой целью, после распознавания опасного состояния, кардиовертер-дефибриллятор наносит разряд от 12 до 35 Дж, что в большинстве случаев восстанавливает нормальный ритм, либо по крайней мере купирует жизнеугрожающие нарушения ритма. Если первый разряд был неэффективен, аппарат может повторить его до 6 раз. Кроме того современные ИКД помимо собственно разряда могут использовать различные схемы нанесения частой и залповой стимуляции, а также программированной стимуляции с различными параметрами. Это во многих случаях позволяет без нанесения разряда купировать жизнеугрожающие нарушения ритма. Тем самым кроме клинического эффекта достигается бо́льший комфорт для пациента (нет болезненного разряда) и экономия батареи прибора.
Опасность от кардиостимулятора
править
Кардиостимулятор — это высокотехнологичный прибор, реализующий множество современных технических и программных решений. В нём в том числе предусмотрено обеспечение многоступенчатой безопасности.
При появлении внешних помех в виде электромагнитных полей стимулятор переходит в асинхронный режим работы, то есть перестает реагировать на эти помехи. Кроме того, большую роль в предотвращении ингибирования внешними помехами работы кардиостимулятора играет программирование конфигурации параметра чувствительности стимулируемой камеры на так называемую биполярную конфигурацию.
При развитии тахисистолических нарушений ритма двухкамерный стимулятор производит автоматическое переключение режимов из DDD(R)-режима в один из «полудвухкамерных» режимов (например, DDI(R), VDI) или в однокамерный (VVI(R)), чтобы обеспечить стимуляцию желудочка с безопасной частотой. После восстановления синусового ритма происходит автоматический возврат первично запрограммированного двухкамерного режима стимуляции.
При разряде батареи стимулятор отключает часть встроенных функций, чтобы обеспечить жизнеспасающую стимуляцию (VVI) ещё некоторое время (в среднем 3 месяца) — до замены батареи.
Кроме этого применяются иные механизмы обеспечения безопасности пациента.
В последние годы широко обсуждается в СМИ возможность целенаправленного причинения вреда пациенту с кардиостимулятором, обладающим возможностью дистанционного обмена с программатором. Принципиально такая возможность существует, что было убедительно показано. Однако следует учесть:
- бо́льшая часть ныне применяемых зарубежных и все отечественные кардиостимуляторы требуют для программирования близкого контакта с головкой программатора, то есть не поддаются дистанционному воздействию вообще;
- потенциальный хакер должен иметь в своем распоряжении сведения о кодах обмена с кардиостимулятором, которые являются технологическим секретом фирмы-производителя, что не является существенным препятствием. Попытка воздействовать на стимулятор без этих кодов приведет к тому, что он как при любых прочих недетерминируемых помехах перейдет в асинхронный режим и перестанет вообще воспринимать внешнюю информацию, следовательно, не нанесёт вреда;
- сами возможности воздействия стимулятора на сердце конструктивно ограничены из соображений безопасности;
- хакер должен знать, что у данного пациента имеется стимулятор вообще, конкретной марки, в частности, а также — что данному пациенту по его состоянию здоровья вредны конкретные воздействия.
Таким образом, опасность подобного покушения на пациента представляется невысокой. Вероятно, производители ИВР примут в дальнейшем меры по криптографической защите протоколов дистанционного обмена.
Принципиально, как и любой иной прибор, кардиостимулятор может отказать. Однако с учётом высокой надёжности современной микропроцессорной техники и наличием у стимулятора дублированных систем безопасности — это происходит крайне редко, вероятность отказа составляет сотые доли процента. Вероятность отказа с принесением вреда пациенту ещё меньше.
Следует поинтересоваться у своего врача — как будет проявляться отказ конкретного стимулятора и что предпринимать в этом случае.
Однако само наличие в организме инородного тела — тем более электронного прибора — всё же требует от пациента соблюдения определённых мер безопасности.
Правила поведения для пациента с кардиостимулятором
править
Любой пациент с кардиостимулятором должен соблюдать некоторые ограничения:
- запрещается подвергаться воздействию мощных магнитных и электромагнитных полей, полей СВЧ, а также и непосредственному воздействию любых магнитов вблизи места имплантации;
- при лучевой терапии категорически запрещено подвергать облучению область, в которой находится кардиостимулятор или имплантируемый кардиовертер-дефибриллятор, поскольку воздействие ионизирующего излучения может привести к выходу имплантата из строя.
- запрещается подвергаться воздействию электрического тока;
- запрещается выполнять магнитно-резонансную томографию (МРТ). В 2011 году на рынок вышли несколько систем стимуляции, которые позволяют выполнять МРТ при соблюдении определённых условий, в настоящее время количество МРТ-совместимых систем стимуляции постоянно растет;
- запрещается использовать бо́льшую часть методов физиотерапии (прогревания, магнитотерапию и т. д.) и многие косметологические вмешательства, связанные с электрическим воздействием (конкретный перечень нужно уточнять у врачей);
- запрещается проводить ультразвуковое исследование (УЗИ) с направлением луча на корпус стимулятора;
- запрещается наносить удары в грудь в область имплантации стимулятора, пытаться смещать аппарат под кожей;
- запрещается применять монополярную электрокоагуляцию при хирургических вмешательствах (в том числе эндоскопических), применение биполярной коагуляции должно быть максимально ограничено, в идеале — не применять совсем. В 2013 году в Российском национальном исследовательском медицинском университете защищена диссертация и проведено клинико-экспериментальное исследование, сделавшее возможным применение монополярной электрокоагуляции у пациентов с кардиостимулятором при соблюдении определенных условий
Мобильный или иной беспроводной телефон желательно не подносить ближе 20—30 см к стимулятору, следует держать его в другой руке. Аудиоплеер лучше располагать также не вблизи от стимулятора. Можно пользоваться компьютером и подобными ему устройствами, в том числе портативными. Можно выполнять любые рентгеновские исследования, в том числе компьютерную томографию (КТ).
Можно работать по дому или на участке, использовать инструмент, в том числе электроинструмент, при условии его исправности (чтобы не было поражения электрическим током). Следует ограничить применение перфораторов и электродрелей, а также газонокосилок. Косить вручную и колоть дрова следует с осторожностью, при возможности лучше отказаться от этого.
Можно заниматься физкультурой и спортом, избегая контактно-травматических его видов и не допуская вышеупомянутого механического воздействия на область стимулятора. Нежелательны большие нагрузки на плечевой пояс. В первые 1—3 месяца после имплантации желательно ограничить движения рукой со стороны имплантации, избегая резких подъёмов выше горизонтальной линии и резких отведений в сторону. Через 2 месяца указанные ограничения обычно снимаются. Разрешается заниматься плаванием.
Средства контроля в магазинах и аэропортах («рамки») испортить стимулятор не могут, однако желательно либо совсем не проходить их (для чего предъявить охране карточку владельца кардиостимулятора), либо сократить пребывание в зоне их действия до минимума. [2]
Пациент с кардиостимулятором должен своевременно являться к врачу для проверки прибора с использованием программатора. Крайне желательно знать про себя: марку (название) имплантированного прибора, дату и повод имплантации.
Работа кардиостимулятора существенно меняет картину электрокардиограммы (ЭКГ). При этом работающий стимулятор так изменяет форму комплексов на ЭКГ, что по ним становится невозможно судить о чём-либо. В частности, работа стимулятора может маскировать ишемические изменения и инфаркт миокарда. С другой стороны, так как современные стимуляторы работают «по требованию», отсутствие признаков работы стимулятора на электрокардиограмме ещё не означает его поломку. Хотя нередки случаи, когда средний медицинский персонал, а иногда и врачи при этом без должных оснований заявляют пациенту «у Вас не работает стимулятор», что сильно нервирует больного. Помимо этого, длительное наличие правожелудочковой стимуляции меняет и форму собственных комплексов ЭКГ, иногда имитируя ишемические изменения. Этот феномен носит название «синдром Шатерье».
Таким образом, интерпретация ЭКГ при наличии кардиостимулятора затруднена и требует специальной подготовки; при подозрении на острую патологию сердца (ишемию, инфаркт) их наличие/отсутствие следует подтверждать другими методами (чаще — лабораторным). Критерием правильной/неправильной работы стимулятора чаще является не обычная ЭКГ, а проверка с программатором и в ряде случаев суточное ЭКГ-мониторирование.
ЭКГ-заключение у пациента с кардиостимулятором
править
При описании ЭКГ у пациента с имплантированным ИВР (искусственным водителем ритма) указывается:
- наличие кардиостимулятора;
- режим его работы, если это известно или однозначно (следует учесть, что у двухкамерных стимуляторов возможны различные режимы работы, переход между которыми может осуществляться непрерывно, в том числе beat-to-beat, то есть в каждом сокращении);
- описание собственных комплексов (при их наличии) по стандартам обычной ЭКГ (обязательно указывать в расшифровке, что интерпретация проводится по собственным комплексам);
- суждение о нарушении работы ИВР («нарушение функции детекции», «нарушение функции стимуляции», «нарушение электронной схемы»), если на это есть основания.
При описании суточного ЭКГ у пациента с ИВР указывается:
- соотношение ритмов (сколько времени регистрировался какой ритм, в том числе ритм ИВР в режиме);
- частоты ритма по обычным правилам описания холтеровского монитора;
- стандартная расшифровка данных монитора;
- сведения о выявленных нарушениях работы ИВР («нарушение функции детекции», «нарушение функции стимуляции», «нарушение электронной схемы»), если на это есть основания, при этом все типы выявленных нарушений, а при небольшом количестве эпизодов — и все эпизоды должны быть иллюстрированы в заключении распечаткой фрагментов ЭКГ в описываемый момент времени. В случае отсутствия признаков нарушения функции ИВР допустима запись «признаков нарушения функции ИВР не выявлено».
Следует учесть, что при анализе работы современных ИВР целый ряд функций (гистерезис, псевдо-Венкебах, переключение режимов и прочие ответы на тахикардию, MVP и т. д.) могут имитировать неправильную работу стимулятора. Причем не существует способов отличить правильную работу от неправильной по ЭКГ. Врач функциональной диагностики, если он не имеет специальной подготовки по программированнию стимуляторов и не имеет в своём распоряжении исчерпывающих данных о запрограммированных режимах данного конкретного ИВР у данного пациента, не вправе выносить окончательные суждения об адекватности работы ИВР (кроме случаев явного нарушения функций прибора). В сомнительных случаях следует направлять пациентов на консультации по месту программирования/проверки ИВР.
Джон Эванс прожил 112 лет, кардиостимулятор ему был установлен в 108 лет.[3]
Эмилио Маркес Флорес прожил 113 лет, кардиостимулятор ему поставили в возрасте 101 год.[4]
Арне Ларссон (1915-2001) был первым пациентом, которому установили кардиостимулятор в 1958 году, после этого он прожил ещё 43 года, он сменил 26 кардиостимуляторов.[5]
- Кардиология
- Проводящая система сердца
- Стимулятор
- ↑ UN Comtrade Commodity Classifications
- ↑ Посохов И.Н., Праскурничий Е.А. Оценка пригодности к авиапутешествиям пациентов с нарушениями ритма сердца // Вестник аритмологии. — 2023. — Т. 30, № 1. — C.e11-e18 — doi: 10.35336/VA-2023-3-1196
- ↑ John Evans | Gerontology Wiki | Fandom. Дата обращения: 20 января 2022. Архивировано 20 января 2022 года.
- ↑ Самому старому мужчине на Земле почти 113 лет | Новости на Gazeta.ua
- ↑ Кардиостимулятор: история одного прибора | Культура и стиль жизни в Германии и Европе | DW | 08.10.2018. Дата обращения: 20 января 2022. Архивировано 20 января 2022 года.
- Кардиостимуляция : [арх. 17 октября 2022] / О. Л. Бокерия // Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов. — М. : Большая российская энциклопедия, 2004—2017.
- Электрокардиостимуляция : [арх. 15 июня 2024] // Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов. — М. : Большая российская энциклопедия, 2004—2017.
