Оригинальные препараты и дженерики – отличия и особенности
Вы когда-нибудь задумывались, почему на аптечных полках так много препаратов, которые содержат одно и то же действующее вещество ― например, молекулу ибупрофена? Знакомьтесь, одно из лекарств — это оригинал, а остальные — его дженерики. Что это за препараты? Это лекарства, созданные по образу и подобию препарата-первопроходца [1].
Рассказываем, в чём их особенности и подводные камни. Подробно остановимся на том, какие препараты считаются оригинальными, а какие – дженериками, чем отличаются дженерики от оригинальных лекарств.

Права на фото Сервье
Что такое дженерики?
Дженерики ― это копии оригинальных лекарственных средств, с такими же составом активных действующих веществ и формой выпуска [2]. В российском законодательстве дженерики принято называть воспроизведенными лекарственными препаратами, а оригиналы ― референтными лекарственными препаратами [2]. В обиходе для оригинальных препаратов также употребляется ряд синонимов: оригинал, оригинатор, референтный препарат, эталонный, первый препарат. У дженериков также существует ряд понятий «заменителей» — копия, аналог, воспроизведенный препарат. Обращение дженериков и оригинальных препаратов регулируются Федеральным законом (ФЗ) № 61 от 12.04.2010 [2].
Оригинальные препараты на государственном уровне защищаются патентами. После того, как действие патента на эталонный препарат заканчивается, другие фармацевтические компании могут выпускать свои дженерики. Чтобы понять, оригинальный это препарат или дженерик, можно спросить врача или сотрудника аптеки либо воспользоваться помощью специальных интернет-ресурсов – о них расскажем в конце статьи.
Сравнение оригинальных препаратов и дженериков
Несмотря на то, что в основе оригинала и дженерика — молекула одного и того же активного вещества, аналог лекарства отличается от оригинального по ряду критериев, и ставить знак равенства между не всегда возможно.
Рассказываем детально, чем отличается дженерик от эталонного препарата.
Особенности создания лекарственных препаратов и их исследований
Чтобы появиться на аптечных полках, впервые синтезированные препараты проходят дорогостоящие исследования, доказывающие их безопасность и эффективность. Производитель вкладывает деньги, силы, время и труд учёных в:
- Доклинические исследования – химические, физические, биологические, фармакологические и токсикологические. На этом этапе научными методами изучается и оценивается эффективность и безопасность лекарственных средств. Проводятся на клеточных культурах и лабораторных животных.
- Клинические исследования. Это исследования уже с участием человека. Они выявляют или подтверждают клинические и/или фармакологические эффекты исследуемых препаратов в сравнении с плацебо (веществами, не имеющими явных лечебных свойств, которые используются в качестве имитации лечебного препарата), оценивают терапевтический эффект, выясняют нежелательные реакции, изучают особенности всасывания, распределения, метаболизма и выведения лекарства из организма.
Поэтому порой на создание одного нового лекарства и его тщательную проверку уходит 12-20 лет и очень много средств [3,8].
В воспроизведённых препаратах используется та же формула действующего вещества, которая уже была изучена производителями-первооткрывателями. Это позволило на законодательном уровне закрепить менее объемные и жесткие регистрационные требования. В итоге дженерик поступает в продажу быстрее, пройдя заметно меньшее количество исследований. Например, в России для дженериков НЕ обязательно проведение масштабных клинических и доклинических исследований фармакологической активности, поисковые исследования и изучение полного профиля безопасности [2]. А для оригиналов это ― обязательные условия.
В итоге ситуация с созданием воспроизведённых лекарственных средств обстоит так:
- Доклинические и клинические испытания по оценке эффективности и безопасности (терапевтической эквивалентности) могут не проводиться.
- Часто производители дженериков ограничиваются только клиническим исследованием биоэквивалентности ― определением скорости и степени всасывания дженерика относительно референтного препарата при приеме в одинаковых дозах и лекарственных формах на основании определения их концентрации в жидкостях и тканях. [8].
Но этих данных может быть не достаточно, чтобы говорить о равнозначном терапевтическом действии дженерика и первого лекарства. Чтобы это выяснить, нужно провести клиническое исследование терапевтической эквивалентности, которое сможет подтвердить, что сравниваемые препараты обладают сопоставимой эффективностью и безопасностью. Но согласно действующему законодательству, для дженериков проведение такого исследования не обязательно.
Регистрация оригинальных препаратов и их аналогов
Для выхода на рынок референтные препараты и дженерики проходят разные пути регистрации.
После создания и регистрации оригинальной молекулы, законодательства многих стран предоставляют первому производителю патентную защиту [1]. Россия — не исключение. Патент дает производителю эксклюзивные права (временную монополию) на производство и продажу препарата с конкретной молекулой в течение ограниченного времени. Государственная регистрация первого лекарственного средства с оригинальным действующим веществом подтверждает, что препарат оригинален, безопасен, эффективен и прошёл все необходимые исследования и испытания [1]. Это нужно, чтобы сбалансировать права производителей оригинальных препаратов на возмещение своих затрат.
Когда срок действия патента заканчивается, другие компании могут выводить на рынок свои аналоги. Поэтому первые дженерики могут появляться спустя 10-20 лет [1, 9]. При этом чтобы дженерик вышел, ему не требуется такое количество испытаний, проверок и документов, будет достаточно одного из ранее упомянутых исследований — биоэквивалентности или терапевтической эквивалентности (чаще выбирают первое). А вместо отчёта о результатах собственных доклинических исследований фармацевтическая компания может предоставить обзор научных работ о результатах доклинических исследований действующего вещества [2].
То есть, процесс регистрации дженериков может быть проще: их производители подтверждают сопоставимость действующего вещества дженерика с действующим веществом оригинала и предоставляют обзор исследований, уже проведенных для референтного препарата.
Эффективность
Согласно закону, фармацевтические компании, производящие дженерики, в большей части случаев не обязаны подтверждать терапевтическую эквивалентность — что их препарат полностью аналогичен эталонному по эффективности и безопасности. При регистрации воспроизведенных лекарственных средств достаточно подтвердить одинаковые с референтными:
- скорость всасывания, поступления к месту действия и выведения из организма
- концентрацию активного вещества
- форму выпуска лекарства [1]
Если оригинал ― это препарат в форме таблеток, то и дженерик должен выпускаться в таблетках. В идеале качество активного действующего вещества тоже должно совпадать: быть очищено от примесей и содержаться в нужном количестве.
Важно упомянуть, что в любом лекарственном препарате есть активные действующие вещества, а есть вспомогательные: наполнители, красители, ароматизаторы и другие компоненты [5]. Они создают среду для активной молекулы. Производитель дженерика имеет право использовать те вспомогательные вещества, которые считает нужными и подходящими. По этой причине дженерик и эталонное средство могут иметь разный цвет, вкус, запах и иные органолептические характеристики [5]. Такое отличие дженерика от оригинала допускается.
Однако практика показывает, что вспомогательные компоненты недооценивать не стоит. На это есть как минимум две причины.
- Вспомогательные компоненты дженериков могут вызвать побочные эффекты, которых нет у референтных лекарств. Одно канадское исследование [6] показало, что у пациентов, принимавших генерические версии трех различных препаратов для снижения артериального давления, наблюдалось увеличение частоты побочных эффектов: на 8% для лозартана, на 12% для валсартана и на 14% для кандесартана. Авторы исследования не изучали, насколько хорошо эти лекарства снижают давление ― только присутствие побочных эффектов.
- Состав и способы получения вспомогательных веществ не раскрываются производителями оригинальных препаратов, поэтому два лекарства даже с одним аналогичным активным веществом могут отличаться по терапевтическому действию и профилю безопасности [5, 9, 10]. В России сложно узнать, обладают ли два препарата с похожим составом схожим терапевтическим действием, потому что дженерики не проходят некоторых необходимых для этого доклинических и клинических исследований. Например, сравнивая первый кларитромицин и 65 его дженериков [4], учёные выяснили следующее: в 6 дженериках содержание активной молекулы не соответствовало стандартам оригинала, у 28 количество высвобождавшегося при растворении активного компонента было ниже, чем у эталонного лекарства, у 12 был превышен лимит примесей и вспомогательных веществ. В итоге 46 дженериков из 65 не соответствовали референтному препарату по качеству, эффективности и безопасности.
То есть даже если два лекарства будут биологически эквивалентными, их терапевтический эффект может различаться, несмотря на идентичные инструкции по медицинскому применению.
Цена
Как правило отличить оригинальный препарат от дженерика может помочь стоимость препарата – чаще всего дженерики дешевле оригинала, иногда значительно . Производители референтных и воспроизводимых лекарств несут разные затраты с момента разработки оригинальной молекулы до доставки своих препаратов на аптечную полку.
Процесс работы над эталонным лекарством всегда обходится дороже. Затраты на его разработку и производство включают в себя расходы на:
- синтез новой субстанции,
- доклинические и клинические исследования,
- крупномасштабные испытания лекарств,
- рекламу, маркетинг, продвижение [1].
Затраты производителя дженерика в сравнении с производителем оригинального препарата могу быть значительно ниже, поскольку препарат создаётся «по проторенной дорожке» и не проходит большую часть исследований и испытаний. Это делает его значительно дешевле по данным американского Федерального агентства лекарственных препаратов (FDA) [6]. Кроме того, когда несколько компаний выпускают свою версию одного и того же препарата, конкуренция возрастает, что также может способствовать снижению цены [6].
Как правило, по вышеизложенным причинам дженерики стоят дешевле.
Как узнать оригинальный препарат или дженерик?
Есть несколько способов, как определить дженерик:
- Спросить у врача или сотрудника аптеки. Это можно сделать как на приёме, так и посредством телемедицины.
- Узнать название молекулы действующего вещества. Его можно найти в интернете, например, здесь, по торговому наименованию. Также на сайте государственного реестра лекарственных средств (ГРЛС) в разделе «Новости» периодически публикуются обновления списка взаимозаменяемых лекарственных препаратов. Список оформлен в виде таблицы, в которой в первом столбце указан референтный (оригинальный) препарат, а далее торговые наименования его дженериков.
- Воспользоваться Единым реестром зарегистрированных лекарственных средств Евразийского экономического союза. В этом реестре есть строка поиска, в которую можно ввести торговое наименование интересующего вас препарата и увидеть его «вид» в столбце «характеристики лекарственного препарата», например, оригинальный или воспроизведенный.
Можно ли заменять эталонный препарат дженериком?
Дать однозначный ответ на вопрос «что лучше ― аналог или оригинал лекарства?» сложно.
На практике разница между дженериком и оригиналом зависит от добросовестности производителя воспроизведённого препарата. Например, если производитель стремится любыми способами удешевить продукцию, то он будет экономить ― но сложно предположить, на чём. Иногда производство переносится в страны третьего мира, где рабочая сила дешевле; в другом случае компания использует другие консерванты, которые, однако, не уступают по качеству; а в третьем ― экономит на качестве сырья. Однако в случае производства лекарственных препаратов сложно представить полностью безобидную экономию. Экономия на качестве сырья может сказаться на терапевтической эффективности. Лечение таким препаратом может быть как неэффективным, так и нанести вред здоровью пациента. По этой причине отличия оригинала и дженерика не следует упускать из вида, особенно, когда речь идёт о лечении хронических состояний.
Важно научиться выбирать качественные препараты для лечения, которые не вызывают сомнения и не подвергают организм рискам. Поэтому всегда необходимо консультироваться с врачом, уточнять статус лекарственного препарата и его сочетаемость с другими средствами. В аптеке вам могут предложить приобрести препарат — аналог, копию, дженерик или просто «такой же, но только дешевле», то вам предлагают воспроизведённое лекарство. И если у вас нет полной уверенности в предлагаемом аналоге, то стоит задуматься над предлагаемой экономией с позиции экономии на здоровье. Ведь от этого зависит самое главное — качество вашей жизни и жизни ваших близких.
-
Список использованных источников:
-
1. Generic Drugs: Answers to Common Questions. Webmd (https://www.webmd.com/healthy-aging/generic-drugs-answers-to-common-questions) Дата обращения: 11.04.2023
-
2. Федеральный закон от 12 апреля 2010 года N 61-ФЗ «Об обращении лекарственных средств». С изменениями на 19 декабря 2022 года. Редакция, действующая с 1 марта 2023 года (https://docs.cntd.ru/document/902209774)
-
3. What’s the difference between brand-name and generic prescription drugs? Scientific American (https://www.scientificamerican.com/article/whats-the-difference-betw-2004-12-13/) Дата обращения: 11.04.2023
-
4. Лопина, О. Д. С. Ю. Сереброва. Дженерики и оригинальные ЛС. // РМЖ. (https://www.rmj.ru/articles/gastroenterologiya/dzheneriki-i-originalnye-ls/#ixzz7yNgcHP8R)
-
5. Generic medicines. Health Navigator NZ (https://www.healthnavigator.org.nz/medicines/g/generic-medicines/) Дата обращения: 11.04.2023
-
6. Leclerc J, Blais C, Rochette L, Hamel D, Guénette L, Poirier P. Impact of the Commercialization of Three Generic Angiotensin II Receptor Blockers on Adverse Events in Quebec, Canada: A Population-Based Time Series Analysis. Circ Cardiovasc Qual Outcomes. 2017 Oct;10(10):e003891. doi: 10.1161/CIRCOUTCOMES.117.003891. PMID: 28974512. (https://www.ahajournals.org/doi/pdf/10.1161/CIRCOUTCOMES.117.003891)
-
7. Generic Drugs: Questions & Answers. FDA (https://www.fda.gov/drugs/questions-answers/generic-drugs-questions-answers) Дата обращения: 11.04.2023
-
8. Верлан Н.В., Ковальская Г.А., Жукова Д.Я., Кочкина Е.О., Солодухина О.А. качественная клиническая практика №3 2016 г
-
9. Жукова Д. Я., Ковальская Г. Н. Оригинальные и дженерические лекарственные средства в терапевтической практике // БМЖ. 2011. №7.
-
10. Соколов А.В., Кукес В.Г., Бунятян Н.Д., Родина Т.А., Прокофьев А.Б., Архипов В.В., Красных Л.М., Сокова Е.А. ТЕРАПЕВТИЧЕСКАЯ ЭКВИВАЛЕНТНОСТЬ, БИОЭКВИВАЛЕНТНОСТЬ И ВЗАИМОЗАМЕНЯЕМОСТЬ ЛЕКАРСТВЕННЫХ СРЕДСТВ // Врач. 2015. №10.
Линия лекарственных средств Детралекс®
Современный подход к лечению варикоза – системный. Он включает в себя применение средств для приема внутрь и наружных средств.

Марина Блинова
Ведущая рубрики
Западные санкции, нарушение логистики и уход некоторых фарм.брендов привели к новому тренду – росту спроса на дженерики. По статистике, уже более 60% рынка занимают отечественные копии зарубежных лекарств. И в первую очередь наши производители стараются наладить выпуск наиболее востребованных антибиотиков, гормональных и онкопрепаратов.
В чем особенности таких препаратов?
Оригинальный препарат
— перед выходом на рынок проходит долгие исследования и клинические испытания. После доказанной эффективности и безопасности лекарство получает патент. И 20 лет право производить его имеет только одна компания.
Дженерик
— полностью идентичный по химической формуле препарат, выпуск которого начинается только после окончания патента оригинала.
Плюс дженерика: дешевле оригинала (нет затрат на разработку, исследования проще).
Минус дженерика: возможны побочные эффекты (производитель дженерика вправе добавлять вспомогательные вещества).
Аналог
— препарат, схожий по действию с оригиналом, но различный по составу.
Примеры оригинала, дженерика, аналога:
- Мелаксен — оригинальный препарат
- Мелатонин, Велсон — дженерики
- Мелатонин Плюс В6 — аналог
Помните, что из-за различий во вспомогательных (у дженерика) и активных (у аналога) веществах подбирать замену должен специалист, не делайте это самостоятельно. И не стесняйтесь расспросить фармацевта о составе препарата.
Читайте также в рубрике «Аптечный словарик»
В последние годы в фармакотерапии наблюдается рост доли дженериков. Хорошо ли это для пациентов? Чтобы ответить на этот вопрос, нужно понять, что такое дженерики, как создаются оригинальные лекарства, и наконец, чем отличается непатентованный препарат от оригинального (кроме названия и цены).
Многие европейские страны поддерживают дженерики. Оценки специалистов показывают, что их доля на рынке лекарств уже составляет около 70-80%.
Какие вопросы, касающиеся применения дженериков, волнуют врачей?
Еще несколько лет назад при сравнении оригинальных и генерических препаратов разница в цене между ними была разительной. Сейчас цены на оригинальные лекарства и дженерики близки, но означает ли это равнозначность в свойствах и качестве? Специалисты постоянно спорят на тему равнозначности дженериков (генериков) и оригинальных лекарств. К вопросам, остающимся без ответа, можно отнести следующее:
- Идентичны ли генерики оригинальным лекарствам?
- Какие сложности возникают с производством копий лекарств, идентичных оригиналу?
Оригинальные лекарства — дорогая инновация
Фармацевтическая компания разрабатывает препарат с определенным активным веществом, начинает производство и открывает продажи. Так на аптечных полках появляются новые оригинальные лекарства.
Выход на рынок с новым активным веществом или новым препаратом — это сложный процесс, который может длиться несколько лет. Кроме того, разработка лекарств несет в себе огромный риск множества лабораторных испытаний, часто заканчивающихся дорогостоящими неудачами. Нетрудно догадаться, что разработка состава, годы исследований, клинические испытания и решение официальных вопросов по допуску к испытаниям и лицензированию стоят миллионы долларов.
По какому маршруту пойдет новый препарат, прежде чем он попадет в аптеки?
- Первый этап — лабораторное исследование, которое также является попыткой изучить возбудителя или механизм заболевания, против которого направлено лекарство. Из многих тысяч молекул с многообещающими свойствами исследовательские группы обычно выбирают только несколько сотен или несколько десятков вариантов, обладающих наибольшим терапевтическим потенциалом.
- Затем активные вещества направляют на стадию доклинических исследований. С предметных стекол лабораторного микроскопа, группы веществ, отфильтрованных еще раз, переносятся для тестирования на животных. Начальная стадия тестирования обычно длится несколько лет и позволяет оценить эффективность препарата, его потенциал и побочные эффекты. Все это сводит к минимуму риск побочных эффектов в клинических испытаниях на людях.
Когда несколько молекул пережили испытания, показав себя с лучшей стороны, их направляют на клинические испытания. Опыты обычно делятся на несколько этапов, в которых принимают участие группы здоровых людей и пациентов с различными заболеваниями. Клинические испытания определяют, среди прочего, безопасную дозировку, влияние на конкретное заболевание, наиболее распространенные побочные эффекты.
На последнем этапе клинических испытаний проверяется эффективность нового препарата. И даже если все исследовательские группы оценили эффективность и прочие достоинства — это не означает конец процесса вывода нового препарата на рынок. Производитель проходит сложный и длительный процесс регистрации — документирование всех выполненных анализов, предоставление толстых папок с медицинской документацией за все годы исследований активного вещества.
Патент на здоровье…
Учитывая, сколько времени и денег фармацевтическая компания тратит на создание лекарства с определенным веществом, неудивительно, что производители имеют право на патентную защиту для своего открытия. Патент позволяет производить и продавать новый препарат только компании, которая успешно пошла по пути инноваций.
Патентная защита длится 20 лет, возможно продление патента до 25 лет. Только по истечении этого времени появляется возможность представить на рынке дженерик, то есть препарат, воссоздающий действие оригинального препарата.
Что такое дженерики
В производстве дженериков все очень серьезно. Непатентованное лекарственное средство, то есть заменитель, или, другими словами — эквивалент исходного лекарственного средства, должно не только содержать такое же активное вещество, что и исходное лекарственное средство, но и также отвечать нескольким ограничительным требованиям.
Универсальный препарат должен иметь:
- одинаковую форму, например, капсула / таблетка / порошок для растворения в воде;
- такую же биодоступность — т. е. количество активного вещества, которое из заданной дозы количественно попадет в кровоток и будет в равной степени абсорбировано;
- идентичное фармакологическое действие.
Препарат-дженерик также тестируется, но в этом случае задача — подтвердить его эффективность по сравнению с оригиналом. То есть измеряется:
- доступность лекарства, что отражает качество препарата;
- токсичность;
- биоэквивалентность — определяется в многоступенчатой биофармацевтической системе классификации.
Когда дженерик наконец поступит в продажу, монополия единственного производителя на рынке автоматически прекращается. Производство дженерика гораздо дешевле, а сокращение расходов на фармакотерапию распространяется не только на отдельного пациента, но и на страну.
Иными словами, дженерики — точные копии оригинальных препаратов, кроме одной детали: дженерики могут содержать другие вспомогательные вещества, при условии, конечно, что это не снижает их эффективность.
Иногда, однако, это может оказать негативное влияние на лечение. Например: на основе исходного препарата создается дженерик, который работает также, но имеет лактозу в покрытии. Люди, которые не переносят лактозу, не смогут использовать это лекарство.
По этой причине производитель непатентованного лекарственного средства не может, например, похвастаться клиническими испытаниями, проведенными для контрольного лекарственного средства.
Различия существуют
Те, кто не хочет видеть различий между оригинальными и генерическими лекарствами, заявляют, что во всех случаях применяются одни и те же критерии биоэквивалентности, клинической эффективности и безопасности, поэтому говорить о различиях между продуктами некорректно.
Но нельзя не признавать, что для дженериков более вероятны возникновение дефектов при производстве или несоответствие технологических возможностей производителя требованиям к качеству лекарств. Расхождения также могут быть вызваны некоторыми объективными причинами.
- Во-первых, регистрация дженериков менее строгая, чем оригиналов. Во многих странах государственные органы, регулирующие рынок лекарств, выдают разрешения на продажу генерических лекарств исключительно на основании их биохимической идентичности, биоэквивалентности оригиналу без необходимости проведения клинических испытаний. Однако, биоэквивалентность лекарств еще не гарантирует единообразной клинической эффективности и безопасности.
- С другой стороны, производители генериков неохотно проводят сравнительные исследования своих продуктов, чтобы дать аргументированный ответ на вопрос, идентичны ли производимые ими лекарства оригиналам.
Директивы Европейского агентства по лекарственным средствам (EMEA) гласят, что клинические испытания обязательны только для биологических генериков (моноклональные антитела, иммуноглобулины), в остальном дженерики ограничиваются тестами на биоэквивалентность.
Дженерик может отличаться от эталона не только из-за технологических проблем, несоответствий оригиналу и недостатков в процессе синтеза молекулы действующего вещества, но и по другим причинам:
- при изготовлении препарата вероятно использование дополнительных веществ и материалов;
- возможно изменение цвета;
- возможно изменение плотности и др. свойств оболочки;
- возможно несоответствие аромата и т. д.
Дополнительные вещества, даже если они не изменяют активность препарата, могут изменять фармакокинетические параметры, продолжительность действия, соотношение пиковых значений и т. д.
По этим причинам случайная замена этического (эталонного) лекарственного препарата генерическим для некоторых больных не рекомендуется, так как это может иметь непредсказуемые последствия: могут возникнуть клинически значимые различия в фармакодинамической активности, силе клинических эффектов, продолжительности, побочных эффектах, переносимости.
Причина популярности оригинальных лекарств — клинические преимущества
Пациенты, успешно контролирующие, например, гипертонию с помощью оригинального лекарства, могут не только разочароваться, но и испытать осложнения сердечно-сосудистых заболеваний из-за перехода на генерическую версию. Например, популярный в Европе препарат Небиволол был зарегистрирован Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США. Но оказалось, что заявленные свойства небиволола верны только тогда, когда речь идет об эталонной версии лекарства Небилет.
После разработки большого числа генериков небиволола, в научной медицинской литературе появляются публикации о том, что они не всегда соответствуют референсному Небилету. и замена оригинального лекарственного средства небивололом другого производителя может осложнить лечение. Например, сообщалось, что замена этического Небилета на генерическую версию небиволола снизила антигипертензивный эффект.
После перехода на дженерик могут появиться расхождения в клинической активности и других параметрах. Связаны они с тем, что действующее вещество небиволола состоит из смеси изомеров ( до 16 различных изомеров), из них в процессе производства необходимо отделить два активных. Это очень сложная технологическая задача, она может превратиться в непреодолимую для дженериковых компаний.
Таким образом, при замене эталонного лекарства на генерический следует проявлять осторожность и бдительность, учитывая возможные изменения артериального давления, различные измененные фармакодинамические эффекты, возможное увеличение дозы препарата и т. д.
При смене этичного препарата на дженерики врачи также должны предупреждать пациентов о возможных изменениях гемодинамики и самочувствия.
Можно ли заменять оригинальные лекарства дженериками?
Да! При условии, что пациент хорошо его переносит. Экономия на разнице в цене между оригинальными и непатентованными лекарствами существенная, а эффективность аналогичная.
Однако что произойдет, если непатентованное лекарство будет давать побочные эффекты, которые не вызывало оригинальное лекарство? В России — ничего, придется купить оригинал. А во многих Европейских странах пациент с осложнениями имеет право обратиться в Национальный фонд здравоохранения, и ему покроют расходы на лечение побочных эффектов заменителя.
С экономической точки зрения, проблема дженериков и оригинальных лекарств основана на балансе потери и приобретения выгоды, и наиболее важную роль здесь играет врач, задача которого состоит в оценке риска использования заменителя лекарства в конкретном случае. Также врач должен информировать пациента о наличии вспомогательных веществ, присутствующих в дженерическом препарате или, наоборот, в оригинальном лекарстве, если требуется заменить непатентованную терапию терапией оригинальным препаратом.
Без подробных данных, включающих не только стоимость лечения с использованием дженериков, но и общую стоимость, включая лечение побочных эффектов, невозможно оценить, дешевле ли медикаментозная терапия с использованием дженериков. Также невозможно классифицировать дженерики и оригинальные препараты, разделяя их на лучшие и худшие. Одно можно сказать наверняка: необходимость в использовании дженериков заключается в недостаточной доступности или дороговизне оригинальных лекарств.
Дженерик вместо оригинального препарата по рецепту — слушать ли аптекаря?
Фармацевт обязан по просьбе пациента, который приходит в аптеку с рецептом на более дорогой оригинальный препарат, предложить дженерик в том же количестве и той же дозе, что и препарат, прописанный в рецепте. Исключение составляют случаи, когда врач указывает в рецепте «не менять».
Но решение о замене лекарственного средства в фармакотерапии — от исходного лекарственного средства до аналога и наоборот всегда следует согласовывать с врачом — такое решение должно быть очень хорошо продуманным.
Когда нельзя заменить оригинал дженериком
Эксперты указывают, что референсный лекарственный препарат может быть заменен только конкретным генерическим продуктом, прошедшим исследования биоэквивалентности и идентичности. Несоблюдение этого правила может иметь серьезные последствия — рецидив или ухудшение течения болезни, осложнения и так далее.
При переходе с биологического эталонного лекарственного препарата на дженерик рекомендуется особая осторожность со стороны клинициста, поскольку их терапевтические эффекты в некоторых случаях могут существенно различаться, несмотря на молекулярную идентичность этих лекарственных препаратов.
- Для тяжелобольных (особенно в критических состояниях) рекомендуется использовать только референсные варианты лекарственных средств, указанные в стандарте лечения, без риска с лекарствами с недоказанной эквивалентностью.
- С особой осторожностью следует относиться к пациентам с сердечно-сосудистыми заболеваниями. Очень важно, чтобы достигнутые целевые параметры артериального давления, частоты пульса, ритма и другие поддерживались постоянно.
Замена референсного лекарства на дженерик создает реальный риск неспособности обеспечить стабильные гемодинамические параметры, с клиническими последствиями или даже такими осложнениями, как внезапное повышение артериального давления, ишемическая болезнь сердца, обострение сердечной недостаточности, различные аритмии и другие.
Поэтому не рекомендуется менять референсное лекарство на генерическое больным с хроническими и серьезными патологиями. А если необходимо изменить лекарство, следует проявлять большую осторожность, наблюдать за состоянием пациента. При отсутствии других вариантов референтный лекарственный препарат может быть заменен генериком, с проведенными (специфическими) исследованиями биоэквивалентности.
Вероятность того, что оригинальное (эталонное) лекарство может быть заменено неполным генериком, увеличивается по мере появления на рынке большего количества коммерческих версий этого лекарства.
Среди препаратов, используемых для лечения нарушений функции щитовидной железы, основную группу составляют гормональные средства. Выбор их на фарм. рынке России, к сожалению, не велик. А в последние годы ещё и сократился.
Сегодня я хочу остановиться на препаратах для лечения гипотиреоза, сниженной функции щитовидной железы. Эта группа препаратов состоит из 3 подгрупп, если их так разделить условно. Препараты тироксина (Т4) – замещающие гормон Т4, более известный, как Л-тироксин, о нём позже будет отдельный разговор.
Препараты трийодтиронина (Т3), замещающие гормон Т3 – о нём очень хочется сейчас рассказать, и 3 группа — комбинированные препараты, включающие в себя Т4 и Т3, иногда ещё и йод (в дозе 100-200 мкг).
Если с препаратами Т4 на фарм. рынке ещё всё нормально, препарат есть, а главное, в разных дозах. То с препаратами Т3 всё хуже – их просто нет. Несколько лет в нашей стране препараты Т3 не продавались. Часть таблеток не прошла процедуру перерегистрации препарата на территории России в контролирующих организациях, а другие вообще сняли с производства.
В эти годы у небольшого процента пациентов стала наблюдаться нечувствительность к Т4, и соответственно, стойкий гипотиреоз, который в том числе требовал замещения дополнительно и препаратами, содержащими Т3. Учитывая огромную распространенность тиреоидной патологии, общее количество нуждающихся в Т3 людей оказалось достаточно большим.
Также очень важен препарат — Т3 детям с гипотиреозом (врождённым или приобретённым), которые активно растут и развиваются, особенно для «созревания» клеток головного мозга, для развития памяти, внимания, интеллекта.
Также Т3 может использоваться в комплексном лечении диффузного нетоксического зоба и многоузлового зоба с размером узлов менее 2 см, после операций на щитовидной железе, при АИТе в сочетании с гипотиреозом, при гипертрофической форме или многоузловой форме.
Чтобы понять важность Т3 в организме, привожу ниже облегчённую схему образования гормонов щитовидной железе.
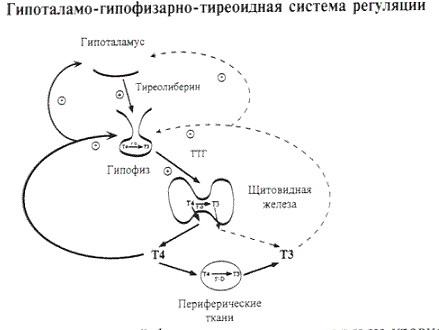
По схеме видно, что Т3 образуется в организме путём перехода из Т4, он является более активным, и непосредственно «работает» на уровне тканей и органов-мишеней, ещё и за счёт того, что соотношение Т4 и Т3 в организме 1:10, то есть триойдтиронина в 10 раз должно быть больше, что учитывается при лечении.
Вот почему при полной заместительной дозе Т4 при гипотиреозе и «нормальном» уровне ТТГ, сохраняется недомогание – вялость, слабость, плохо снижается вес, рассеянно внимание, то есть в организме не хватает Т3.
Есть препараты, позволяющие восполнить дефицит Т3 в организме
- это препараты лиотиронина или трийодтиронина , в России их нет и не выпускают, но за границей они есть под названиями:
- Тибон 100 мкг и 20 мкг, Sanofi,
- Трийод Тиронин 50 мкг, Берлин Хеми (Германия),
- Цитомель 5 мкг, 24 мкг, Улиманн-Эйрард (Швейцария).
- Цитомель 25 мкг, Меррель Дау Франция, Динкель (Турция).
- Циронин 25 мкг, 50 мкг, Мейджа (США).
- Цитомель 5 мкг, Смиф Кляйм США S Кляйм Френч (Канада, Голландия).
- Цитомель 25 мкг, С.Т. Рит Бельгия SK США, SK Френч (Канада, Голландия).
- Цитомель 50 мкг, Смит Кляйм (США).
- Линомель 25 мкг, Смит Кляйм (Аргентина).
- Неотироимад 5 мкг, 25 мкг, (Португалия).
- Ро-теранин 25 мкг, 50 мкг, Робинзон (США).
- Тертоксин 25 мкг (инъекц. раствор), Глаксо (Дания).
- Тертоксин 20 мкг, Глаксо Дания, Великобритания, (Южная Африка).
- Тибон-форте 20 мкг, 100 мкг, Хехст (Германия).
- Тиротардин инъекционный 100 мкг (сухое вещество), Хенинг Берлин (Германия).
- Ти-тре 5 мкг, 20 мкг, Глаксо (Италия).
- Тиромель 25 мкг, Ибрахим (Турция).
- Тиранин 25 мкг, Абелло (Испания)
- Трийодтиронин 20 мкг, Никомед (Швеция).
- Трийод. Санабо 25 мкг, Санабо (Австрия).
- Трийод 50 50 мкг, Берлин-Хеми (Германия).
- Трийод. Лео 25 мкг, Лео (Испания).
- Цитовер Т3 50 мкг, Vermodje
Самостоятельно таблетированный трийодтиронин не применяется (для этого есть «узкие» показания), в лечении заболеваний щитовидной железы обычно подбирается комбинация Т4 и Т3 в соотношении, их подбирает только лечащий врач.
Автор статьи: Мурзаева И.Ю., врач – эндокринолог
По данным ВОЗ, в 2008 году глобальные расходы на здравоохранение составили 5,7 триллионов долларов (www.who.int.),
по мнению экспертов ВОЗ ни в одной стране мира в настоящее время нет
достаточных средств на здравоохранение. Причина этого — рост цен на
медицинские услуги и ЛС. Для снижения стоимости фармакотерапии ВОЗ и
другие международные организации рекомендуют проведение политики
дженерических замен ЛС.
Дженерики (генерики) – это ЛС, которые содержат ту же активную субстанцию, что и оригинальный препарат. Когда срок действия патента на оригинальное ЛС заканчивается, на фармацевтический рынок поступают дженерики — «копии» оригинальных ЛС. В соответствии с законом, дженерик не должен быть запатентован. Дженерик выходит на фармацевтический рынок при соблюдении двух условий: доказаны эквивалентность дженерика и оригинального ЛС по качественному и количественному составу (фармацевтическая эквивалентность) и биоэквивалентность (фармакокинетическая эквивалентность). В то же время в нашей стране до недавнего времени для дженериков не проводилось испытаний для установления клинической терапевтической эквивалентности на больных и клинической терапевтической эффективности со специальным вниманием к безопасности и переносимости при применении у пациентов. Эти две стадии испытаний всегда проводятся для оригинальных препаратов и требуют больших финансовых затрат. В частности, по данным FDA для дженерика рабепразола ОН-ТАЙМ (компания – производитель ТЕВА) не проводились исследования клинической и терапевтической эквивалентности. Именно поэтому дженерики всегда дешевле оригинальных ЛС.
В РФ доля дженериков на фармацевтическом рынке превышает 70%, однако их эффективность и безопасность часто остается без внимания. В настоящее время в Европейском Союзе и в США отрицательно относятся к фармакокинетической эквивалентности как к единственному способу оценки взаимозаменяемости ЛС. Все чаще слышатся требования о проведении клинических исследований наиболее важных для здоровья общества дженериков. Как было уже сказано, в связи с введенными новыми законодательными нормами, к 2018 году сведения о взаимозаменяемости дженериков должны быть внесены в их инструкцию. Клиническая терапевтическая эквивалентность подразумевает проведение как ограниченных, так и крупных клинических исследований эффективности дженерика при конкретном заболевании, должно быть проведено также изучение сравнительной эффективности оригинального и воспроизведенного препарата [22].
Возникли такие требования потому, что стало очевидным наличие различий в отношении к дженерикам между лечащими врачами и регулирующими органами, регистрирующими ЛС. Поскольку дженерик и оригинальный препарат содержат одну и ту же активную субстанцию, врач полагает, что дженерик, который он выписывает пациенту, терапевтически эквивалентен оригинальному препарату. Однако это не всегда так. Почему же дженерики, которые содержат такую же активную субстанцию и характеризуются сходной с оригинальным ЛС биоэквивалентностью могут обладать худшей терапевтической эффективностью?
В первую очередь, согласно законодательству дженерик может содержать 95% активной субстанции [23]. Дженерики могут производиться с использованием другого технологического процесса, что может влиять как на количество, так и на состав примесей. Например, в оригинальном препарате ксеникал (ингибитор кишечных липаз фирмы Hoffman-La Roche) методами высокоэффективной жидкостной хроматографии и масс-спектрометрии обнаружено 3 примеси, а в дженерике орсотен (КRKA) – 13 [24]. Однако наличие определенного вида примесей даже в небольших количествах может снижать терапевтическую эффективность ЛС. Кроме того, может различаться и форма субстанции: она может быть как аморфной, так и в виде различных кристаллов. Для омепразола, например, запатентовано около 10 различных кристаллических форм. Они могут различаться по растворимости, химической реакционноспособности (например, по скорости гидролиза или окисления), механическим изменениям (например, таблетки крошатся при хранении, при этом кинетически предпочтительная форма может превращаться в термодинамически более стабильную), по чувствительности к распаду при высокой влажности.
Кроме того, все ЛС – это комбинированные препараты, которые помимо активной субстанции (химического реагента с определенными свойствами) содержат значительное количество дополнительных химических соединений, обеспечивающие его доставку к органам-мишеням, консервацию во время хранения, облегчающие всасывание или растворение в биологических жидкостях и т.д. Чтобы получить максимальный эффект ЛС, его употребляют не в виде собственно активной субстанции, то есть, химического вещества, а в сочетании со вспомогательными веществами, обеспечивающими и поддерживающими его лекарственное действие. Изменение состава и количества дополнительных компонентов ЛС, даже при наличии той же самой активной субстанции, может снизить терапевтическую эффективность препарата-дженерика, по сравнению с оригинальным ЛС, хотя фармацевтически они могут быть эквивалентными.
С целью определения биоэквивалентности оригинального ЛС и дженерика проводят двухфазное перекрестное (исследуемый препарат и препарат сравнения) рандомизированное исследование биоэквивалентности для определения значений AUC, Cmax и Tmax, обычно с участием 18–36 пациентов. При этом биоэквивалентность подтверждается, если границы двустороннего 90%-ного доверительного интервала для отношения среднегеометрических значений показателя AUC и Cmax/AUC для изучаемого препарата и препарата сравнения находятся в пределах 80-125%, а для показателя Сmax – в пределах 70-143%. Однако существуют ЛС, для которых характерна высокая вариабельность фармакокинетических параметров между отдельными субъектами. Если эти очень вариабельные ЛC характеризуются еще и высокой вариабельностью в партии (то есть, т. е., при переходе от таблетки к таблетке), то это создает дополнительный вклад в варибельность фармакокинетических параметров. Проблема изучения биоэквивалентности препаратов с высокой вариабельностью фармакокинетических параметров заключается не только в необходимости включения в исследование биоэквивалентности большего количества здоровых добровольцев, но и в том, что в популяции есть индивидуумы, которые по-разному реагируют на одну и ту же активную субстанцию, представленную в разных формулировках [25].
Все это в совокупности может привести к тому, что дженерик и оригинальное ЛС могут существенно различаться. Исследование, в котором сравнивался оригинальный кларитромицин (фирма Abbott Laboratories) и 65 его дженериков, находящихся на фармацевтическом рынке 18 стран, подтвердило это [26]. Было обнаружено, что в 6 препаратах-дженериках содержание активного вещества не соответствовало стандартам компании-разработчика, у 28 препаратов количество высвобождавшегося при растворении активного компонента было ниже, чем у оригинального, у 12 ЛС был превышен 3%-ный лимит посторонних примесей и 0,8% лимит для 6,11 ди-O-метилэритромицина A. В итоге 46 дженериков из 65 не соответствовали критериям компании, разработавшей оригинальное ЛС.
Немногочисленные работы, в которых сравнивалась терапевтическая эквивалентность дженериков и оригинальных препаратов ИПП, подтверждают, что они не всегда эквивалентны терапевтически. Cравнение эффективности оригинального омепразола и дженериков (Omeprazole-Towa, Ovulance, Omerap) в подавлении секреции кислоты показало, что днем эффективность действия, измеряемая по проценту времени с внутригастральным рН более 4, сравнима для всех препаратов и значительно выше, чем у плацебо. Однако в течение ночи наблюдались прорывы секреции кислоты, вследствие чего процент времени с рН более 4 при лечении Omeprazole-Towa и Omerap был незначительно выше, чем при лечении плацебо [27].
Сравнение эффекта Париета и одного из дженериков рабепразола, проведенное украинскими исследователями показало, что есть существенные различия в их терапевтической эффективности [28]. Если антисекреторный эффект Париета достигался через 100 минут после приема, то дженерик рабепразола начинал действовать лишь через 160 минут, длительность удержания внутригастрального рН выше 4 при приеме дженерика была почти в 2 раза меньше, чем у Париета, и, наконец, при проведении эрадикации Н. pylori с использованием в качестве ИПП Париета и дженерика рабепразола эффективность составила 92 и 66%, соответственно. Это означает, что врач, выписывающий пациенту дженерик с неисследованной терапевтической эквивалентностью, руководствуясь общепринятым мнением, что «это то же самое, но дешевле», может быть разочарован результатами лечения.
Рис. 17. Париет® 20 мг и ОН-ТАЙМ, рабепразол компании «Тева» 20 мг, исследование биоэквивалентности, 47 здоровых добровольцев
Public Assessment Report UK MHRA (Агентство по регулированию лекарств и медицинских изделий Великобритании http://www.mhra.gov.uk/home/groups/par/documents/websiteresources/con102788.pdf

И, наконец, недавно полученные данные по прямому сравнению фармакокинетических параметров Париета и дженерика рабепразола, проведенные с использованием 47 здоровых добровольцев, показывают, что AUC для дженерика рабепразола (ОН-ТАЙМ, компания –производитель Тева) составляет лишь 93,6% от оригинального препарата, а Сmax – 91,5% (рис. 19).
Необходимость исследования терапевтической эквивалентности оригинальных препаратов и дженериков ИПП можно обосновать следующим фактом: доказано, что биодоступность ИПП снижается при обострении язвенной болезни двенадцатиперстной кишки [18]. Графически это явление наиболее ярко продемонстрировано на примере дженерика лансопразола, для которого проводилось фармакокинетическое исследование при однократном введении в дозе 20 мг у здоровых добровольцев, у пациентов с гастродуоденитом и с язвенной болезнью двенадцатиперстной кишки в различные фазы заболевания (рис. 20). Оказалось, что у больных с обострением язвенной болезни, по сравнению со здоровыми добровольцами, относительная биодоступность препарата f=54,0%, fI=49,5%, максимальная степень всасывания 40,9%.
Относительная биодоступность (относительная степень всасывания) f (при расчете за период времени от нуля до бесконечности), fI (при расчете за период времени от нуля до забора последней пробы крови) и максимальная степень всасывания (fII) здесь рассчитываются как отношения средних значений соответственно AUC0-∞ , AUC0-t и Cmax у больных с обострением язвенной болезни и здоровых добровольцев.
Рис. 18. Динамика усреднённых концентраций лансопразола в плазме крови после однократного приёма лансопразола в дозе 30 мг
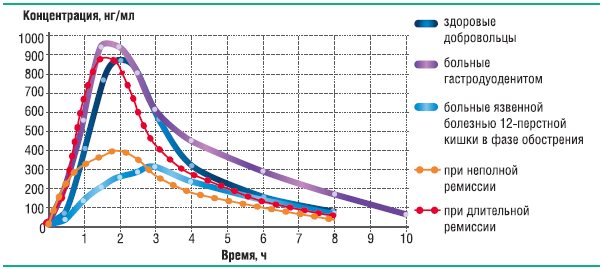
Абсорбция лансопразола резко снижается при обострении язвенной болезни и при неполной ремиссии (стадия «красного» рубца), и всасывание восстанавливается через 6 месяцев после обострения. Данное явление не может быть объяснено генетическими особенностями пациентов, так как подобную динамику фармакокинетических показателей мы наблюдали у одних и тех же пациентов в различные фазы заболевания. Таким образом, фармакокинетика лансопразола у здоровых добровольцев и у больных с обострением язвенной болезни двенадцатиперстной кишки неодинакова, следовательно, биоэквивалентность дженерика и оригинального лансопразола, как и других ИПП у больных с язвенной болезнью, не может быть гарантирована.
Сравнительное исследование фармакокинетики дженерика омепразола и оригинального препарата эзомепразола показало, что при однократном применении обоих препаратов в одинаковых дозах (20 мг) значения Cmax и AUC эзомепразола превышают таковые омепразола, что подтверждает данные о более высокой биодоступности эзомепразола за счет снижения биотрансформации с помощью CYP2С19. При обострении язвенной болезни абсорбция обоих ЛС снижается, но в разной степени (рис. 21). Относительная биодоступность дженерика омепразола f=61,0%; fI=61,1%; максимальная степень всасывания fII=46,7%. Относительная биодоступность оригинального препарата эзомепразола f=66,5%; fI=70,3%; максимальная степень всасывания fII=65,0%.
Табл. 2. Параметры сравнительной фармакокинетической оценки биодоступности дженериков омепразола, лансопразола и оригинального эзомепразола и Париета у здоровых добровольцев и пациентов с обострением язвенной болезни двенадцатиперстной кишки при однократном пероральном приеме [18]
![Табл. 2. Параметры сравнительной фармакокинетической оценки биодоступности дженериков омепразола, лансопразола и оригинального эзомепразола и Париета у здоровых добровольцев и пациентов с обострением язвенной болезни двенадцатиперстной кишки при однократном пероральном приеме [18] Табл. 2. Параметры сравнительной фармакокинетической оценки биодоступности дженериков омепразола, лансопразола и оригинального эзомепразола и Париета у здоровых добровольцев и пациентов с обострением язвенной болезни двенадцатиперстной кишки при однократном пероральном приеме [18]](https://www.rmj.ru/upload/medialibrary/76c/76c9d4a2dd365ca10c9930888f059270.jpg)
Наиболее стабильную биодоступность при обострении язвенной болезни демонстрирует оригинальный рабепразол – Париет. Его относительная биодоступность f=82,0%; fI=81,5%; и максимальная степень всасывания fII=80,9% (рис. 21). Усредненные фармакокинетические кривые для Париета у здоровых добровольцев и у больных с обострением язвенной болезни представлены на рис. 22.
Рис. 19. Динамика концентрации Париета (оригинального рабепразола) в плазме крови здоровых добровольцев и больных язвенной болезнью после однократного приема 20 мг препарата
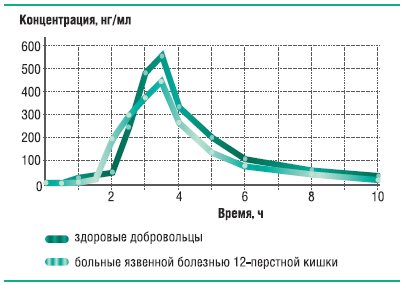
Таким образом, для присутствующих на российском фармацевтическом рынке и широко используемых препаратов ИПП нами было показано, что при обострении язвенной болезни биодоступность дженериков снижается на 38,9-50,5%, а оригинальных препаратов – на 18,0-33,5%; максимальная степень всасывания снижается у дженериков на 53,3-59,1%, а у оригинальных препаратов на 19,1-35,0%.
Причины снижения биодоступности ИПП при обострении язвенной болезни не изучались. Возможно, каким-то образом изменяется активность метаболизирующих энзимов или ферментов транспортеров. Вероятно, вспомогательные вещества, входящие в лекарственные формы производителей каким-то образом влияют на стабильность ИПП в лекарственных формах или на абсорбцию через воспаленные слизистые оболочки. До формирования каких-либо выводов необходимо проведение полноценных лабораторных и клинических исследований. Однако некоторые данные уже могут быть представлены к обсуждению: обеспечение стабильности лекарственной формы в средах с различными значениями рН.
Одним из методов сравнения дженериков, согласно рекомендациям ВОЗ, являются испытания in vitro, так называемое испытание дозированной формы по тесту «растворение». Для ИПП тест «растворение» особенно актуален, так как все они неустойчивы в кислоте, и для сохранности доставки активного действующего вещества в тонкий кишечник применяют лекарственные формы, заключенные в полимерные кишечнорастворимые оболочки.
Лекарственные формы ИПП испытывают по тесту «растворение» в средах с низкими (обычно рН 1,2) и высокими (pH≥6,8) значениями рН. При рН 1,2 лекарственные формы ИПП разрушаться не должны. При максимально высоких значениях рН (индивидуальные для разных ИПП значения максимального рН выбирают исходя, например, из значений изоэлектрической точки и т.д) активное действующее вещество должно полностью высвобождаться из лекарственной формы. То есть, при выполнении данного теста определяется стабильность лекарственных форм ИПП в условиях, приближенных по значениям рН к внутрижелудочному содержимому и внутрипросветному содержимому тонкой кишки.
Однако при выполнении стандартного теста «растворение», который может продемонстрировать одинаковые кривые растворения оригинального препарата и дженерика, не учитывается, что при промежуточных значениях рН кинетика растворения может не быть одинаковой и зависеть от качества кишечнорастворимых полимерных оболочек. Почему нужно знать, одинаково ли высвобождаются лекарственный препарат и дженерик при промежуточных значениях рН? Например, потому, что практически для всех пациентов с обострением язвенной болезни характерно наличие высокоамплитудных колебаний внутрижелудочного рН, связанных с дуоденогастральным рефлюксом, при которых после значительного повышения рН происходит достаточно быстрое его снижение до очень кислых значений за счет высокой интенсивности кислотопродукции. Если таких высокоамплитудных колебаний нет, это свидетельствует о торпидном течении язвенной болезни. Дуоденогастральный рефлюкс характеризуется быстрыми подъемами внутрижелудочного рН выше 4. О патологическом дуоденогастральном рефлюксе, характерном для большинства кислотозависимых заболеваний пищеварительного тракта, свидетельствуют быстрые подъемы рН выше 7.
Практически у всех больных с обострением язвенной болезни двенадцатиперстной кишки во время дуоденогастрального рефлюкса рН поднимается до 3 или 4, 7, а часто и до 9. Если предположить, что полимерная оболочка лекарственной формы ИПП частично растворяется на высоте рефлюкса, то последующее снижение рН должно привести к разрушению частично или полностью высвободившегося некислотоустойчивого активного действующего вещества.
Кроме того, известно, что через несколько дней курсового применения эффективных антисекреторных препаратов среднесуточные значения внутрижелудочного рН превышают значения 4, и это является необходимым условием для, например, успешного заживления эрозий в пищеводе. Если лекарственное средство в кишечнорастворимой оболочке будет нестабильным при этом значении рН, тем более, при рН 3, препарат будет разрушаться уже в желудке.
Был проведен тест «растворение» дженерика омепразола и оригинального препарата эзомепразола в средах с рН=3 и рН=4. Результаты представлены на рис. 23.
Табл. 3. Доля омепразола и эзомепразола в растворе в зависимости от времени экспозиции в средах с рН=3 и рН=4
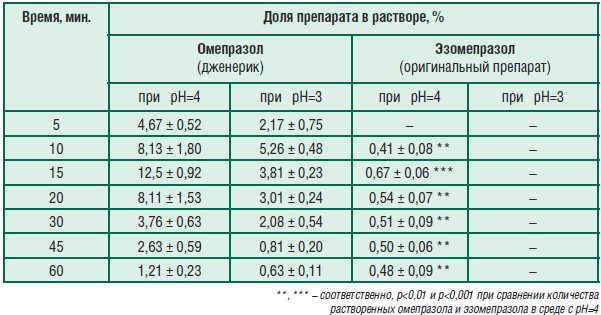
Показано, что при обоих значениях рН в растворе оказывается большее количество дженерика, чем оригинального препарата, вне зависимости от времени экспозиции препаратов в среде растворения. При этом качество лекарственного средства в кишечнорастворимой оболочке тем выше, чем меньше действующего вещества выходит в раствор при заданных в тесте условиях. Истинное количество массы действующего вещества, которое растворяется при данных значениях рН, установить не представляется возможным из-за их нестабильности в кислой среде (рН 4 – все еще кислая среда). Анализ результатов исследования показал, что в условиях, аналогичных по уровню рН и длительности экспозиции в среде растворения условиям в просвете желудка при дуоденогастральном рефлюксе, дженерик в большей степени, чем оригинальный препарат, высвобождается из кишечнорастворимой лекарственной формы. Производители оригинального препарата, вероятно, используют кишечнорастворимый полимер, более устойчивый к действию дуоденогастрального рефлюкса, также как и к условиям среды желудка при курсовом применении антисекреторных средств, чем производители исследованного дженерика. Если есть вероятность, что неустойчивый в кислой среде препарат выпускается в кишечнорастворимой оболочке худшего качества, разрушающейся при фармакологической кислотосупрессии или при высокоамплитудных колебания рН, связанных с дуоденогастральным рефлюксом у больных с обострением язвенной болезни двенадцатиперстной кишки, соответствие дженерика оригинальному препарату должно подтверждаться не стандартным тестом «растворения», а клиническими исследованиями терапевтической эквивалентности. Однако до недавнего времени в РФ указанные доводы никак не были учтены в регламенте проведения лабораторных и клинических исследований, необходимых для регистрации препаратов – дженериков. В настоящее время, согласно 429-ФЗ до 2018 года для каждого дженерика должна быть подтверждена взаимозаменяемость.
Мы имеем честь представить вам результаты исследования, которое очевидно станет основополагающим для дальнейших испытаний ЛС, выпускающихся в кишечнорастворимых лекарственных формах. В тесте сравнительной кинетики растворения была изучена растворимость таблеток оригинального рабепразола (Париет) и двух воспроизведенных лекарственных средств с действующим веществом рабепразол (ВЛС1 и ВЛС2), зарегистрированных в РФ для медицинского применения. Исследуемые ЛС были приобретены в аптеках г. Москвы в июле-сентябре 2015 года. Условия проведения сравнительного теста растворения выбирались с расчетом, что они будут имитировать патологический дуоденогастральный рефлюкс и курсовую кислотосупрессию, которая возникает вследствие применения самих же сравниваемых ИПП. Кинетику растворения рабепразола изучали в итоге в средах с рН 7,0 и рН 4,0.
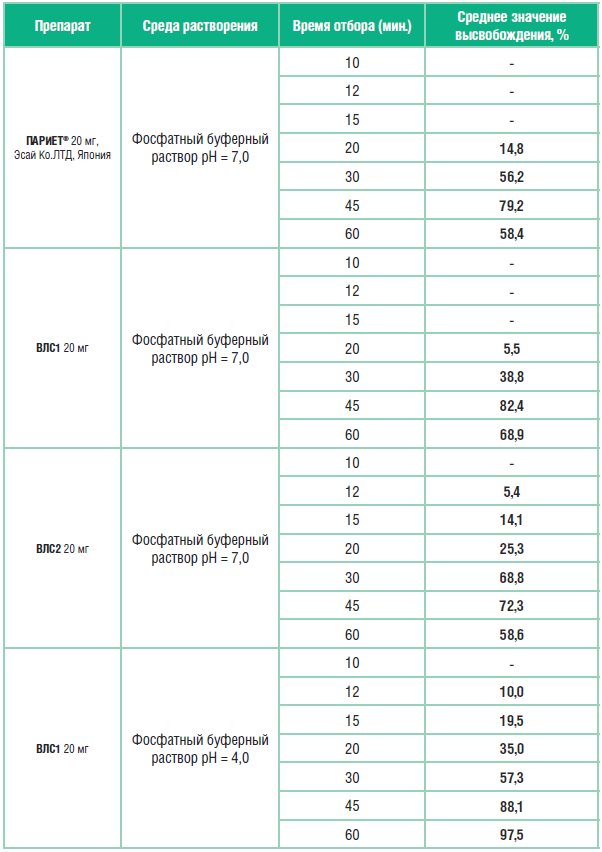
Усредненные значения количества рабепразола натрия, высвободившегося в раствор из изучаемых лекарственных средств (таблетки 20 мг), приведены в таблице 4.
Как видно из представленных данных, высвобождение рабепразола в среде растворения с рН=7,0 из препарата ВЛС2 начинается с 12-ой минуты, а из препаратов Париет и ВЛС1 – с 20-й минуты. Согласно данным по фармакокинетике рабепразола и сведениям по доле времени, в течение которого при патологическом рефлюксе внутрижелудочный рН превышает значение 7,0, это означает, что рабепразол будет выходить из лекарственной формы ВЛС2 под влиянием патологического дуоденогастрального рефлюкса уже в желудке. К 45 минутам в раствор переходит из препарата Париет 79,2% рабепразола натрия, из препарата ВЛС1 – 82,4%, из препарата ВЛС2 – 72,3%.
В среде растворения с рН 4,0 высвобождение рабепразола натрия происходит только из таблеток ВЛС1, что свидетельствует о неустойчивости его кишечнорастворимой оболочки в среде желудка с рН 4,0 (оптимальные среднесуточные значения рН при адекватной курсовой кислотосупрессии).
Усредненные профили растворения Париета и ВЛС1; Париета, ВЛС2 в среде растворения рН 7 представлены на рисунках 24 и 25. Усредненный профиль растворения препарата ВЛС1 в среде растворения рН 4,0 представлен на рисунке 26.
Эти данные означают, что у ВЛС1 через несколько дней от начала его курсового применения, когда среднесуточные значения рН содержимого желудка установятся на оптимальных значениях, будет преждевременно разрушаться собственная кишечнорастворимая оболочка. Таким образом, можно ожидать, что при курсовом применении ВЛС1 будет сам снижать собственную клиническую эффективность.
Рис. 20. Усредненные профили кинетики высвобождения рабепразола натрия из препаратов Париет® и ВЛС1 в фосфатном буферном растворе рН 7,0
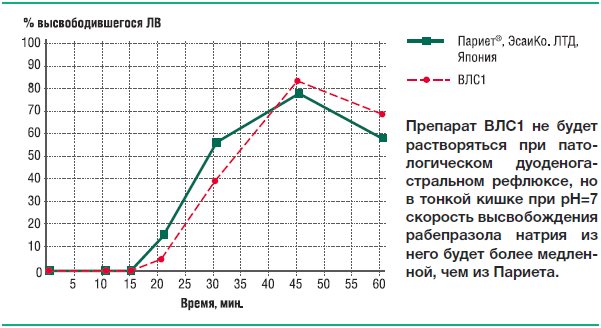
Рис. 21. Усредненные профили кинетики высвобождения рабепразола натрия из препаратов Париет® и ВЛС2 в фосфатном буферном растворе рН 7,0
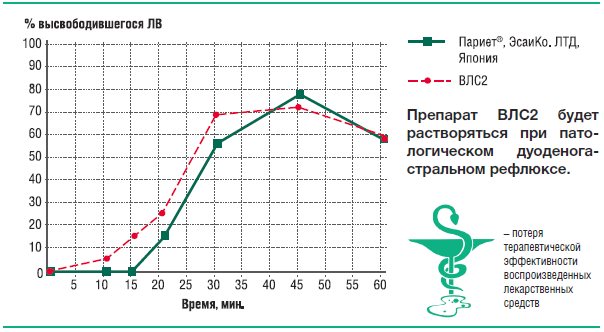
ВЛС2 не будет вызывать подобного эффекта, однако, он неустойчив к действию патологического дуоденогастрального рефлюкса, и на подъеме рН≥7 его кишечнорастворимая оболочка теряет герметичность, а некислотоустойчивый рабепразол оказывается беззащитным перед следующим за рефлюксом падением рН.
Таблица 4. Результаты кинетики растворения исследуемых препаратов рабепразола
Как это происходит, представлено на рисунке 23. В одной пробирке в одном растворе, имитирующем действие патологического дуоденогастрального рефлюкса, находятся таблетки Париета и ВЛС2. На фотографии видно, что растворяется только одна таблетка. Обе таблетки были извлечены из раствора и высушены. Видно, что таблетка, расположенная на поверхности справа, сохранила свою форму и герметичность. Она только утратила надпись (Париет). Оболочка таблетки слева (ВЛС2) разорвана по шву, обнажая содержимое.
Рис. 22. Усредненные профили кинетики высвобождения рабепразола натрия из препаратов Париет® и ВЛС1 в фосфатном буферном растворе рН 4,0
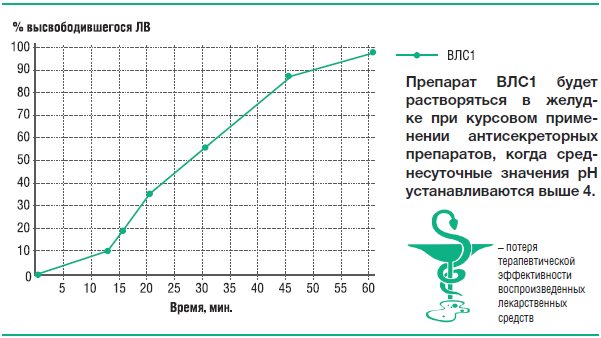
Если во время патологического дуоденогастрального рефлюкса из лекарственной формы высвобождается рабепразола натрий, то при восстановлении гиперацидности, связанной с высокой интенсивностью внутрижелудочной кислотопродукции, препарат частично разрушается уже в желудке. Т.е. биодоступность рабепразола снижается (Рис. 24).
Таким образом, ВЛС1 и ВЛС2, представленные на российском фармацевтическом рынке, не будут обладать должным фармакодинамическим эффектом и клинической эффективностью у больных с кислотозависимыми заболеваниями пищеварительного тракта, по сравнению с оригинальным препаратом (Париет).
Данная проблема касается не только препаратов рабепразола натрия, выпускаемых в таблетках, покрытых кишечнорастворимой оболочкой. На рисунках 25 и 26 представлены 3 образца пеллет (содержимого капсул: гранул, покрытых кишечнорастворимыми оболочками) разных ИПП, помещенных в среду с рН=4. Время экспозиции в данном растворе 30 мин. В образце слева пеллеты разрушены, раствор над ними мутный. В образце справа внешних признаков повреждения пеллет нет (есть незначительное их окрашивание), однако, наблюдается помутнение раствора над ними. В образце посередине наблюдается сохранение целостности, исходной окраски пеллет и прозрачность раствора над ними.
Рис. 25. Состояние пеллет разных ИПП через 30 мин. экспозиции в растворе с рН=4

Рис. 26. Состояние пеллет разных ИПП через 30 мин. экспозиции в растворе с рН=4 (контрастный фон для демонстрации помутнения раствора над пеллетами)

